Img00057 (2)
61
w stanie ciekłym, jak i stałym, w zależności od temperatury i składu. Można z nich odczytać zakresy stabilności faz ciekłych i stałych występujących w danym układzie.
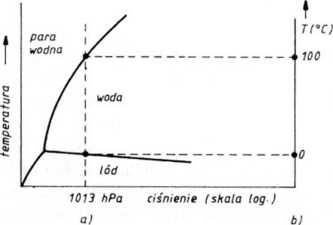
Przykładem wykresu równowagi fazowej jest wykres zmiany stanu wody w funkcji ciśnienia i temperatury (rys. 1.80-2). Dla stałego ciśnienia wykres staje się jednowymiarowy (rys. 1.80-2b) — dla temperatury: krzepnięcia i parowania, fazy (stała i ciekła oraz ciekła i gazowa) znajdują się w równowadze. W przypadku stopów metali zmiany zachodzą przy stałym ciśnieniu, natomiast czynnikiem zmiennym jest skład stopu. Powstaje wtedy dwuwymiarowy wykres: temperatura/stężenie składników.
O) b)
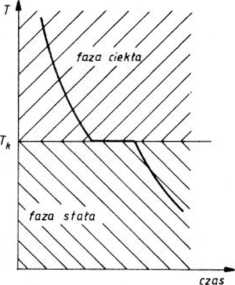
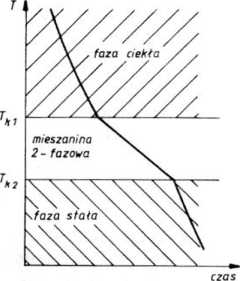
Rys. 1.80— 1. Krzywe schładzania: czystego metalu (a) oraz stopu (b)
para
wodna
woda
lód
Rys. 1.80—2. Wykres równowagi faz dla lodu, wody i pary wodnej (a); temperatury przemian dla H20 przy ciśnieniu atmosferycznym b)
1.81. Rozpatrzmy, wykorzystując do tego celu wykresy równowagi faz, przebieg procesów wywołanych zmianami temperatury w dwuskładnikowym stopie czystych metali tworzących roztwór stały.
Sposób konstruowania wykresu równowagi faz stopu dwuskładnikowego ilustruje rys. 1.81-1. Określa się krzywe chłodzenia dla czystych metali - składników stopu
Wyszukiwarka
Podobne podstrony:
31768 Slajd15 (98) Produkty wybuchu będące w stanie stałym ■ W zależności od wielkości materiału
skanowanie0056 (17) 542 TABULA RASA jak zwykle w zależności od tego, co się mierzy i w jaki sposób.
page0145 135 WROŃSKIEGO ŻYCIE 1 PRACE. gdzie x jest współczynnikiem stałym, zależnym od tarcia gazu
palezastych Jakaś cecha może być zarówno plezjomorficzna jak i apomorficzna w zależności od polaryza
IMG463 W zależności od wysokości roślin można wyodrębnić trzy strefy, w których mogą być sadzone drz
POLITECHNIKA LUBELSKA > zmiana twardości próbek w zależności od temperatury (ko
P4250080 120 temperatura gazu jest najwyższa. Według [3], w zależności od temperatury chłodzone są n
Str353 353 Tabl. 18.3.4. Wartość ciśnień obliczeniowych w zależności od temperatury
HPIM0966 Prężność nasyconej pary wodnej w zależności od temperatury i rodzaju powierzchni parującejE
Stany fizyczne polimerów w zależności od temperatury: I — stan szklisty-kruchy II
więcej podobnych podstron