DSC01349 (10)
Hiperwalencyjność
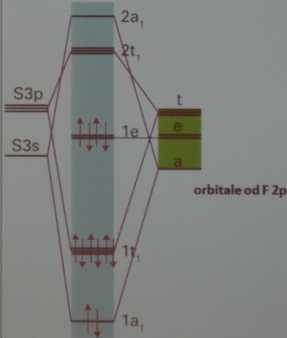
W przypadku cząsteczki SF6 liczba elektronów walencyjnych wynosi 12.
SFs: lat2 lt8 le4
Istnieją zatem cztery orbitale wiążące i dwa niewiążące.
Używanie h iperwa lencyj ności do opisu tej cząsteczki nie jest zatem potrzebne.
Ponadto, można stwierdzić, że para elektronowa może brać udział w wiązaniu wiącej niż dwóch atomów, a więc jest zdelokalizowana.
s
SF,
energia
Wyszukiwarka
Podobne podstrony:
DSC01348 (9) Cząsteczki wieloatomowe - NH3 Liczba elektronów walencyjnych w NH3 wynosi 8. NH,: iMj2
Stosunkowo łatwo jest zaobserwować efekty falowe w przypadku cząstek lekkich, np. elektronów (małe o
S + 2e~ — S2" S2-: ls22s22p63s23p6 lub [Ne] 3s23p6 = [Ar]. Liczba elektronów walencyjnych w duż
3 (368) ns!n liczba elektronów walencyjnych w wolnym atomie minus ilość elektronów walencyjnych w at
LICZBA MIEJSC NIENASYCENIA Dla cząsteczki o wzorze liczba miejsc nienasycenia N wy
Podstawy fizykochemiczne Postacie energii cząsteczki Energia stanów elektronowych ~1 -r 10 eV (UV-Vi
DSC01032 [1024x768] 26.01.10 2. Modyfikując błonę lipidową cząsteczkami obdarzonymi ładunkami elektr
DSC01337 (10) 2J Introdukcja - zamierzone lub przypadkowe wprowadzanie nierodzimych gatunków roślin
DSC01341 (10) System transportuelektronów: ■ przenosi elektrony od donora do
DSC01350 (11) Niedobór elektronów Istnienie cząsteczek wykazujących niedobór elektronów (wg Lewisa)
DSC01364 (10) B Urozoodpomok Oikreana liczba 1* Skalać oosvaadc EM 2011
396 [1024x768] NIEKTÓRE RÓWNOWAGI W ROZTWORACH ELEKTROLITÓW 405 « 10" 5. W tym przypadku można
Zdjęcie0116 (3) W przypadku membrany amonitowej stężenie elektrolitu od strony katody maleje, a od s
więcej podobnych podstron