116486

A Q = cm AT
Wielkość c określoną następująco:
1 A Q C ~ m AT
nazywamy ciepłem właściwym
Ilość dostarczonego ciepła, potrzebnego na zmianę temperatury ciała o AT, zależy również od warunków w jakich ten proces następuje:
cx
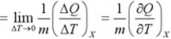
gdzie X charakteryzuje typ przemiany - przemiana izobaryczna (X=p) lub izochoryczna
(X=V).
Dalej będziemy zajmowali się ciepłem potrzebnym na ogrzanie 1 mola substancji o 1 stopień. Oznaczymy je pizez „C"a jego wymiarem będzie:
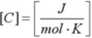
|
Przykłady: | |
|
Cr=\ |
[fi |
|
C = 1 |
fal |
|
p \ |
^T)„ |
- ciepło właściwe przy stałej objętości.
- ciepło właściwe przy stałym ciśnieniu.
Istnieje ogólny związek pomiędzy Cv i Cp dla dowolnej substancji i w dowolnym stanie skupienia. Rozważmy energię wewnętrzną substancji jako funkcję U(T,V) :
dU =
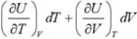
(3)
Z I zasady termodynamiki mamy:
(4)
dO:f„ = dU + pdV
Wstawiając (3) do (4) dostajemy:
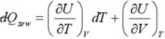
dV + pd\r
Jeśli dV = 0, to:
2
Wyszukiwarka
Podobne podstrony:
Scan00466 33. Cwoi u- tcco ■y cm AtaX> . 3
100 kort s 19 " FOln Elfenbensfarvot kort: KI p ot kcrt one- or-nsim Overśt pi sideł- Sk.:-e*
59191 PA160074 (2) SSa jest wielkością wektorową, gdyż dla jej jednoznacznego opisania należy określ
100 kort s 19 " FOln Elfenbensfarvot kort: KI p ot kcrt one- or-nsim Overśt pi sideł- Sk.:-e*
100 kort s 19 2 " FOln Elfenbensfarvot kort: KI p ot kcrt one- or-nsim Overśt pi sideł- Sk.:-
4. DEFINICJA Wartością bezwzględną liczby x € R nazywamy liczbę
Definicja dywergencji Dywergencją pola wektorowego W nazywamy pole skalarne określone następująco ,
37709 PA160075 (2) Siła jest wielkością wektorową, gdyż dla jej jednoznacznego opisania należy okreś
241a Schemat do modelu 1 romb wykonany śg. fantazyjnym 18 cm E ^ aT M . schemat obwódki <5>^-
where the term 181.6/(vj/-0.634) is the specific resistivity (fi.cm) at no current and at 30°C; the
img053 (21) 12 Tom I Wielkości $A, &B, $c określają normatywy niezbędnej powierzchni la przecho
IMG 3@ Określ punkt początkowy: Aktualna szerokość linii: 0.0000 Określ następny punkt lub
P2270807 07 d) Rlx) = I^JLl x -1 4.2. wyznacz dziedzinę funkcji wymiernych określonych następuj*™ x2
więcej podobnych podstron