87026

4
Metody badania struktury związków chemicznych, część "spcktro".
Imię i nazwisko:................................................................................................ Warszawa, 9.022004 r.
PREREKWIZYTY:.....................
Zadaik i
W widmie IR tlenku węgla uClsO, zmierzonym w temp. 300K, występuje pasmo absorpcji dla v= 2143,27 cm'1. Zakładając przybliżenie energii drgati modelem oscylatora harmonicznego wyznaczyć względne obsadzenie poziomów energetycznych, pomiędzy którymi nastąpiło to przejście. Wykazać, że przejście to jest dozwolone.
Zadanie 2
W widmie rotacyjnym chlorowodoru ‘H^Cl wystąpiły m.in. sąsiednie pasma o liczbach falowych: 104,13 cm'1 i 124,73 cm'1. Obliczyć:
- moment bezwładności cząsteczki
- długość wiązania w tej cząsteczce
- liczby kwantowe rotacji (j) odpowiadające poziomom między którymi nastąpiły przejścia.
Zadanie 3
Porównać fragmentację alkoholu etylowego CH3-CH2-OH (M=46) i eteru dietylowego CH3-CH2-O-CH2-CH3 (M=74) w badaniach MS. Narysować widma MS obu związków, uwzględniając tylko podstawowe rozpady. Zaproponować tworzenie pików metastabilnych w obu widmach. Czy wystąpią jednakowe jony w widmach obu tych związków?
Zadanie 4
Dozwolone wartości energii rotacyjnej w przybliżeniu modelem rotatora sztywnego dane są wyrażeniem: Ei=Bj(j+l). Obliczyć różnicę energii dwóch najniższych poziomów energetycznych rotacji cząsteczki chlorowodoru ‘H^Cl w tym przybliżeniu. Obliczyć X i v fotonu, który wywołałby pierwsze możliwe przejście energetyczne. Zaznaczyć to przejście na odpowiednim diagramie poziomów energetycznych. Długość cząsteczki chlorowodoru wynosi 1,27 A.
Zadanie 5
Związek karbonylowy C,HnO wykazuje w widmie ‘H NMR tylko jeden sygnał 5’H: 1,52 ppm. Sygnał ten jest ostrym singletem. Określić strukturę związku. Zinterpretować sygnały w widmie.
Zadanie 6
Wiedząc, że wektor spinu jądra *H (1=1/2) ma tylko dwa możliwe ułożenie w przestrzeni obliczyć różnicę energii oddziaływania momentu magnetycznego tego jądra (w obu ułożeniach) z zewnętrznym polem magnetycznym o natężeniu 50 000 G. współczynnik magnetogiryczny y=77 000 G'ł,s'ł
Zadanie 7
Narysować przewidywane widmo :H NMR związku o stniknirze:
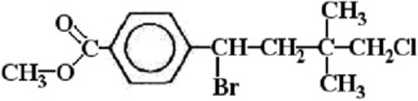
Określić orientacyjne położenia sygnałów w widmie. Podać intensywności poszczególnych sygnałów, również w multipletach. Przypisać sygnały odpowiednim grupom protonów. Narysować diagram poziomów energetycznych uzasadniający rozszczepienie sygnałów. Narysować możliwe ułożenia przestrzenne spinu protonu wchodzącego w rezonans. Obliczyć wartości długości wektora spinu i jego składowej zetowej.
Zadanie 8
Omówić wpływ stożków przesłaniania grupy karbonylowej na przesunięcia chemiczne sąsiednich protonów widmie ‘H NMR acetofenonu CJlsCOCH*
Wyszukiwarka
Podobne podstrony:
3 Metody badania struktury związków chemicznych, część "spcktro". Imię i
5 Metody badania struktury związków chemicznych, część "spektro". Imię i
Metody badania struktury związków chemicznych, część "spektro". 1 Imię i
2 Metody badania struktury zwięzków chemicznych, część "spcktro". Imię i
6 Metody badania struktury związków chemicznych, cześć "spektro". Imię i
B Metody badania struktury związków chemicznych, część "spektro". Imię i
Metody badania struktury związków chemicznych, część "spektro". Imię i
więcej podobnych podstron