2231428862
Z równania stanu gazu doskonałego wynika, że
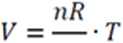
P
Podczas przemiany izobaiycznej stałe jest ciśnienie i liczba moli, a zatem objętość jest wprost proporcjonalna do temperatury:
V~T
Wykresem zależności proporcji wprost jest linia prosta, która przechodzi (lub przedłuża się) przez punkt (0.0) w układzie współrzędnych. Wykres przedstawionej w zadaniu zależności V(T) spełnia te warunki: jest fragmentem linii prostej przechodzącej przez punkt (0.0). a w związku z tym przedstawia on przemianę izobaryczną.
71R
Ciśnienie obliczymy przyrównując współczynnik proporcji do wyrażenia —: AV nR 0,1 m3 0,2 mol-8.31 „J. K
a =
AT
oraz a =
200 K
P
p = 3 324 Pa
Wyszukiwarka
Podobne podstrony:
Obiegi gazowe w maszynach cieplnych PRZEMIANY I PRAWA GAZOWE Równanie stanu gazu doskonałego (równan
HP8 strona6 / e = c, P Vp Rm (10) Natomiast po podstawieniu równania stanu gazu doskonałego do równ
P1010014 (2) , 2.5. Równanie stanu gazu doskonałego4- fi otrzymujemy: pub pv nvtr = Nkr J « «(aV f
2.3. Współczynnik ściśliwości Równanie stanu gazu doskonałego: pV = nRT
Skorzystamy z równania stanu gazu doskonałego w celu zapisania wyrażenia pozwalającego wyznaczyć Tc.
Dsc01082(1) 24. Równanie stanu gazu doskonałego to: v NR<3>pr‘— B) /?/? P _AT V . __ RN01
e = c. P-V
moodle fizyczna 4 1 1 Punkty: 1/1 8 moli gazu spełniającego równanie stanu gazu doskonałego sprężono
DS11111111 Kolokwium Termodynamika lechnic/na ET1 wykłady I 01 Omówić Równanie stanu gazu doskonałeg
Równanie Van der Izaaka Równanie stanu gazu doskonałego pV = nRT dobrze opisuje gazy rzeczywiste ale
Slajd1 Równanie stanu gazu doskonałegopV=nRT J mol K p - bezwzględna wartość ciśnienia n - liczba mo
39623 MechanikaI2 Równanie stanu gazu doskonałego Równanie Clapeyrona • dla m kg:pV = mRT R - stała
więcej podobnych podstron