
Nr 1/2006 Tom 1
5
¯ywienie dojelitowe w warunkach domowych
Home enteral nutrition
Marek Pertkiewicz
Klinika Chirurgii Ogólnej i ¯ywienia Klinicznego AM w Warszawie
STRESZCZENIE.
Czêstoœæ stosowania ¿ywienia dojelitowego w warunkach domowych (¿.d.d.) wzros³a i w krajach rozwiniêtych wynosi od
250 do 415 chorych/milion mieszkañców. W Polsce ¿ywieniem dojelitowym w warunkach domowych jest leczonych znacznie mniej chorych,
naprawdopodobniej z powodu braku organizacji i refinansowania kosztów tego leczenia. ¯.d.d. jest leczeniem ze wskazañ ¿yciowych dla
chorych, którzy nie mog¹ jeœæ, a jednoczeœnie jedn¹ z najbardziej ekonomicznie efektywnych metod opieki w prawie wszystkich dziedzinach
medycyny. Warunkiem bezpiecznego prowadzenia ¿.d.d. i unikniêcia powik³añ jest odpowiednia kwalifikacja chorych, szkolenie i monitorowa-
nie. Poniewa¿ Narodowy Fundusz Zdrowia zdecydowa³ o refinasowaniu ¿.d.d. od 2007 roku, celem pracy jest przedstawienie wskazañ, metod
i aspektów ekonomicznych ¿.d.d. oraz przedstawienie tej nowej w Polsce metody leczenia pracownikom s³u¿by zdrowia.
S³owa kluczowe: ¿ywienie dojelitowe w warunkach domowych, powik³ania, metody, wskazania do ¿.d.d.
SUMMARY.
Prevalence of home enteral nutrition (HEN) has growing up to 250–415/million population in most developed countries but in
Poland is much lower, most probably due to lack of organisation and reimbursement of HEN costs. HEN is life saving for patients unable to eat
and also one from the most economically effective methods of care in nearly all fields of medicine. However, appropriate patients selection,
training and monitoring are essential to provide safe therapy and to avoid complications. As the National Health Fund has finally decided to
reimburse HEN from 2007, the aim of this paper is to review indications, methods and economic aspects of home enteral nutrition and to
describe this method for health care professionals not familiar with HEN.
Key words: home enteral nutrition, complications, methods, indications for HEN
Idea podawania p³ynnych diet chorym jest stara jak œwiat.
W staro¿ytnym Egipcie stosowano wlewki z wina, mleka
i chleba, a w Rzymie, gdy chory nie móg³ ³ykaæ, p³ynn¹ dietê
podawano przez srebrne rurki. W roku 1598 Capivacceaus
przez wydr¹¿on¹ rurkê podawa³ p³ynny pokarm do prze³yku
[wg 2]. W XIX wieku opisano metody wytwarzania gastro-
stomii i jejunostomii od¿ywczych, w tym najbardziej znane
Kadera, Witzela i Stamma. Wykonywano je najczêœciej ze
wskazañ „¿ywieniowych” u chorych z niedro¿noœci¹ prze³y-
ku lub nowotworami ¿o³¹dka. Chorych, jeœli prze¿yli opera-
cjê, wypisywano do domu z zaleceniem podawania do prze-
toki zmiksowanych zup z dodatkiem jajek, mleka i cukru.
Z powodu Ÿle rokuj¹cej choroby podstawowej, niskiej war-
toœci podawanych diet oraz czêstych powik³añ miejscowych,
wyniki takiego od¿ywiania nie mog³y byæ dobre.
Plany podboju kosmosu spowodowa³y rozwój nowoczesnego
¿ywienia dojelitowego (¿.d.). Diety elementarne, nazywane tak-
¿e dietami astronautów, dla których je pierwotnie opracowa-
no, znalaz³y zastosowanie w od¿ywianiu ciê¿ko chorych w koñcu
lat 60. Bardziej kompletne i lepiej zbilansowane, ni¿ najbar-
dziej wymyœlne miksowane diety z produktów naturalnych,
szybko zdoby³y uznanie, a zwi¹zany z potencjalnie olbrzymim
rynkiem zbytu rozwój badañ naukowych, postêp w wytwarzaniu
diet oraz opracowanie nowoczesnego sprzêtu do ich podawa-
nia sprawi³y, ¿e obecnie ¿.d. jest mo¿liwe w wielu sytuacjach
klinicznych w szpitalu i w domu [48].
Poznanie klinicznych nastêpstw niedo¿ywienia tak¿e przyczy-
ni³o siê do rozwoju ¿.d. O ile jednak nastêpstwa kliniczne nie-
do¿ywienia poznano doœæ wczeœnie, do niedawna nie zdawa-
no sobie sprawy ze zwi¹zanych z nim kosztów. Ocenia siê, ¿e
roczny koszt niedo¿ywienia zwi¹zanego z chorob¹ wynosi
w Wielkiej Brytanii ponad 7,3 miliarda funtów i dwukrotnie
przewy¿sza koszty leczenia oty³oœci i jej nastêpstw. Na global-
ne koszty niedo¿ywienia sk³adaj¹ siê dodatkowe koszty lecze-
nia szpitalnego (3,8 miliarda funtów), opieki d³ugotermino-
wej (2,6 miliarda funtów), wizyt lekarskich (0,49 miliarda
funtów) oraz sztucznego ¿ywienia (0,15 miliarda funtów).
Porównanie poszczególnych pozycji wskazuje, ¿e niezale¿-
nie od korzyœci klinicznych taniej jest zapobiegaæ ni¿ leczyæ
rozwiniête niedo¿ywienie i jego nastêpstwa [21].
Poniewa¿ karmienie by³o i jest problemem nie tylko w ostrym
okresie choroby, ale i w czasie rekonwalescencji, a czasem
brak mo¿liwoœci od¿ywiania drog¹ naturaln¹ pozostaje na
resztê ¿ycia, ju¿ w latach 80. w USA i w Kanadzie ¿.d. zaczê-
to stosowaæ w warunkach domowych u chorych, których
mo¿na by³o wypisaæ do domu, a którzy nie mogli od¿ywiaæ
siê w sposób naturalny, posiadaj¹c sprawny przewód pokar-
mowy [1, 10, 59]. ¯.d.d. jest tym bardziej uzasadnione, ¿e
leczenie niedo¿ywienia wymaga znacznie wiêcej czasu ni¿
rozwój wyniszczenia.
Termin „¿ywienie dojelitowe” (¿ywienie drog¹ przewodu po-
karmowego,
enteral nutrition) oznacza ¿ywienie p³ynnymi die-
tami wytwarzanymi przemys³owo i o sk³adzie czêsto dostoso-
wanym do zaburzeñ metabolizmu chorego. Unia Europejska
za ¿ywienie dojelitowe uznaje wszystkie metody ¿ywienia, które
wykorzystuj¹ produkty ¿ywnoœciowe specjalnego przeznacze-
nia medycznego, niezale¿nie od drogi ich podawania. Stan-
dardy ¯ywienia Pozajelitowego i Dojelitowego Polskiego To-
warzystwa ¯ywienia Pozajelitowego i Dojelitowego za
¿ywienie dojelitowe uznaj¹ podawanie diet przemys³owych
do przewodu pokarmowego drog¹ inn¹ ni¿ doustna; poda-
wanie diet przemys³owych drog¹ doustn¹ okreœlono jako
karmienie doustne [44]. Rozró¿nienie karmienia doustne-
go od karmienia przez zg³êbnik lub przetokê od¿ywcz¹ ma
znaczenie z uwagi na zasady przepisywania i/lub refundacji,
które s¹ ró¿ne w ró¿nych krajach [1, 38]. Mo¿na rozwa¿aæ
zmniejszenie kosztów doustnego podawania diet przemys³o-
wych, ponoszonych przez pacjenta, poprzez wprowadzenie
odpowiednich preparatów na listy leków refundowanych,
nie mo¿na natomiast refundowaæ kosztów suplementarne-
go ¿ywienia doustnego w taki sam sposób, jak ¿ywienia przez
zg³êbnik lub przetokê od¿ywcz¹.
W wielu krajach termin „¿ywienie dojelitowe w warunkach
domowych” (¿.d.d.) odnosi siê jedynie do podawania diet

Nr 1/2006 Tom 1
6
Postêpy ¯ywienia Klinicznego
przez zg³êbnik lub przetokê. W niewielu obejmuje tak¿e do-
ustne podawanie diet przemys³owych, a czasem tak¿e su-
plementów diety. W niektórych krajach ¿.d.d. jest ograni-
czone do niektórych chorób lub standardowych diet.
Niemniej, we wszystkich krajach Europy Zachodniej,
w Czechach i na Wêgrzech w 1999 roku koszty ¿.d.d. by³y
pokrywane w ca³oœci lub w wiêkszoœci przez system ochrony
zdrowia lub firmy ubezpieczeniowe [28, 38].
W roku 1992 w USA ¿.d.d. otrzymywa³o 152 000 chorych za
cenê oko³o 10 000–15 000 USD rocznie [29]. W ci¹gu dziesiê-
ciu lat liczba ta wzros³a do 344 000 chorych (4 razy wiêcej
ni¿ w innych krajach), a roczny koszt ¿.d.d. jednego chorego
oceniano na 18 000 USD [2, 47]. Jeœli jednak chory wymaga³
stosowania diety specjalistycznej, koszty wzrasta³y do 55 000
USD rocznie [47]. Najczêstszym wskazaniem by³y choroby
nowotworowe, dysfagia neurogenna, niedo¿ywienie, zabu-
rzenia wch³aniania i choroba Leœniowskiego-Crohna; 15%
chorych otrzymywa³o tak¿e ¿ywienie pozajelitowe [32, 47].
W Europie Zachodniej ¿.d.d. rozwija³o siê wolniej, pocz¹tko-
wo w Wielkiej Brytanii, Niemczech, Austrii i Francji, a nieco
póŸniej we W³oszech i w innych krajach [33, 38]. ¯.d.d. uzna-
no oficjalnie jako metodê leczenia w 1988 roku we W³o-
szech i we Francji, w 1990 w Czechach, w 1996 w Belgii,
w 1998 w Hiszpanii, a w 1999 roku w Danii [28, 38].
W Wielkiej Brytanii w roku 2000 ¿.d.d. otrzymywa³o oko³o
15 000 chorych doros³ych i 5000 dzieci – od 150 do 280 na
milion mieszkañców w ró¿nych czêœciach wyspy [22]. Wiêk-
szoœæ chorych otrzymywa³o ¿.d.d. z powodu neurogennej
dysfagii; drug¹ grupê wskazañ stanowili chorzy z nowotworami
prze³yku, jamy ustnej i krtani oraz ¿o³¹dka [5, 22]. Byli to ciê¿-
ko chorzy – jedynie 2% chorych by³o w pe³ni aktywnych, po-
nad 70% nie opuszcza³o domu, a 86% wymaga³o sta³ej opie-
ki. Oceny z roku 2003 podaj¹ liczbê 20 000–25 000 chorych;
wzrost o 20% rocznie obserwowano g³ównie w regionach
lecz¹cych mniej chorych.
W Hiszpanii Krajowy Rejestr Chorych ¿.d.d. w roku 2001
obejmowa³ 3458 chorych leczonych pod opiek¹ 22 szpita-
li, a w 2003 roku – 3858 chorych [45, 46]. Najczêstszym
wskazaniem by³a neurogenna dysfagia i nowotwory. Oko³o
po³owy chorych, g³ównie z nowotworami, od¿ywiano doust-
nie [18, 46]. ¯.d.d. wymaga oko³o 150–250 chorych na milion
mieszkañców [16], a koszty dobowe wynosz¹ od 7,7 euro
przy podawaniu doustnym, do 27,7 euro przy podawaniu
diet przez zg³êbnik [18].
We Francji w latach 1990–1999 jeden oœrodek wprowadzi³
¿.d.d. u 4297 chorych. Poprawê jakoœci ¿ycia uzyskano u pra-
wie 60% chorych za cenê oko³o 20 USD dziennie [63].
Wed³ug danych z 76 oœrodków w³oskich w latach 1992–1999,
g³ówne wskazania do wprowadzenia ¿.d.d. stanowi³y: brak
mo¿liwoœci od¿ywiania drog¹ naturaln¹ i zaburzenia po³yka-
nia. Chorzy onkologiczni stanowili 52% wszystkich chorych.
Liczba oœrodków prowadz¹cych ¿.d.d. wzros³a z 46 w roku
1992 do 76; w roku 1992 prowadzono ¿.d.d. u 777 cho-
rych, a w roku 1999 u 6846. Wiêkszoœæ oœrodków, podobnie
jak i wiêkszoœæ leczonych chorych, pochodzi³a z pó³nocnych
W³och. O ile w roku 1992 wiêkszoœæ chorych otrzymywa³a ¿.d.d.
przez zg³êbnik nosowo-¿o³¹dkowy, w kolejnych latach obser-
wowano wzrost liczby chorych ¿ywionych przez PEG [62].
W Irlandii Pó³nocnej w 2002 roku ¿.d.d. leczono ponad 700
chorych, w tym 75% doros³ych i 25% dzieci.
W Polsce wskazania i zasady ¿ywienia dojelitowego opisano
w roku 1986 [57]. Chocia¿ ju¿ w roku 1984 prowadzi³em ¿.d.d.
chorego z przetok¹ prze³ykow¹ po totalnej resekcji ¿o³¹dka,
doprowadzaj¹c do jej zagojenia, to z wielu powodów rozwój
¿.d.d. w Polsce nastêpowa³ nad wyraz opornie. Wykonywane
w szpitalach procedury chirurgicznego lub endoskopowego
dostêpu do ¿.d.d. by³y i s¹ refundowane przez NFZ, podobnie
jak ¿.d. prowadzone w szpitalu. Natomiast po wypisie ze szpi-
tala pozostawiony sam sobie chory lub jego najbli¿si w latach
90. musieli „za³atwiaæ” diety przemys³owe i sprzêt do ich po-
dawania, a w XXI wieku kupowaæ diety i sprzêt. Przy mie-
siêcznych kosztach rzêdu 2000–2500 z³otych ¿.d.d. dla wielu
chorych by³o za drogie i zmusza³o do stosowania niepe³no-
wartoœciowych p³ynnych diet kuchennych.
Wskazania
¯ywienie dojelitowe w warunkach domowych (¿.d.d.) jest
wskazane u chorych, którzy nie mog¹ w wystarczaj¹cym za-
kresie od¿ywiaæ siê drog¹ doustn¹, mo¿liwe jest natomiast
wykorzystanie dalszych odcinków przewodu pokarmowego.
S¹ to g³ównie chorzy z zaburzeniami po³ykania lub niedro¿-
noœci¹ w górnym odcinku przewodu pokarmowego, których
¿ywienie drog¹ przewodu pokarmowego jest mo¿liwe pod
warunkiem uzyskania dostêpu do sprawnego odcinka prze-
wodu pokarmowego. Wœród przyczyn dysfagii neurogennej
nale¿y wymieniæ: udary naczyniowe i urazy oœrodkowego uk³a-
du nerwowego, stwardnienie zanikowe boczne, miasteniê
i zespo³y miasteniczne, miopatie, polineuropatie, chorobê Par-
kinsona, chorobê Alzheimera i inne zespo³y otêpienne, stward-
nienie rozsiane, nowotwory i choroby infekcyjne, a u dzieci
mózgowe pora¿enie dzieciêce [5, 6, 11, 15, 29, 30]. Do czê-
stych wskazañ nale¿¹ choroby nowotworowe [29, 51]. Cho-
rzy na nowotwory s¹ szczególnie nara¿eni na niedo¿ywienie,
a jego przyczyny s¹ zwykle z³o¿one i spowodowane chorob¹,
leczeniem przeciwnowotworowym oraz anoreksj¹ [51]. ¯.d.d.
jest stosowane najczêœciej u chorych z nowotworami w górnym
odcinku przewodu pokarmowego, mechanicznie uniemo¿li-
wiaj¹cymi od¿ywianie u chorych zdyskwalifikowanych od le-
czenia onkologicznego (nowotwory jamy ustnej, krtani, prze-
³yku, ¿o³¹dka i trzustki) oraz w czasie radioterapii stosowanej
w leczeniu tych nowotworów, która powoduj¹c popromien-
ne uszkodzenie œluzówek przewodu pokarmowego utrudnia
lub uniemo¿liwia od¿ywianie [18, 51]. Coraz czêœciej ¿.d.d.
jest prowadzone w przebiegu leczenia nastêpstw ostrego za-
palenia trzustki, w leczeniu przewlek³ego zapalenia trzustki,
mukowiscydozy, chorób zapalnych jelit, zw³aszcza choroby Le-
œniowskiego-Crohna, w celu przygotowania do operacji oraz
leczenia powik³añ chirurgicznych, a nawet w przebiegu nie-
powœci¹gliwych wymiotów ciê¿arnych [2, 3, 9, 26, 43, 49,
56, 60, 61].
W wielu sytuacjach decyzja o rozpoczêciu ¿.d.d. jest prosta.
Jeœli jednak dotyczy chorego z otêpieniem starczym, zaawan-
sowanym nowotworem lub w stanie wegetatywnym, decy-
zja o rozpoczêciu ¿.d.d. powinna braæ pod uwagê tak¿e
wp³yw ¿.d.d. na jakoœæ ¿ycia pacjenta i byæ podjêta wspól-
nie z rodzin¹ i/lub opiekunem chorego. Jeœli decyzja o ¿.d.d.
zostanie podjêta, przed wypisem do domu nale¿y byæ pew-
nym czy pacjent lub jego opiekun zostali dostatecznie prze-
szkoleni w zakresie metod i mo¿liwych powik³añ ¿.d.d. oraz
czy zapewniono dostawê sprzêtu i leków [2].
Przeciwwskazania do ¿.d. to: niedro¿noœæ przewodu pokar-
mowego poni¿ej miejsca podawania diety, biegunki, wstrz¹s,
ciê¿ka niewydolnoœæ lub brak przewodu pokarmowego oraz
brak zgody chorego.

Nr 1/2006 Tom 1
7
¯ywienie dojelitowe w warunkach domowych
Podstaw¹ skutecznego ¿.d.d. jest uzyskanie odpowiedniego
dostêpu do przewodu pokarmowego, przeszkolenie chore-
go lub jego opiekuna oraz dobranie odpowiedniej do po-
trzeb chorego i celu leczenia diety [2].
Organizacja
Jak wynika z przegl¹du wskazañ, ¿.d.d. jest najczêœciej stoso-
wane u ciê¿ko chorych, którym nale¿y dostarczyæ do domu
odpowiednie preparaty i sprzêt do ich podawania. Kto mo¿e
to zrobiæ? Wydawaæ by siê mog³o, ¿e po zapewnieniu drogi
podawania i przeszkoleniu chorego lub jego opiekuna w szpitalu
najlepiej wykona to firma wyspecjalizowana w opiece domo-
wej lub firma zajmuj¹ca siê wy³¹cznie dostawami diet i sprzêtu.
Jednak tak nie jest – 47% chorych otrzymuje niew³aœciwe die-
ty lub nieodpowiedni sprzêt, a zainteresowanie chorym czêsto
ogranicza siê do potwierdzenia odbioru dostawy [25, 55]. Po-
niewa¿ opieka i nadzór medyczny nad chorym pozostawione
s¹ podstawowej opiece zdrowotnej, brak wiedzy i szkoleñ po-
woduj¹, ¿e zwykle pozostawia wiele do ¿yczenia. Wraz ze
wzrastaj¹c¹ liczb¹ chorych ¿.d.d. organizowano tak¿e
w oparciu o serwis organizowany przez firmy farmaceutyczne
produkuj¹ce diety przemys³owe [11]. Poniewa¿ pacjenci wy-
magaj¹cy ¿.d.d. to zwykle ciê¿ko chorzy, wymagaj¹cy poza
¿.d.d. tak¿e specjalistycznego leczenia, to oparcie ¿.d.d.
na prowadz¹cym leczenie specjalistycznym oddziale szpitalnym
ma tê zaletê, ¿e w przypadku wskazañ do rehospitalizacji jest
ona ³atwiejsza i chory znajduje siê szybko pod opiek¹ znaj¹ce-
go go zespo³u lecz¹cego.
W USA ¿.d.d. jest najczêœciej zapewniane przez firmy dostar-
czaj¹ce sprzêt medyczny. Nie zapewniaj¹ one ¿adnej opieki
medycznej [32]. W 2001 roku jedna z firm dostarcza³a zaopa-
trzenie dla 5486 chorych ¿.d.d., z których 36% stanowi³y dzieci.
Chorzy kompleksowo leczeni, np. z zapaleniem trzustki, lub
dzieci wymagaj¹ce stosowania diet specjalistycznych wyma-
gaj¹ dok³adnego monitorowania klinicznego i oceny medycz-
nej co 1–2 miesi¹ce. Poniewa¿ te konsultacje nie s¹ refinanso-
wane, opieka nad tymi chorymi jest niewystarczaj¹ca [31, 32].
Podobnie, opieka medyczna zapewniana przez firmy jest nie-
wystarczaj¹ca dla chorych w wieku podesz³ym [54].
W Wielkiej Brytanii, podobnie jak w USA, du¿¹ rolê
w prowadzeniu ¿.d.d. odgrywa pielêgniarka i dietetyk [1, 36].
Pielêgniarka pomaga w pierwszym okresie ¿.d.d., zwykle przez
tydzieñ, a potem okresowo odwiedza chorego. Dietetyk do-
biera i ew. modyfikuje program. W wyj¹tkowych przypadkach
chory mo¿e wymagaæ czêstszych wizyt pielêgniarek, wspó³-
praca lekarzy rodzinnych jest zwykle niedostateczna z powodu
braku wystarczaj¹cego przeszkolenia [36, 41], podobnie jak
i pielêgniarek œrodowiskowych, które wymagaj¹ znacznie bar-
dziej profesjonalnego szkolenia ni¿ obecnie [58].
Dostêp do przewodu pokarmowego
Dostêp do przewodu pokarmowego powinien umo¿liwiaæ
d³ugotrwa³e podawanie diet przy minimalnym obci¹¿eniu dla
pacjenta. Mo¿na wykorzystaæ jeden z piêciu sposobów uzy-
skania dostêpu do przewodu pokarmowego [13, 19]:
• zg³êbnikowanie przez nos z umieszczeniem wewnêtrzne-
go koñca zg³êbnika w ¿o³¹dku, dwunastnicy lub jelicie cien-
kim,
• wytworzenie przetoki od¿ywczej do ¿o³¹dka (gastrosto-
mia) lub pocz¹tkowego odcinka jelita cienkiego (jejuno-
stomia),
• chirurgicznie przez laparotomiê lub za pomoc¹ metod la-
paroskopowych,
• endoskopowo – za pomoc¹ endoskopu wprowadzanego
do przewodu pokarmowego,
• radiologicznie – poprzez nak³ucie pow³ok i ¿o³¹dka lub
jelita pod kontrol¹ rtg lub usg.
W ka¿dym przypadku konieczne jest uszczelnienie miejsca
wprowadzenia drenu do ¿o³¹dka lub jelita i umocowanie ich
do pow³ok. Jejunostomiê mo¿na wytworzyæ chirurgicznie,
laparoskopowo lub przez nak³ucie pod kontrol¹ rtg/usg. Cza-
sem permanentny dostêp do jelita cienkiego uzyskuje siê
wprowadzaj¹c zg³êbnik operacyjnie przez ¿o³¹dek (gastroje-
junostomia od¿ywcza). Zalet¹ tego dostêpu jest mo¿liwoœæ
za³o¿enia drenu o wiêkszej œrednicy, dobre uszczelnienie,
³atwoœæ wymiany i mo¿liwoœæ usuniêcia bez koniecznoœci
zamykania otworu w ¿o³¹dku. Podszycie œciany ¿o³¹dka do
pow³ok nie powoduje ryzyka zwê¿enia ani nie stanowi miej-
sca skrêcenia jelita wokó³ umocowania pêtli jelita do po-
w³ok. W przypadku wprowadzania endoskopowego, wytwa-
rza siê gastrostomiê, a nastêpnie wprowadza zg³êbnik przez
PEG do jelita (PEG/PEJ). PEJ (przezskórna endoskopowa jeju-
nostomia) jest rzadko mo¿liwa do wykonania [13].
Ka¿da z tych metod ma swoje zalety i wady; przed za³o¿e-
niem nale¿y przedyskutowaæ wybór metody z chorym i/lub
jego rodzin¹ lub opiekunem, bior¹c pod uwagê potrzeby
chorego, aktywnoœæ, czas leczenia, lepkoœæ i objêtoœæ poda-
wanej diety oraz sposób jej podawania.
Przyjmuje siê, ¿e jeœli czas ¿ywienia nie bêdzie d³u¿szy ni¿ 4–6
tygodni, dostêpem z wyboru jest zg³êbnik za³o¿ony przez
nos [2, 13]. Przeciwwskazaniem do wprowadzania zg³êbni-
ka przez nos s¹: zwê¿enia prze³yku uniemo¿liwiaj¹ce wpro-
wadzenie zg³êbnika, z³amanie nosa i krwawienie z nosa oraz
z³amanie podstawy czaszki. Wzglêdnym przeciwwskazaniem
jest obecnoœæ ¿ylaków prze³yku. W przypadku wyboru zg³êb-
nika zak³adanego przez nos nale¿y pamiêtaæ o tym, ¿e ³atwo
ulegaj¹ one usuniêciu lub przemieszczeniom, a jedyn¹ pewn¹
metod¹ potwierdzenia ich po³o¿enia jest badanie radiolo-
giczne z kontrastem. Zg³êbniki s¹ preferowan¹ drog¹ ¿ywie-
nia ma³ych dzieci oraz m³odych, aktywnych chorych, którzy
podaj¹ dietê w godzinach nocnych. Chorzy ci po odpowied-
nim przeszkoleniu sami wprowadzaj¹ sobie zg³êbnik przez
nos, a na dzieñ usuwaj¹ go.
Decyduj¹cym czynnikiem w wyborze miejsca karmienia jest
czynnoœæ ¿o³¹dka i zwi¹zane z nieprawid³owym opró¿nianiem
¿o³¹dka ryzyko zach³yœniêcia. Zaburzenia lub brak odruchu kasz-
lowego, zaburzenia œwiadomoœci, zach³yœniêcie w wywiadzie
oraz refluks ¿o³¹dkowo-prze³ykowy nakazuj¹ umieszczenie
koñca zg³êbnika poni¿ej odŸwiernika. W przypadku ¿.d.d. cho-
rych z przewlek³ym zapaleniem lub w okresie rekonwalescen-
cji po przebytym ostrym zapaleniu trzustki, koniec zg³êbnika
nale¿y umieœciæ w jelicie cienkim, i to im dalej, tym lepiej [56].
Jeœli od¿ywianie ma trwaæ d³u¿ej, zaleca siê wykonanie prze-
toki od¿ywczej. Przeciwwskazania do wytworzenia przetoki
od¿ywczej obejmuj¹: niedro¿noœæ przewodu pokarmowego
poni¿ej miejsca za³o¿enia przetoki, zaburzenia krzepniêcia
i wodobrzusze. Obecnie wiêkszoœæ gastrostomii zak³ada siê
endoskopowo; za³o¿enie chirurgiczne lub pod kontrol¹ rtg/usg
wybiera siê w przypadku niedro¿nego prze³yku, gdy nie
mo¿na wprowadziæ endoskopu.
Wiêkszoœæ zestawów PEG ma bardzo d³ug¹ czêœæ zewnêtrzn¹
(rurka d³ugoœci nawet 30–40 cm). Po za³o¿eniu PEG nale¿y tê
czêœæ skróciæ do 12–15 cm tak, aby mo¿na by³o bez problemu

Nr 1/2006 Tom 1
8
Postêpy ¯ywienia Klinicznego
za³o¿yæ opatrunek i umocowaæ PEG. W przeciwnym razie wy-
staj¹ca z cia³a 30 cm rurka staje siê utrapieniem dla chorego.
Po wygojeniu miejsce wyprowadzenia PEG powinno byæ
codziennie myte wod¹ z myd³em. Codziennie nale¿y braæ
prysznic, a po wygojeniu rany (7–10 dni) mo¿na siê k¹paæ.
Nale¿y codziennie obracaæ PEG i pierœcieñ mocuj¹cy, aby
unikn¹æ sta³ego ucisku na tkanki. Trzeba sprawdzaæ, czy nie
ma zbyt du¿ego ucisku pierœcienia na tkanki. Dla wygody
i lepszego samopoczucia chorego gastrostomia mo¿e byæ
wymieniona na tzw. niskoprofilow¹ gastrostomiê (n.g). N.g.
jest prawie niewidoczna, co zapewnia dobry efekt kosme-
tyczny, umo¿liwia pe³n¹ aktywnoœæ i zwykle mo¿e byæ utrzy-
mywana przez wiele miesiêcy bez koniecznoœci wymiany.
Podstaw¹ powodzenia n.g. jest dobranie rozmiaru i d³ugoœci
urz¹dzenia do szerokoœci i d³ugoœci kana³u ¿o³¹dkowo-skórne-
go za pomoc¹ specjalnej miarki. N.g. koñczy siê na poziomie
skóry i ma zastawkê uniemo¿liwiaj¹c¹ wyciek z ¿o³¹dka. Do-
stêpne s¹ dwa rodzaje n.g. – z nadmuchiwanym balonikiem
i grzybkiem w kszta³cie dysku lub rozgwiazdy. Jeœli wybieramy
tzw. zestaw z grzybkiem, wymiany mo¿na dokonaæ po 3 mie-
si¹cach od za³o¿enia gastrostomii, poniewa¿ urz¹dzenie zak³a-
da siê pod znacznym naciskiem, co mo¿e groziæ rozerwaniem
kana³u. W przypadku modelu z balonikiem wymiany mo¿na
dokonaæ po 3 tygodniach. N.g. jest trudna do wymiany, zw³asz-
cza w przypadku modelu z grzybkiem, i wymaga specjalnych
³¹czników do pod³¹czania zestawów do podawania diet, co
powoduje, ¿e n.g. i pos³ugiwanie siê nimi jest drogie.
Szkolenie chorego lub opiekuna
Przed rozpoczêciem ¿.d.d. chory lub jego opiekun musi byæ
przeszkolony w zakresie zasad i metod ¿ywienia dojelitowe-
go w domu oraz wykazaæ znajomoœæ i praktyczne opano-
wanie tych zasad. Szkolenie zwykle prowadzi siê w szpitalu
w okresie dobierania diety. Niektóre zespo³y prowadz¹ to
szkolenie w warunkach domowych.
Szkolenie w zakresie ¿ywienia dojelitowego w warunkach
domowych powinno obejmowaæ:
• pos³ugiwanie siê sprzêtem do ¿ywienia dojelitowego,
• zasady przechowywania i sprawdzania przydatnoœci do
u¿ycia diet i sprzêtu,
• aseptyczne przygotowywanie i podawanie mieszaniny
od¿ywczej,
• zasady podawania innych leków oraz wiadomoœci
o zgodnoœci z mieszanin¹ od¿ywcz¹,
• ustawianie i kontrolê szybkoœci wlewu mieszaniny od¿yw-
czej,
• zasady opieki nad zg³êbnikiem lub przetok¹ od¿ywcz¹,
• zasady pos³ugiwania siê pomp¹ infuzyjn¹ do ¿ywienia
dojelitowego,
• zasady oceny stanu pacjenta i monitorowania skuteczno-
œci leczenia,
• zasady zapobiegania, rozpoznawania i postêpowania
w przypadku wyst¹pienia powik³añ, zw³aszcza zagra¿aj¹-
cych ¿yciu lub uniemo¿liwiaj¹cych karmienie, jak wymio-
ty, zaciek wokó³ stomii, nudnoœci, zaparcie lub wzdêcie,
• zasady porozumiewania siê z lekarzem prowadz¹cym
i zespo³em leczenia ¿ywieniowego w domu,
• zasady od¿ywiania doustnego (jeœli mo¿liwe) i podawania
innych leków,
• zasady higieny osobistej, zw³aszcza higieny jamy ustnej [44].
Szkolenie powinno byæ prowadzone wg listy, a nabyte umie-
jêtnoœci potwierdzone egzaminem. Chory lub jego opiekun
powinien otrzymaæ odpowiednie materia³y szkoleniowe
w formie pisemnej. Nale¿y dokonywaæ okresowej kontroli
prawid³owoœci postêpowania chorego lub opiekuna
w zakresie leczenia ¿ywieniowego i w razie potrzeby prze-
prowadziæ ponowne szkolenie [1, 13, 44].
Istotne jest zmniejszenie ryzyka zaka¿enia; w przypadku cho-
rego od¿ywianego przez zg³êbnik konieczne jest zapewnie-
nie higieny jamy ustnej i jej sanacja, a nastêpnie codzienna
toaleta jamy ustnej i mycie zêbów [13]. Konieczna jest era-
dykacja wspó³istniej¹cego zaka¿enia grzybiczego.
Wypis do domu nastêpuje, gdy chory lub opiekun wyrazili
zgodê na leczenie i zostali przeszkoleni w zakresie przygoto-
wania i podawania diet, zasad podawania leków, utrzymy-
wania dro¿noœci zg³êbnika i pos³ugiwania siê pomp¹ oraz
po zapewnieniu dostaw leków i sprzêtu niezbêdnego do
¿.d.d., a tak¿e objêciu chorego programem nadzoru [13, 58].
Wybór diety
Wyboru diety zwykle dokonuje siê w szpitalu. Obowi¹zuje
zasada, ¿e wypis do domu nastêpuje po upewnieniu siê, ¿e
chory jest stabilny metabolicznie, podawana dieta zapewnia
odpowiedni¹ poda¿ wody i nie obserwuje siê zaburzeñ wod-
no-elektrolitowych.
Przed rozpoczêciem ¿.d. nale¿y wyrównaæ wspó³istniej¹ce nie-
dobory elektrolitów, a u chorych niedo¿ywionych tak¿e nie-
dobory witamin, przede wszystkim tiaminy, zwykle drog¹ do-
¿yln¹. Z uwagi na niebezpieczeñstwo zwi¹zane z niedoborami,
od pocz¹tku ¿ywienia nale¿y podawaæ wszystkie niezbêdne
witaminy i pierwiastki œladowe. Dotyczy to zw³aszcza cho-
rych w wieku podesz³ym. O ile zapotrzebowanie na bia³ko
i energiê okreœla siê na podstawie oceny ¿ywieniowej i celu
leczenia, to o rodzaju stosowanej diety decyduje czynnoϾ prze-
wodu pokarmowego oraz zdolnoœæ trawienia i wch³aniania.
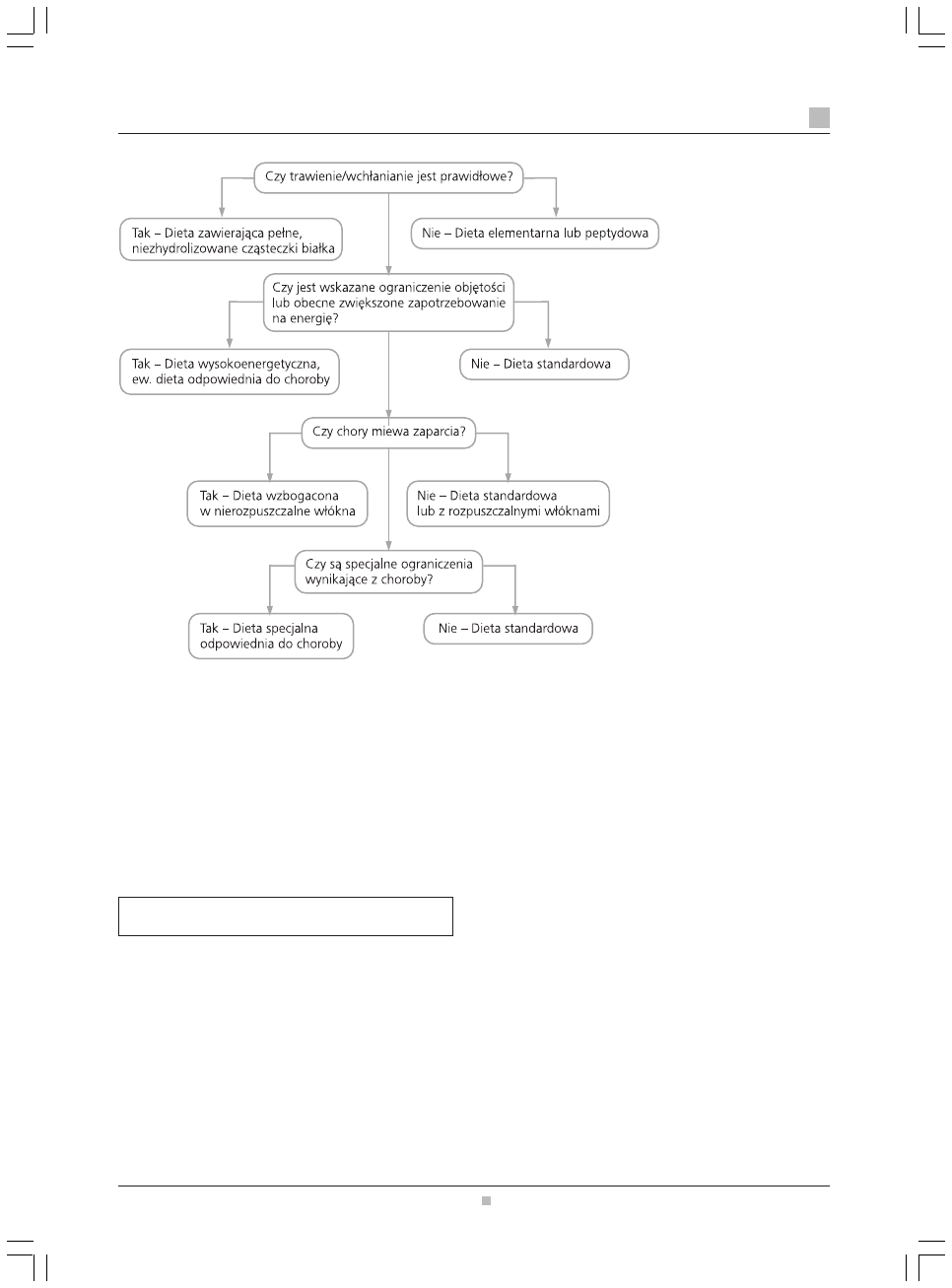
Algorytm wyboru diety przedstawia rycina 1.
W czasie ¿.d.d. najczêœciej stosuje siê diety standardowe lub
wzbogacone w resztki, a czêsto naprzemiennie jedne i drugie.
Diety wzbogacone w resztki stosuje siê u chorych ze sk³on-
noœci¹ do biegunek i u chorych z tendencj¹ do zaparæ. Z jednej
strony, absorbuj¹ one nadmiar wody w jelicie cienkim,
z drugiej – w jelicie grubym zwiêkszaj¹ objêtoœæ stolca. Roz-
puszczalne w³ókna u³atwiaj¹ kontrolê glikemii i lipidemii,
a fermentuj¹c do krótko³añcuchowych kwasów t³uszczowych
dostarczaj¹ pokarm dla komórek nab³onka jelita grubego.
U chorych z zaburzeniami trawienia/wch³aniania stosuje siê
diety peptydowe. Zawieraj¹ one mieszaninê t³uszczu MCT
i niewielk¹ dawkê t³uszczu LCT w celu pokrycia zapotrzebo-
wania na niezbêdne kwasy t³uszczowe oraz oligosacharydy
lub maltodekstryny. U chorych z niewydolnoœci¹ nerek mo¿e
byæ wskazane zastosowanie jednej z diet nerkowych. Rów-
nie¿ u chorych z niewydolnoœci¹ w¹troby lub chorobami p³uc
mo¿e byæ wskazane zastosowanie odpowiedniej diety.
Od¿ywianie dojelitowe chorych na cukrzycê wymaga poda-
¿y odpowiedniej do zapotrzebowania diety oraz równole-
g³ego podawania doustnych leków przeciwcukrzycowych lub
insuliny w taki sposób, aby wartoœci glikemii nie przekracza-
³y 150 mg/%, nie by³o glikozurii, kwasicy ketonowej oraz
napadów hipoglikemii. Cel ten u³atwia zastosowanie diety
bogatoresztkowej, zapewniaj¹cej dobow¹ poda¿ 30 g resz-
tek, przy jednoczesnym usuniêciu z diety szybko wch³aniaj¹-
cych siê wêglowodanów, do których zalicza siê dwu-, oli-
go- i polisacharydy. U chorych na nowotwory nale¿y rozwa¿yæ
wskazania do zastosowania diety wzbogaconej w omega-3
kwasy t³uszczowe lub dodanie suplementu omega-3 kwa-
sów t³uszczowych do diety standardowej.
Nr 1/2006 Tom 1
9
Zwykle diety bezsmakowe s¹ izotoniczne (300 mOsm/kg
wody); diety o wy¿szej osmolarnoœci mog¹ przy podawaniu
do jelita powodowaæ wydzielanie wody do œwiat³a przewo-
du pokarmowego i powodowaæ biegunkê.
W czasie ¿.d.d. podstawowe znaczenie ma zapewnienie
odpowiedniej poda¿y wody [23]. Nale¿y równie¿ uwzglêd-
niæ straty drogami nienaturalnymi oraz koniecznoœæ wydale-
nia produktów przemiany bia³ka.
Podstawowe zapotrzebowanie na wodê doros³ych okreœla
siê wg wzoru:
Podstawowe zapotrzebowanie na wodê =10
× 100 ml +
+10
× 50 ml + (masa cia³a – 20) × 20 ml
Wiêkszoœæ diet o standardowym stê¿eniu 1 kcal/ml zawiera
80% wody, a diety zagêszczone zaledwie 65–70%; oznacza
to, ¿e chory otrzymuj¹cy 1500 kcal otrzyma oko³o 1200 ml
wody. Chory o masie 60 kg wymaga wiêc dodatkowo oko³o
1000–1300 ml wody ka¿dego dnia, a chory z dodatkowymi
stratami (np. biegunka, poty, leki moczopêdne) jeszcze wiê-
cej [2]. W przeciwnym razie odwodnienie bêdzie przyczyn¹
rehospitalizacji, ciê¿kich powik³añ lub nawet œmierci chore-
go. Jeœli ¿ywienie jest podawane do gastrostomii, uzupe³nie-
nie dodatkowej poda¿y wody jest ³atwe; mo¿na dodaæ wodê
do diety lub podawaæ j¹ osobno w dawkach podzielonych
w ci¹gu dnia, wykorzystuj¹c p³yny obojêtne lub herbatê. Je-
œli jednak dieta jest podawana do jejunostomii, podanie sa-
mej wody do jejunostomii mo¿e byæ powodem biegunki lub
Rycina 1.
Algorytm wyboru diety do ¿ywienia dojelitowego
nawet perforacji jelita [50]. Dlatego najbezpieczniej jest do-
daæ wodê do mieszaniny od¿ywczej, unikaj¹c nadmiernego
rozcieñczenia diety lub – co jest trudniejsze – u¿ywaæ izoto-
nicznego p³ynu podawanego po zakoñczeniu wlewu,
np. mieszaniny glukozy z sol¹ fizjologiczn¹. Dodanie wody
do diety w butelce lub w pojemniku jest trudne i dlatego
najchêtniej u¿ywamy pojemników, do których przelewa siê
dietê przed podaniem i do których dodaje siê odpowiedni¹
dawkê wody.
Podawanie diet
Teoretycznie, naj³atwiej i najbezpieczniej stosowaæ diety go-
towe, dostarczane w 500 ml pojemnikach. Do ¿o³¹dka dietê
podajemy w bolusach, a przy podawaniu do dwunastnicy
lub jelita – zawsze we wlewie. W warunkach szpitalnych przy
podawaniu diety do ¿o³¹dka zwykle stopniowo zwiêkszamy
objêtoœæ diety podawanej w stê¿eniu 1 kcal/ml. Zalecan¹ me-
tod¹ rozpoczynania podawania diety do dwunastnicy lub je-
lita jest stopniowe zwiêkszanie najpierw objêtoœci, a nastêpnie
stê¿enia diety. Rozpoczynaj¹c podawanie diety od stê¿e-
nia 0,5–0,75 kcal/ml, podajemy j¹ z szybkoœci¹ 10–15 ml/h
i zwiêkszamy tempo podawania diety co 12–24 godziny
o 25 ml/h. Po osi¹gniêciu szybkoœci podawania 100 ml/h,
przy dobrej tolerancji przez chorego, zwiêkszamy stê¿enie
diety o 0,25 kcal/ml co 12–24 h. Czêstoœæ wystêpowania
objawów niepo¿¹danych zmniejsza ci¹g³y równomierny wlew
sterowany pomp¹ perystaltyczn¹.
¯ywienie dojelitowe w warunkach domowych
Nr 1/2006 Tom 1
10
Postêpy ¯ywienia Klinicznego
Stopniowe zwiêkszanie szybkoœci podawania i stê¿enia die-
ty nie jest potrzebne, jeœli okres g³odzenia nie przekracza
kilku dni. Korzystne jest ¿ywienie z 5–6-godzinn¹ przerw¹,
a przy ¿ywieniu do¿o³¹dkowym podawanie diety w porcjach
po 250 ml w ci¹gu 10–15 minut lub po 500 ml w ci¹gu 15–
–30 minut z 2–4-godzinn¹ przerw¹.
Przy ¿ywieniu do ¿o³¹dka w domu i osi¹gniêciu porcji doce-
lowej mo¿liwe jest podawanie diety strzykawkami Janette´a
o objêtoœci 100–150 ml. Jest to naj³atwiejsza forma karmie-
nia, ale chory musi byæ przyzwyczajony do dawek 300–500
ml/porcjê. Zaleca siê podawanie diety w dzieñ, a nie w nocy.
Podobnie, u wielu z tych chorych wystarczy grawitacyjne
podawanie diety. U¿ycie pompy jest konieczne u chorych
z jejunostomi¹ od¿ywcz¹, cukrzyc¹ i zaburzeniami wch³a-
niania [2].
W celu utrzymania dro¿noœci zg³êbnika nale¿y przep³ukiwaæ
go przed ka¿d¹ przerw¹ lub przy ¿ywieniu ci¹g³ym co naj-
mniej 2–4 razy na dobê sol¹ fizjologiczn¹ lub ja³ow¹ wod¹
do przep³ukiwania. Do przep³ukiwania gastrostomii mo¿na
u¿ywaæ herbaty lub przegotowanej wody; do przep³ukiwa-
nia jejunostomii nale¿y u¿ywaæ wy³¹cznie sterylnej wody lub
roztworu soli fizjologicznej. Uniesienie górnej po³owy cia³a
o 20–30% zmniejsza ryzyko aspiracji.
Zaleca siê rutynowe monitorowanie zalegania w ¿o³¹dku.
Program kontroli zalegania w ¿o³¹dku
1. Podaæ do ¿o³¹dka 200–400 ml wody lub 0,9% NaCl.
2. Zatkaæ zg³êbnik na dwie godziny.
3. Po 2 h pod³¹czyæ zg³êbnik do pojemnika.
4. Odzyskanie ponad po³owy podanej objêtoœci oznacza
z³e opró¿nianie ¿o³¹dka – nale¿y rozwa¿yæ modyfika-
cjê sposobu podawania.
5. Zaleca siê powtarzaæ przed ka¿dym podaniem nowej
porcji lub raz na dobê.
Aby unikn¹æ przypadkowego usuniêcia, nale¿y okresowo
kontrolowaæ mocowanie zg³êbnika do skóry lub nosa.
Sprawdzenie po³o¿enia koñca zg³êbnika obowi¹zuje po
wprowadzeniu i przy podejrzeniu przemieszczenia. Najdo-
k³adniejsze jest badanie radiologiczne, czasem wystarczy
os³uchiwanie w czasie insuflacji powietrza lub aspiracja
strzykawk¹. Zaleca siê wdro¿enie programu kontroli po³o-
¿enia zg³êbnika.
Program kontroli po³o¿enia zg³êbnika
1. Zaznaczyæ miejsce wyprowadzenia z nosa.
2. Kontrolowaæ po³o¿enia znacznika co 8 godzin.
3. Zagl¹daæ do gard³a
– przy wlewie ci¹g³ym co 8 godzin,
– przy podawaniu w bolusie – przed nastêpn¹ porcj¹.
Przy podejrzeniu przemieszczenia koniecznie kontrolowaæ
po³o¿enia pod rtg.
Podawanie leków
Podawanie leków stanowi problem, zw³aszcza w czasie ¿.d.d.
[2, 6, 13]. Nie ma zarejestrowanych leków przeznaczonych
do podawania przez zg³êbnik ani z ¿.d. Teoretycznie mo¿na
podawaæ leki w p³ynie; przy podaniu do jelita mog¹ byæ one
przyczyn¹ biegunki, kolki, a nawet wymiotów. W przypadku
w¹tpliwoœci nale¿y zasiêgn¹æ porady farmaceuty. Najczêœciej
rozciera siê leki w moŸdzierzu, rozpuszcza w wodzie i po
wymieszaniu podaje przez zg³êbnik.
Obowi¹zuje zasada niepodawania leków z diet¹. Przed po-
daniem leku nale¿y przerwaæ podawanie diety, przep³ukaæ
zg³êbnik, podaæ lek, ponownie przep³ukaæ zg³êbnik
i rozpocz¹æ podawanie diety [2].
Monitorowanie
Monitorowanie jest konieczne, zw³aszcza w pocz¹tkowym
okresie leczenia. Jeœli chorego mo¿na zwa¿yæ, nale¿y moni-
torowaæ masê cia³a oraz diurezê i liczbê wypró¿nieñ. Zwy-
kle w pocz¹tkowym okresie ¿.d.d. badania biochemiczne wy-
konuje siê raz na miesi¹c, a potem co 2–3 miesi¹ce.
Chorzy nieprzytomni lub unieruchomieni wymagaj¹ trans-
portu do szpitala lub regularnych wizyt domowych. Nale¿y
ustaliæ sposób kontaktu z zespo³em lecz¹cym. Monitoro-
wanie po³o¿enia zg³êbnika obejmuje pomiar d³ugoœci zg³êb-
nika od nozdrzy do koñca zewnêtrznego, a przetoki od¿yw-
czej pomiar d³ugoœci drenu wyprowadzonego ponad
pow³oki. Zaleca siê prowadzenie karty nadzoru wg poni¿-
szego wzoru na s. 11.
Problemy zg³aszane przez chorych leczonych
¿ywieniem dojelitowym w warunkach domowych
Chorzy ¿.d.d. zg³aszaj¹ wiele problemów [23, 35]. Do naj-
czêstszych nale¿y zatykanie siê zg³êbnika. Ci, którzy sami
zak³adaj¹ zg³êbnik, skar¿¹ siê na problemy z zak³adaniem
zg³êbnika i podra¿nienie nosa. Do czêstych problemów nale¿¹
zapalenie i podra¿nienie skóry wokó³ przetoki od¿ywczej,
zaciek lub wyciek oraz problemy z ubraniem i wygl¹dem,
gdy przetokê widaæ spod koszulki. Do czêstych nale¿¹ skargi
na bezsennoœæ i trudnoœci z zasypianiem oraz z uprawianiem
seksu, w czym, choæ w ró¿ny sposób, przeszkadza i zg³êbnik
w nosie i przetoka od¿ywcza [23, 35]. Biegunki utrudniaj¹
wyjœcie z domu. Trzeba wyt³umaczyæ chorym, jaka jest przy-
czyna problemu i jak go unikn¹æ. Dobrze jest dopasowaæ
codzienny plan ¿ywienia do programu dnia. Zamiast ko-
szulki zaleca siê noszenie szerokiego pasa, który ukrywa
przetokê od¿ywcz¹ [13, 35]. Odpowiednie mocowanie
zg³êbnika zmniejsza ryzyko usuniêcia [13]. Problemem, któ-
ry trudno zwalczyæ, jest niemo¿noœæ jedzenia, zw³aszcza
u m³odszych chorych z dysfagi¹, oraz uczucie uzale¿nienia
od pompy [2].
Tabela 1.
Sposób i miejsce podawania diet
Sposób podawania
Miejsce podawania
Rozpoczynanie od¿ywiania
Dawkowanie docelowe
Bolus
¯o³¹dek
6
× 50 ml/24 h
6–8
× 300–500 ml/24 h
Ci¹g³y wlew
Dwunastnica lub jelito
10–15 ml/h
120–350 ml/h
Nr 1/2006 Tom 1
10
Postêpy ¯ywienia Klinicznego
Stopniowe zwiêkszanie szybkoœci podawania i stê¿enia die-
ty nie jest potrzebne, jeœli okres g³odzenia nie przekracza
kilku dni. Korzystne jest ¿ywienie z 5–6-godzinn¹ przerw¹,
a przy ¿ywieniu do¿o³¹dkowym podawanie diety w porcjach
po 250 ml w ci¹gu 10–15 minut lub po 500 ml w ci¹gu 15–
–30 minut z 2–4-godzinn¹ przerw¹.
Przy ¿ywieniu do ¿o³¹dka w domu i osi¹gniêciu porcji doce-
lowej mo¿liwe jest podawanie diety strzykawkami Janette´a
o objêtoœci 100–150 ml. Jest to naj³atwiejsza forma karmie-
nia, ale chory musi byæ przyzwyczajony do dawek 300–500
ml/porcjê. Zaleca siê podawanie diety w dzieñ, a nie w nocy.
Podobnie, u wielu z tych chorych wystarczy grawitacyjne
podawanie diety. U¿ycie pompy jest konieczne u chorych
z jejunostomi¹ od¿ywcz¹, cukrzyc¹ i zaburzeniami wch³a-
niania [2].
W celu utrzymania dro¿noœci zg³êbnika nale¿y przep³ukiwaæ
go przed ka¿d¹ przerw¹ lub przy ¿ywieniu ci¹g³ym co naj-
mniej 2–4 razy na dobê sol¹ fizjologiczn¹ lub ja³ow¹ wod¹
do przep³ukiwania. Do przep³ukiwania gastrostomii mo¿na
u¿ywaæ herbaty lub przegotowanej wody; do przep³ukiwa-
nia jejunostomii nale¿y u¿ywaæ wy³¹cznie sterylnej wody lub
roztworu soli fizjologicznej. Uniesienie górnej po³owy cia³a
o 20–30% zmniejsza ryzyko aspiracji.
Zaleca siê rutynowe monitorowanie zalegania w ¿o³¹dku.
Program kontroli zalegania w ¿o³¹dku
1. Podaæ do ¿o³¹dka 200–400 ml wody lub 0,9% NaCl.
2. Zatkaæ zg³êbnik na dwie godziny.
3. Po 2 h pod³¹czyæ zg³êbnik do pojemnika.
4. Odzyskanie ponad po³owy podanej objêtoœci oznacza
z³e opró¿nianie ¿o³¹dka – nale¿y rozwa¿yæ modyfika-
cjê sposobu podawania.
5. Zaleca siê powtarzaæ przed ka¿dym podaniem nowej
porcji lub raz na dobê.
Aby unikn¹æ przypadkowego usuniêcia, nale¿y okresowo
kontrolowaæ mocowanie zg³êbnika do skóry lub nosa.
Sprawdzenie po³o¿enia koñca zg³êbnika obowi¹zuje po
wprowadzeniu i przy podejrzeniu przemieszczenia. Najdo-
k³adniejsze jest badanie radiologiczne, czasem wystarczy
os³uchiwanie w czasie insuflacji powietrza lub aspiracja
strzykawk¹. Zaleca siê wdro¿enie programu kontroli po³o-
¿enia zg³êbnika.
Program kontroli po³o¿enia zg³êbnika
1. Zaznaczyæ miejsce wyprowadzenia z nosa.
2. Kontrolowaæ po³o¿enia znacznika co 8 godzin.
3. Zagl¹daæ do gard³a
– przy wlewie ci¹g³ym co 8 godzin,
– przy podawaniu w bolusie – przed nastêpn¹ porcj¹.
Przy podejrzeniu przemieszczenia koniecznie kontrolowaæ
po³o¿enia pod rtg.
Podawanie leków
Podawanie leków stanowi problem, zw³aszcza w czasie ¿.d.d.
[2, 6, 13]. Nie ma zarejestrowanych leków przeznaczonych
do podawania przez zg³êbnik ani z ¿.d. Teoretycznie mo¿na
podawaæ leki w p³ynie; przy podaniu do jelita mog¹ byæ one
przyczyn¹ biegunki, kolki, a nawet wymiotów. W przypadku
w¹tpliwoœci nale¿y zasiêgn¹æ porady farmaceuty. Najczêœciej
rozciera siê leki w moŸdzierzu, rozpuszcza w wodzie i po
wymieszaniu podaje przez zg³êbnik.
Obowi¹zuje zasada niepodawania leków z diet¹. Przed po-
daniem leku nale¿y przerwaæ podawanie diety, przep³ukaæ
zg³êbnik, podaæ lek, ponownie przep³ukaæ zg³êbnik
i rozpocz¹æ podawanie diety [2].
Monitorowanie
Monitorowanie jest konieczne, zw³aszcza w pocz¹tkowym
okresie leczenia. Jeœli chorego mo¿na zwa¿yæ, nale¿y moni-
torowaæ masê cia³a oraz diurezê i liczbê wypró¿nieñ. Zwy-
kle w pocz¹tkowym okresie ¿.d.d. badania biochemiczne wy-
konuje siê raz na miesi¹c, a potem co 2–3 miesi¹ce.
Chorzy nieprzytomni lub unieruchomieni wymagaj¹ trans-
portu do szpitala lub regularnych wizyt domowych. Nale¿y
ustaliæ sposób kontaktu z zespo³em lecz¹cym. Monitoro-
wanie po³o¿enia zg³êbnika obejmuje pomiar d³ugoœci zg³êb-
nika od nozdrzy do koñca zewnêtrznego, a przetoki od¿yw-
czej pomiar d³ugoœci drenu wyprowadzonego ponad
pow³oki. Zaleca siê prowadzenie karty nadzoru wg poni¿-
szego wzoru na s. 11.
Problemy zg³aszane przez chorych leczonych
¿ywieniem dojelitowym w warunkach domowych
Chorzy ¿.d.d. zg³aszaj¹ wiele problemów [23, 35]. Do naj-
czêstszych nale¿y zatykanie siê zg³êbnika. Ci, którzy sami
zak³adaj¹ zg³êbnik, skar¿¹ siê na problemy z zak³adaniem
zg³êbnika i podra¿nienie nosa. Do czêstych problemów nale¿¹
zapalenie i podra¿nienie skóry wokó³ przetoki od¿ywczej,
zaciek lub wyciek oraz problemy z ubraniem i wygl¹dem,
gdy przetokê widaæ spod koszulki. Do czêstych nale¿¹ skargi
na bezsennoœæ i trudnoœci z zasypianiem oraz z uprawianiem
seksu, w czym, choæ w ró¿ny sposób, przeszkadza i zg³êbnik
w nosie i przetoka od¿ywcza [23, 35]. Biegunki utrudniaj¹
wyjœcie z domu. Trzeba wyt³umaczyæ chorym, jaka jest przy-
czyna problemu i jak go unikn¹æ. Dobrze jest dopasowaæ
codzienny plan ¿ywienia do programu dnia. Zamiast ko-
szulki zaleca siê noszenie szerokiego pasa, który ukrywa
przetokê od¿ywcz¹ [13, 35]. Odpowiednie mocowanie
zg³êbnika zmniejsza ryzyko usuniêcia [13]. Problemem, któ-
ry trudno zwalczyæ, jest niemo¿noœæ jedzenia, zw³aszcza
u m³odszych chorych z dysfagi¹, oraz uczucie uzale¿nienia
od pompy [2].
Tabela 1.
Sposób i miejsce podawania diet
Sposób podawania
Miejsce podawania
Rozpoczynanie od¿ywiania
Dawkowanie docelowe
Bolus
¯o³¹dek
6
× 50 ml/24 h
6–8
× 300–500 ml/24 h
Ci¹g³y wlew
Dwunastnica lub jelito
10–15 ml/h
120–350 ml/h

Nr 1/2006 Tom 1
11
Powik³ania ¿ywienia dojelitowego w warunkach
domowych
Powik³ania ¿ywienia dojelitowego dzielimy na techniczne,
metaboliczne, pokarmowe i septyczne. W czasie ¿.d.d. naj-
czêstsze powik³ania to powik³ania pokarmowe (0,16/chore-
go) i mechaniczne (0,15/chorego). Wed³ug innych autorów,
najczêœciej dochodzi do zatkania zg³êbnika (44,5%), powi-
k³añ pokarmowych (30,5%) i innych powik³añ mechanicz-
nych (21,7%); najrzadziej wystêpuj¹ powik³ania metabolicz-
ne (3,3%) [15]. Z powodu powik³añ ¿.d.d. zmar³o oko³o 3%
chorych [2, 14].
Do typowych powik³añ technicznych zwi¹zanych ze zg³êbni-
kiem nale¿¹: wypadniêcie, zatkanie lub przemieszczenie zg³êb-
nika. U chorych z zaburzeniami po³ykania i odkrztuszania
mo¿e dojœæ do przemieszczenia zg³êbnika do tchawicy lub
oskrzeli ju¿ w czasie wprowadzania, a u wszystkich w ka¿dym
momencie od¿ywiania. Nierozpoznane przemieszczenie
zg³êbnika grozi powik³aniami – zach³yœniêciem i zapaleniem
p³uc. Chory lub jego opiekun powinien byæ przeszkolony,
jak unikaæ i jak rozpoznawaæ przemieszczenie zg³êbnika.
Powinien równie¿ znaæ sytuacje, w których czêsto dochodzi
do przemieszczenia wewnêtrznego koñca zg³êbnika (kaszel,
wymioty, nag³e szarpniêcie czy poci¹gniêcie za zg³êbnik).
Jeœli wynik os³uchiwania nadbrzusza w czasie insuflacji po-
wietrza jest w¹tpliwy, a próba aspiracji nieudana, konieczna
jest radiologiczna kontrola po³o¿enia koñca zg³êbnika przed
rozpoczêciem karmienia, zw³aszcza u chorych o du¿ym ry-
zyku zach³yœniêcia. Ryzyko zach³yœniêcia mo¿na zmniejszyæ,
unosz¹c górn¹ czêœæ ³ó¿ka, o 30%. Nie nale¿y jednak umiesz-
czaæ chorego w pozycji siedz¹cej lub podk³adaæ poduszki,
która wygina chorego. Taki manewr zwiêksza ciœnienie we-
wn¹trzbrzuszne i mo¿e nasilaæ zarzucanie diety do prze³yku.
W czasie d³ugotrwa³ego ¿.d.d. czêste (56%) s¹ powik³ania
wynikaj¹ce ze zu¿ycia sprzêtu – pêkniêcie koñcówek zg³êb-
ników lub przetok [2, 14]. Pêkniêciu najczêœciej ulega miej-
sce po³¹czenia zestawu do diety z koñcem zg³êbnika lub prze-
toki. O ile zapasowe koñcówki i ³¹czniki s¹ dostêpne w innych
krajach, w Polsce ich brak i czêsto konieczna jest wymiana
zg³êbnika.
Czêste i trudne do leczenia s¹ zatkania zg³êbników i przetok
od¿ywczych [2]. Zapobieganie zatkaniu polega na okreso-
wym przep³ukiwaniu zg³êbnika lub przetoki i u¿ywaniu strzy-
kawek o objêtoœci co najmniej 50 ml. Najczêstsz¹ przyczyn¹
zatkania jest niestaranne przep³ukiwanie zg³êbnika lub za-
pominanie o tej czynnoœci, podawanie zbyt gêstej diety, po-
dawanie leków oraz próby podawania zmiksowanych po-
karmów naturalnych.
Do odetkania zatkanego zg³êbnika u¿ywa siê ciep³ej wody,
coca-coli, mieszaniny dwuwêglanów z pankreatyn¹ oraz cie-
p³ego alkoholu 70% [2].
Najczêstszym powik³aniem przetok od¿ywczych jest zaka¿enie
wokó³ przetoki [41]. Miejsce wokó³ przetoki powinno byæ sta-
rannie myte i odka¿ane; po zagojeniu rany lepiej nie u¿ywaæ
opatrunków. Zewnêtrzna p³ytka uszczelniaj¹ca powinna byæ
dociœniêta nie za mocno, aby unikn¹æ martwicy, i nie za s³abo,
gdy¿ zbyt luŸna przetoka jest powodem zacieku treœci pokar-
mowej, pieczenia i zaka¿enia wokó³ przetoki. W przypadku
utrzymuj¹cego siê wycieku, konieczne jest odpowiednie lecze-
nie miejscowe i stosowanie opatrunków adsorbuj¹cych p³yn.
Nie zaleca siê stosowania maœci i kremów. Czasem w miejscu
wprowadzenia pojawia siê ziarnina; mo¿e byæ konieczne jej
usuniêcie chirurgiczne lub przypalenie azotanem srebra.
Przypadkowe usuniêcie przetoki od¿ywczej mo¿e groziæ za-
paleniem otrzewnej lub zaciekiem i zaka¿eniem pow³ok
¯ywienie dojelitowe w warunkach domowych
Karta nadzoru chorego leczonego ¿.d.d.
Poniedzia³ek
Wtorek
Œroda
Czwartek
Pi¹tek
Sobota
Niedziela
Data
Masa cia³a (kg)
Poda¿ diety (ml)
Poda¿ wody (ml)
Liczba wypró¿nieñ
Diureza (ml) lub liczba mikcji
Wymioty (tak/nie)
Podawane leki
1.
2.
3.
4.
AktywnoϾ
Inne spostrze¿enia
Kontrola zalegania
Dro¿noœæ zg³êbnika/stomii
Szczelnoœæ po³¹czeñ
Mocowanie zg³êbnika/stomii
Po³o¿enie zg³êbnika/stomii
Nr 1/2006 Tom 1
12
Postêpy ¯ywienia Klinicznego
wokó³ kana³u przetoki, zw³aszcza gdy usuniêto przetokê
za³o¿on¹ niedawno. Dlatego konieczne jest pewne moco-
wanie i czêsta kontrola.
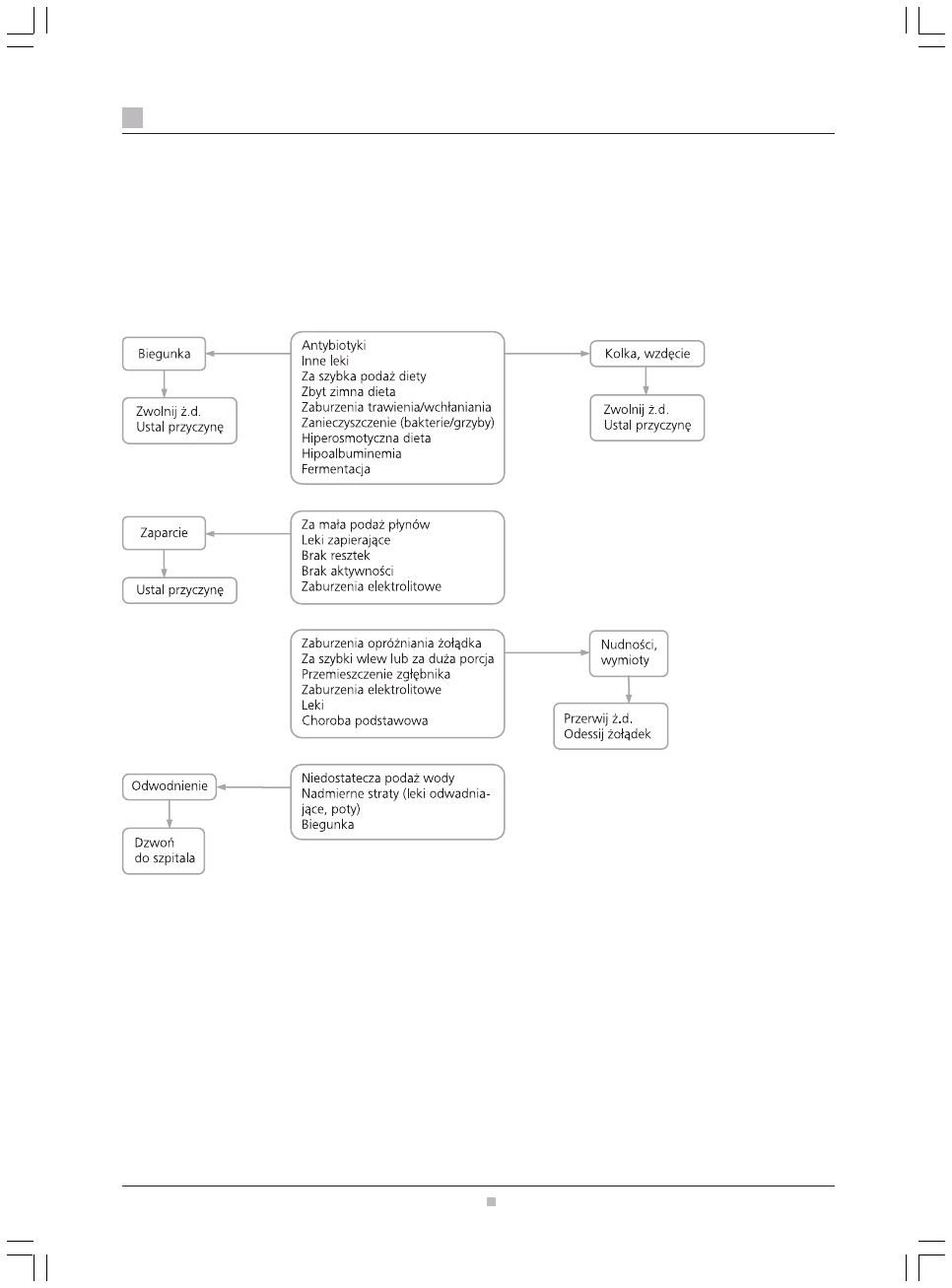
Do powik³añ pokarmowych zwi¹zanych z podawaniem die-
ty nale¿¹: biegunka, kolka, wzdêcie, nudnoœci i wymioty,
a w przypadku nieprzestrzegania wskazañ do podawania
poni¿ej odŸwiernika – zach³yœniêcie.
Najczêstszym powik³aniem jest biegunka, której przyczyn¹
mo¿e byæ zbyt szybkie podawanie lub za wysokie stê¿enie
diety, niedobór laktazy, zaka¿enie diety lub zestawu do po-
dawania, niska temperatura diety, brak resztek, zaburzenia
trawienia lub wch³aniania bia³ka lub t³uszczów, podawane
leki, przemieszczenie zg³êbnika i hipoalbuminemia. Lecze-
nie biegunki polega na ustaleniu i usuniêciu przyczyny, po-
daniu leków zwiêkszaj¹cych wch³anianie lub zmniejszaj¹cych
wydzielanie, a jeœli to nie pomaga, zmniejszenie lub prze-
rwanie ¿ywienia dojelitowego i czasowe przejœcie na ¿ywie-
nie pozajelitowe. Powodem zaparæ mo¿e byæ brak resztek
w diecie lub niedobór p³ynów.
Z powik³añ metabolicznych najczêœciej wystêpuj¹ hiperka-
liemia, hipofosfatemia, hiperglikemia i hipomagnezemia [40].
Uporczywe biegunki lub za ma³a poda¿ wody mog¹ byæ
powodem odwodnienia.
Rycina 2.
Przyczyny powik³añ pokarmowych ¿ywienia dojelitowego i zasady postêpowania
Powik³ania septyczne mog¹ byæ spowodowane zaka¿eniem
diety lub kolonizacj¹ przewodu pokarmowego i górnych dróg
oddechowych [4, 8, 34].
•
ród³em zaka¿enia diety mog¹ byæ
jej sk³adniki, otoczenie, sprzêt stosowany do przygotowa-
nia i mieszania diet, przenoszenie diety do pojemnika, nie-
w³aœciwe przechowywanie, personel, sprzêt do podawania
i zg³êbniki oraz sam chory [4, 34]. Wsteczna migracja bakterii
z jelita do pojemnika z diet¹ i namno¿enie siê tych bakterii
w diecie, a nastêpnie powrót w krytycznej iloœci do jelita
mo¿e byæ powodem ciê¿kiego ogólnoustrojowego zaka¿enia.
Migracji zapobiega komora kroplowa w zestawie do podawa-
nia diet. Zaka¿eniu z zewn¹trz zapobiega stosowanie p³ynnych
diet w gotowych pojemnikach i wymiana zestawów do poda-
wania co 24 godziny. Otwarte pojemniki mo¿na przechowy-
waæ do 24 godzin w lodówce. Ryzyko zaka¿enia zmniejsza
mycie zêbów i p³ukanie jamy ustnej, a u chorych od¿ywianych
przez zg³êbnik codzienne czyszczenie otworów nosowych [42].
Nale¿y pamiêtaæ, ¿e wszystkie czynnoœci zwi¹zane z ¿.d.d. na-
le¿y wykonywaæ w sposób aseptyczny; w przypadku od¿ywia-
nia przez jejunostomiê lub podawania diety do jelita obowi¹-
zuj¹ takie same zasady, jak przy dostêpie ¿ylnym [2, 13, 42].
Ocenia siê, ¿e 11% chorych z powik³aniami wymaga rehospi-
talizacji, 30–45% mo¿na leczyæ ambulatoryjnie, a w 50–69%
przypadków wystarczy porada telefoniczna [14].
,
Z

Nr 1/2006 Tom 1
13
Wyniki ¿ywienia dojelitowego w warunkach
domowych a jakoœæ ¿ycia
Chorzy, którzy nie mog¹ siê od¿ywiaæ drog¹ doustn¹,
a u których mo¿na wykorzystaæ do karmienia ni¿ej po³o¿one
odcinki przewodu pokarmowego, cierpi¹ na ró¿ne choroby
podstawowe. Brak mo¿liwoœci od¿ywiania jest najczêœciej
jednym z objawów choroby. Wœród dzieci dominuj¹ pacjen-
ci z nienowotworowymi chorobami przewodu pokarmowe-
go i z tego powodu wyniki ¿.d.d. i jakoœæ ¿ycia jest dobra
[39]. Pierwszy rok ¿.d.d. prze¿ywa prawie 95% dzieci [15,
20]. U ponad po³owy po 1–3 latach leczenia powraca zdol-
noœæ do ¿ywienia drog¹ naturaln¹, a jakoœæ ¿ycia poprawia
siê wraz z popraw¹ stanu od¿ywienia [20].
Wœród doros³ych najczêstszym wskazaniem do ¿.d.d. s¹ neu-
rogenne zaburzenia po³ykania, g³ównie po udarze mózgu,
oraz niedro¿noœæ górnego odcinka przewodu pokarmowe-
go u chorych z nowotworami prze³yku, jamy ustnej i krtani
oraz ¿o³¹dka. S¹ to zwykle ciê¿ko chorzy – jedynie 2–5%
chorych jest w pe³ni aktywnych, ponad 70% nie opuszcza
domu, a 70–86% wymaga sta³ej opieki [12, 23, 41, 53].
Jakoœæ ¿ycia jest zwykle gorsza ni¿ w grupie chorych niewy-
magaj¹cych ¿.d.d. [52]. Wiek i rodzaj choroby powoduj¹, ¿e
wyniki ¿.d.d. na pierwszy rzut oka wydaj¹ siê z³e – zaledwie
13–20% chorych wraca do ¿ywienia doustnego, a 30–50%
umiera w ci¹gu pierwszego roku leczenia [22, 23, 27, 30].
Niemniej, s¹ to dwa razy lepsze wyniki odleg³e ni¿ w domach
przewlek³ej opieki w USA [7, 37], a 25% stale wymagaj¹-
cych ¿.d.d. prze¿ywa ponad 5 lat. Podobnie, rokowanie cho-
rych z nieoperacyjnymi nowotworami jest z³e. Jednak oko³o
20% z nich prze¿ywa ponad rok, a nie umiera z g³odu po
miesi¹cu. Dobre wyniki i dobr¹ jakoœæ ¿ycia uzyskuje siê
u chorych m³odszych, leczonych ¿.d.d. z powodu innych
wskazañ ni¿ dysfagia [52]. U chorych z nowotworami, któ-
rzy nie mog¹ jeœæ, zw³aszcza w okresie radioterapii, ¿.d.d.
pozwala na zakoñczenie leczenia przeciwnowotworowego
i utrzymanie lub nawet poprawê stanu od¿ywienia, a zatem
i jakoœci ¿ycia. Zasadniczym efektem ¿.d.d. jest umo¿liwie-
nie ciê¿ko chorym pobytu w domu z rodzin¹; chorzy ci wy-
magaj¹ rehospitalizacji przez zaledwie od 0,5–0,6 do 2%
czasu leczenia ¿.d.d., co odci¹¿a szpitale i pozwala unikn¹æ
zaka¿eñ szpitalnych [1].
¯ywienie dojelitowe w warunkach domowych
Piœmiennictwo
1. Adams MM, Wirsching RG:
Guidelines for planning home enteral
feedings. J Am Diet Assoc 1984, 84: 68–71.
2. Barnadas G:
Navigating Home Care: Enteral Nutrition Part
One. Practical Gastroenterology 2003, 27: 13–14,16,19–20,
22, 24, 26, 33, 35.
3. Bertrand PC, Piquet MA, Bordier I, Monnier P, Roulet M:
Preope-
rative nutritional support at home in head and neck cancer pa-
tients: from nutritional benefits to the prevention of the alcohol
withdrawal syndrome. Curr Opin Clin Nutr Metab Care 2002, 5:
435–40.
4. Bott L, Husson MO, Guimber D, Michaud L i wsp.:
Contamina-
tion of gastrostomy feeding systems in children in a home-ba-
sed enteral nutrition program. J Pediatr Gastroenterol Nutr 2001,
33: 266–70.
5. British Artificial Nutrition Survey (BANS) (BAPEN), Elia M:
Indica-
tions for home enteral tube feeding in the UK. Clinical Nutri-
tion 1998, 17, Supplement 1: 49.
6. Caglia P, Luca S, Gandolfo L, Amodeo C:
Enteral nutrition in
patients with chronic neurological diseases. Minerva Gastroen-
terol Dietol 2000, 44: 199–206.
7. Carey TS, Hanson L, Garrett JM, Lewis C i wsp.:
Expectations and
outcomes of gastric feeding tubes. Am J Med 2006, 119: 527.
8. Casewell MW, Cooper JE, Webster M:
Enteral feeds contamina-
ted with Enterobacter cloacae as a cause of septicaemia. BMJ
1981, 282: 973.
9. Chin K-F, Townsend S, Wong W, Miller GV:
A prospective cohort
study of feeding needle catheter jejunostomy in an upper ga-
strointestinal surgical unit. Clinical Nutrition 2004, 23: 691–6.
10. Chrysomilides SA, Kaminski MV Jr:
Home enteral and parente-
ral nutritional support: a comparison. Am J Clin Nutr 1981, 34:
2271–5.
11. Committee of the British Artificial Nutrition Survey (BANS) (BA-
PEN), Elia M:
Home enteral tube feeding in the UK: growth and
patient care. Clinical Nutrition 1998, 17, Supplement 1: 48.
12. Cortez-Pinto H, Pinto-Correia A, Camilo ME, Tavares L, Carneiro
de Moura M:
Long-term management of percutaneous endo-
scopic gastrostomy by a nutritional support team. Clinical Nutri-
tion 2002, 21: 27–31
13. CREST:
Guidelines for the management of enteral tube feeding.
2004.
14. Crosby J, Duerksen D:
A retrospective survey of tube-related
complications in patients receiving long-term home enteral nu-
trition. Dig Dis Sci 2005, 50: 1712–7.
15. Daveluy W, Guimber D, Mention K, Lescut D i wsp.:
Home ente-
ral nutrition in children: an 11-year experience with 416 pa-
tients. Clinical Nutrition 2005, 24: 48–54.
16. De Luis DA, Aller R, Izaola O, Terroba MC i wsp:
Experience of 6
years with home enteral nutrition in an area of Spain. Eur J Clin
Nutr 2006, 60: 553–7.
17. De Luis DA, Aller R, de Luis J, Izaola O i wsp.:
Clinical and bio-
chemical characteristics of patients with home enteral nutrition
in an area of Spain. Eur J Clin Nutr 2003, 57: 612–15.
18. de Luis Roman D, Aller de la Puente R, de Luis Roman J, Cuellar
Olmedo LA i wsp.:
Home enteral nutrition: analysis of efficiency
in a Health District. Rev Clin Esp 2003, 203: 317–20.
19. de Wit LM, Nieboer M, Wipkink A, Overbeeke N i wsp.:
Diffe-
rences between hospitals in home enteral nutrition. Clinical
Nutrition 1995, 14, Supplement 2: 42.
20. Diamanti A, Pietrobattista A, Gambarara M:
Home enteral nu-
trition in children: A 17-year period experience. Clinical Nutri-
tion 2006, 25: 173–4.
21. Elia M, Stratton C, Russell C, Green C, Pan F:
The cost of dise-
ase-related malnutrition in the UK and economic considerations
for the use of oral nutritional supplements (ONS) in adults.
BAPEN 2005.
22. Elia M, Stratton RJ, Holden C, Meadows N i wsp.:
Home arti-
ficial nutritional support: the value of the British Artificial Nu-
trition Survey. Clin Nutr 2001, 20, Suppl.1: 61–6.
23. Elia M, Stratton RJ, Holden C, Meadows N i wsp.:
Home enteral
tube feeding following cerebrovascular accident. Clin Nutr 2001,
20: 27–30.
24. Evans S, Holden C, MacDonald A:
Home enteral feeding audit 1
year post-initiation. J Hum Nutr Diet 2006, 19: 27–9.
25. Evans, S, MacDonald A, Holden C:
Home enteral feeding audit.
J Hum Nutr Diet 2004, 17: 537–42.

Nr 1/2006 Tom 1
14
Postêpy ¯ywienia Klinicznego
26. Fernadez-Banares F, Cabre E, Esteve-Comas M, Gassull MA:
How
effective is enteral nutrition in inducing clinical remission in acti-
ve Crohn’s disease? A meta-analysis of the randomized clinical
trials. JPEN 1995, 19, 356–64.
27. Galletti R, Finocchiaro E, Fadda M, Mancino V i wsp.:
Survival
analysis in patients affected by chronic neurological disorders in
home enteral nutrition (HEN). Clinical Nutrition 2003, 22, Sup-
plement 1: S93.
28. Hebuterne X, Bozzetti F, Moreno Villares JM, Pertkiewicz M i wsp.:
Home enteral nutrition in adults: a European multicentre survey.
Clinical Nutrition 2003, 22: 261–6.
29. Howard L, Ament M, Fleming R i wsp.:
Current use and clinical
outcome of home parenteral and enteral nutrition therapies in
the United States. Gastroenterology 1995, 109: 355–65.
30. Howard L:
Home parenteral and enteral nutrition in cancer pa-
tients. Cancer 1993, 72 (11 Suppl): 3531–41.
31. Howard P:
Home enteral feeding: II. A health service perspecti-
ve. Clin Nutr 2001, 20, Suppl.1: 71-5.
32. Ireton-Jones C:
Home enteral nutrition from the provider’s per-
spective. JPEN 2002, 26, Suppl. 5: S8–9.
33. Kolb S, Lenz A, Platzer E, Sailer D i wsp.:
Serum concentrations
of vitamins A, B
1
, B
6
, and E in patients with Crohn’s disease
receiving oligopeptide tube feeding (home enteral nutrition).
Clinical Nutrition 1986, 5, Supplement 1: 51.
34. Levny J, Van Laethem Y, Verhaegan G:
Contaminated enteral
nutrition solutions as a cause of nosocomial blood stream infec-
tions. JPEN 1981, 5: 76–9.
35. Liley AJ, Manthorpe J:
The impact of home enteral tube feeding
in everyday life: a qualitative study. Health Soc Care Community
2003, 11: 415–22.
36. McNamara EP, Flood P, Kennedy NP:
Home tube feeding: an
integrated multidisciplinary approach. J Hum Nutr Diet 2001,
14: 13–19.
37. Mitchell SL, Tetroe JM:
Survival after percutaneous endoscopic
gastrostomy placement in older patients. J Gerontol 2000, 55A:,
M735–M739.
38. Moreno JM, Shaffer J, Staun M, Hebuterne X i wsp.:
Survey on
legislation and funding of home artificial nutrition in different
European countries. Clinical Nutrition 2001, 20 (2): 117–23.
39. Moreno Villares JM, Pedron Giner C, Martinez Costa C, Oliveros
Leal L i wsp.:
Home enteral nutrition in Spain. Results of the regi-
ster of the Spanish Society of Pediatric Gastroenterology, Hepato-
logy and Nutrition in 2003. An Pediatr (Barc) 2006, 64: 239–43.
40. Park RHR, Galloway A, Shenkin A, MacKenzie JF, Russell RI:
Ma-
gnesium deficiency in patients on home enteral nutrition. Clini-
cal Nutrition 1990, 9: 147–9.
41. Parker T, Neale G, Elia M:
Home enteral tube feeding in East
Anglia. Eur J Clin Nutr 1996, 50: 47–53.
42. Patchell CJ, Anderton A, Holden C, MacDonald A i wsp.:
Redu-
cing bacterial contamination of enteral feeds. Arch Dis Child
1998, 78: 166–168.
43. Pearce CB, Collett J, Goggin PM, Duncan HD:
Enteral nutrition
by nasojejunal tube in hyperemesis gravidarum. Clinical Nutri-
tion 2001, 20: 461–4.
44. Pertkiewicz M, Korta T, Ksi¹¿yk J i wsp.:
Standardy ¿ywienia po-
zajelitowego i dojelitowego. Wyd. Lek. PZWL, Warszawa 2005.
45. Planas M, Castella M, Garcia Luna PP, Chamorro J i wsp.:
Home
Enteral Nutrition: National Registry 2001. Nutr Hosp 2004, 19:
145–9.
46. Planas M, Lecha M, Garcia Luna PP, Pares RM i wsp.:
National
Registry of Home Enteral Nutrition 2003. Nutr Hosp 2006, 21:
71–4.
47. Reddy P, Malone M:
Cost and outcome analysis of home paren-
teral and enteral nutrition. JPEN 1998, 22: 302–10.
48. Russell CA:
Home enteral tube feeding: I. The role of industry.
Clin Nutr 2001, 20, Suppl.1: 67–9.
49. Ryan AM, Rowley SP, Healy LA, Flood PM i wsp.:
Post-oesopha-
gectomy early enteral nutrition via a needle catheter jejunosto-
my: 8-year experience at a specialist unit. Clinical Nutrition 2006,
25: 386–93.
50. Schloerb PR, Wood JG, Casillan AJ, Tawfik O, Udobi K:
Bowel
necrosis caused by water in jejunal feeding. JPEN 2004, 28: 27–9.
51. Schneider S, Blanc-Vincent MP, Nitenberg G, Senesse P i wsp.:
Standards, options and recommendations for home parenteral
or enteral nutrition in adult cancer patients. Bull Cancer 2001,
88: 605–18.
52. Schneider SM, Pouget I, Staccini P, Rampal P, Hebuterne X:
Qu-
ality of life in long-term home enteral nutrition patients. Clinical
Nutrition 2000, 19: 23–8.
53. Schneider SM, Raina C, Pugliese P, Pouget I i wsp.:
Outcome
of patients treated with home enteral nutrition. JPEN 2001,
25: 203–9.
54. Silver HJ, Wellman NS, Arnold DJ, Livingstone A, Byers PM:
Ol-
der adults patients receiving home enteral nutrition: enteral re-
gimen, provider involvement and health care outcomes. JPEN
2004, 28: 92–8.
55. Simon EP, Showers N, Blumenfield S, Holden G, Wu X:
Delivery
of home care services after discharge: what really happens. He-
alth Soc Work 1995, 20: 5–14.
56. Stanga Z, Giger U, Marx A, DeLegge MH: Effect of jejunal long-
term feeding in chronic pancreatitis. JPEN 2005, 29: 12–20.
57. Szczygie³ B, Pertkiewicz M, Korta T, Cebulski W, Majewska K:
¯ywienie dojelitowe. Pol Tyg Lek 1986, 41: 163–9.
58. White G, Whitehead K:
Enteral tube feeding training for nurses
and care assistants. Br J Community Nurs 2001, 6: 557–8, 560,
562–4.
59. Winkler HR:
Procedures for home enteral nutrition. J Can Diet
Assoc 1985, 46: 195–8.
60. Yoder AJ, Parrish CR, Yeaton P:
A retrospective review of the
course of patients with pancreatitis discharged on jejunal
feedings. Nutr Clin Pract 2002, 17: 314–20.
61. Zachos M, Tondeur M, Griffiths AM:
Enteral nutritional therapy
for induction of remission in Crohn’s disease (Cochrane Review),
[w:] The Cochrane Library, Issue 3, Chichester 2004.
62. Gaggiotti G, Orlandoni P, Ambrosi S, Catari M:
Italian Home
Enteral Nutrition (IHEN) Register: Data collection and aims. Cli-
nical Nutrition 2001, 20, Suppl. 2: 69–72.
63. Vayre P, Cabrit R, Bernard PF, Hureau J:
Home enteral nutrition:
functional partnership experience in the network of care of the
Centre Medical de Forcilles, 1990–1999. Bull Acad Natl Med
1999, 183: 1655–64.
Wyszukiwarka
Podobne podstrony:
Żywienie dojelitowe w warunkach domowych wskazania, powikłania i wyniki
Żywienie dojelitowe w warunkach domowych chorych z zaawansowanym nowotworem złośliwym
Żywienie dojelitowe prezentacja
zywienie dojelitowe id 594284 Nieznany
zywienie dojelitowe a pozajelitowe
Terapia dr Gersona w warunkach domowych, Zdrowie, medycyna
Terapia dr Gersona w warunkach domowych, Zdrowie
RUS Szczadiłow J Oczyszczanie płuc w warunkach domowych
Terapia dr Gersona w warunkach domowych, wersja uaktualniona
6 Aktywnosc fizyczna w NS co moze pacjent w warunkach domowych Rehabilitacja
Neony LED wykonanie w warunkach domowych
Fotopolis pl High speed photography w warunkach domowych
Preparaty do zywienia dojelitow Nieznany
Ciepło i zimnolecznictwo w warunkach domowych
Definicja(zywienie dojelitowe, sonda, zglebnik, przetoki
Pielęgnacja dłoni i płytek paznokciowych w warunkach domowych, Technik usług kosmetycznych
więcej podobnych podstron