„Każda substancja jest trucizną
i nie ma substancji, która by nie była trucizną.”
Paracelsus
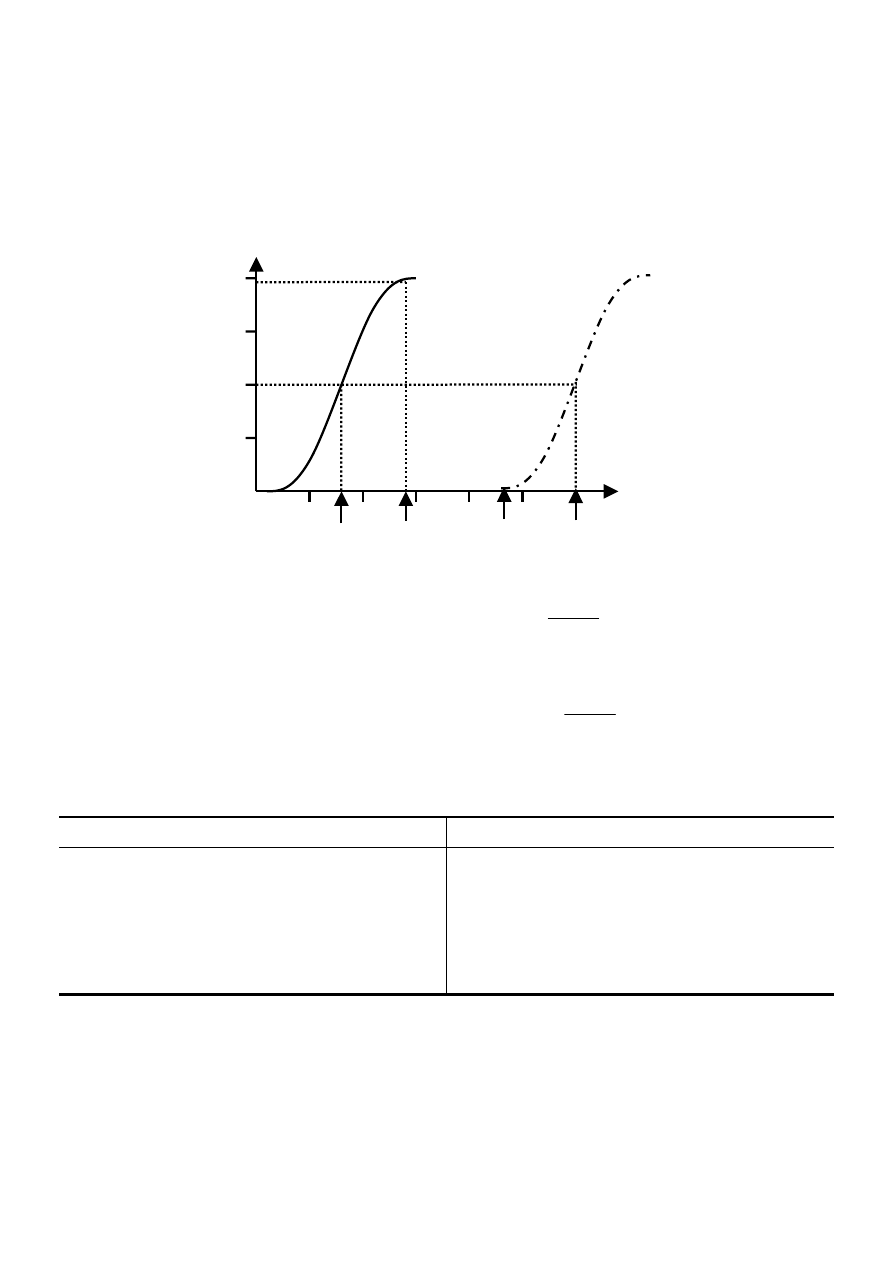
Działania niepożądane i toksyczne leków
100%
50%
ED
50
LD
50
LD
1
ED
99
Indeks terapeutyczny
50
50
ED
LD
=
Margines bezpieczeństwa
99
1
ED
LD
=
Wartości LD
50
różnych substancji u szczura
Substancja LD
50
(mg/kg)
Etanol 13
600
Aldehyd octowy
1 900
Amitryptylina 530
Digitoxyna 24
Protoweratryna 5
(za: MA Hollinger, 1995, „CRC Handbook of Toxicology”, CRC Press)
1

Klasyfikacja toksyczności substancji
Stopień
toksyczności
Określenie potoczne
Pojedyncza LD
50
u szczura
1
nadzwyczaj toksyczna
< 1 mg/kg
2
bardzo toksyczna
1-50 mg/kg
3 umiarkowanie
toksyczna
50-500
mg/kg
4 mało toksyczna
0,5-5 g/kg
5 praktycznie
nietoksyczna
5-15
g/kg
6
w zasadzie nieszkodliwa
> 15 g/kg
(za: MA Hollinger, 1995, „CRC Handbook of Toxicology”, CRC Press)
Należy pamiętać, że system oceny toksyczności oparty wyłącznie na
takich wskaźnikach jak indeks terapeutyczny, czy LD
50
ma niewielkie
znaczenie praktyczno-lecznicze. Nie uwzględnia m.in.:
•
różnic międzygatunkowych między zwierzętami a człowiekiem
•
innych rodzajów toksyczności (np. talidomid jest w takiej klasyfikacji
mało toksyczny)
•
korzyści terapeutycznych ze stosowania danego leku (lek może być
toksyczny ale jednocześnie ratujący życie)
Bardziej miarodajny jest stosunek ryzyka do korzyści (
risk/benefit ratio
),
który uwzględnia korzyść jaką odniesie populacja osób leczonych mimo
ryzyka wystąpienia działań niepożądanych. Nie da się go jednak
wyliczyć w jakichś bezwzględnych jednostkach (jak np. policzyć u
chorych leczonych aminoglikozydami stosunek ryzyka wystąpienia
głuchoty względem korzyści wyleczenia zapalenia płuc?)
2

Rodzaje niekorzystnych reakcji na leki
Działania niepożądane powodowane przez leki można podzielić na dwie
grupy:
•
powiązane z głównym działaniem leku (np. krwawienie po lekach
przeciwkrzepliwych) – reakcje typu A
•
niepowiązane z głównym działaniem leku (np. hepatotoksyczność
paracetamolu) – reakcje typu B
Reakcje typu A
•
występują najczęściej wskutek:
•
przedawkowania leku
•
zmienionej farmakokinetyki leku u pacjenta
•
interakcji leku z innymi substancjami
•
zwykle dają się przewidzieć
•
w wielu przypadkach skutki tego typu działań są odwracalne po
odstawieniu leku, czasem jednak mogą być poważne (leki
przeciwkrzepliwe krwawienie, leki hipoglikemizujące śpiączka).
Reakcje typu B
•
często wywoływane przez reaktywne metabolity i/lub reakcje
immunologiczne
•
zazwyczaj są rzadkie (inaczej lek byłby eliminowany w testach
klinicznych) i ciężkie (inaczej ich wystąpienie nie byłoby wiązane z
lekiem)
•
mogą pojawić się w sposób nieprzewidywalny jako:
•
reakcje idiosynkrazji: chloramfenikol aplazja szpiku
•
reakcje alergiczne: penicylina reakcja anafilaktyczna
•
czasem ich wystąpienie można przewidzieć, jeśli lek jest stosowany
np.:
•
w dużych dawkach: paracetamol hepatotoksyczność,
aminoglikozydy ototoksyczność, nefrotoksyczność
•
w czasie ciąży: talidomid fokomelia
•
w czasie choroby: sulfonamidy hemoliza w przebiegu niedoboru
G6PD
3
Narząd
Lek/sytuacja kliniczna
Dz. niepożądane
Typ reakcji
A
B
NN
Serce
Antagoniści receptorów β
Niewydolność krążenia
+
Doksorubicyna
Niewydolność krążenia
+
Digoksyna
Arytmia +
Mózg
Lewodopa,
bromokryptyna
Halucynacje
+
Etanol
(odstawienie)
Halucynacje
+
Antagoniści receptorów muskarynowych
Upośledzenie pamięci
+
Chlorpromazyna
Złośliwy zesp. poneuroleptyczny
+
Zmysły
Wzrok
Etambutol,
chlorochina
Ślepota
(makulopatia)
+
Słuch
Aminoglikozydy
Głuchota
+
Smak
Kaptopril
Zniekształcenie
smaku
+
Dotyk/ból
Winkrystyna
Ból i drętwienie
+
Układ ruchu
Antagoniści receptorów β
Zmęczenie
+
Fibraty
(zapalenie mięśni)
Bóle
mięśniowe
+
Diuretyki
Dna
moczanowa
+
Prednizolon
Osteoporoza
+
Fenytoina
Osteomalacja
+
Układ
pokarmowy
Żołądek NLPZ
Wrzód
trawienny
+
Trzustka
Asparginaza
Zapalenie
trzustki
+
Okrężnica
Klindamycyna,
amoksycylina
Biegunki
+
Wątroba
Fenytoina
Zapalenie
wątroby
+
Woreczek żółciowy
Oktreotyd
Kamica
żółciowa
+
Płuca
Antagoniści receptorów β
Zaostrzenie astmy
+
Amiodaron
Włóknienie śródmiąższowe
+
4

Narząd
Lek/sytuacja kliniczna
Dz. niepożądane Typ
reakcji
A
B
NN
Układ
Kaptopril
Ostra niewydolność nerek
+
moczowo-płciowy NLPZ
Ostra
niewydolność nerek
+
Aminoglikozydy
Ostra
niewydolność
nerek
+
Nadużywanie leków przeciwbólowych
Przewlekła niewydolność nerek
+
Cyklofosfamid
Krwotoczne zap. pęcherza
+
Tiazydy
Zaburzenia
erekcji
+
Układ endokrynny /
Tiazydy
Hiperglikemia
+
metabolizm Poch.
Sulfonylomocznika
Hipoglikemia
+
Amiodaron
Dysfunkcja
tarczycy
+
Chlorpromazyna,
haloperidol
Ginekomastia/mlekotok
+
Układ
krwiotwórczy
Erytrocyty Metyldopa
Anemia
hemolityczna
+
Leukocyty
Karbimazol
Neutropenia
+
Trombocyty
Chinina
Trombocytopenia
+
Wszystkie krwinki
Chloramfenikol
Anemia
aplastyczna
+
Krzepnięcie
Stilbestrol
Zakrzepica
+
Heparyna,
Warfaryna
Krwawienia
+
Skóra
Penicyliny
Wysypki
odropodobne
+
Allopurinol, sulfonamidy
Uogólniony rumień
wielopostaciowy
+
Wieloukładowe
Hydralazyna
Jatrogenny
zespół toczniowy
+
Płód
Eretrinat,
Fenytoina
Teratogeneza
+
Karcynogeneza
Leki
immunosupresyjne/cytotoksyczne
Nowotwór
+
(za: Rang 2000, „Pharmacology”, Churchil Livingstone, Edinburgh)
5

Ogólne mechanizmy toksyczności leków
na poziomie komórkowym
Uszkodzenie lub śmierć komórki najczęściej jest wywoływane przez
reaktywne metabolity leku (substancje toksyczne same w sobie rzadko
są stosowane jako leki). Dlatego narządami szczególnie narażonymi na
działania toksyczne są wątroba i nerki bezpośrednio zaangażowane w
metabolizm i wydalanie leków.
Aktywne metabolity leków mogą brać udział w reakcjach
cytotoksycznych poprzez:
•
Interakcje kowalencyjne:
o łączenie się z:
DNA (związki mutagenne karcyno-, teratogeneza)
białkami (np. amanitadyna muchomora sromotnikowego
wiąże aktynę)
lipidami, węglowodorami i in.
•
Interakcje niekowalencyjne, np.:
o kaskada reakcji wywoływana przez toksyczne rodniki tlenowe
zmiana przepuszczalności błon, reakcje z białkami i in.
o zmniejszenie ilości glutationu zaburzenie równowagi
procesów red-ox
o modyfikacja grup sulfhydrylowych kluczowych enzymów
zaburzenia funkcjonowania komórki
Śmierć komórki w wyniku tego typu uszkodzeń następuje raczej
wskutek apoptozy niż nekrozy.
Hepatotoksyczność leków
•
Wątroba jest pierwszym narządem narażonym na działanie
aktywnych metabolitów leków powstałych w wyniku reakcji I fazy
zachodzących w enzymach mikrosomalnych hepatocytów
•
Uszkodzenie komórek wątroby może manifestować się w różny
sposób – od nieprawidłowości w badaniach laboratoryjnych (
↑AspAT,
↑AlAT) do ostrej martwicy lub marskości wątroby
6
•
Różnorakie mogą być mechanizmy uszkodzenia wątroby przez leki
lub ich metabolity:
•
w większości przypadków cytotoksyczność wskutek interakcji
kowalencyjnych lub niekowalencyjnych – paracetamol,
izoniazyd
•
żółtaczka zastoinowa (zwykle odwracalna) – chlorpromazyna
•
reakcje immunologiczne – halotan
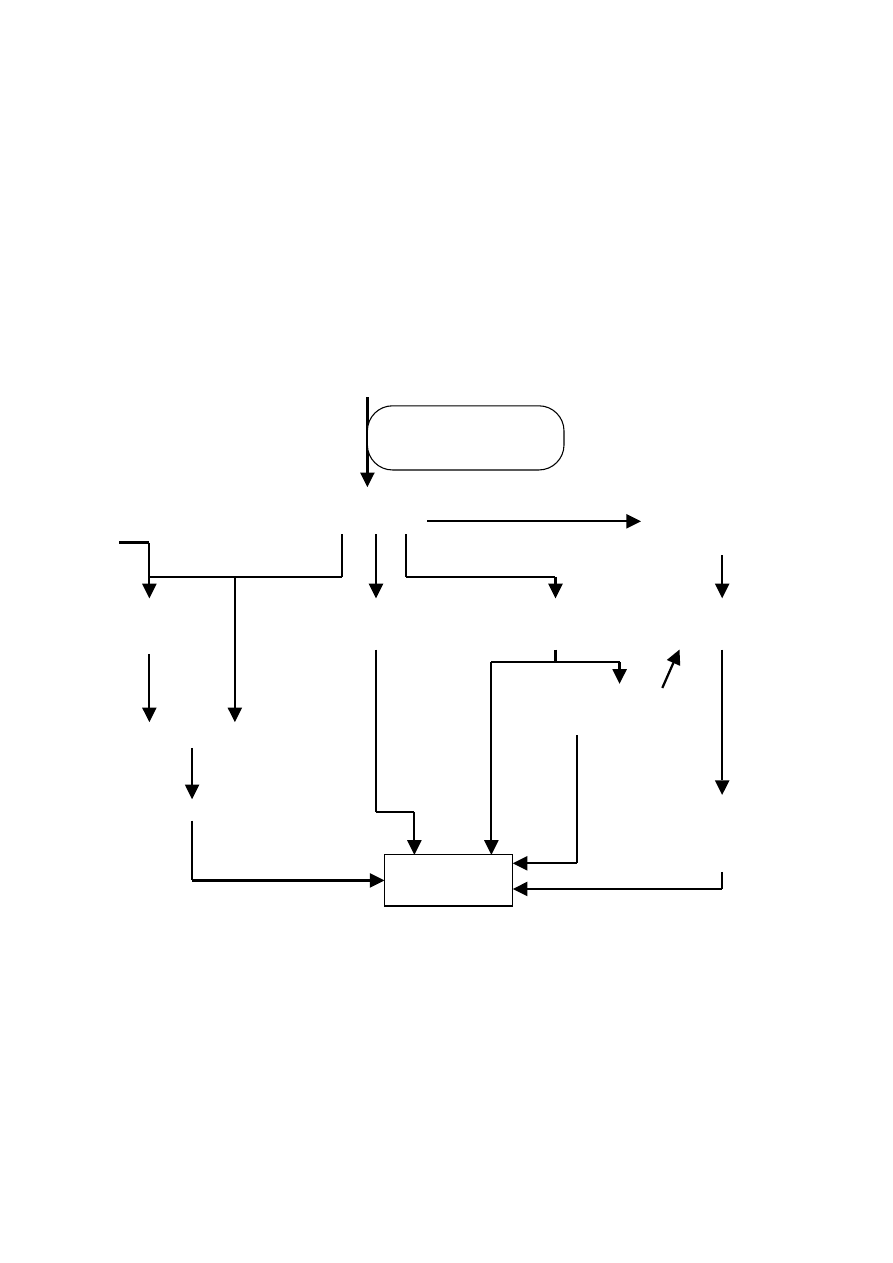
Paracetamol a uszkodzenie wątroby:
Toksyczne dawki
paracetamolu
Imina N-acetylo-p-benzochinonu
(NAPBQI)
Połączenia
NAPBQI-GSH
Zmniejszenie GSH
Stres oksydacyjny
ŚMIERĆ
KOMÓRKI
Połączenia
NAPBQI z białkami
Peroksydacja
lipidów
Ciągły wzrost
stężenia Ca
2+
Utlenianie grup SH
na komórkowej
ATP-azie Ca
2+
GSH
Zwiększona
przepuszczalność
błon
Stymulacja enzymów
degradujących
indukowanych Ca
2+
Oksydazy P-450 o
mieszanej funkcji
(za: Bobbis AR et al. 1989; Nelson SD, Pearson PG 1990 Annu Rev Pharmacol
Toxicol 30: 169)
Przy wysokich dawkach paracetamolu wysyceniu ulegają enzymy
sprzęgające. Oksydazy P-450 mieszanej funkcji przekształcają go
wówczas w reaktywny metabolit – iminę N-acetylo-p-benzochinonu
(NAPBQI), która poprzez interakcje kowalencyjne i niekowalencyjne
prowadzi do śmierci hepatocytów. Proces ten nasila zmniejszenie ilości
GSH oraz indukcja enzymów P-450. Jako odtrutkę w zatruciu
paracetamolem stosuje się acetylocysteinę zwiększającą syntezę GSH.
7

Nefrotoksyczność
Nerki są kolejnym narządem szczególnie narażonym na działanie
aktywnych metabolitów leków. W procesie zagęszczania moczu w
kanalikach rośnie stężenie wszystkich substancji (w tym toksycznych),
co prowadzić może do martwicy brodawek i/lub kanalików nerkowych
wskutek ogólnych mechanizmów uszkodzenia komórek.
Nefrotoksyczność mogą powodować liczne leki np.:
Niesterydowe leki przeciwzapalne poprzez:
•
hamowanie syntezy prostaglandyn ostra niedokrwienna
niewydolność nerek, retencja sodu i wody
•
reakcje alergiczne śródmiąższowe zapalenie nerek
niewydolność nerek, proteinuria
•
nefropatię analgetyczną (głównie fenacetyna) martwica brodawek
nerkowych, przewlekła niewydolność nerek
Kaptopril:
•
w dużych dawkach uszkodzenie kłębków
Cyklosporyna:
•
zmiana dynamiki naczyniowej ciągły wzrost oporu naczyniowego,
↓ filtracji, układowe nadciśnienie
8
Karcynogenność leków
Karcynogeny są to substancje chemiczne wywołujące nowotwory
poprzez bezpośrednią reakcję z DNA lub działanie w późniejszym etapie
karcynogenezy. Można je podzielić na:
Karcynogeny genotoksyczne (mutageny):
•
działają bezpośrednio na DNA (np. wiążą się z O
6
guaniny)
•
zapoczątkowują transformację nowotworową poprzez zmiany w
protoonkogenach lub genach supresorowych
•
największe znaczenie mają substancje zawarte w zanieczyszczeniach
środowiska, dymie papierosowym, ew. dodatkach do żywności; leki
raczej rzadko są genotoksyczne (cytostatyki)
Karcynogeny epigenetyczne:
•
nie powodują uszkodzeń genetycznych, lecz zwiększają
prawdopodobieństwo wystąpienia nowotworu:
•
Promotory:
o zwiększają prawdopodobieństwo rozwoju nowotworu z
komórek uszkodzonych genetycznie (po zadziałaniu
mutagenów)
o np. kwasy żółciowe, sacharyna w dużych dawkach
•
Kokarcynogeny
o zwiększają prawdopodobieństwo rozwoju nowotworu, jeśli
są zastosowane równocześnie z czynnikami
genotoksycznymi
o np. węglowodory aromatyczne
•
Hormony
o niektóre nowotwory są hormonozależne – rak sutka,
prostaty
o rak endometrium rozwija się wskutek hiperplazji
endometrium przy długotrwałej ekspozycji na działanie
estrogenów; obecność gestagenów (ciąża, środki
antykoncepcyjne) działa protekcyjnie
Ta sama substancja może wykazywać jednocześnie działanie
genotoksyczne, oraz ułatwiające i/lub kokarcynogenne. Smog czy dym
papierosowy zawierają liczne substancje karcynogenne o różnym
mechanizmie działania.
9

Wpływ leków na płód. Teratogeneza.
Czynniki zewnętrzne (fizyczne, chemiczne - w tym leki) mogą wywierać
wpływ na rozwój płodu. Termin teratogeneza używany jest dla
określenia dużych malformacji strukturalnych (w odróżnieniu od
hipotrofii czy dysplazji). Zależnie od okresu zadziałania danego czynnika
wystąpić mogą uszkodzenia różnego rodzaju i stopnia.
Rozwijający się płód ssaków przechodzi trzy fazy:
Stadium blastocysty (0-16 dzień)
•
podział komórek
•
czynniki cytotoksyczne i genotoksyczne zwykle powodują
obumarcie i poronienie zarodka
Organogeneza (17-60 dzień)
•
dalsze podziały, migracja i różnicowanie się komórek
•
kluczowy okres rozwoju narządów – ew. teratogeneza zachodzi w
tym właśnie okresie
•
organizacja zarodka zachodzi w ściśle określonym porządku –
rodzaj deformacji zależy więc od czasu ekspozycji na teratogen:
Działanie teratogenne talidomidu
Dzień ciąży Typ
deformacji
21. – 22.
malformacje oczu, defekty n. czaszkowych
24. – 27.
fokomelia kończyn górnych
28. – 29.
fokomelia kończyn górnych i dolnych
30. – 36.
malformacja rąk, stenoza odbytu
(za: Rang 2000, „Pharmacology”, Churchil Livingstone, Edinburgh)
Histiogeneza i dojrzewanie funkcjonalne (II i III trymestr)
•
rozwój płodu w tym okresie uzależniony jest od dostarczania
składników żywnościowych oraz gry hormonalnej
•
duże malformacje strukturalne w tym okresie nie zachodzą, ale
substancje szkodliwe mogą wpływać na wzrost i rozwój płodu
•
ostatecznie kształtuje się układ płciowy i nerwowy – czynniki
szkodliwe doprowadzić mogą do zaburzeń rozwoju narządów
płciowych lub upośledzenia umysłowego
10

Leki zaburzające rozwój płodu u człowieka
Lek Wywoływane uszkodzenie
Talidomid
Fokomelia, wady serca, zarośnięcie światła jelit i in.
Penicylamina
Ubytki skóry i in.
Warfaryna
Siodełkowaty nos, opóźnienie wzrostu, wady kończyn, oczu, OUN
Kortykosteroidy
Rozszczep podniebienia, zaćma wrodzona (rzadko)
Androgeny
Maskulinizacja
płodów żeńskich
Estrogeny
Atrofia
jąder u płodów męskich
Stilbestrol
Gruczołowatość pochwy u płodów żeńskich, rak pochwy lub szyjki macicy 20 lat
później
Leki przeciwdrgawkowe
Fenytoina
Rozszczepy wargi i/lub podniebienia, mikrocefalia, opóźnienie rozwoju
umysłowego
Kwas walproinowy
Wady cewy nerwowej, np. rozszczep kręgosłupa
Karbamazepina
Opóźnienie wzrostu głowy płodu
Leki cytotoksyczne (zwł. antagoniści
kw. foliowego)
Wodogłowie, rozszczep podniebienia, wady cewy nerwowej
Aminoglikozydy
Uszkodzenie nerwu czaszkowego VIII
Tetracykliny
Zabarwienie
kości i zębów, cienkie szkliwo zębów, upośledzony rozwój kości
Etanol
Alkoholowy zespół płodowy
Retinoidy
Wodogłowe i in.
Inhibitory konwertazy angiotensyny
Skąpowodzie, niewydolność nerek
(Wg: Juchau 1989 Annu Rev Pharmacol Toxicol 29: 165)
11

Klasyfikacja FDA leków stosowanych w ciąży
A
Badania z grupą kontrolną nie wykazały istnienia ryzyka dla
płodu w I trymestrze, możliwość uszkodzenia płodu wydaje się
bardzo mało prawdopodobna.
B
Badania na zwierzętach nie wskazują na istnienie ryzyka dla
płodu, ale nie przeprowadzono badań z grupą kontrolną u ludzi
lub
Badania na zwierzętach wykazały działanie niepożądane na
płód, ale badania w grupie kobiet ciężarnych nie potwierdziły
istnienia ryzyka dla płodu.
C
Badania na zwierzętach wykazały działanie teratogenne lub
zabójcze dla płodu, ale nie przeprowadzono badań z grupą
kontrolną kobiet
lub
Nie przeprowadzono odpowiednich badań ani na zwierzętach,
ani u ludzi.
D
Istnieją dowody na niekorzystne działanie leku na płód, ale w
pewnych sytuacjach klinicznych potencjalne korzyści z jego
zastosowania przewyższają ryzyko (np. w stanach
zagrażających życiu lub chorobach, w których inne, bezpieczne
leki nie mogą być zastosowane lub są nieskuteczne).
X
Badania przeprowadzone na zwierzętach lub u ludzi wykazały
nieprawidłowości płodu w wyniku stosowania danego leku bądź
istnieją dowody na niekorzystne działanie leku na płód ludzki i
ryzyko zdecydowanie przewyższa potencjalne korzyści z jego
zastosowania.
12

Reakcje alergiczne na leki
Reakcje alergiczne są częstą formą reakcji niepożądanej na leki.
Większość leków ma zbyt małą masę cząsteczkową, by być
immunogennymi. Są one
haptenami
tzn. tworzą właściwy antygen po
kowalencyjnym połączeniu z białkiem. Tego typu wiązania tworzone są
zwykle przez aktywne metabolity leku powstałe wskutek jego
metabolizmu w wątrobie lub np. fotoaktywacji w skórze pod wpływem
światła słonecznego (fotoalergia).
Stwierdzenie, że działanie niepożądane danego leku ma podłoże
alergiczne, nie zawsze jest proste. Hipoteza taka jest prawdopodobna,
jeśli:
•
czas wystąpienia reakcji jest różny od czasu pojawienia się efektu
farmakologicznego (pojawia się po kilku dniach od zastosowania,
albo po kilku dawkach leku)
•
nadwrażliwość występuje po dawkach zbyt małych, by wywołać efekt
farmakologiczny
•
objawy są niezależne od działania farmakologicznego leku i
odpowiadają jednemu z typów reakcji alergicznych wg Gella i
Coombsa (I, II, III lub IV)
I. Nadwrażliwość natychmiastowa (anafilaksja)
•
łączenie antygenu z IgE związanymi z komórkami tucznymi
powoduje natychmiastową degranulację – uwolnienie
mediatorów reakcji zapalnej
II. Cytotoksyczność zależna od przeciwciał
•
łączenie przeciwciała z antygenem związanym na powierzchni
komórki fagocytoza, cytotoksyczność, aktywacja dopełniacza
III. Nadwrażliwość zależna od kompleksów immunologicznych
•
kompleksy antygen-przeciwciało odkładają się w tkankach
aktywacja układu dopełniacza, napływ neutrofili
IV. Nadwrażliwość opóźniona typu komórkowego
•
uczulone uprzednio limfocyty T, przy powtórnym kontakcie z
antygenem uwalniają limfokiny napływ makrofagów,
zapalenie, uwalnianie mediatorów zapalenia
13

Ważne klinicznie objawy nadwrażliwości na leki
Wstrząs anafilaktyczny
•
nagła, zagrażająca życiu reakcja typu I
•
uwalniane w procesie degranulacji mediatory reakcji zapalnej
(histamina, cytokiny i in.) powodują takie objawy jak - rumień,
pokrzywka, obrzęk, skurcz oskrzeli, spadek ciśnienia krwi
•
najczęściej ze wszystkich leków powodują go penicyliny
•
także prokaina, preparaty jodu, salicylany, sulfonamidy
•
w leczeniu – adrenalina (lek ratujący życie), difenhydramina,
hydrokortyzon
Reakcje hematologiczne
•
głównie reakcje typu II, także III lub IV
•
krążące przeciwciała wiążą się z kompleksem lek-makrocząsteczka na
powierzchni komórek krwi aktywacja dopełniacza, atak
cytotoksyczny leukocytów
•
sulfonamidy, metyldopa
niedokrwistość hemolityczna
•
NLPZ, klozapina, tiazydy
agranulocytoza
•
chinina, heparyna, tiazydy
trombocytopenia
•
chloramfenikol
niedokrwistość aplastyczna
Alergiczne uszkodzenie wątroby
•
reakcje typu II i III
•
trifluoroacetylochlorek, metabolit halotanu, wiąże się z
makrocząsteczkami na powierzchni hepatocytów tworząc immunogen
aktywacja limfocytów T
k
zniszczenie komórki uwolnienie
kompleksów antygen-przeciwciało reakcje typu III
Inne
•
skórne wysypki - zwykle typ IV (z udziałem komórek), czasem I;
średnio nasilone, rzadko – śmiertelne złuszczanie skóry
•
toczeń polekowy wskutek indukcji wytwarzania dużej ilości
przeciwciał przeciwko własnemu organizmowi – hydralazyna,
prokainamid
14
Wyszukiwarka
Podobne podstrony:
VI Działanie niepożądane i toksyczne
Leki zmniejszajace dzialania niepozadane lekow przeci wnowotworowych
3 TOKSYCZNOŚĆ, MECHANIZMY DZIAŁANIA I?WKOWANIE LEKÓW
Działania niepożądane leków
Działanie toksyczne leków układu krążenia i hemostazy
Działanie toksyczne leków układu krążenia i hemostazy
Leki zmniejszajace dzialania niepozadane lekow przeci wnowotworowych
Prezentacja tekst, Patofizjologia L(3) - Toksyczność leków ...+ (ksera), TOKSYCZNOŚĆ LEKÓW DZIAŁAJĄC
Działania niepożądane leków przeciwpsychotycznych II generacji
(2,3) Działania nieporządane, toksytczne leków Metabolizm, czynniki wpływające na działanie substanc
Działania niepożądane nlpz
działania niepozadane NLPZ
ćwiczenie3 interakcje dzialania niepozadane
Dzialania niepozadane cytostatykow
środki kontrastowe- działanie niepożądane, ER
działanie niepożądane chemioterapii nowotworów, Medycyna, Farmakologia, 23. Chemioterapia przeciwnow
więcej podobnych podstron