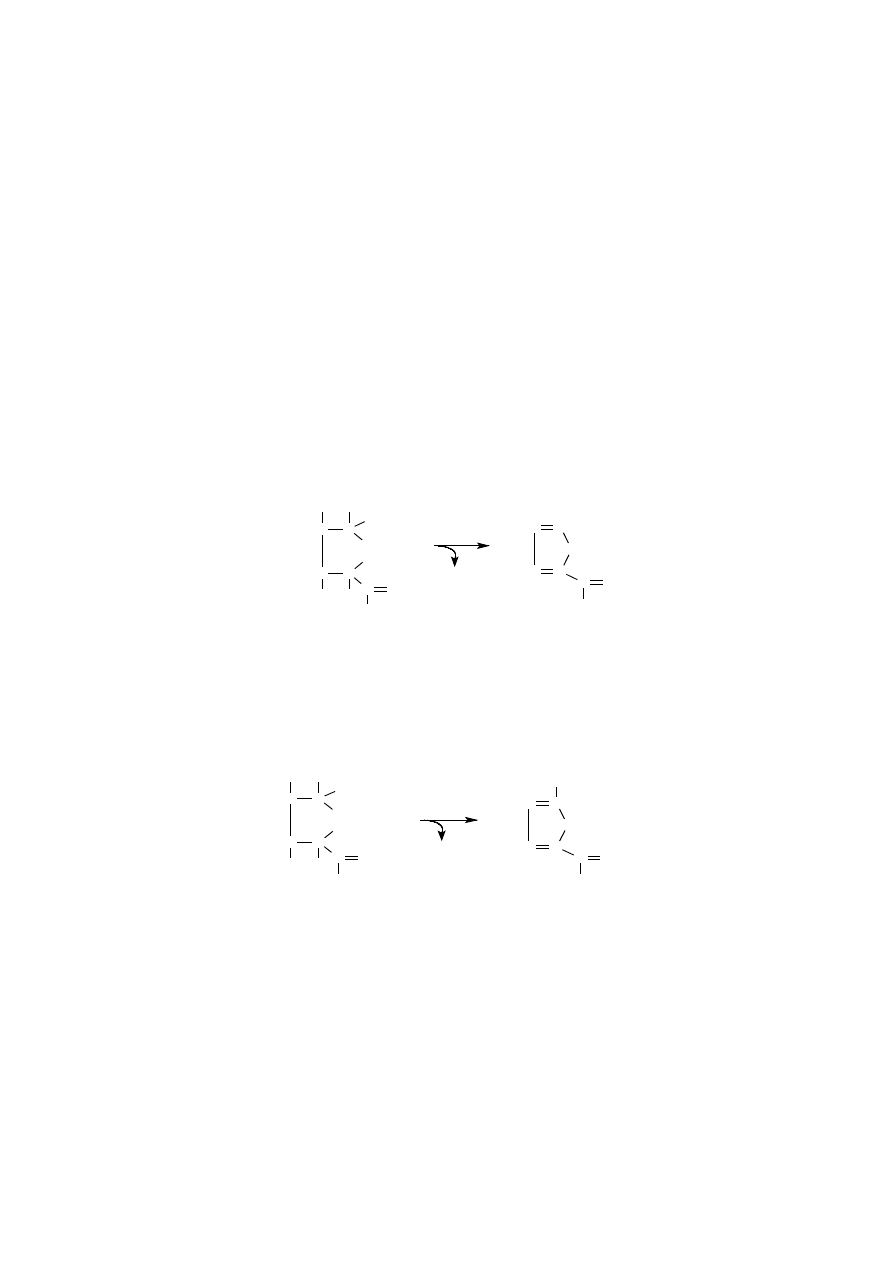
1
7.
JAKOŚCIOWA ANALIZA
WĘGLOWODANÓW
Monosacharydy pod wpływem stężonych kwasów (octowego, solnego lub siar-
kowego) i podwyższonej temperatury ulegają odwodnieniu. Na działanie roz-
cieńczonych kwasów w temperaturze pokojowej są stosunkowo odporne. Od-
wodnienie pentoz prowadzi do wytworzenia furfuralu, natomiast odwodnienie
heksoz tworzy 5-hydroksymetylenofurfural.
Odwodnieniu najłatwiej ulegają pentozy, natomiast wśród heksoz ketozy. Disa-
charydy reagują wolniej niż monosacharydy, lecz szybciej od polisacharydów.
Furfural i 5-hydroksymetylenofurfural kondensują z różnymi fenolami, chino-
nami lub aminami aromatycznymi, tworząc różnobarwne połączenia, które wy-
korzystywane są do wykrywania, różnicowania i oznaczeń ilościowych cukrów.
H C
H C
H O
H O
C
C
H
H
H
C
O H
O H
O
H
H C
H C
C H
C
C
H
O
O
3 H
2
O
p ento za
furfural
H C
H C
C
C
C
H
O
O
C H
2
O H
H C
H C
H O
H O
C
C
H
H
C H
2
O H
C
O H
O H
H
O
3 H
2
O
he k s o za
5 - hyd ro k s ym e tyle no furfura l
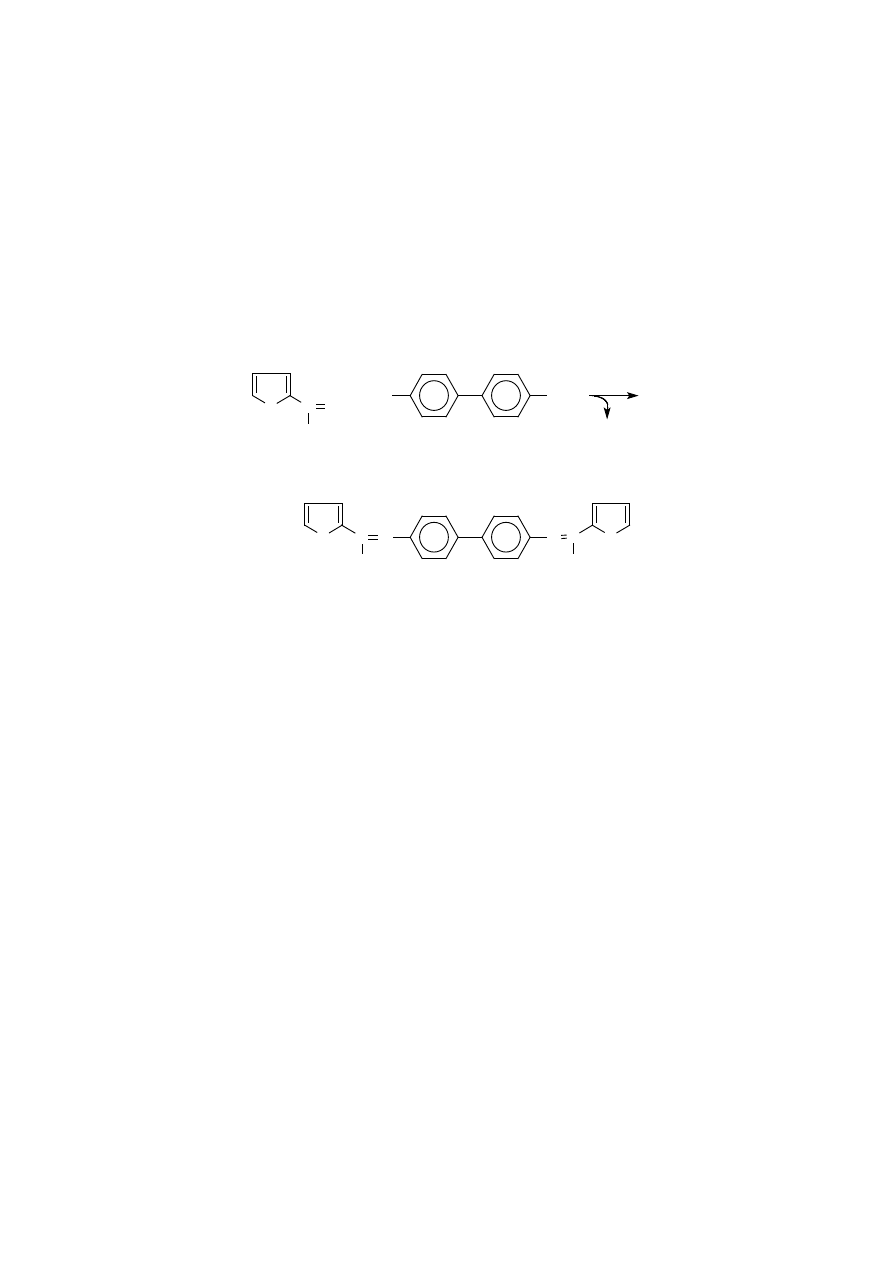
2
1. Odróżnianie pentoz od heksoz – reakcja Taubera
Zasada:
Furfural, powstający z pentozy pod wpływem lodowatego kwasu octowego,
kondensuje z benzydyną, dając produkt o barwie czerwonej. Heksozy w tych
warunkach dają zabarwienie żółte lub brunatne.
Wykonanie:
•
Przygotować dwie probówki zawierające po:
– 0,5 ml 4% roztworu benzydyny w lodowatym CH
3
COOH.
•
Dodać:
– 1 kroplę 0,5% roztworu ksylozy (lub rybozy) do pierwszej probówki,
– 1 kroplę 0,5% roztworu glukozy do drugiej probówki.
•
Obie próby ogrzać do wrzenia w łaźni wodnej, po czym natychmiast schłodzić
pod bieżącą wodą. Porównać wyniki reakcji w obu próbach.
2. Odróżnianie ketoz od aldoz – reakcja Seliwanowa
Zasada:
Ketozy w środowisku 12% roztworu HCl i po 30 sekundach ogrzewania są
przekształcone w 5-hydroksymetylenofurfural, natomiast w tych warunkach
aldozy pozostają niezmienione, pozwala to na zróżnicowanie heksoz. Wytwo-
rzony 5-hydroksymetylenofurfural kondensuje z rezorcyną, tworząc kompleks
o zabarwieniu czerwonowiśniowym. Bardzo ważne jest utrzymanie powyż-
O
C
H
O
2
H
2
N
NH
2
3 H
2
O
+
furfural
benzydyna
czerwony kompleks
N
O
C
H
N
C
H
O

3
szych warunków doświadczenia, zarówno stężenia kwasu solnego, jak i czasu
ogrzewania.
Zwiększenie stężenia roztworu HCl i wydłużenie czasu trwania ogrzewania
może spowodować, że aldozy ulegną podobnej przemianie, dając dodatni wynik
reakcji.
Wykonanie:
•
Przygotować dwie probówki, do których odmierzyć:
– do pierwszej probówki 1 ml 0,5% roztworu galaktozy (lub glukozy),
– do drugiej probówki 1 ml 0,5% roztworu fruktozy.
•
Do każdej próby dodać dokładnie po 0,5 ml stężonego HCl (otrzyma się roz-
twór o stężeniu 12%).
•
Próby ogrzewać we wrzącej łaźni wodnej przez 30 sekund, następnie schło-
dzić pod bieżącą wodą.
•
Do każdej próby dodać kryształek rezorcyny i ponownie ogrzać do wrzenia.
•
Porównać wyniki reakcji w obu próbach.
O
C
O
H
HO H
2
C
O H
HO
2
+
5- hydroksymetylenofurfural
rezorcyna
kompleks czerwono- wiśniowy
H
O
C
O
H
2
C
O H
HO
kompleks czerwonowiśniowy

4
ANALIZA JAKOŚCIOWA SKROBI
Zasada:
Strukturę skrobi tworzą dwa glukany, amyloza i amylopektyna. W roztworach
liniowy łańcuch amylozy zwija się w przestrzeni, tworząc lewoskrętną heliksę,
w której na jeden skręt przypada 6 reszt glukozy. Helikalną strukturę prze-
strzenną amylozy stabilizują wiązania wodorowe, powstające między wolnymi
grupami hydroksylowymi monocukrów.
3. Reakcja skrobi z jodem
Zasada:
Amyloza tworzy kompleks z jodem o barwie niebieskiej, którą zawdzięcza te-
mu, że ma strukturę uporządkowanej helisy, z pustym wnętrzem wypełnionym
jodem.
kompleks jodu z amylozą
Zabarwienie nie jest wynikiem reakcji chemicznej, lecz skutkiem uwięzienia
cząsteczek jodu wewnątrz helisy. Jod wewnątrz helisy znajduje się w odmien-
nym otoczeniu niż w roztworze i ma inną barwę. Barwa wynika z ruchu elek-
tronów wzdłuż łańcucha cząsteczek jodu, wypełniającego wnętrze helisy amy-
lozy oraz z pochłaniania światła przez cały kompleks. Natomiast podczas
ogrzewania helisa amylozy rozwija się, skutkiem zerwania wiązań wodoro-
wych, uwalniając uwięziony jod i barwa zanika. Amylopektyna z jodem daje
barwę fioletowoczerwoną. Natomiast skrobia z jodem daje zabarwienie fioleto-
woniebieskie.

5
Wykonanie:
•
Do probówki odmierzyć 1 ml 1% roztworu kleiku skrobiowego i dodać 1 kro-
plę rozcieńczonego roztworu jodu w jodku potasu (płynu Lugola o barwie
słomkowej). Zaobserwować powstałe zabarwienie.
•
Następnie próbę ogrzać do wrzenia na łaźni wodnej, zaobserwować, czy za-
barwienie znika.
•
Próbę schłodzić pod bieżącą wodą, zaobserwować, czy zabarwienie powraca.
ODCZYNNIKI
4% roztwór benzydyny w CH
3
COOH lodowatym; 0,5% roztwór ksylozy (lub
rybozy); 0,5% roztwór glukozy; 0,5% roztwór fruktozy; 0,5% roztwór galakto-
zy; stężony HCl; rezorycyna in subst.; 1% roztwór kleiku skrobiowego (1 g
skrobi zawiesić w 10 ml zimnej wody, po czym zawiesinę tę wlać do 80 ml
wrzącej wody – po rozpuszczeniu ostudzić i uzupełnić wodą do 100 ml); roz-
twór jodu w jodku potasu (płyn Lugola – 2 g KJ rozpuścić w 5 ml H
2
O i w tym
roztworze rozpuścić 1 g jodu, po czym uzupełnić wodą do 300 ml – jest to roz-
twór macierzysty, który przed użyciem rozcieńcza się 150 razy).
NOTATKI
Wyszukiwarka
Podobne podstrony:
07 Węglowodany, analiza jakościowa
Analiza jakościowa kationów i anionów, Analiza jakościowa
1 ćwiczenie (Analiza jakościowa wody) OZNACZANIE CHLORKÓW I SIARCZANÓW
Wybrane metody analizy jakościowej. Reakcje analityczne wybranych anionów, sprawka z chemi utp rok I
27 Kardas Prusak Gajek Analiza jakosci wyrobow
1 ćwiczenie (Analiza jakościowa wody) OZNACZANIE ZWIĄZKÓW AZOTU
analiza jakościowa kationów
Badanie właściwości i analiza jakościowa tłuszczów
1 ćwiczenie (Analiza jakościowa wody) PARAMETRY FIZYCZNE WODY
4.Analiza jakościowa kationów. Reakcja kationu manganu (Mn2+). NaOH, NH4OH, MnSO4., Państwowa Wyższa
cwiczenie 4 Analiza jakosciowa zwiazkow org
3 Analiza jakosciowa elektrolitow plynow ustrojowych
Analiza jakościowa aniony (2)
Elementy analizy jakosciowej kationy id 112043
analiza jakosciowa
27 12 10 01 12 07 egzamin analiza 2009 2
Labolatorium analizy jakosciowe Nieznany
więcej podobnych podstron