
Oznaczanie
Oznaczanie
kwasowości
kwasowości
Analiza żywności - ćwiczenia
Analiza żywności - ćwiczenia

W produktach roślinnych, a zwłaszcza
W produktach roślinnych, a zwłaszcza
w owocach, występują głównie
w owocach, występują głównie
hydroksykwasy, które oprócz
hydroksykwasy, które oprócz
kwaśności wykazują pewien właściwy
kwaśności wykazują pewien właściwy
im przyjemny posmak, a także
im przyjemny posmak, a także
obniżają wartość pH. Należą tu trzy
obniżają wartość pH. Należą tu trzy
główne kwasy:
główne kwasy:
jabłkowy,
jabłkowy,
cytrynowy,
cytrynowy,
winowy,
winowy,
oraz w mniejszych ilościach kwas
oraz w mniejszych ilościach kwas
bursztynowy, szczawiowy.
bursztynowy, szczawiowy.

W przeciwieństwie do owoców, w
W przeciwieństwie do owoców, w
których kwasy organiczne występują w
których kwasy organiczne występują w
postaci wolnej, w warzywach, z
postaci wolnej, w warzywach, z
wyjątkiem rabarbaru i pomidorów,
wyjątkiem rabarbaru i pomidorów,
kwasy występują w formie związanej, w
kwasy występują w formie związanej, w
postaci soli wapnia, potasu lub sodu.
postaci soli wapnia, potasu lub sodu.
Obecność kwasów w owocach i
Obecność kwasów w owocach i
warzywach stanowi przeszkodę dla
warzywach stanowi przeszkodę dla
rozwoju drobnoustrojów, a jednocześnie
rozwoju drobnoustrojów, a jednocześnie
ułatwia proces ich utrwalania.
ułatwia proces ich utrwalania.

Zawartość kwasów ogółem jest największa
Zawartość kwasów ogółem jest największa
w owocach niedojrzałych, a w okresie
w owocach niedojrzałych, a w okresie
dojrzewania (czy przechowywania) notuje
dojrzewania (czy przechowywania) notuje
się pewne obniżenie kwasowości.
się pewne obniżenie kwasowości.
Owoce dojrzałe wykazują kwasowość w
Owoce dojrzałe wykazują kwasowość w
granicach od 0,2% aż do 3% przy czym w
granicach od 0,2% aż do 3% przy czym w
ziarnkowych (jabłka, gruszki) jest ona
ziarnkowych (jabłka, gruszki) jest ona
rzędu 0,2-0,8%, w pestkowych 0,8-1,5%, w
rzędu 0,2-0,8%, w pestkowych 0,8-1,5%, w
jagodowych od 1% aż do 3%. Kwasowość
jagodowych od 1% aż do 3%. Kwasowość
cytryn może przekraczać nawet 5%.
cytryn może przekraczać nawet 5%.

W kwaśnych odmianach jabłek ponad 90%
W kwaśnych odmianach jabłek ponad 90%
kwasów ogółem przypada na kwas
kwasów ogółem przypada na kwas
jabłkowy, natomiast pozostałość stanowi
jabłkowy, natomiast pozostałość stanowi
kwas cytrynowy oraz inne kwasy. Podobny
kwas cytrynowy oraz inne kwasy. Podobny
skład kwasów występuje w śliwkach oraz
skład kwasów występuje w śliwkach oraz
czereśniach i wiśniach. W owocach
czereśniach i wiśniach. W owocach
jagodowych dominuje kwas cytrynowy, np.
jagodowych dominuje kwas cytrynowy, np.
w czarnych porzeczkach 21,5-28,2 mg/kg,
w czarnych porzeczkach 21,5-28,2 mg/kg,
w czerwonych porzeczkach 16,2-22,8
w czerwonych porzeczkach 16,2-22,8
mg/kg, w truskawkach 6,6-8,7 mg/kg.
mg/kg, w truskawkach 6,6-8,7 mg/kg.

Podobnie jak w owocach, w warzywach
Podobnie jak w owocach, w warzywach
dominującymi kwasami są jabłkowy i
dominującymi kwasami są jabłkowy i
cytrynowy, które najczęściej występują
cytrynowy, które najczęściej występują
w postaci jabłczanu i cytrynianu
w postaci jabłczanu i cytrynianu
potasowego.
potasowego.
Kwasowość warzyw jest dużo niższa niż
Kwasowość warzyw jest dużo niższa niż
owoców,
z
wyjątkiem
rabarbaru,
owoców,
z
wyjątkiem
rabarbaru,
którego kwasowość może wynosić 1,0-
którego kwasowość może wynosić 1,0-
1,4% (jako kwas jabłkowy).
1,4% (jako kwas jabłkowy).
W
innych
warzywach,
np.
w
W
innych
warzywach,
np.
w
pomidorach,
kapuście,
marchwi,
pomidorach,
kapuście,
marchwi,
kwasowość jest prawie dziesięciokrotnie
kwasowość jest prawie dziesięciokrotnie
mniejsza w porównaniu z rabarbarem.
mniejsza w porównaniu z rabarbarem.

Ponadto
warzywa
zawierają
Ponadto
warzywa
zawierają
niewielkie ilości innych kwasów, tj.
niewielkie ilości innych kwasów, tj.
kwasu bursztynowego, fumarowego,
kwasu bursztynowego, fumarowego,
chinowego,
izocytrynowego,
chinowego,
izocytrynowego,
szczawiowego. Inne nielotne kwasy,
szczawiowego. Inne nielotne kwasy,
jak:
malonowy,
akonitowy,
jak:
malonowy,
akonitowy,
szikimowy, występują rzadko i tylko
szikimowy, występują rzadko i tylko
w śladowych ilościach.
w śladowych ilościach.

Rodzaje kwasowości
Rodzaje kwasowości
Kwasowość czynna
Kwasowość czynna
, która wyraża się jako
, która wyraża się jako
stężenie jonów hydroniowych /H
stężenie jonów hydroniowych /H
3
3
O
O
+/
+/
lub
lub
tradycyjnie jonów wodorowych /H
tradycyjnie jonów wodorowych /H
+
+
/ w
/ w
roztworze. Ilościowo określa się ją jako
roztworze. Ilościowo określa się ją jako
pH = -log/ H
pH = -log/ H
3
3
O
O
+
+
/
/
lub –log/H
lub –log/H
+
+
/.
/.
Kwasowość czynna określa nam odczyn
Kwasowość czynna określa nam odczyn
roztworu
i
oznacza
się
ją
roztworu
i
oznacza
się
ją
potencjometrycznie lub kolorymetrycznie
potencjometrycznie lub kolorymetrycznie

Pehamter

Kwasowość
potencjalną
Kwasowość
potencjalną
/miareczkową ogólną lub całkowitą/,
/miareczkową ogólną lub całkowitą/,
która obejmuje całkowitą zawartość
która obejmuje całkowitą zawartość
jonów
wodorowych
ulegających
jonów
wodorowych
ulegających
reakcji
zobojętniania.
Można
ja
reakcji
zobojętniania.
Można
ja
oznaczyć
przez
miareczkowanie
oznaczyć
przez
miareczkowanie
mianowanym
roztworem
mianowanym
roztworem
wodorotlenku.
wodorotlenku.

Kwasowość lotną
Kwasowość lotną
, czyli zawartość
, czyli zawartość
jedynie
kwasów
lotnych,
które
jedynie
kwasów
lotnych,
które
ulegają
oddestylowaniu
z
para
ulegają
oddestylowaniu
z
para
wodną. Zasada oznaczania polega na
wodną. Zasada oznaczania polega na
zobojętnieniu
kwasów
lotnych
zobojętnieniu
kwasów
lotnych
uprzednio oddestylowanych z parą
uprzednio oddestylowanych z parą
wodną z badanej próbki przez
wodną z badanej próbki przez
miareczkowanie 0,1 M NaOH
miareczkowanie 0,1 M NaOH

W celu oddestylowania wszystkich
W celu oddestylowania wszystkich
kwasów /nawet związanych/ na
kwasów /nawet związanych/ na
próbkę należy podziałać kwasem
próbkę należy podziałać kwasem
ortofosforowym lub winowym.
ortofosforowym lub winowym.
Kwasowość lotną oznacza się np. w
Kwasowość lotną oznacza się np. w
sokach owocowo-warzywnych, winie,
sokach owocowo-warzywnych, winie,
melasie.
melasie.

Występowanie w tych produktach
Występowanie w tych produktach
lotnych kwasów oddestylowanych z
lotnych kwasów oddestylowanych z
para wodną jest wynikiem procesów
para wodną jest wynikiem procesów
fermentacyjnych wywołanych przez
fermentacyjnych wywołanych przez
bakterie /psucia się produktów/.
bakterie /psucia się produktów/.
Dlatego
też
zawartość
kwasów
Dlatego
też
zawartość
kwasów
lotnych stanowi kryterium jakości
lotnych stanowi kryterium jakości
produktu.
produktu.

Oznaczanie
kwasowości
Oznaczanie
kwasowości
miareczkowej
jest
ważne
dla
miareczkowej
jest
ważne
dla
produktów
żywnościowych,
które
produktów
żywnościowych,
które
posiadają właściwości buforujące /np.
posiadają właściwości buforujące /np.
mąka/, ponieważ w ich przypadku
mąka/, ponieważ w ich przypadku
kwasowość czynna nie w pełni
kwasowość czynna nie w pełni
charakteryzuje
ilość
związków
charakteryzuje
ilość
związków
kwaśnych.
kwaśnych.

Metody oznaczania
Metody oznaczania
kwasowości
kwasowości
Kwasowość wyraża się różnie w
Kwasowość wyraża się różnie w
zależności od gałęzi przemysłu
zależności od gałęzi przemysłu
spożywczego.
spożywczego.
W przemyśle zbożowo-młynarskim i
W przemyśle zbożowo-młynarskim i
piekarniczym pod pojęciem stopnia
piekarniczym pod pojęciem stopnia
kwasowości rozumie się taką ilość
kwasowości rozumie się taką ilość
kwasów w 100 g badanego produktu,
kwasów w 100 g badanego produktu,
która zobojetnia 1 cm
która zobojetnia 1 cm
3
3
1M NaOH
1M NaOH

W przemyśle gorzelniczym używa się
W przemyśle gorzelniczym używa się
stopni Delbr
stopni Delbr
ü
ü
cka /
cka /
o
o
D/.
D/.
Jeden stopień
Jeden stopień
Delbr
Delbr
ü
ü
cka odpowiada 1 cm
cka odpowiada 1 cm
3
3
1M
1M
NaOH zużytego do zobojętniania 20
NaOH zużytego do zobojętniania 20
cm
cm
3
3
próbki.
próbki.

W
przemyśle
mleczarskim
W
przemyśle
mleczarskim
kwasowość mleka i jego przetworów
kwasowość mleka i jego przetworów
określa się w
określa się w
stopniach Soxleta-
stopniach Soxleta-
Henkela /
Henkela /
o
o
SH/.
SH/.
Jeden stopień SH
Jeden stopień SH
wyraża taką ilość kwasów zawartych
wyraża taką ilość kwasów zawartych
w 100 cm
w 100 cm
3
3
mleka która zobojetnia 1
mleka która zobojetnia 1
cm
cm
3
3
0,25 M NaOH.
0,25 M NaOH.

W przemyśle mleczarskim używa się
W przemyśle mleczarskim używa się
także
także
stopni Soxleta /
stopni Soxleta /
o
o
S/.
S/.
Jeden
Jeden
stopień Soxleta odpowiada takiej
stopień Soxleta odpowiada takiej
ilości kwasów zawartych w 50 cm
ilości kwasów zawartych w 50 cm
3
3
mleka, która zobojętnia 1 cm
mleka, która zobojętnia 1 cm
3
3
0,25 M
0,25 M
NaOH.
NaOH.

Kwasowość mleka można podawać
Kwasowość mleka można podawać
również w
również w
stopniach Th
stopniach Th
ë
ë
rnera /
rnera /
o
o
T/.
T/.
1
1
o
o
T równa się takiej ilości kwasów
T równa się takiej ilości kwasów
zawartych w 100 cm
zawartych w 100 cm
3
3
mleka, która
mleka, która
zobojetnia 1 cm
zobojetnia 1 cm
3
3
0,1 M NaOH.
0,1 M NaOH.

Według Dornic’a kwasowość można
Według Dornic’a kwasowość można
wyrazić
w
procentach
kwasu
wyrazić
w
procentach
kwasu
mlekowego. Jeden
mlekowego. Jeden
stopień Dornica-
stopień Dornica-
Marshala /
Marshala /
o
o
DM/
DM/
równa się 0,1 cm
równa się 0,1 cm
3
3
0,111M NaOH na 100 cm
0,111M NaOH na 100 cm
3
3
mleka.
mleka.
W przeliczeniu uwzględnia się fakt, że
W przeliczeniu uwzględnia się fakt, że
1 cm
1 cm
3
3
zużyty do zobojętnienia 9 cm
zużyty do zobojętnienia 9 cm
3
3
mleka
odpowiada
0,01%
kwasu
mleka
odpowiada
0,01%
kwasu
mlekowego
mlekowego

Wykonanie analiz -
Wykonanie analiz -
przykłady
przykłady
Oznaczanie kwasowości czynnej /pH/
Oznaczanie kwasowości czynnej /pH/
metodą potencjometryczną
metodą potencjometryczną
Przed przystąpieniem do analizy należy nastawić
Przed przystąpieniem do analizy należy nastawić
pehametr za pomocą buforu o wartości pH
pehametr za pomocą buforu o wartości pH
zbliżonej do badanego produktu. Następnie
zbliżonej do badanego produktu. Następnie
przelać badana próbkę do naczynia pehametru
przelać badana próbkę do naczynia pehametru
lub do zlewki o poj. 50 cm
lub do zlewki o poj. 50 cm
3
3
i przystąpić do
i przystąpić do
oznaczenia pH.
oznaczenia pH.

Oznaczenie kwasowości
Oznaczenie kwasowości
miareczkowej w mleku
miareczkowej w mleku
Do kolby stożkowej o pojemności 250
Do kolby stożkowej o pojemności 250
ml odmierzyć 50 ml mleka, dodać 2 ml
ml odmierzyć 50 ml mleka, dodać 2 ml
2%
roztworu
fenoloftaleiny
i
2%
roztworu
fenoloftaleiny
i
miareczkować 0,25 M NaOH aż do
miareczkować 0,25 M NaOH aż do
otrzymania
lekko
różowego
otrzymania
lekko
różowego
zabarwienia utrzymującego się przez
zabarwienia utrzymującego się przez
30 s. wynik oznaczenia podać w
30 s. wynik oznaczenia podać w
stopniach: Soxleta, Soxleta-Henkela i
stopniach: Soxleta, Soxleta-Henkela i
Turnera.
Turnera.

Fenoloftaleina
Fenoloftaleina
(nazwa
chemiczna:
(nazwa
chemiczna:
dihydroksyftalofenon, wzór sumaryczny:
dihydroksyftalofenon, wzór sumaryczny:
C
C
20
20
H
H
14
14
O
O
4
4
) – organiczny związek chemiczny,
) – organiczny związek chemiczny,
stosowany głównie jako wskaźnik pH.
stosowany głównie jako wskaźnik pH.
W stanie czystym jest to bezbarwna
W stanie czystym jest to bezbarwna
substancja krystaliczna nierozpuszczalna
substancja krystaliczna nierozpuszczalna
w wodzie, rozpuszczalna w alkoholach. W
w wodzie, rozpuszczalna w alkoholach. W
laboratoriach spotykana jest głównie jako
laboratoriach spotykana jest głównie jako
ok. 1%, bezbarwny roztwór w etanolu.
ok. 1%, bezbarwny roztwór w etanolu.
Fenoloftaleina
jest
wskaźnikiem
Fenoloftaleina
jest
wskaźnikiem
alkacymetrycznym, tzn. zmienia formę z
alkacymetrycznym, tzn. zmienia formę z
bezbarwnej w środowisku kwaśnym lub
bezbarwnej w środowisku kwaśnym lub
obojętnym
na
malinowoczerwoną
w
obojętnym
na
malinowoczerwoną
w
środowisku zasadowym.
środowisku zasadowym.

Oznaczanie kwasowości potencjalnej w
Oznaczanie kwasowości potencjalnej w
przetworach owocowo-warzywnych
przetworach owocowo-warzywnych
Po dokładnym rozdrobnieniu i wymieszaniu
Po dokładnym rozdrobnieniu i wymieszaniu
produktu odważyć /z dokładnością 0,01 g/ 25 g
produktu odważyć /z dokładnością 0,01 g/ 25 g
próbki w zlewce o pojemności 250 ml, dodać ok.
próbki w zlewce o pojemności 250 ml, dodać ok.
100 ml wody destylowanej i zagrzać do wrzenia.
100 ml wody destylowanej i zagrzać do wrzenia.
Następnie roztwór oziębić i przenieść ilościowo do
Następnie roztwór oziębić i przenieść ilościowo do
kolby miarowej na 250 ml, dopełnić wodą do kreski i
kolby miarowej na 250 ml, dopełnić wodą do kreski i
po wymieszaniu pozostawić na 15 minut. Zawartość
po wymieszaniu pozostawić na 15 minut. Zawartość
kolby przesączyć przez fałdowany sączek. Pobrać
kolby przesączyć przez fałdowany sączek. Pobrać
10 ml przesączu do kolby stożkowej na 100 ml i
10 ml przesączu do kolby stożkowej na 100 ml i
miareczkować 0,1 M NaOH stosując jako wskaźnik
miareczkować 0,1 M NaOH stosując jako wskaźnik
dla
płynów
jasnych
3-4
krople
roztworu
dla
płynów
jasnych
3-4
krople
roztworu
fenoloftaleiny, natomiast dla płynów ciemnych użyć
fenoloftaleiny, natomiast dla płynów ciemnych użyć
papierka
wskaźnikowego
(miareczkowanie
papierka
wskaźnikowego
(miareczkowanie
zakończyć gdy kropla płynu miareczkowanego
zakończyć gdy kropla płynu miareczkowanego
naniesiona na papierek da zabarwienie identyczne z
naniesiona na papierek da zabarwienie identyczne z
barwa skali odpowiadającą pH 8)
barwa skali odpowiadającą pH 8)

Wynik podać w gramach odpowiedniego
Wynik podać w gramach odpowiedniego
kwasu na 100 g produktu wg wzoru:
kwasu na 100 g produktu wg wzoru:
a*m*K
a*m*K
X = --------------- * 100
X = --------------- * 100
g
g
a-objętość roztworu NaOH użytego do miareczkowania
a-objętość roztworu NaOH użytego do miareczkowania
m- molowość roztworu NaOH
m- molowość roztworu NaOH
g- ilość badanego produktu [g lub ml]
g- ilość badanego produktu [g lub ml]
K - współczynnik
K - współczynnik
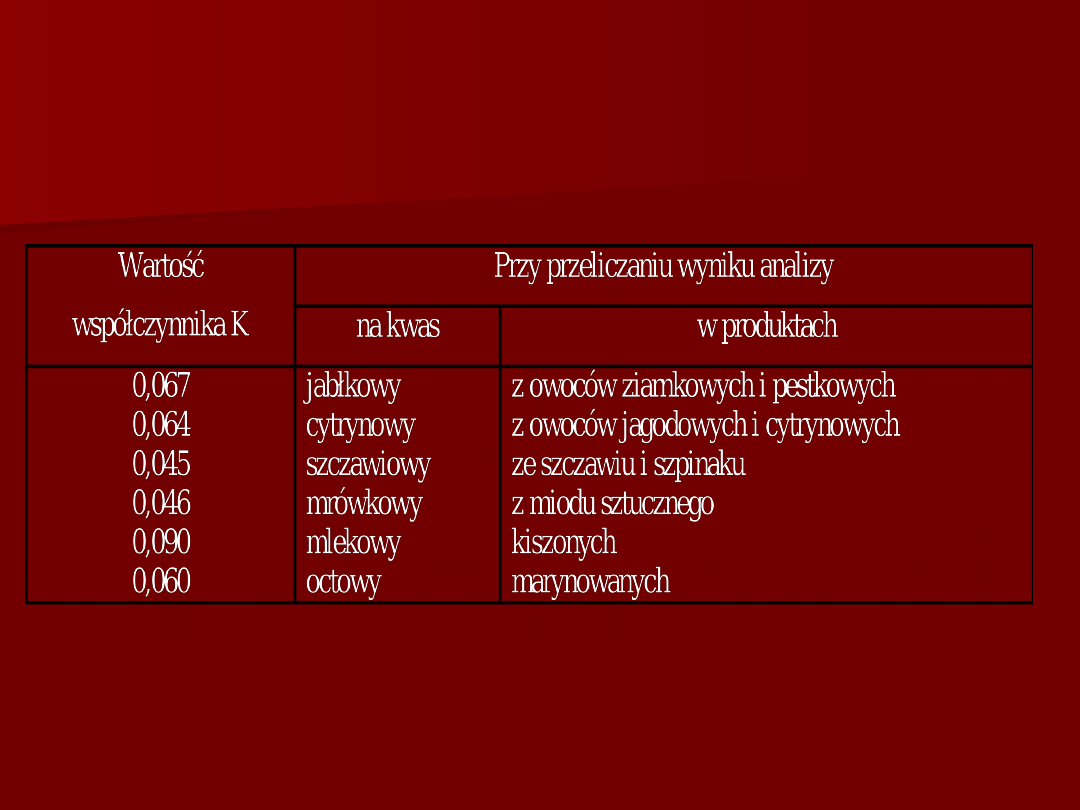
Tabela 1. Wartości współczynnika „K”
Tabela 1. Wartości współczynnika „K”
używanego przy oznaczaniu kwasowości
używanego przy oznaczaniu kwasowości
według PN-71/A-75101
według PN-71/A-75101

Oznaczanie kwasowości potencjalnej w
Oznaczanie kwasowości potencjalnej w
przetworach owocowo-warzywnych przez
przetworach owocowo-warzywnych przez
miareczkowanie potencjometryczne
miareczkowanie potencjometryczne
Po dokładnym rozdrobnieniu i wymieszaniu
Po dokładnym rozdrobnieniu i wymieszaniu
produktu odważyć /z dokładnością 0,01 g/ 25 g
produktu odważyć /z dokładnością 0,01 g/ 25 g
próbki w zlewce o pojemności 250 ml, dodać ok.
próbki w zlewce o pojemności 250 ml, dodać ok.
100 ml wody destylowanej i zagrzać do wrzenia.
100 ml wody destylowanej i zagrzać do wrzenia.
Następnie roztwór oziębić i przenieść ilościowo do
Następnie roztwór oziębić i przenieść ilościowo do
kolby miarowej na 250 ml, dopełnić wodą do kreski i
kolby miarowej na 250 ml, dopełnić wodą do kreski i
po wymieszaniu pozostawić na 15 minut. Zawartość
po wymieszaniu pozostawić na 15 minut. Zawartość
kolby
przesączyć
przez
fałdowany
sączek.
kolby
przesączyć
przez
fałdowany
sączek.
Następnie do zlewki o pojemności 100 ml wlać
Następnie do zlewki o pojemności 100 ml wlać
badany roztwór, zanurzyć w nim elektrody
badany roztwór, zanurzyć w nim elektrody
potencjometru i po uruchomieniu mieszadła
potencjometru i po uruchomieniu mieszadła
elektromagnetycznego
włączyć
potencjometr.
elektromagnetycznego
włączyć
potencjometr.
Miareczkować 0,1 M NaOH do pH 6 dość szybko, a
Miareczkować 0,1 M NaOH do pH 6 dość szybko, a
następnie powoli kroplami do pH 8,1 ±0,05.
następnie powoli kroplami do pH 8,1 ±0,05.
Kwasowość ogólną wyrazić w gramach kwasu /w
Kwasowość ogólną wyrazić w gramach kwasu /w
zależności od produktu/ na 100 g lub 100 ml
zależności od produktu/ na 100 g lub 100 ml
produktu wg wcześniejszego wzoru.
produktu wg wcześniejszego wzoru.

Oznaczanie kwasowości lotnej w
Oznaczanie kwasowości lotnej w
winie
winie
Do kolby płaskodennej o poj. 250 ml
Do kolby płaskodennej o poj. 250 ml
odmierzyć pipetą 50 ml wina i zagęścić go do
odmierzyć pipetą 50 ml wina i zagęścić go do
połowy nad małym płomieniem. Następnie
połowy nad małym płomieniem. Następnie
podłączyć kolbę do zestawu do destylacji z
podłączyć kolbę do zestawu do destylacji z
parą wodną i prowadzić destylację do
parą wodną i prowadzić destylację do
otrzymania około 200 ml destylatu /ok. 1h/.
otrzymania około 200 ml destylatu /ok. 1h/.
Otrzymany destylat ogrzać do wrzenia, dodać
Otrzymany destylat ogrzać do wrzenia, dodać
3-4
krople
roztworu
fenoloftaleiny
i
3-4
krople
roztworu
fenoloftaleiny
i
miareczkować 0,1M NaOH do lekko różowego
miareczkować 0,1M NaOH do lekko różowego
zabarwienia utrzymującego się przez 30s.
zabarwienia utrzymującego się przez 30s.
Wynik wyrazić w gramach kwasu na 1 litr
Wynik wyrazić w gramach kwasu na 1 litr
wina.
wina.
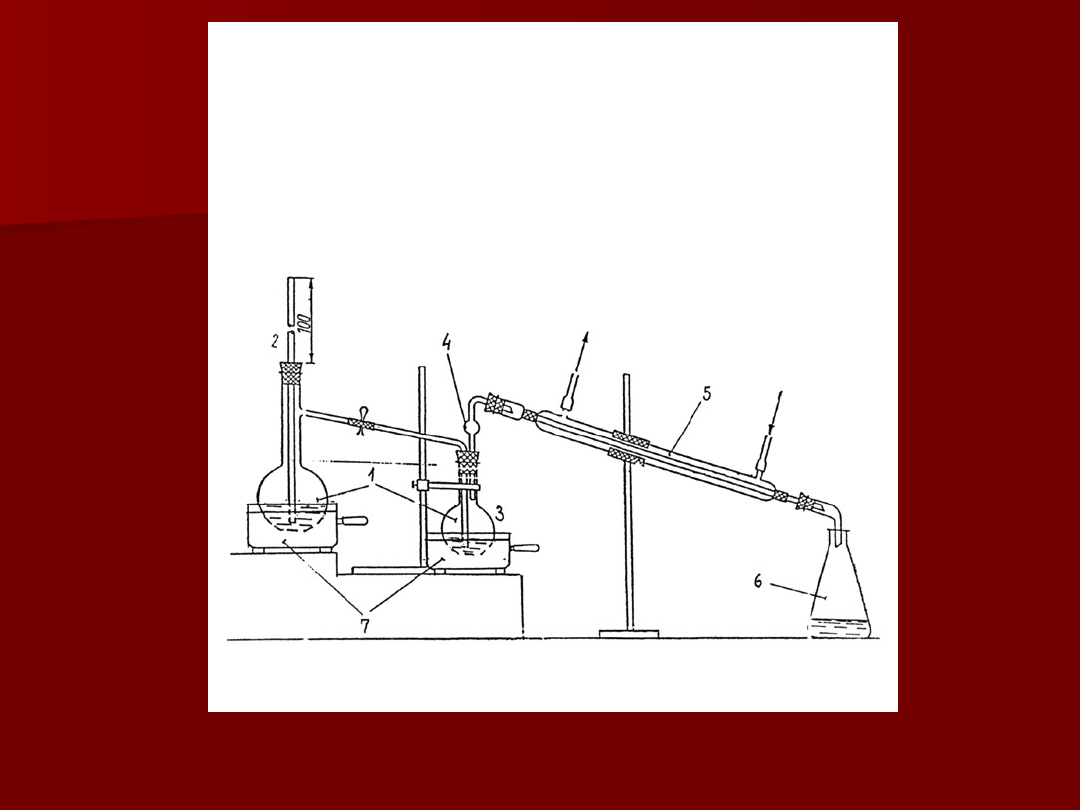
1- wytwornica pary, 2-rurka ciśnieniowa, 3-kolba destylacyjna (próbek), 4-
deflegmator, 5- chłodnica, 6- odbieralnik kwasu lotnego 7-łaźnia elektryczna
Kolba płaskodenna
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
Wyszukiwarka
Podobne podstrony:
Oznaczanie kwasowości Wymiennej i Glinu Wymiennego metodą So, gleboznawstwo
3 Oznaczanie kwasowooci wymienn Nieznany (2)
Oznaczanie zawartości wody i suchej masy, oznaczanie kwasowości, oznaczanie zawartości białek i tłus
Oznaczanie kwasowosci, O Z N A C Z A N I E K W A S O W O Ś C I P R O D U K T Ó W
Oznaczanie kwasowości wybranych produktów spożywczych
Analiza ilościowa-objętościowe oznaczanie kwasów i zasad, Energetyka, I rok, chemia
sprawozdanie oznaczanie kwasowości, 2 rok, analiza
2. Oznaczanie kwasowości miareczkowej soku owocowego met odą potecjometryczną, Oznaczanie kwasowości
Oznaczanie kwasowości, Tż, Analiza żywności II, Sprawozdania
Oznaczenie kwasowoci i zasadowoci wody wodocigowej
Oznaczenie kwasowości, inżynieria ochrony środowiska kalisz, Analiza Chemiczna Wody i Ścieków
Oznaczanie kwasowości wymiennej hydrolitycznej potrzeb wapnowania zakwaszania
Oznaczenie kwasowości i zasadowości
Ocena jakosci, cwiczenia6, Oznaczanie kwasowości ogólnej w produkcji ogrodniczej
Oznaczanie kwasowości
Oznaczanie kwasowości Wymiennej i Glinu Wymiennego metodą So, gleboznawstwo
Oznaczanie kwasowości miareczkowej soków owocowych
więcej podobnych podstron