
BIODEGRADACJA

5.05.21
2
BIODEGRADACJA
•
Wszystko co powstało w drodze biosyntezy
ulega biodegradacji
•
Adaptacja ekosystemu do biodegradacji
związków ropopochodnych i polimerów
syntetycznych – kilkadziesiąt lat

5.05.21
3
PODSTAWOWE POJĘCIA
•
Degradacja
•
nieodwracalny proces wskutek którego materiał
ulega zmianom fizycznym i chemicznym
prowadzącym do wzrostu entropii
•
Biodegradacja
•
degradacja katalizowana przez układy
biologiczne, prowadząca do mineralizacji i/lub
produkcji biomasy

5.05.21
4
PODSTAWOWE POJĘCIA
•
Mineralizacja
•
konwersja substancji organicznych do naturalnie
występujących substancji nieorganicznych
•
Biodegradowalność
•
zdolność materiału do ulegania biodegradacji
•
określana za pomocą specyficznych testów

5.05.21
5
TYPY TECHNICZNYCH PROCESÓW
ROZKŁADU ZANIECZYSZCZEŃ
•
Tlenowe:
•
metoda osadu czynnego
•
Beztlenowe
•
fermentacja metanowa
•
otrzymywanie wodoru

5.05.21
6
TYPY TECHNICZNYCH PROCESÓW
ROZKŁADU ZANIECZYSZCZEŃ
•
Tlenowe:
•
metoda osadu czynnego
•
Beztlenowe
•
fermentacja metanowa
•
otrzymywanie wodoru

5.05.21
7
TLENOWE I BEZTLENOWE PROCESY
BIODEGRADACJI
•
Proces tlenowy:
C
x
H
y
O
z
+ O
2
CO
2
+ H
2
O + biomasa
•
Proces beztlenowy
C
x
H
y
O
z
CH
4
+ CO
2
+ H
2
O + biomasa

METODA OSADU CZYNNEGO
•
Polega zasadniczo na:
•
napowietrzaniu osadu czynnego wraz ze
ściekami w komorach napowietrzania,
•
oddzieleniu osadu od oczyszczonych już ścieków
w osadniku wtórnym.
•
Proces trwa kilka-kilkunacie godzin.
5.05.21
8
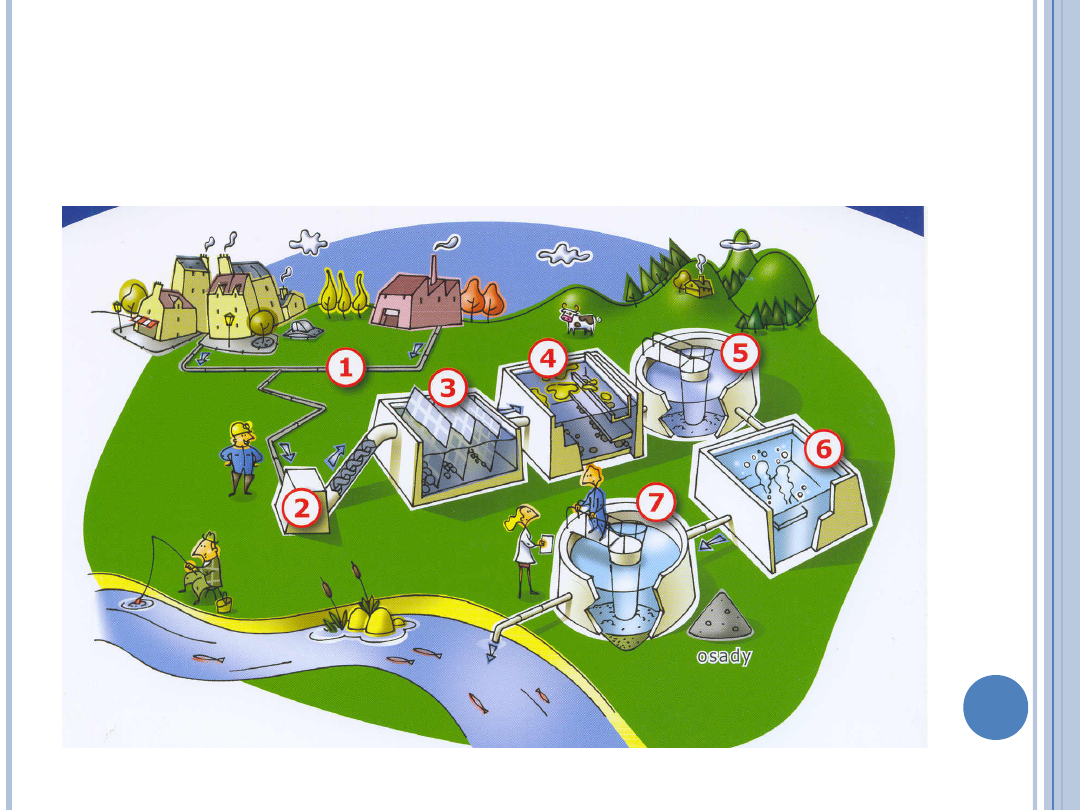
ETAPY OCZYSZCZANIA ŚCIEKÓW

ETAPY OCZYSZCZANIA ŚCIEKÓW
•
oczyszczanie mechaniczne
•
oczyszczanie biologiczne
•
separacja i przeróbka osadów ściekowych
tzw. osadu nadmiernego
5.05.21
10

OCZYSZCZANIE MECHANICZNE
•
kraty
•
usuwanie ze ścieków elementów stałych o
stosunkowo dużych rozmiarach
•
piaskowniki
•
usuwanie drobniejszych cząstek stałych,
głównie mineralnych
•
osadnik wstępny
•
zatrzymywanie zawiesin łatwo
sedymentujących
•
usuwanie cząstek lżejszych od wody (np.
tłuszczów)

OCZYSZCZANIE BIOLOGICZNE
•
komora napowietrzania
•
następuje utlenianie związków organicznych
zawartych w ściekach; doprowadzane powietrze
ścieki i osad czynny w stałym ruchu
•
osadnik wtórny
•
oddzielenie kłaczków osadu czynnego od
oczyszczonych ścieków, część osadzonego osadu
czynny jest zawracana do komór napowietrzania
•
w procesie tym następuje ciągły przyrost
mikroorganizmów wtórnych jako tzw. osad
nadmierny
•
osad nadmierny musi być przerabiany
.
5.05.21
12

5.05.21
13
TLENOWE METODY OCZYSZCZANIA
ŚCIEKÓW
•
Metoda osadu czynnego
•
Osad czynny - kłaczkowata zawiesina złożona
głównie z bakterii i pierwotniaków.
•
Kłaczki osadu czynnego (makroskopowych rozmiarów
skupiska bakterii) charakteryzują się dużą
powierzchnią czynną i w konsekwencji są zdolne do
sorbowania substancji zawartych w ściekach.

PRZERÓBKA OSADÓW
•
Jest prowadzona aż do mementu kiedy w
składowanych osadach nie zachodzą procesy
metaboliczne, a temperatura jest równa
temperaturze otoczenia
•
fermentacja beztlenowa
•
kompostowanie
•
osad nadmierny stanowi 40-60% materii
organicznej poddawanej przeróbce tlenowej
•
ze ścieków milionowego miasta powstaje
codziennie prawie 40 ton osadu nadmiernego
5.05.21
14

PRZERÓBKA BIOGENÓW
•
Azot i fosfor
•
Azot
•
metoda nitryfikacji i denitryfikacji
•
następuje biologiczne utlenianie związków azotowych
do azotanów, a następnie ich redukcja to gazowego
azotu
•
nitryfikacja wymaga warunków tlenowych
•
Nitrosomonas spp. utleniają azot amonowy do azotynów
•
Nitrobacter spp. i Nitrospira spp. utleniają azotyny do
azotanów
5.05.21
15
AZOT
•
Nitryfikacja
NH
4+
+ 1,5 O
2
NO
2-
+ 2H
+
+ 2H
2
O
NO
2-
+ 0,5 O
2
NO
3-
•
Denitryfikacja
NO
3-
+ 10H
+
+ 10e N
2
+ 2OH
-
+ 4H
2
O
NO
2-
+ 6H
+
+ 10e N
2
+ 2OH
-
+ 2H
2
O
5.05.21
16

FOSFOR
•
Bakterie akumulujące fosfor magazynują go
aż do zawartości 20%
•
następnie są oddzielane od oczyszczanej wody i
stosowane jako nawóz
•
Niekiedy jest konieczne usuwanie chemiczne
przez wytrącanie nierozpuszczanych soli
żelaza lub glinu
5.05.21
17

KOMPOSTOWANIE
•
Egzotermiczny, tlenowy, rozkład wilgotnych
substancji organicznych zachodzący z
udziałem mikroorganizmów
•
Stanowi intensyfikację naturalnych procesów
naturalnego rozkładu tlenowego
•
W jego wyniku tworzy sie tzw. humus
zawierający kwasy fulwowe, kwasy
huminowe, huminy oraz zwiększone ilości zw.
azotu i fosforu
5.05.21
18

HUMUS
•
Próchnica, humus - bezpostaciowe,
organiczne szczątki w różnym stadium
mikrobiologicznego i fizykochemicznego
rozkładu, głównie roślinne, nagromadzone w
glebie lub na jej powierzchni
•
Humus - supramolekularna struktura relatywnie
niskocząsteczkowych biomolekuł (M<1000
).
Najbardziej trwała frakcja gleby (trwała w czasie
dziesiątków, setek a nawet tysięcy lat). Ciemna
barwa pochodzi od struktur chinonowych
zamkniętych w domenach hydrofobowych.
5.05.21
19

FAZY KOMPOSTOWANIA
Wstępne kompostowanie
Intensywne kompostowanie
Kompostowanie właściwe
Dojrzewanie kompostu
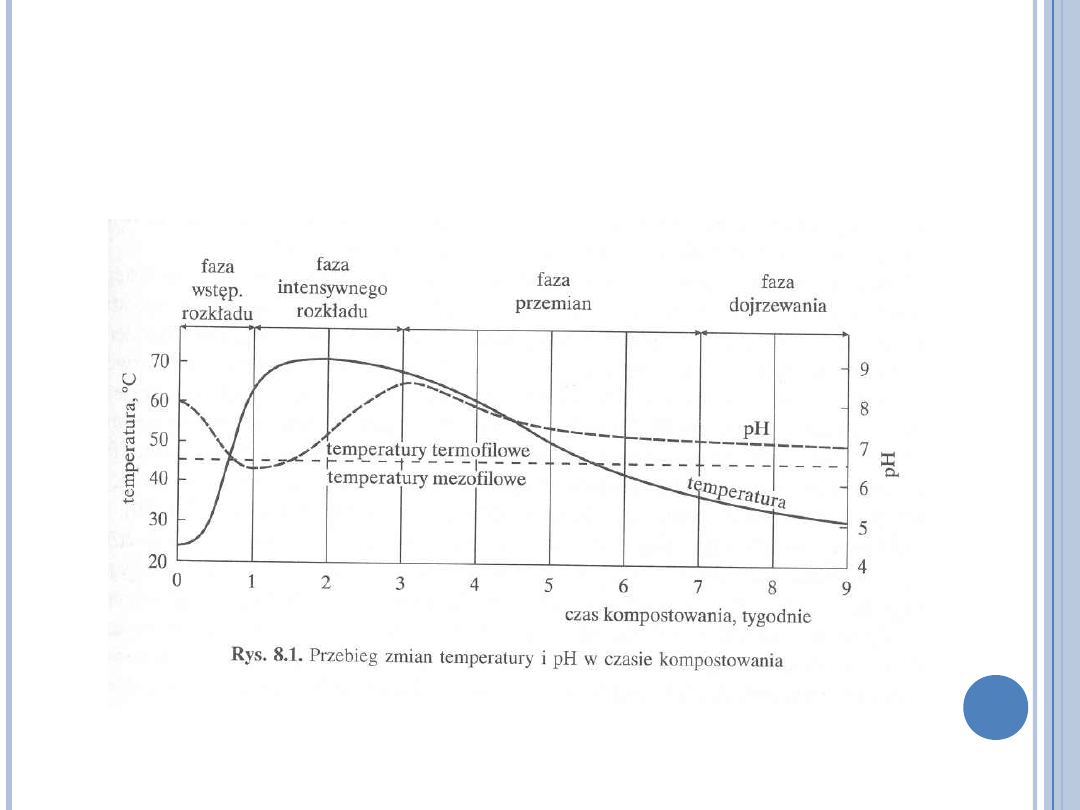
FAZY KOMPOSTOWANIA
(A. JĘDRCZAK, BIOLOGICZNE PRZETWARZANIE
ODPADÓW, PWN 2007)
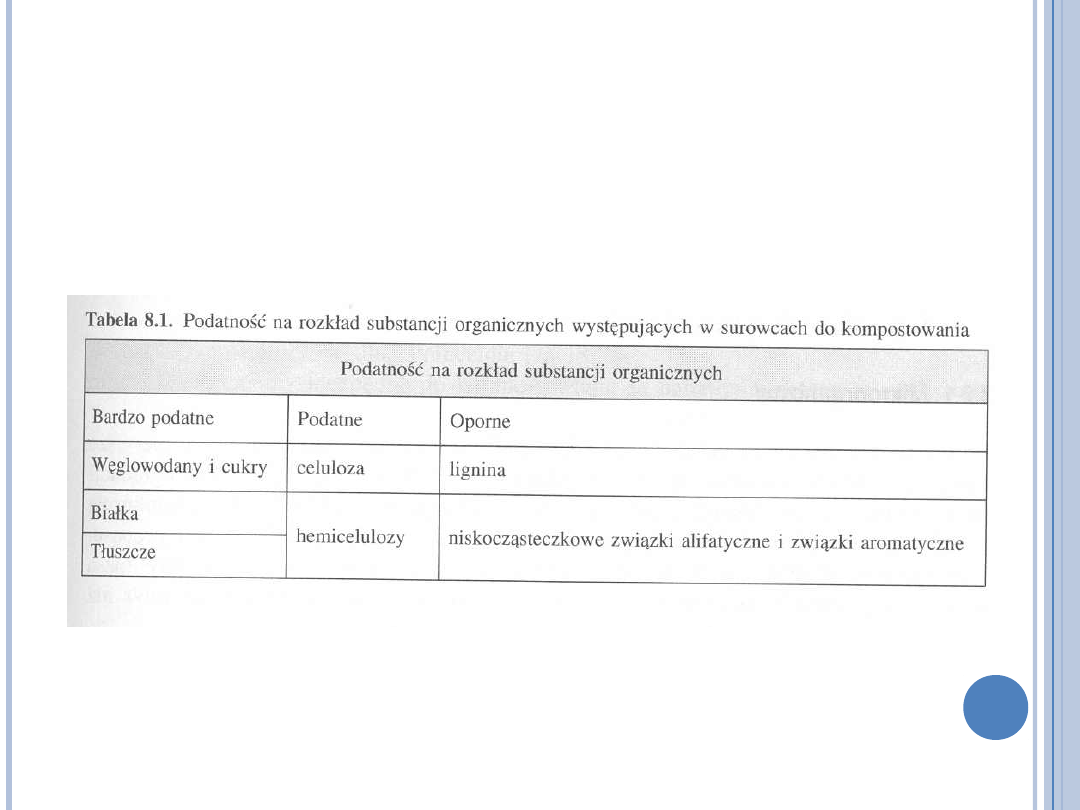
PODATNOŚĆ NA KOMPOSTOWANIE
(A.
JĘDRCZAK, BIOLOGICZNE PRZETWARZANIE ODPADÓW, PWN 2007)
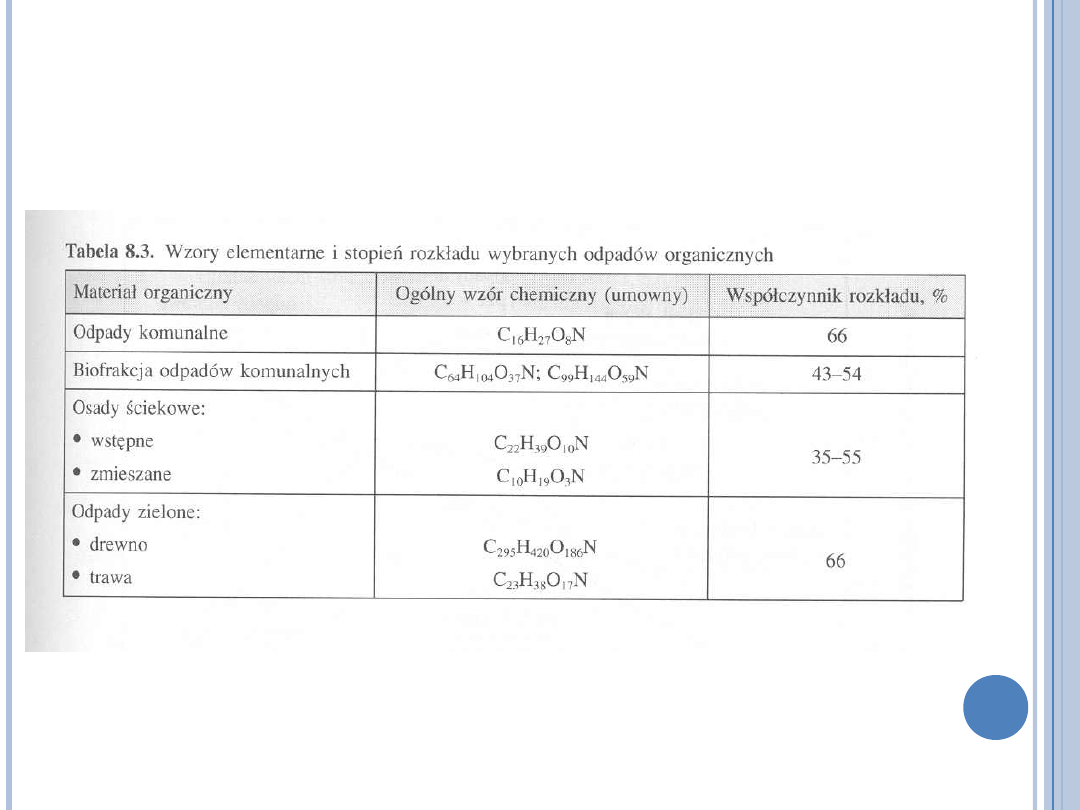
PODATNOŚĆ NA KOMPOSTOWANIE
(A.
JĘDRCZAK, BIOLOGICZNE PRZETWARZANIE ODPADÓW, PWN 2007)
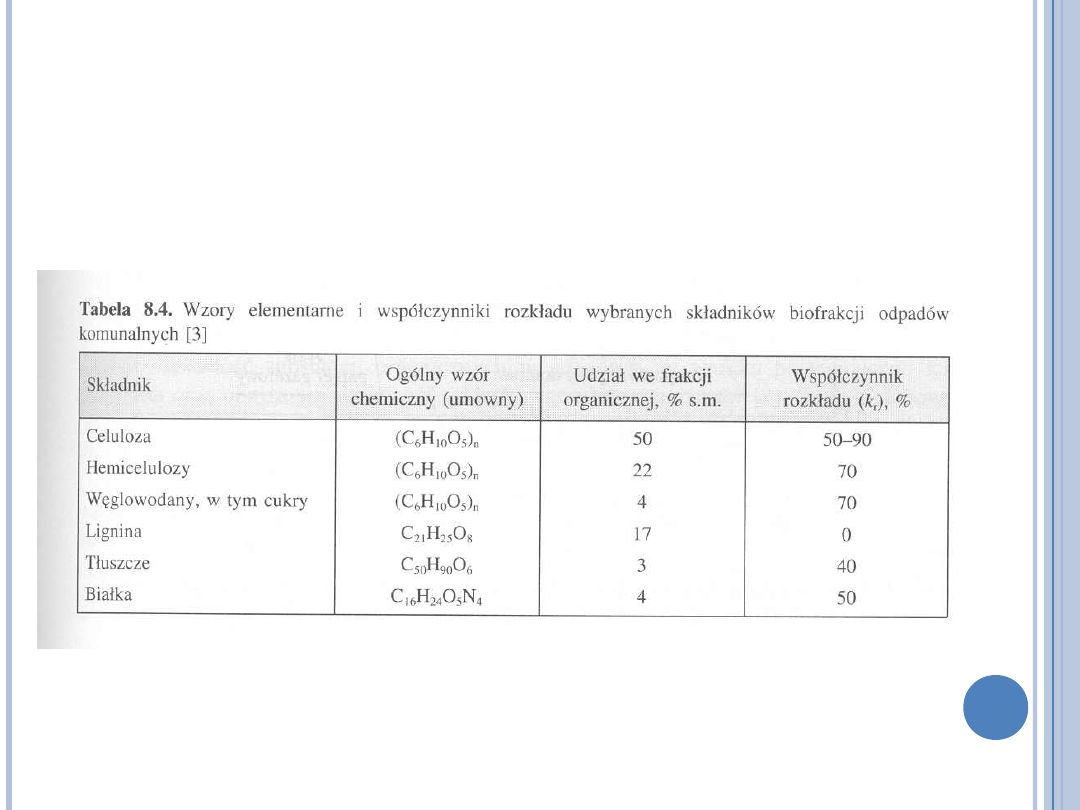
PODATNOŚĆ NA KOMPOSTOWANIE
(A.
JĘDRCZAK, BIOLOGICZNE PRZETWARZANIE ODPADÓW, PWN 2007)
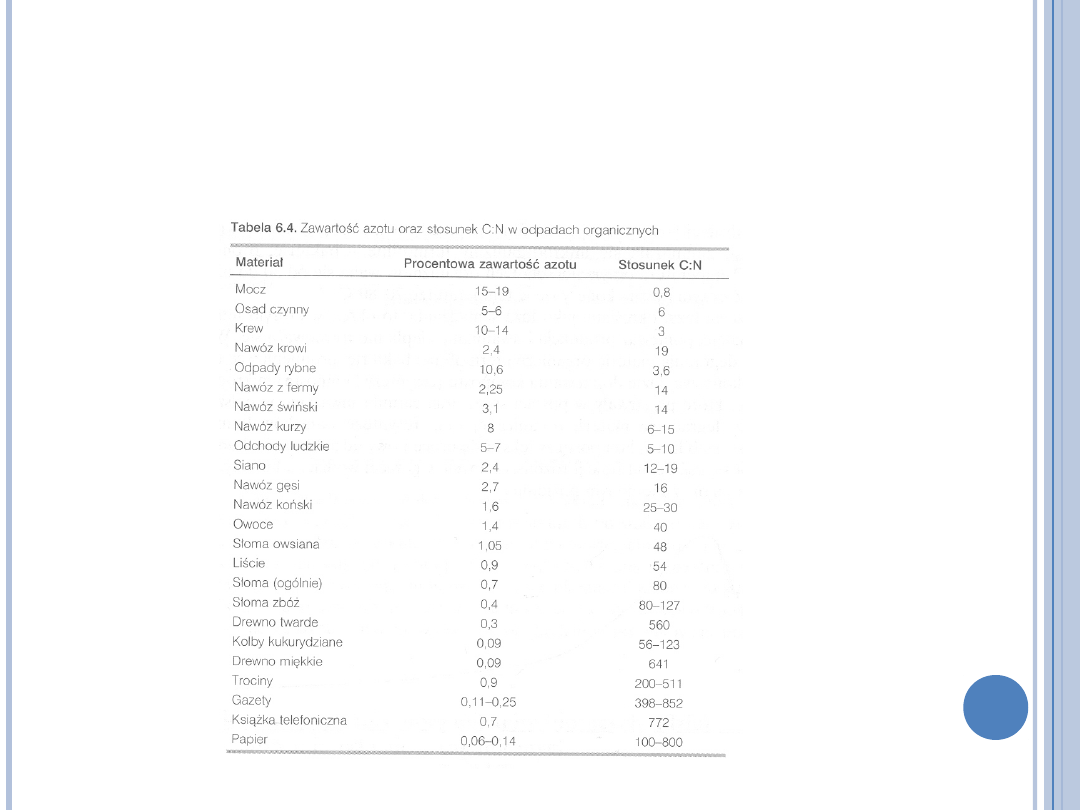
PRZYDATNOŚĆ ODPADÓW
ORGANICZNYCH DO
KOMPOSTOWANIA
(M.K. BŁASZCZYK MIKROORGANIZMY W OCHRONIE ŚRODOWISKA
PWN 2007)
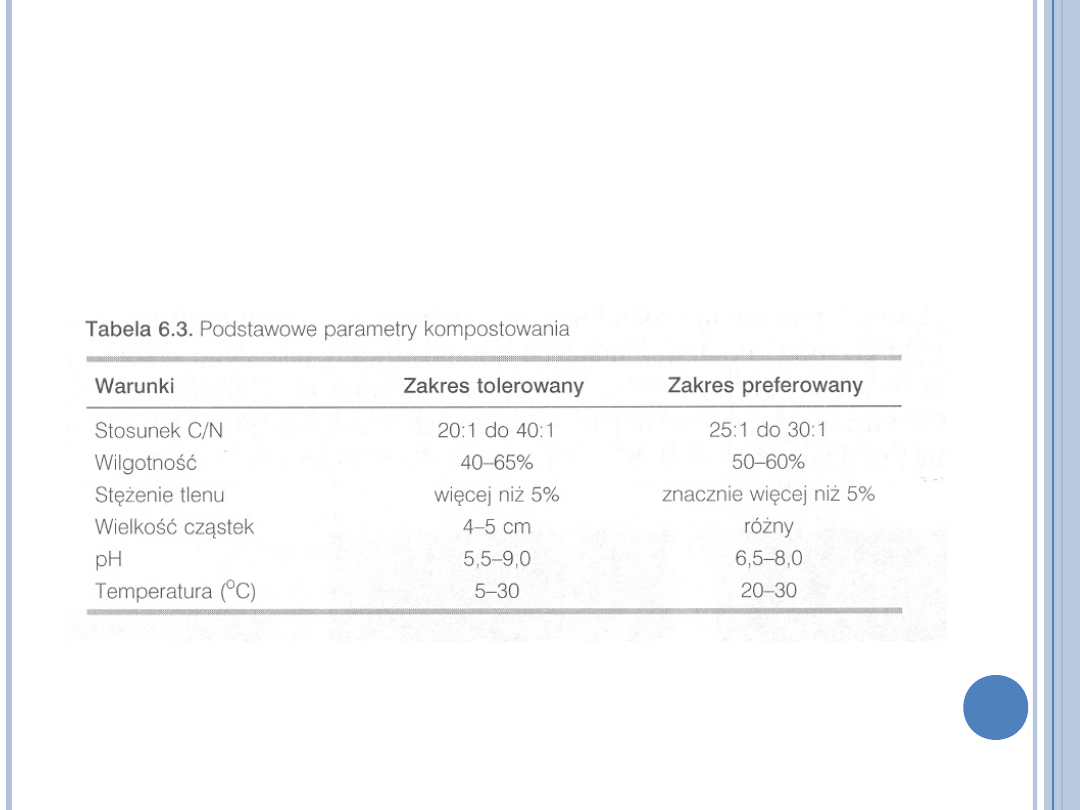
WARUNKI PROCESU
KOMPOSTOWANIA
(M.K. BŁASZCZYK MIKROORGANIZMY W OCHRONIE ŚRODOWISKA PWN
2007)

MIKROORGANIZMY W PROCESIE
KOMPOSTOWANIA
Bakterie
Promieniowce
odgrywają dużą rolę w przetwarzaniu związków
trudnorozkładalnych (celuloza, chityna)
są odpowiedzialne za ziemisty zapach kompostu
Grzyby
Pierwotniaki
odgrywają rolę drugorzędną, są elementami
łańcucha pokarmowego
Wrotki
występują w miejscach o podwyższonej
wilgotności, są elementami łańcucha pokarmowego
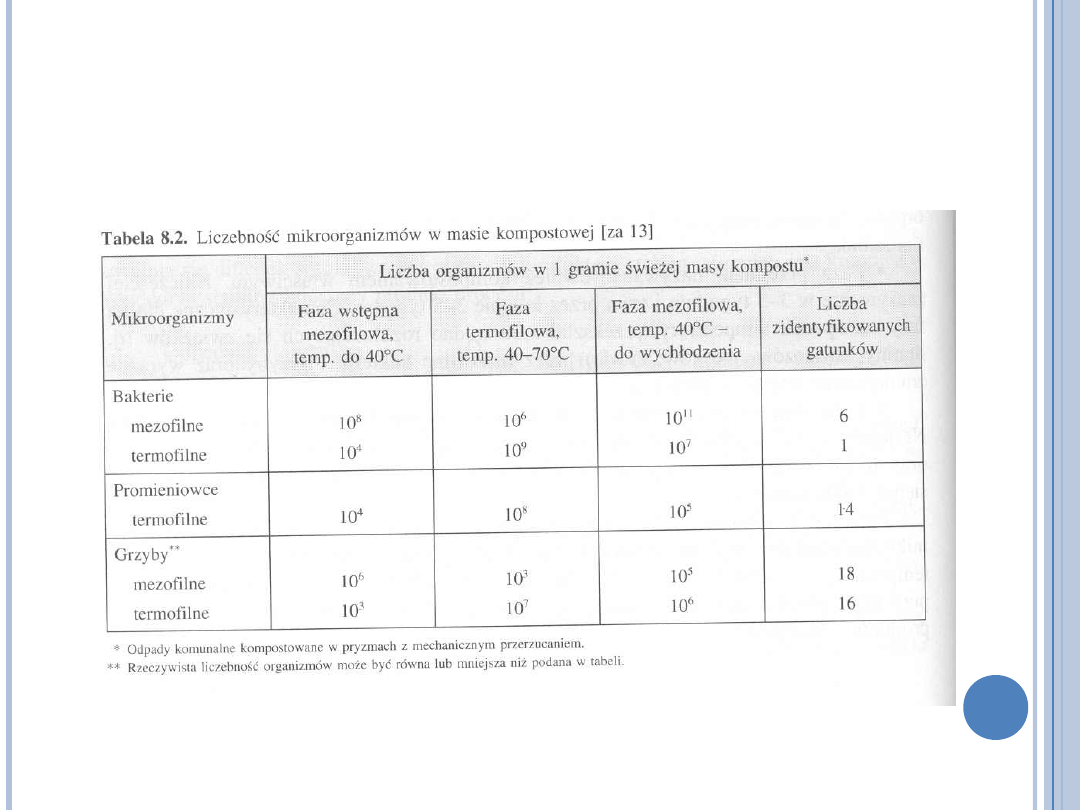
MIKROORGANIZMY W PROCESIE
KOMPOSTOWANIA

KOMPOST
Nawóz organiczny wytwarzany z odpadów
roślinnych i zwierzęcych w wyniku częściowego
rozkładu tlenowego realizowanego przez
mikroorganizmy
Cechy dobrego kompostu:
ciemna barwa
zapach ziemisty
jednolite uziarnienie
wilgotność 25-35%
pH 6,0-7,8
niska zawartość metali ciężkich, małe stężenie soli
rozpuszczalnych, brak organizmów
chorobotwórczych oraz aktywnych nasion chwastów

KORZYŚCI ZE STOSOWANIA
KOMPOSTU
Podwyższenie zawartości węgla organicznego
w glebie
Zwiększenie aktywności biologicznej gleby
Poprawa struktury gleby
zwiększenie pojemności wodnej gleb
piaszczystych
ułatwienie przepływu wody i powietrza w glebach
ciężkich

KLASYFIKACJA KOMPOSTU
Świeży:
materiał wyjałowiony w procesie intensywnego
kompostowania
zawiera dużo substancji organicznych (C:N = 25-
30:1)
może negatywnie oddziaływać na system korzeniowy
roślin
Dojrzały:
powstały z kompostu świeżego przez dalsze
kompostowanie
zawiera mniej substancji organicznych (C:N nie
powinien być niższy niż 15:1)

JAKOŚĆ KOMPOSTU
Dobry – otrzymywany z selektywnie
zbieranych bioodpadów i odpadów zielonych
Niskiej jakości – otrzymywany ze
zmieszanych odpadów komunalnych –
brak
zbytu!!!

STABILNOŚĆ I DOJRZAŁOŚĆ
KOMPOSTU
Stabilizacja kompostu – stopień
przekształcenia (utlenienia) substancji
organicznych w formy bardziej stabilne
Dojrzałość – przydatność do końcowego
wykorzystania
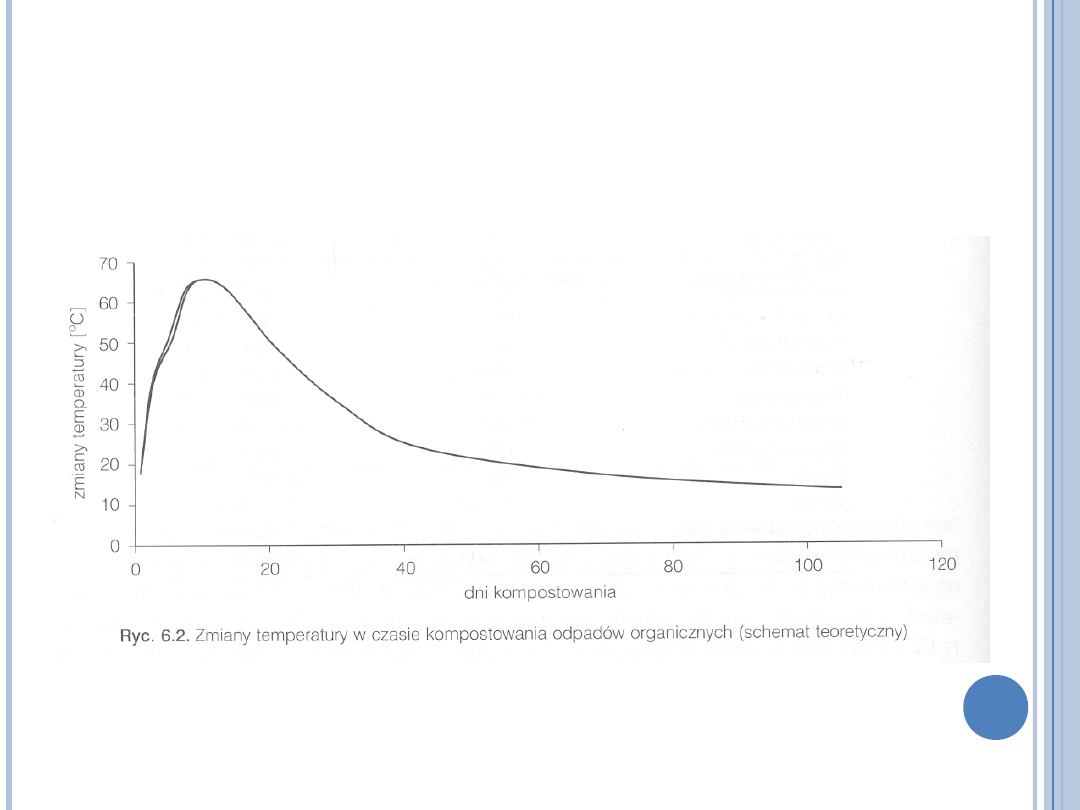
KINETYKA KOMPOSTOWANIA
(M.K. BŁASZCZYK
MIKROORGANIZMY W OCHRONIE ŚRODOWISKA PWN 2007)
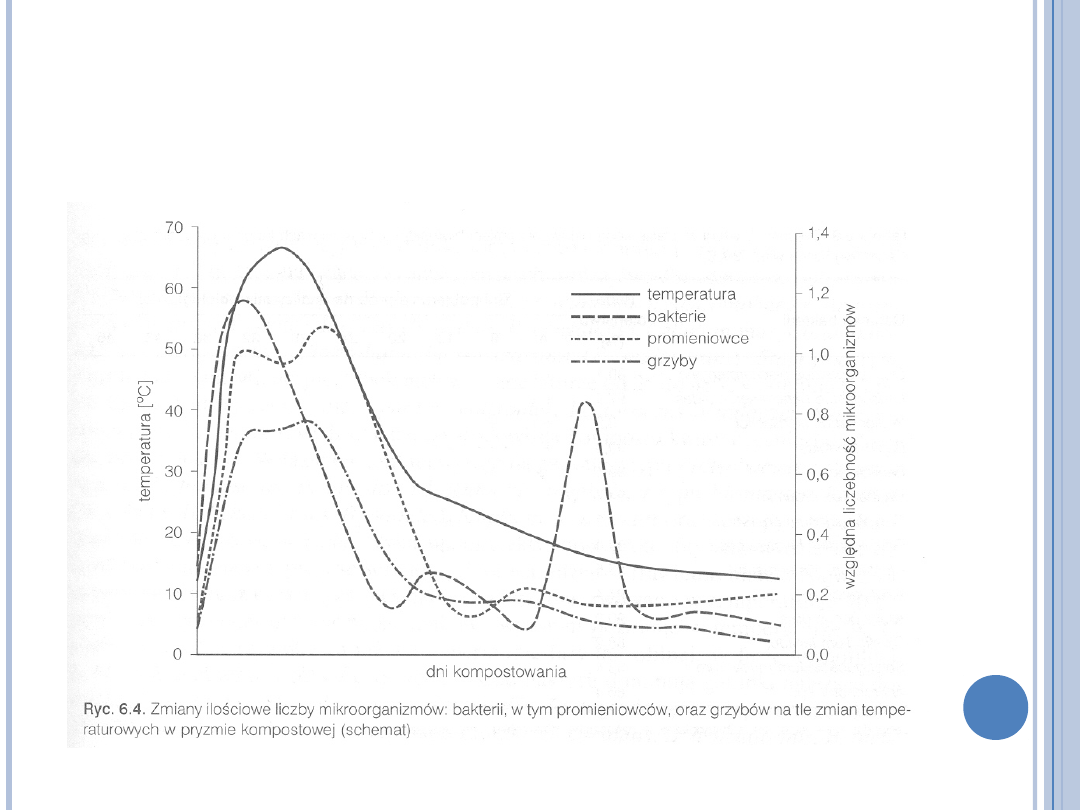
KINETYKA KOMPOSTOWANIA
(M.K. BŁASZCZYK
MIKROORGANIZMY W OCHRONIE ŚRODOWISKA PWN 2007)

BILANS KOMPOSTOWANIA
(M.K. BŁASZCZYK MIKROORGANIZMY W
OCHRONIE ŚRODOWISKA PWN 2007)

NIESPECYFICZNE METODY
ANALITYCZNE OCENY
BIODEGRADOWALNOŚCI
•
Pomiar spadku:
•
ChZT
•
BZT
•
RWO
•
Pomiar ilości wytworzonego CO
2
•
Obliczenie TZT

5.05.21
38
CHEMICZNE ZAPOTRZEBOWANIE
TLENU - CHZT
•
Ilość tlenu, wyrażona w mg/dm
3
, równoważna
ilości utleniacza chemicznego, tj.
dichromianu potasu lub nadmanganianu
potasu zużytego na utlenienie związków
organicznych

CHEMICZNE ZAPOTRZEBOWANIE
TLENU - CHZT
•
Założeniem jest iż niemal wszystkie
substancje organiczne mogą być w pełni
utlenione do dwutlenku węgla
•
nie uwzględnia utleniania azotu
•
po procesie utleniania azot uwalnia sie w postaci
amoniaku
•
wynik podaje sie najczęściej jako ilość mg O
2
/dm
3
5.05.21
39

CHEMICZNE ZAPOTRZEBOWANIE
TLENU - CHZT
C
x
H
y
O
z
N
n
+ (x + y/4 - z/2 – 3/4n) O
2
xCO
2
+ (y/2 – 3n/2) H
2
O + nNH
3
Nitryfikacja
NH
3
+ 2O
2
HNO3 + H
2
O
5.05.21
40

OZNACZANIE CHZT PRZY POMOCY
DICHROMIANU POTASU
C
x
H
y
O
z
N
n
+ mCr
2
O
7-2
+ (8m + n)H
+
xCO
2
+ (y + 8n – 3n)/2 H
2
O + nNH
4+
+2mCr
+3
•
stosuje się najczęściej 0,25 N roztwór
dichromianu potasu
•
stężenie dwuchromianu potasu zależy od spodziewanego
COD. Dla COD poniżej 50 mg/l stosuje się stężenia niższe
•
roztwór zakwasza się kwasem siarkowym
•
nadmiar dwuchromianu potasu oznacza się
przez miareczkowanie [NH
4
]
2
[Fe][SO
4
]
2
·6H
2
O
wobec ferroiny jako wskaźnika
5.05.21
41

OZNACZANIE CHZT PRZY POMOCY
MADMANGANIANU POTASU
•
KMnO
4
ma znacznie słabsze właściwości
utleniające niż K
2
Cr
2
O
7
•
Oznaczone wartości ChZT często są niższe
niż BZT
5.05.21
42

OZNACZANIE CHZT
•
Jest opisane w odpowiednich normach
•
ISO 6060:1989 „Water quality - Determination of
the chemical oxygen demand”
•
PN-74/C-04578.03 „Woda i ścieki - Badania
zapotrzebowania tlenu i zawartości węgla
organicznego - Oznaczanie chemicznego
zapotrzebowania tlenu (ChZT) metodą
dwuchromianową”
5.05.21
43

5.05.21
44
BIOLOGICZNE ZAPOTRZEBOWANIE
TLENU
•
Ilość tlenu zużyta do biologicznego utlenienia
związków organicznych
•
jeśli proces biochemicznego utleniania trwa 5 dni
wówczas określamy BZT
5
•
jeśli proces biochemicznego utleniania trwa 20
dni wówczas określamy BZT
20

OZNACZANIE BZT
5
•
Próbę rozcieńcza się dejonizowaną wodą
wysyconą tlenem, zaszczepia
mikroorganizmami osadu czynnego i mierzy
zawartość tlenu,
•
następnie próbę szczelnie się zamyka,
zabezpiecza przed światłem aby uniknąć
fotosyntezy, pozostawia w temp. 20°C na 5
dni i po tym czasie ponownie mierzy
zawartość tlenu
•
różnica pomiędzy początkową i końcową
zawartością tlenu odpowiada BZT
5
5.05.21
45

TEORETYCZNE ZAPOTRZEBOWANIE
TLENU
•
Obliczane na podstawie składu substancji
podlegających biodegradacji
•
wyraża się jako ilość mg O
2
/mg substratu
•
W przypadku związków zawierających azot
najczęściej podobnie jak w przypadku ChZT
zakłada się tworzenie związków azotowych
zredukowanych (amoniak)
•
jeśli założy się iż związki azotowe również ulegają
utlenieniu wówczas mówimy o stechiometryczny,
lub całkowitym zapotrzebowaniem na tlen
5.05.21
46

OBLICZANIE TZT
CH
3
COOH + 2O
2
= 2CO
2
+ 2H
2
O
•
1 mol CH
3
COOH zużywa 2 mole tlenu
M
kw. octowego
= 60
M
tlenu
= 32
TZT =
2*32g/60g = 64mg/60mg = 1,07 mg O
2
/mg kw.
octowego
5.05.21
47

RWO – ROZPUSZCZALNY WĘGIEL
ORGANICZNY
•
Mierzy się w przesączu po odfiltrowaniu
cząstek stałych w próbach
5.05.21
48

5.05.21
49
OCENA
BIODEGRADOWALNOŚCI W
TESTACH PRZESIEWOWYCH
•
Znaczna podatność na biodegradację
związków organicznych rozpuszczalnych w
wodzie:
•
eliminacja 70% RWO; lub
•
eliminacja 60% BZT; lub
•
utworzenie 60% CO
2

5.05.21
50
ZWIĄZKI NIEROZPUSZCZALNE W
WODZIE
•
Charakteryzowane są przez dużą wartość
logarytmu współczynnika podziału
oktanol/woda
•
Ulegają bioakumulacji

KRYTERIA BIODEGRADOWALNOŚCI
ZWIĄZKÓW ORGANICZNYCH

BIODEGRADACJA KSENOBIOTYKÓW
Czynniki warunkujące biodegradację
związków organicznych
•
Stężenie rozkładanej substancji i jej toksyczność w
stosunku do mikroorganizmów
•
Obecność innych źródeł węgla i energii niż
rozkładana substancja
•
Struktura i właściwości fizykochemiczne badanej
substancji
•
Rodzaj i ilość mikroorganizmów
•
Skład mineralny podłoża
•
Natlenienie, temperatura, pH, naświetlenie

MECHANIZMY BIODEGRADACJI
WĘGLOWODORÓW

MECHANIZMY BIODEGRADACJI
WĘGLOWODORÓW
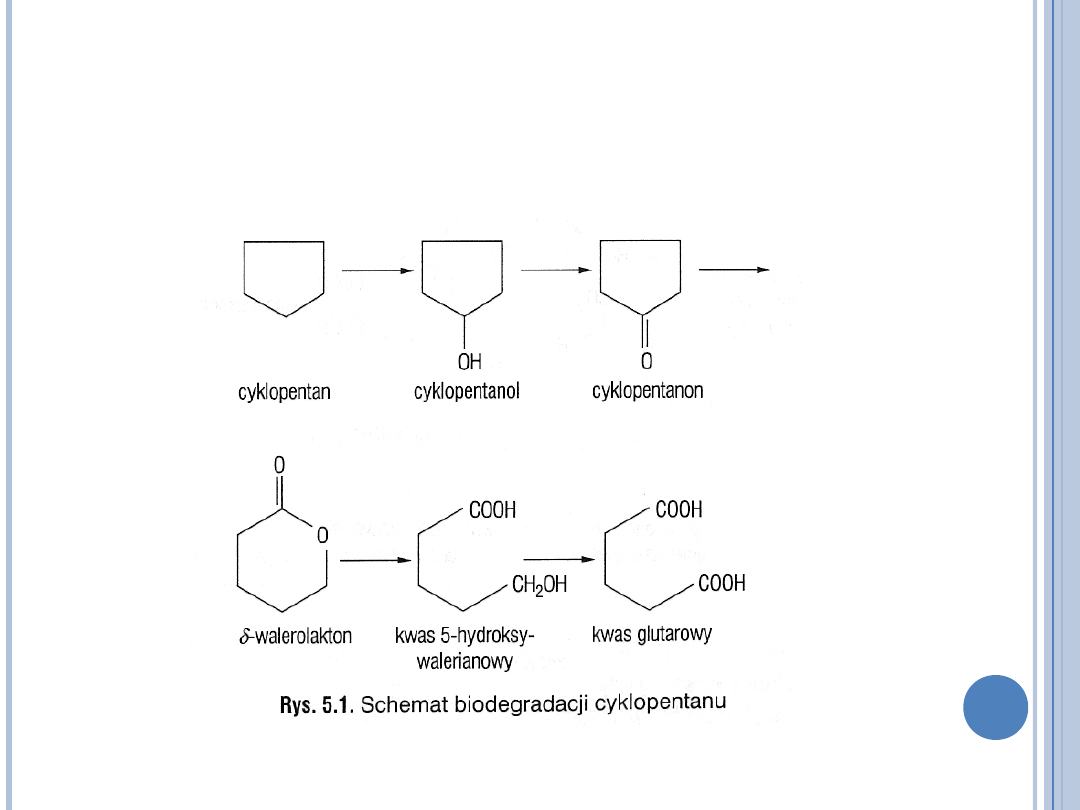
MECHANIZM BIODEGRADACJI
WĘGLOWODORÓW CYKLICZNYCH
(E. KLIMIUK, M.
ŁEBKOWSKA, BIOTECHNOLOGIA W OCHRONIE ŚRODOWISKA PWN 2004)
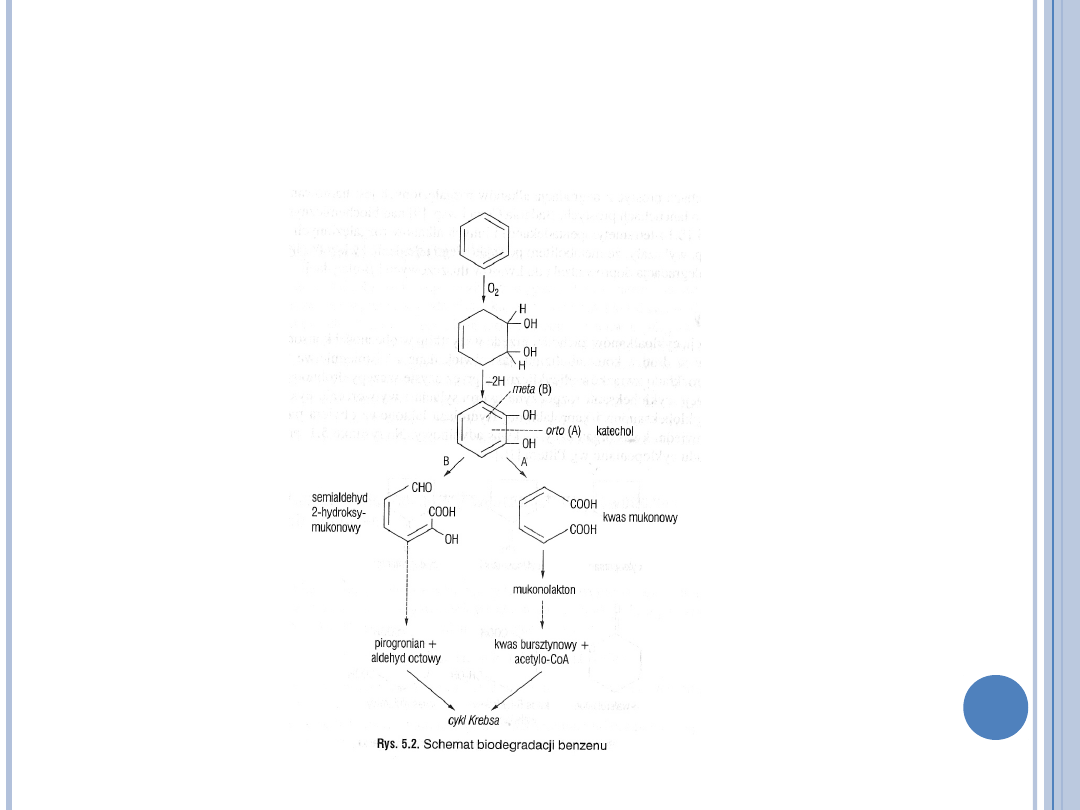
MECHANIZM BIODEGRADACJI
WĘGLOWODORÓW AROMATYCZNYCH
(E. KLIMIUK, M. ŁEBKOWSKA, BIOTECHNOLOGIA W OCHRONIE ŚRODOWISKA PWN 2004)
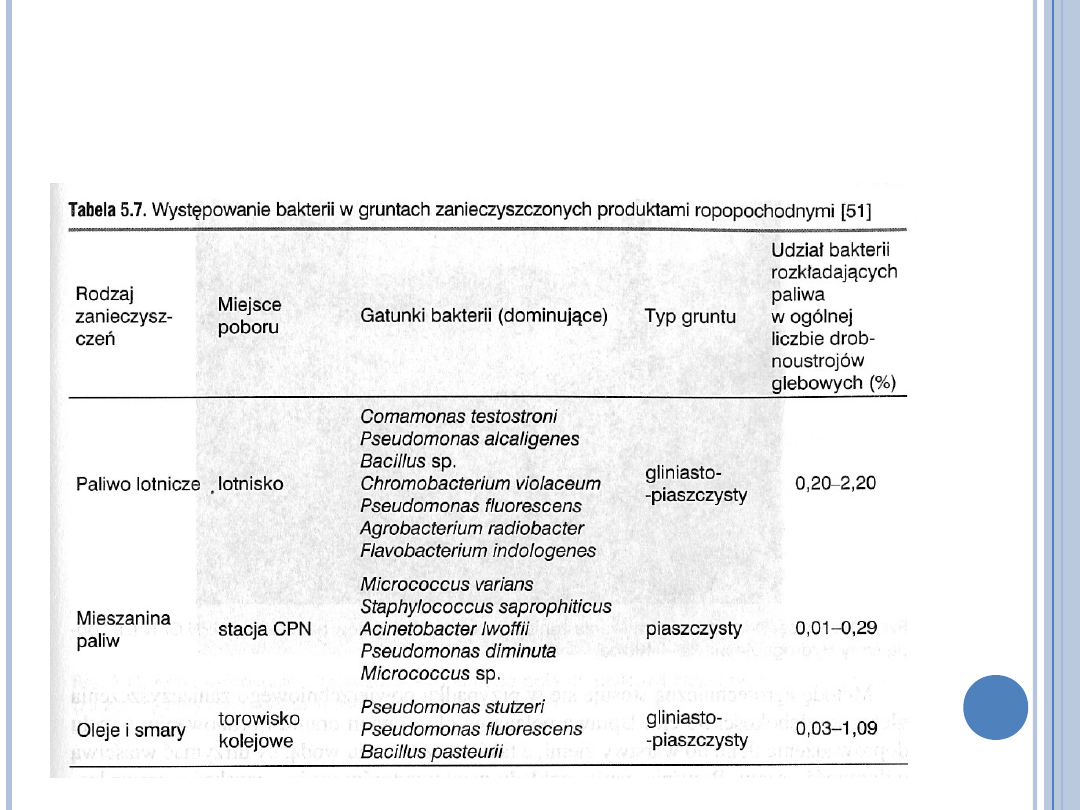
MIKROORGANIZMY DEGRADUJĄCE
PRODUKTY ROPOPOCHODNE
(E. KLIMIUK, M. ŁEBKOWSKA,
BIOTECHNOLOGIA W OCHRONIE ŚRODOWISKA PWN 2004)

MIKROORGANIZMY DEGRADUJĄCE
PRODUKTY ROPOPOCHODNE
Wiele mikroorganizmów wykazuje zdolność
do metabolizmu węglowodorów,
Bakterie
Pseudomonas, Micrococcus, Alcaligenes, Aeromonas, Flavobacterium,
Vibrio, Acinetobacter, Mycobacterrium, Bacillus, Arthrobacter
Grzyby
Candida, Saccharomyces, Fusarium, Penicillum, Aspergilus, Rhizopus,
Geotrichum
Promieniowce
Actinomyces, Nocardia, Streptomyces
Cyjanobakterie i glony
Oscillatoria, Anabaena, Nostoc, Chlorella, Chalmydomonas,
Scendemus, Phormidium
Jako jedyne źródło węgla tylko 0,01-1%
mikroorganizmów glebowych

MECHANIZMY POBIERANIA
WĘGLOWODORÓW PRZEZ
MIKROORGANIZMY
Zachodzi dzięki wytwarzaniu przez mikroorganizmy
substancji powierzchniowo-czynnych (biosurfaktanty)
różna struktura:
glikolipidy, acylopoliole, lipopeptydy, kwasy tłuszczowe, fosfolipidy,
tłuszcze obojętne
kompleksy polisacharydów, kwasów tłuszczowych i białek
pochodzą z częściowo rozłożonych otoczek lub ścian
komórkowych
Dodatek egzogennych biosurfaktantów przyspiesza
proces bidegradacji
Biodegradacji węglowodorów sprzyja hydrofobowa
powierzchnia komórek (beketrie Gram-)

METODY REMEDIACJI GRUNTÓW
In situ
bez wybierania zanieczyszczonego gruntu
Ex situ
po usunięciu gruntu z miejsca skażenia
Spalanie
Ekstrakcja
Przedmuchiwanie gruntu parą wodną z
jednoczesnym odsysaniem
Metody biologiczne

SPOSOBY BIOREMEDIACJI GRUNTÓW
Stymulacja autochtonicznej mikroflory
Wprowadzanie do gruntu mikroorganizmów
aktywnych w rozkładzie zanieczyszczeń
wyizolowane z gruntu i ponownie namnożone
przygotowane w postaci gotowych preparatów
bakteryjnych lub enzymatycznych
w postaci wolnej bądź immobilizowanej

TECHNICZNE METODY BIOREMEDIACJI
IN SITU
Uprawa gleby
przy zanieczyszczeniu na głębokość do 50 cm
uprawa roślin + okresowe oranie i bronowanie
(natlenianie) oraz zraszanie
zebrany plon nie może być wykorzystany do celów paszowych
Bioekstrakcja
przy głębokim zanieczyszczeniu gleb przepuszczalnych
glebę zasila się hodowlą bakteryjną z dodatkiem
biogenów
Biowentylacja
wprowadzanie powietrza do gruntu
powoduje parowanie i wydmuchiwanie lotnych
węglowodorów
najczęściej tylko jako wspomaganie bioekstrakcji

TECHNICZNE METODY BIOREMEDIACJI
EX SITU
Agrotechniczna
skażoną glebę układa się na geomembranie (folia, glina,
asfalt) izolującej od podłoża
uprawa roślin + okresowe oranie i bronowanie (natlenianie) oraz
zraszanie jak w metodzie in situ
Pryzmowanie
przypomina kompostowanie
pryzmę formuje się na geomembranie i zaszczepia
mikroorganizmami

CZYNNIKI WARUNKUJĄCE
BIOLOGICZNĄ BIOREMEDIACJĘ
GRUNTÓW
Budowa chemiczna węglowodorów
Zawartość tlenu w glebie
Wilgotność, temperatura pH (optymalnie 6-8)
Zawartość biogenów (N, P)
Liczebność (co najmniej 10
5
/g s.m.) i rodzaj
mikroorganizmów
Obecność innych niż węglowodory źródeł
węgla
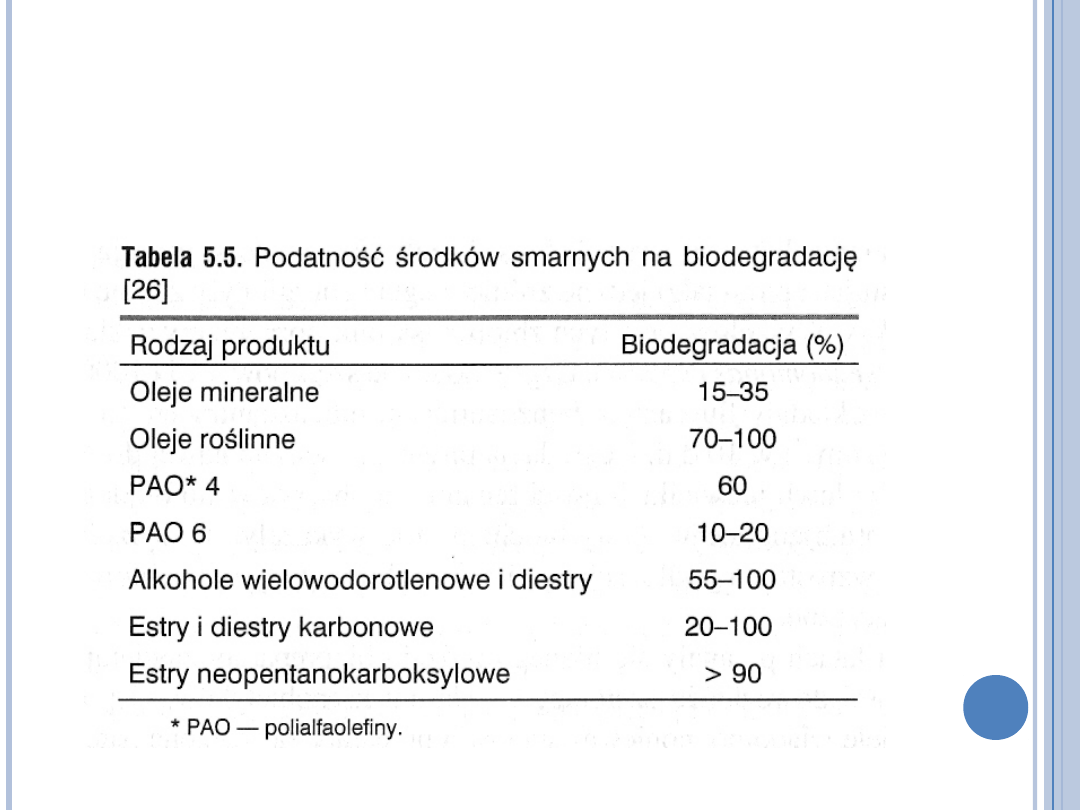
PODATNOŚĆ NA BIODEGRADACJĘ
WĘGLOWODORÓW ALKOHOLI I
ESTRÓW
(E. KLIMIUK, M. ŁEBKOWSKA, BIOTECHNOLOGIA W OCHRONIE ŚRODOWISKA PWN 2004)

PODATNOŚĆ NA BIODEGRADACJĘ
OLEJÓW MINERALNYCH I JADALNYCH
(E.
KLIMIUK, M. ŁEBKOWSKA, BIOTECHNOLOGIA W OCHRONIE ŚRODOWISKA PWN 2004)
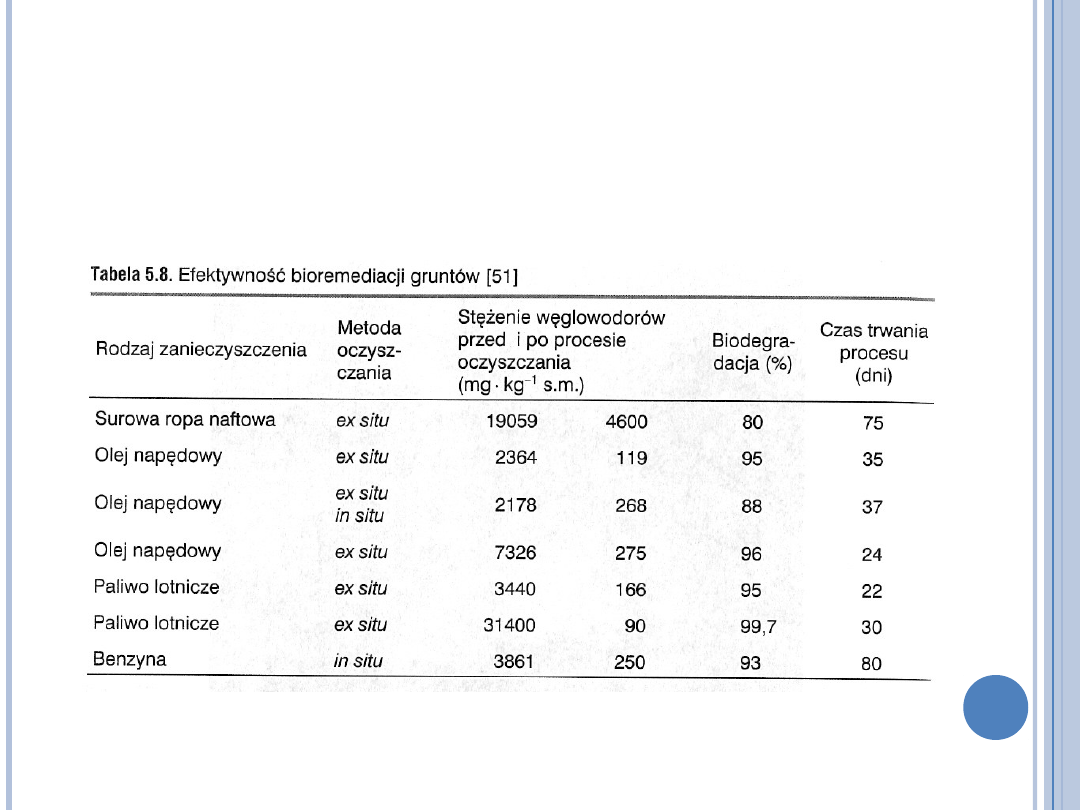
EFEKTYWNOŚĆ BIOREMEDIACJI
GRUNTÓW
(E. KLIMIUK, M. ŁEBKOWSKA, BIOTECHNOLOGIA W OCHRONIE ŚRODOWISKA PWN 2004)

CZYNNIKI STRUKTURALNE WPŁYWAJĄCE NA
BIODEGRADOWALNOŚĆ ZWIĄZKÓW
ORGANICZNYCH
•
Czwartorzędowy atom węgla, rozgałęzienia łańcucha
węglowodorowego, grupy izopropylowe na końcach
łańcucha węglowodorowego
•
Podstawniki halogenowe, nitrowe, nitrozowe,
aminowe, cyjanowe
•
Budowa cykliczna
•
Podstawniki metylowe i hydroksylowe w pierścieniu
aromatycznym
•
Skondensowane pierścienie aromatyczne
•
Ugrupowania epsoksydowe
•
Heteroatomy w pierścieniu aromatycznym
•
Budowa polimeryczna

5.05.21
69
KRYTERIA BIODEGRADOWALNOŚCI
POLIMERÓW
•
Polimer uznaje się za biodegradowalny
(zgodnie z normą ASTM) gdy:
•
jest zdolny do dekompozycji, w wyniku
enzymatycznego działania mikroorganizmów, z
utworzeniem: CO
2
, CH
4
, H
2
O, związków
nieorganicznych lub biomasy, co może być
zmierzone za pomocą standardowych testów w
czasie będącym odzwierciedleniem gospodarki
odpadami

5.05.21
70
KRYTERIA BIODEGRADOWALNOŚCI
POLIMERÓW C.D.
•
Polimer uznaje się za biodegradowalny gdy:
•
jest zdolny do dekompozycji,
w czasie nie
dłuższym od jednego roku
, w typowym
naturalnym środowisku, do którego z reguły
zostają usuwane odpady, w toku naturalnych
biologicznych procesów, z utworzeniem
nietoksycznych węglowych związków glebowych
oraz CO
2
i H
2
O.

5.05.21
71
OCENA BIODEGRADOWALNOŚCI
POLIMERÓW
•
Monitorowanie zmian właściwości polimeru
•
Monitorowanie wzrostu mikroorganizmów
•
Monitorowanie ubytku polimeru
•
Monitorowanie produktów degradacji

5.05.21
72
BIODEGRADACJA WYBRANYCH
POLIMERÓW NATURALNYCH
•
Polimery naturalne:
•
polisacharydy
•
skrobia
•
celuloza
•
białka
•
kauczuki

5.05.21
73
BIODEGRADACJA SKROBI
•
Pełna i kompletna konwersja do CO
2
i
biomasy w ciągu 7 dni
•
zachodzi poprzez rozszczepienie wiązań
glikozydowych przy pomocy szeroko
rozpowszechnionych w przyrodzie enzymów
amylolitycznych, a następnie glikolizę

5.05.21
74
BIODEGRADACJA CELULOZY
•
Pełna i kompletna hydroliza wiązań
glikozydowych i następnie mineralizacja
•
endoglukanazy najpierw atakują obszary
amorficzne
•
obszary krystaliczne są atakowane od
nieredukujących końców przez cellobiohydrolazy

5.05.21
75
BIODEGRADACJA ŻELATYNY
•
Kompletna hydroliza przy pomocy tryspyny
•
generalnie zachodzi poprzez hydrolizę wiązań
peptydowych przy pomocy proteaz
•
podobnie przebiega biodegradacja żelatyny
modyfikowanej przez usieciowanie

5.05.21
76
BIODEGRADACJA KAUCZUKU
NATURALNEGO
•
Kauczuk naturalny – cis-poliizopren
-[CH
2
-C=CH-CH
2
]
n
-
l
CH
3
•
Wolny ubytek masy, niskie
zapotrzebowanie na tlen
•
Mechanizm biodegradacji nieznany
•
w przypadku wyrobów gumowych przebieg
biodegradacji zależy od składu mieszanki
gumowej

5.05.21
77
BIODEGRACJA POLIETYLENU
-[CH
2
-CH
2
]
n
-
•
Proces bardzo wolny 0,35% w ciągu 2,5 roku
•
Utlenianie indukowane przez rodniki,
następnie -oksydacja
•
Proces może być przyspieszany przez
dodatek niektórych substancji np.
fotosensybilizatorów

5.05.21
78
BIODEGRADACJA POLIAMIDU 6
-[(CH
2
)
5
-NH-CO-]
n
-
•
Stosunkowo szybka degradacja oligomerów
M<1000, kompletna degradacja cyklicznych
oligomerów
•
Mechanizm biodegradacji nieznany
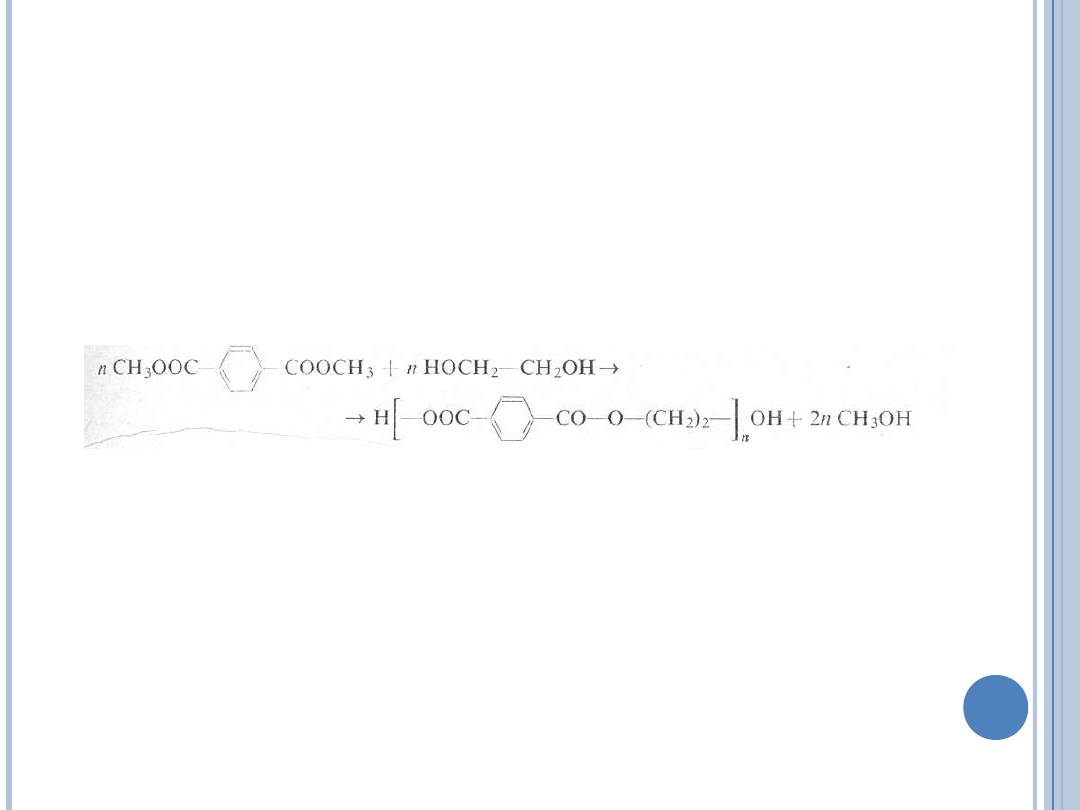
BIODEGRADACJA POLITEREFTALANU
ETYLENU

BIODEGRADACJA POLITEREFTALANU
ETYLENU
•
Nieznany mechanizm degradacji ani
hydrolizy
•
Sprzeczne wyniki inkubacji z różnymi
enzymami
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
- Slide 78
- Slide 79
- Slide 80
Wyszukiwarka
Podobne podstrony:
Wykład 6 2009 Użytkowanie obiektu
Przygotowanie PRODUKCJI 2009 w1
Wielkanoc 2009
przepisy zeglarz 2009
Kształtowanie świadomości fonologicznej prezentacja 2009
zapotrzebowanie ustroju na skladniki odzywcze 12 01 2009 kurs dla pielegniarek (2)
perswazja wykład11 2009 Propaganda
Wzorniki cz 3 typy serii 2008 2009
2009 2010 Autorytet
Cw 1 Zdrowie i choroba 2009
download Prawo PrawoAW Prawo A W sem I rok akadem 2008 2009 Prezentacja prawo europejskie, A W ppt
Patologia przewodu pokarmowego CM UMK 2009
Wykład VIp OS 2009
2009 04 08 POZ 06id 26791 ppt
perswazja wykład1 2009 Wpływy w sferze społeczno politycznej
wyklad 1 oddzialywania miedzyczasteczkowe 2009
choroby trzustki i watroby 2008 2009 (01 12 2008)
Psychometria 2009, Wykład 11, Inwentarz MMPI
więcej podobnych podstron