ZESTAW I
1.Wilgoć bezwzględna gazu jest to gęstość masy pary wodnej gazu wilgotnego. Maksymalna wilgoć gazu w ustalonej temperaturze ρpmax=ρ''
![]()
Wilgoć względna φ jest to stosunek rzeczywistej wilgoci gazu ρp (w. bezwzględnej) do wilgoci maksymalnej ρpmax w tej samej temperaturze wyrażona w procentach lub bezwymiarowo
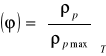
2. Entalpia pary przegrzanej jest sumą entalpii pary nasyconej oraz ciepła przegrzania.
r = i'' - i' => i'' = r + i'
i'' - entalpia pary przegrzanej
r - entalpia pary nasyconej
i' - ciepło przegrzania
inaczej: ip = i'' + cp(tp - t'') => 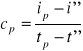
ciepło właściwe cp pary przegrzanej nie jest stałe, lecz zmienia się w zależności od ciśnienia i temperatury.
3. Równanie Bernolliego
Przy ustalonym przepływie w dowolnym przekroju rurociągu suma ciśnienia statycznego, dynamicznego i niwelacyjnego jest wielkością stałą
![]()
gdzie: ρ - gęstość przepływającego czynnika
g - przyśpieszenie ziemskie
h - wysokość położenia
![]()
w - prędkość przepływającego czynnika
4. Kryterium podobieństwa hydrodynamicznego
Do analizy lub opisu złożonych warunków technicznych procesów technologicznych, w przypadkach, w których pewne wielkości zależne są od dużej liczby parametrów trudnych do identyfikacji przez bezpośredni pomiar lub w ogóle niemożliwych do pomiaru, stosowane są metody badań na modelach. Wartości wyznaczonych doświadczalnie na modelu parametrów dotyczą tylko danego przypadku i nie mogą być bezpośrednio przeniesione na proces lub obiekt rzeczywisty. Przeniesienie wyników badań, a w konsekwencji uogólnienie w pewnym stopniu rozwiązuje teoria podobieństwa. Teoria ta ustala warunki podobieństwa dla 2 zjawisk fizycznych i umożliwia uzyskanie zależności właściwych dla dalszej grupy zjawisk. Prawa dotyczące podobieństwa zjawisk fizycznych stosować można tylko dla zjawisk tego samego rodzaju. Zjawiska podobne tego samego rodzaju muszą spełniać podobieństwo geometryczne, hydrodynamiczne i cieplne. 2 układy będą spełniały podobieństwo cieplne, gdy spełnione zostaną warunki podobieństwa geometrycznego, hydrodynamicznego oraz podobieństwa cieplnego.
Liczba podobieństwa Reynoldsa jest kryterium kinematycznym ruchu (określającym rodzaj przepływu [laminarny, turbulętny ])
Re= CD/υ
Gdzie: C - prędkość przepływu płynu [m/s]
D - średnica przewodu [m]
υ- współczynnik kinematyczny lepkości [m2/s]
Liczba Reynoldsa jest bezwymiarowa.
Ruch laminarny Re<2320 || Ruch burzliwy Re>3000
Liczba Reynoldsa określa podobieństwo przepływu. Przepływy są podobne, jeżeli odpowiednie liczby Reynoldsa posiadają jednakową wartość.
4. WENTYLATORY - zalicza się do grupy wirnikowych maszyn roboczych, w których spiętrzenie całkowite nie przekracza 13kPa. Biorąc pod uwagę uzyskiwane spiętrzenie całkowite rozróżnia się wentylatory:
- niskoprężne - uzyskiwane spiętrzenie całkowite do 1 kPa
- średnioprężne - uzyskiwane spiętrzenie całkowite od 1 do 3 kPa
- wysokoprężne - uzyskiwane spiętrzenie całkowite od 3 do 13 kPa
Ze względu na zasadę działania wentylatory dzieli się na:
- ośrodkowe (promieniowe) - kierunek ruchu tłoczonego gazu stycznej do obwodu wirnika
jest prostopadły do osi wirnika.
- osiowe - kierunek ruchu medium jest równoległy do osi wirnika
- mieszane - osiowo - promieniowe
- poprzeczne
- skośne - diagonalne
Zasada działania
Wentylatory wytwarzają spiętrzenia potrzebne w zasadzie tylko do pokonywania oporów przepływu przez sieć i urządzenia, a więc prawie wyłącznie do transportu gazu. Wyższe ciśnienie uzyskuje się w sprężarkach. Wentylatory charakteryzują się następującymi parametrami:
- strumień przepływu (natężenie przepływu, wydatek)
- spiętrzenie całkowite wentylatora ΔpC - różnica ciśnień całkowitych na tłoczeniu i ssaniu wentylatora
- moc wewnętrzna Ni - różnica mocy na wale wentylatora (mocy napędzanej) oraz strat mocy w elementach konstrukcyjnych przenoszenia napędu
- moc użyteczna Nu - moc przekazania czynnikowi jako iloczynu ciśnienia spiętrzania i wydatku wentylatora
- sprawność wewnętrzna wentylatora ηi = Nu/Ni stosunek mocy użytecznej do mocy wewnętrznej
- sprawność ogólna wentylatora η = Nu/Nw stosunek mocy użytecznej do mocy na wale
W przypadku, gdy poszczególne wentylatory nie zapewniają żądanego spiętrzenia całkowitego lub odpowiedniego strumienia objętości czynnika, stosuje się łączenie kilku wentylatorów w układ szeregowy lub równoległy.
Współpraca równoległa
Zwiększenie strumienia objętości uzyskuje się stosując współpracę równoległą wentylatorów. Spiętrzenie całkowite poszczególnych wentylatorów powinno być sobie równe. Strumień objętości układu jest sumą strumieni objętości poszczególnych wentylatorów.
V=V1+V2 przy ΔpC = ΔpC1= ΔpC2
Połączenie równoległe 2 wentylatorów powoduje zwiększenie objętości strumienia jednakże łączny wydatek w punkcie pracy układu A1,2 jest mniejszy nież wydatek sumaryczny wentylatorów pracujących oddzielnie w punktach A1 i A2.
Ciśnienie układu pozostaje niezmienne.
5. SPALANIE - jest to fizyko - chemiczne zjawisko polegające na utlenianiu składników palnych tlenem własnym lub tlenem z powietrza atmosferycznego, w wyniku którego wydziela się ciepło połączenia ze zjawiskami świetlnymi. Produktami ostatecznego utleniania składników palnych paliwa są: - CO2 || - SO2 || - para wodna
Spalanie uważa się za zupełne jeżeli produkty spalania (spaliny) nie zawierają gazowych składników palnych (np. CO,H2,CH4). Jeżeli natomiast stałe produkty spalania (żużel, popiół) nie zawierają wodnego węgla i siarki, spalanie takie uważa się za całkowite. W zależności od szybkości reakcji utlenienia rozróżnia się:
- spalanie powolne - zachodzące w procesach biologicznych i korozji, a wydzielające się ciepło w bardzo długim czasie nie posiada znaczenia technicznego.
- spalanie techniczne - zachodzące w procesach termicznej utylizacji substancji zawierających składniki palne, ciepło ekonomiczne jest wykorzystywane.
W zależności od miejsca występowania spalanie dzieli się na:
- spalanie wewnętrzne - zachodzące w cylindrach silników spalinowych i komorach turbin gazowych.
- spalanie zewnętrzne - zachodzi w komorach spalania kotłów parowych i pieców przemysłowych.
- spalanie otwarte - zachodzące w otwartej przestrzenia - pożary
Z punktu widzenia łatwości łączenia się substancji palnej z utleniaczem rozróżnia się spalanie:
- kinetyczne - substancje palne zmieszane są z tlenem przed rozpoczęciem reakcji spalania
- dyfuzyjne - proces spalania zachodzi równocześnie z procesem mieszania
6. Obl. Ilość tlenu i powietrza do spalania
Minimalna ilość tlenu, którą należy dostarczyć do całkowitego i zupełnego spalania 1 kg paliwa stałego (ciekłego) lub 1 m3 paliwa gazowego zgodnie z równaniem stechiometrycznym nazywa się tlenem stechiometrycznym. Tlen stechiometryczny Ost może być wyrażony w [kmol O2/kmol paliwa], [m3O2/kg paliwa], [m3O2/m3paliwa].
Tlen stechiometryczny pomniejsza się o tlen zawarty w paliwie, gdyż bierze on udział w spalaniu i tę różnicę nazywamy tlenem teoretycznym. Dla paliw niezawierających w swoim składzie wolnego tlenu, ilość tlenu teoretycznego równa jest ilości tlenu stechiometrycznego.
Dla 1 kg węgla kamiennego o danym składzie chemicznym minimalna ilość tlenu dostarczonego do spalenia z powietrzem atmosferycznym, czyli tlenu teoretycznego wynosi:
Ot= Cr/12 + 0,5*Hr/2 + Sr/32 - Or/32 [kmolO2/kgpaliwa]
Gdzie: Cr,Hr,Sr,Or - udziały masowe składników paliwa w stanie roboczym, [kg składnika /kg paliwa]
Dla 1 m3 paliwa gazowego objętość tlenu teoretycznego wyniesie:
Ot=Σi=1zi OSti O2 [m3O2/m3paliwa]
Gdzie : zi - udział objętościowy palnego składnika paliwa
OSti - tlen stechiometryczny palnego składnika paliwa
Ot= 0,5 CO + 0,5 H2 + 3/2 H2S + (n + m/4)CnHm - O2 [m3O2/m3gazu]
Gdzie : CO, H2, H2S, CnHm, O2 - udziały objętościowe skłądników w gazie [m3skłądnika/m3gazu]
Minimalna ilość powietrza, którą należy dostarczyć do całkowitego i zupełnego spalenia 1 kg paliwa stałego i ciekłego lub 1 m3 paliwa gazowego nazywa się powietrzem teoretycznym.
Teoretyczną jednostkową objętość powietrza V0 oblicza się przy założeniu objętościowego składu powietrza suchego: tlen - 21%, azot - 79%
V0 = 100/21 Ot = 4,76 Ot [m3pow./kg paliwa] lub [m3pow./m3paliwa
Spalanie paliw w piecach przemysłowych przeprowadza się przeważnie z ilością powietrza V większą od ilości powietrza teoretycznego V0. Stosunek ilości powietrza całkowitego, dostarczonego do spalania jednostkowej ilości paliwa, do ilości paliwa teoretycznego nazywa się stosunkiem nadmiaru powietrza.
λ=V/V0 = Oc/Ot
Oc = λOt [m3/kg] lub [m3/m3gazu]
Vc=λV0 [m3/kg] lub [m3/m3gazu]
7. WPŁYW PRZEKROJU KOŃCOWEGO DYSZY NA CIŚNIENIE WYPŁYWU na wykresach P-V
Uzyskanie odpowiednich parametrów czynnika wypływającego uwarunkowane jest odpowiednim kształtem dyszy. Jeżeli końcowy przekrój dyszy jest zbyt duży F>Fo wówczas ciśnienie czynnika może osiągnąć w dyszy ciśnienie mniejsze od ciśnienia panującego w otoczeniu, do którego wpływa czynnik, następują tu straty zderzenia się strumienia z czynnikiem otoczenia, co powoduje straty. Jeżeli natomiast przekrój końcowy dyszy jest za mały F<Fo to dalsze rozprężanie do ciśnienia po nastąpi w sposób chaotyczny powodują straty prędkości ( rys. B). Przekrój dyszy powinien być dobrany tak by F=Fo (rys. C).
ZESTAW II
1.Opisac stopien suchości pary wodnej w układzie p-v.
Stopien ilości wyparowanej cieczy czyli tzw. Stopien suchości pary mozna określić dla nastepujacych założeń : jeśli doprowadzone cieplo do 1 kg wody spowodowalo wytworzenie X kg pary a powstalo Y kg wody wówczas X+Y=1 kg.
Objętość mieszaniny: v = v'y+v”x y = 1-x || v = v' +x (v”-v') || x = v - v' / v” - v'
dla v = v' czyli x=0 dolna krzywa graniczna - ciecz
dla v= v” czyli x=1 górna krzywa graniczna - para słucha
v - objętość mieszaniny pary nasyconej i cieczy czyli para wilgotna nasycona
v' - objętość cieczy
v” - obj pary nasyconej suchej
2. Stopień zwilzenia gazu jest to stosnek ilości pary do ilości gazu suchego.
Gramowy stopien zawilzenia : X= Gp / Gg … kg pary / kg gazu suchego
Molowy lub objętościowy stopien zawilzenia. X2= np / ng .. kmol pary / kmol gazu suchego
3.Wyznaczenie wilgotności powietrza na podstawie danych psychometrycznych
Tm = 20 0C T such= 30 0C Róznica psychometryczna ΔT = Tsu - Tm
10. Omówic paliwa odnawialne.
Paliwa odnawialne stanowi biomasa do której zalicza się drewno i słome oraz odpady zawierające substancje palne miedzy innymi odpady komunalne, medyczne, przemysłowe itp. Większość biomasy jest pochodzenia roślinnego i powstala w procesie fotosyntezy z wykorzystaniem energii słonecznej.
11. Szybkość reakcji chemicznych procesu spalania. Równowaga chemiczna.
Szybkość reakcji chemicznej względem substratu Si lub produktu Pi mierzy się ubytkiem liczby moli wybranego substratu lub przyrostem liczby moli produktu w jednostce czasu
αA+βB=>γC+δD ABCD - symbole chemiczne αβγδ - współczynniki stechiometryczne
rf = kf [A]a [B]b kf - stała szybkość reakcji zalezna od temp a,b -wykladniki przedstawiające rzad reakcji względem [A]i[B]
Równowaga chemiczna: dla reakcji Utleniania αA+βB<=>γC+δD
12. Kontrola procesu spalania.
Największe efekty ekonomiczne i energetyczne procesu spalania uzyskuje się podczas całkowitego i zupełnego spalania z teoretycznym stosunkiem nadmiaru powietrza. Jednakze spalanie ze stosunkiem nadmiaru powietrza k=1 może powodowac duze straty stałych i gazowych składników palnych ze względu na utrudniony kontakt tlenu ze składnikami palnymi paliwa. Podstawowymi parametrami kontroli procesu spalania sa : nadmiar powietrza i temperatura spalania
4. Równanie Clausiusa - Clapeyrona dla par.
Jednostkowa praca w układzie p-v równa jest jednostkowemu cieplu w układzie T-s, czyli:
(v” - v')dp=(S” - s')dT
s” - s' = (v” - v')dp/dT S” - s' = r / T
r =T(v”-v')dp/dT
zależność ciepła parowania wody od temperatury - drugie prawo termodynamiki par
5. Wyprowadz różniczkowe równanie ciągłości strugi.
dq = di+d(W2/2) dq = 0 di = -d(W2/2)
Po rozwiązaniu równania i zmianie granic calkowania otrzymamy:
i1-i2 = (W22-W12)/2 i1 +W12/2 = i2 +W22/2 = ic = const
ic = i + W2/2
entalpia własciwa całkowita jest to suma entalpii właściwej statycznej i entalpii właściwej dynamicznej W2/2
Jeżeli pominie się tarcie wówczas róznica entalpii równa będzie pracy technicznej. i1- i2 = It
(W22 - W12 )/ 2 = całka (przedział od 1 do 2) z vdp = It
Po zróżniczkowaniu otrzymuje się różniczkowe równanie ciągłości strugi. Wdw = -vdp
6. Opisac przepływ cieczy elastycznej przy malym spadku cisnienia.
Dla małych spadków cisnienia medium w rurociągu można przyjąć ze objętość własciwa cieczy elastycznej nie ulegnie zmianie także nie napręży się ona podczas przepływu v1=v2=const. Uproszczenie to można zastosowac do przypadku gdy róznica ciśnień nie jest wieksza niż 10%, p/p0 <1.1
W22-W12 /2 = całka(przedział od 1 do 2) vdp= v(p1-p2)= vΔp
7.Kryterium podobieństwa hydrodynamicznego. Liczba Reynoldsa.
W układach podobnych występują podobne wielkości, które dla zjawisk podobnych zachowuja tę samą bezwymiarowa wartość i noszą nazwę liczb podobieństwa, kryteriów podobieństwa lub liczb kryterialnych. Dwa układy będą podobne hydrodynamicznie , gdy stosunek sił bezwładności do sił tarcia występujących podczas przepływu cieczy elastycznej będzie jednakowy czyli gdy będą jednakowe liczby REYNOLDSA.
Re = w*d / ν w - prędkość m/s, d - wymiar liniowy (srednica rurociągu) m, ν - lepkość kinematyczna zalezna od gęstości gazu i lepkości dynamicznej m^2/s
Lepkość kinematyczna ν = η/ ρ
Kryterium podobieństwa kinematycznego Reynoldsa jest stosunkiem sił bezwładności do sił lepkości i posiada postac: Re = ρ w d / η
8. Straty cienienia spowodowane tarciem w rurociągu krótkim i długim.
Rurociągi krótkie : Δpt = λ *(w2 ρ /2) * l / dh l - dł rurociągu, dh - srednica hydrauliczna
Rurociągi długie:
W rurociągach długich podczas przepływu gazu występują wieksze spadki cisnienia gdyz wzdłuż rurociągu zmienia się gęstość. Zakładając stałość λ wzdłuż rurociągu oraz stałą temperature spadek cienienia na calej długości rurociągu wynosi:
Δptd = λ *(w2 ρ/2) * l/dh * p1/pm, cisnienie srednie: pm= (p1+p2) / 2
9. Współpraca dwóch wentylatorów . Połaczenie szeregowe.
W zależności od potrzeb technologicznych dla bardzo szerokich zakresów wydatku medium oraz jego cisnienia stosuje się połaczenia kilku wentylatorów. Połączenie szeregowe 2-uch wentylatorów powoduje zwiekszenie cisnienia wentylatora. Przyrost cisnienia poszczególnych wentylatorów, a wydatek układu nie zmienia się.
ZESTAW III
1. Def. gazu wilgotnego:
Gaz wilgotny jest to roztwór gazu suchego i pary, a większość gazów spotykanych
w przyrodzie i technice zawiera parę wodną. Do najczęściej spotykanych w technice gazów wilgotnych należą: powietrze i spaliny. Para wodna w spalinach pochodzi głównie
ze spalenia wodoru i węglowodorów oraz wilgoci zawartej w paliwie. Przy niezbyt wysokich ciśnieniach gazy podlegają prawu daltona: p = pgazu + ppary
2. Opisać proces suszenia na wykresie i-x:
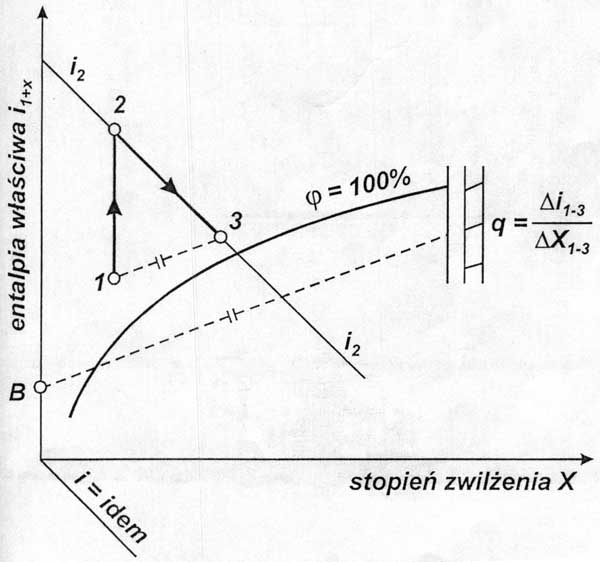
W procesie suszenia wilgotny materiał styka się z gazem nienasyconym wilgocią. Intensywność procesu suszenia jest tym większa im mniejsza jest wilgotność suszącego czynnika. Punkt charakteryzujący stan suszącego powietrza przesuwa
się w układzie i,X po linii prostej, której nachylenie określa wzór:
![]()
pochylenie tej linii niewiele odbiega od pochylenia linii i = idem, dlatego zazwyczaj przyjmuje się że przemiana powietrza w procesie suszenia jest przemianą izentalpową. Wilgotność powietrza odpływającego z suszarki jest mniejsza od 100% (3). Uzyskanie wartości ϕ = 100% było by możliwe tylko w pierwszym etapie suszenia przy nieskończonym długim czasie stykania się suszonego materiału z powietrzem suszonym.
3. Opisać proces parowania wody:
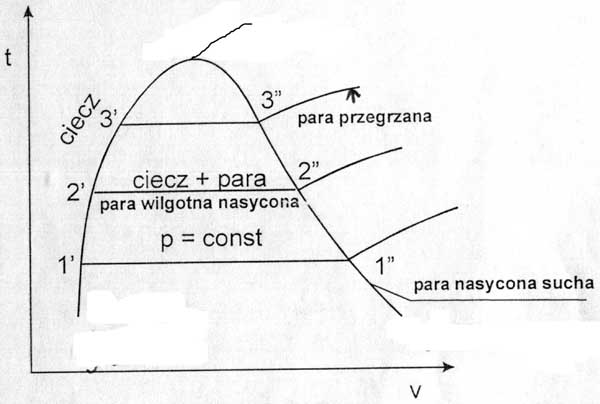
Jeżeli pod tłokiem zamknie się np 1 kg wody i zachowując stałe ciśnienie p1=0,1*105
i będzie się doprowadzać ciepło to objętość będzie się zmieniać przy stałej temp i ciśnieniu od 1' do 1”. Powstająca para wilgotna nasycona w punkcie 1” uzyska stan pary nasyconej suchej. Dalsze doprowadzanie ciepła powyżej punktu 1” spowoduje równoczesny wzrost objętości
i temp a para nasycona sucha uzyska stan pary przegrzanej dla odpowiednio wysokiego ciśnienia uzyskać można punkt, w którym ciecz przejdzie bezpośrednio
w przegrzaną, punkt nazywa się punktem krytycznym (dla wody tk=374,15 C, pk=221,29 MPa), krzywa 1'-2'-3' nazywa się krzywą graniczną i oddziela ciecz od pary nasyconej wilgotnej a 1”-2”-3” górną krzywą graniczną oddzielającą parę nasyconą wilgotną od pary przegrzanej.
4. Ciepło parowania; def., rodzaje.
5. Masowe równianie ciągłości strugi.
![]()
F -przekrój kanału m2 || w - prędkość średnia m/s2 || V- obj. właściwa
Masa cieczy elastycznej jest jednakowa dla prędkości średniej i prędkości rzeczywistej zgodnie z równaniem ciągłości strugi.
6. Wypływ cieczy elastycznej, model wypływu, prędkość wypływu.
Jeżeli w zamkniętym izolowany- zbiorniku znajduje się gaz pod stałym ciśnieniem i zerowa prędkością liniowa, w=0, to podczas wypływu tego gazu:
Z równania entalpii di=cpdt
I - i0 = cp ( t - t0 ) dla w = 0

|| 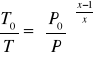
|| ![]()
|| ![]()

7. Teoria podobieństwa, opis ogólny:
Teoria ta ustala warunki podobieństwa dla dwu zjawisk fizycznych i umożliwia uzyskanie zależności właściwych dla dalszej grupy zjawisk podobnych. Zjawiska podobne do tego samego rodzaju muszą spełniać podobieństwo geometryczne, hydrodynamiczne i cieplne. Dwa układy będą spełniały podobieństwo cieplne gdy spełnione zostaną warunki podobieństwa geometrycznego, hydrodynamicznego i cieplnego. Podobieństwo geometryczne polega na podobieństwie kształtu obiektu doświadczalnego i obiektu rzeczywistego sprowadzające się do proporcjonalności pewnych, wybranych wymiarów liniowych a nie równości tych wymiarów. Przykładowo podobieństwo geometryczne jest wówczas gdy stosunek średnic kanału przepływowego do promieni krzywizny w wybranych punktach przekroju będzie stały.
![]()
8. Opory tarcia, praca tarcia
Opór tarcia występuje głownie na ścianie kanału. Jeżeli siłę tarcia między dwoma sąsiednimi przekrojami oddalonymi od siebie o dx oznaczy się przez ds. to praca tarcia wykonana przez strumień w jednostce czasu wyniesie.
![]()
F - przekrój m2
G - masowe natężenie przepływu
Praca tarcia stanowiąca pracę techniczną zgodnie z def:
![]()
Opory przepływu
W przepływach czynnika rzeczywistego (płyn, gaz), ma miejsce strata energii na skutek tarcia oraz oddziaływań przypadkowych w kolanach, załomach, przewężeniach, armaturze itd. Wszystkie te czynniki stanowią dla przepływu znaczne opory, na których zachodzą straty energetyczne. Wielkości strat energetycznych wyrażonych stratą ciśnienia obliczamy wg wzoru: ![]()
Straty ciśnienia wynikłe z oporów miejscowych obliczamy wg wzoru: ![]()
Stratę ciśnienia na skutek tarcia obliczamy wg wzoru: ![]()
k - współczynnik chropowatości rurociągu
![]()
- strata tarcia
λ - współczynnik strat tarcia zależy od liczby Re i chropowatości k:
dla przepływu laminarnego ![]()
|| dla przepływu turbulentnego ![]()
9. Zmiana pkt. pracy wentylatora poprzez zmianę prędkości obr. n wirnika wentylatora.
Mając charakterystykę danego wentylatora zdjętą przy stałej szybkości obrotowej n, można drogą obliczeń znaleźć jego charakterystykę przy innej dowolnej szybkości obrotów, a także innych wentylatorów spełniających podobieństwo geometryczne.
PKT. PRACYWENTYLATORA - Określa on ilość przepływającego czynnika przez sieć przy odpowiednim ciśnieniu całkowitym wytworzonym przez wentylator, co powinno nastąpić przy optymalnej sprawności wentylatora. Zmiana parametrem pracy następuje przy zmianie oporów sieci, co można uzyskać poprzez dławienie gazu, wówczas pkt pracy przesunie się w położenie 2 oraz nastąpi zmniejszenie wydajności z V1 na V2 przy wzroście ciśnienia całkowitego Δpc1 na Δpc2. Zmiana wydajności poprzez dławienie może następować w kierunku jej zmniejszenia.
10. Omówić paliwa stałe
Podział paliw - w zależności od pochodzenia paliwa dzielimy na naturalne i sztuczne, paliwa naturalne dzielą się na recesyjne (roślinne i zwierzęce) i kopalne (gumolity i sapropelily). PALIWA STALE NATURALNE - którego głównymi składnikami są celuloza i lignina oprócz tego drewno zawiera małe ilości soli mineralnych, związki białkowe zawierające azot oraz węglowodany. Świeże drewno zawiera ok. 60% wilgoci.
Torf - jest produktem metamorfozy roślinnej na drodze procesu biochemicznego. Powstanie warstwy torfu o grubości 1 metra ocenia się na 100 lat. Charakteryzuje się duża zwartością wilgoci 90 %, w stanie suchym 15-30%, zawiera siarkę.
Węgiel brunatny - zajmuje pod względem stopnia uwęglenia miejsce pośrednie między torfem a węglem kamiennym. Nazwa węgla pochodzi od jego brunatnej barwy, która posiada większość jego rodzajów. Zawartość wilgoci w złożu węglowym w stanie wydobycia wynosi 10-60%, zawartość siarki wynosi ok. 1,5-3%.
Węgiel kamienny - składa się z trzech zasadniczych składników, substancji palnej składników mineralnych oraz wilgoci. CHS stanowią substancje palne, H2O i popiół stanowią substancje niepalne. Elementarny skład węgla kamiennego stanowią następujące składniki C+H+O+N+S+A+W=100%
Koks - otrzymuje się w wyniku odgazowania węgla kamiennego bez dostępu powietrza prócz koksu otrzymuje się smołę, amoniak, benzol surowy, gaz koksowniczy, wódę pogazową. Produkcję koksu dzielimy na trzy etapy - przygotowanie wsadu - koksowanie - gaszenie koksu.
11. Granica zapłonu
Granica zapłonu - skład mieszanki paliwowo powietrznej, dla której nastąpi zapłon, czyli nadmiar tlenu do spalania λ. Granicą mieszanki ubogiej jest nadmiar tlenu do spalania, natomiast mieszanka bogata charakteryzuje się niedomiarem tlenu w stosunku do tlenu stechiometrycznego. Na wielkość granic zapłonu ma wpływ ciśnienie i temperatura, energia źródła zapłonu oraz domieszki do paliwa. Ze wzrostem temp mieszanki granice zapłonu rozszerzają się, natomiast nieznaczne ciśnienie powoduje zwężenie granic zapłonu, ciśnienie wysokie znacznie je rozszerza.
12. Ciepło spalania i wartość opałowa
Ciepło spalania - ilość energii potrzebnej do spalenia całkowitego i zupełnego jednostki masowej lub objętościowej paliwa, przy czym produkty spalania spaliny zostaną ochłodzone do temperatury początkowej składników biorących udział w spalaniu a para wodna pochodząca z wilgoci paliwa i spalania wodoru ulegnie w całości skropleniu.
Wartość opalowa - ilość energii potrzebnej do spalenia całkowitego i zupełnego jednostki masowej lub objętościowej paliwa, przy czym produkty spalania spaliny zostaną ochłodzone do temperatury początkowej składników biorących udział w scalaniu a para wodna zawarta
w paliwie oraz powstała ze spalania wodoru z tego paliwa znajduje się w postaci pary.
![]()
|| ![]()
= 2500 kJ/kg,
W- całkowita ilość pary wodnej w spalinach.
ZESTAW IV
1. Entalpii gazu wilgotnego φ
Entalpia właściwa gazu wilgotnego odnosi się do tej ilości gazu, która zawiera 1kg lub 1kmol gazu suchego
i1+x = ig + xip
Entalpię gazu wilgotnego oblicza się mnożąc entalpię właściwą przez ilość gazu wilgotnego Gg[kg] lub ng [kmol]
I= Ggi1+x = ng(Mi)i+x2
2. Wykres i-x powietrza wilgotnego
Wykres podający graficzna zależność entalpii właściwej od stopnia nawilżenia powietrza i= f(x) umożliwia wyznaczenie parametrów powietrza wilgotnego dla jednej wartości ciśnienia powietrza (zazwyczaj p = 1bar)
Wykres i-x ujmuje zależność pomiędzy wielkościami i, x (lub pp), φ oraz T. Wykresem można posługiwać się, jeżeli ciśnienie rzeczywiste nie odbiega od przyjętego na wykresie o więcej niż +- 3%. Linie i = idem przebiegają skośnie względem osi rzędnych pod kątem 135o między osiami wykresu tj. i, x. Izotermy powietrza nie zamglonego są liniami prostymi. Im wyższa jest temperatura tym bardziej stromy przebieg jest izoterm.
Linia φ= 100% rozgranicza na wykresie obszar nie zamglonego ,izotermy powyżej zamglonego sa liniami prostymi ich pochylenie zależy od temperatury.
3. Własności pary wodnej
Jeżeli do zamkniętego zbiornika z wodą doprowadzać się będzie ciepło i jeżeli panować tam będzie ciśnienie p to przyrost entalpii wody o temp 0oC wtłoczonej do kotła pompą będzie następująca (z I ZT)
dq = di - vdp => di = dq + vdp
przyrost entalpii di wody będzie obejmował
- ciepło zużyte na podgrzanie wody od 0oC do temp wrzenia odpowiadającej ciśnieniu parowania || qp = cw * tw || cw - ciepło właściwe wody || tw - temp wrzenia
- energie zużyta na pompowanie wody do kotła w którym panuje ciśnienie p, będzie to praca pompowania Lp = pv0 || v0 - objętość wody
- pracę która musi być wykonana przy rozszerzaniu się objętości ogrzewanej wody od objętości v0 do v' dla temp wrzenia tw i konieczności zrobienia miejsca dla przyrostu tej objętości
L = p(v' - v0) =pv' - pv0
Entalpia wody wrzącej będzie sumą powyższych składników
I' = cw *tw + pv0 + pv' - pv0 = cw * tw + pv'
Wielkość pracy pv' jest bardzo mała (dla p = 200Mp, pv'= 1,75 kJ/kg) i w rozważaniach technologicznych może być pominięta Czyli entalpia wrzącej wody równa jest wprost temp wody tw oraz jej entalpii zewnętrznej u'
tw = i' = u' + pv' pv'= 0 tw = i' = u'
4. Para przegrzana
Doprowadzając ciepło do pary nasyconej suchej nei stykającej się z cieczą podnosi się temp bez zmiany ciśnienia pary uzyskując warunki termiczne przegrzania czyli tzw parę przegrzaną.
Przegrzanie pary zaczyna się powyżej górnej krzywej granicznej x=1.Przy doprowadzeniu ciepła przy ciśnieniu pary nasyconej wzrasta temperatura i objętość własna. Równanie Clapeyrona dla gazów doskonałych pV = nRT nie spełnia warunków dla pary przegrzanej i powoduje rozbieżności, dlatego wprowadza się pewne poprawki:
V = [RT/p] -K
p = [RT/V] - M
pv = RT - N
wielkości współczynników korekcyjnych K, M i N w zależności od ciśnienia i temp pary wyznaczono eksperymentalnie. Do obliczeń parametrów pary przegrzanej o ciśnieniach nie przekraczających 12 * 105Pa (12 bar) stosuje się równanie Lindego
pV = RT - 0,016p
dla ciśnień wyższych stosuje się równanie Calleudera
p(V - α)= RT - f(T)
f9T) - poprawka podająca rozbieżność odprawa gazów doskonałych w funkcji temp
przyjmując:
α = 0,001 oraz f(T) = 0,0075(273/T)10/3
równanie Callendera będzie miało postać
(V - 0,001)= [RT/p] - 0,0075 (273/T) 10/3
Na podstawie tego równania sporządzone zostały wykresy pary przegrzanej od ciśnienia 150 bar.
6. Dysza de Lavala
Aby uzyskać największą prędkość przepływu kanał musi być odpowiednio uformowany. Przekrój dyszy początkowo się zmniejsza (dyfuzor) od F do F' a prędkość wzrasta do W', poniżej przekrój zwiększa się (konfuzor) do F0 a prędkość wzrasta do W0 = Wmax, V = ∞. Kanał tego typu nosi nazwę dyszy de Lavala. Dysza umożliwia osiągnięcie prędkości większych od krytycznych tzw. Prędkości nadkrytycznych.
Jeżeli wpływ cieczy elastycznej odbywał się będzie w dyszy, której przekrój krytyczny stanowił będzie zakończenie dyszy wówczas wyrównanie ciśnień z otoczeniem w sposób gwałtowny nastąpi poza kanałem, co spowoduje straty energii wypływającego gazu.
7. Przepływ medium. Opory
Przepływ gazu przez rurociągi (kanały, przewody wentylacyjne) ma zazwyczaj charakter burzliwy, prędkość przepływu jest większa od0,1 m/s. Rozpatrując odcinek rurociągu pomiędzy dwoma przekrojami F1 i F2 równanie Bernulliego można zapisać w postaci:
[ p1+ 0,5(W12 *ρ1)] - [ p2 + 0,5(W22 * ρ2)] = Δpstr
Jak widać z równania suma energii ciśnienia p oraz energii kinetycznej medium zmniejsza się w przekroju 2 o wielkości pracy potrzebnej na pokonanie oporów przepływu na odcinku 1-2. Wielkość tej pracy wyrażona jest spadkiem ciśnienie całkowitego Δpstr i nosi nazwę oporu przepływu.
W rurociągach podczas przepływu rozróżnia się:
- opory tarcia (hydrauliczne) spowodowane tarciem medium o ścinki rurociągu
- opory lokalne (miejscowe) spowodowane przeszkodami konstrukcyjnymi rurociągu
- opory hydrostatyczne wynikające z różnicy ciśnień pomiędzy ośrodkami transportu medium
opory tarcia:
Δpt = k*W2 *λ*ρ*L / 2D || k - współczynnik tarcia || L - długość rurociągu || D- średnica rurociągu || λ - współczynnik oporu tarcia || opory lokalne:
Δp2 = ξ* W2 * ρ / 2 || ξ - współczynnik oporów lokalnych zależy od charakteru konstrukcji, spadek ciśnienia powodują kolanka zwężki
8. Parametry charakterystyczne wentylatorów
Strumień przepływu (natężenie przepływu, wydatek) - masa lub objętość gazu przetłaczającego w jednostce czasu przez wentylator G [kg/s] - V[m3/s]
- spiętrzenie całkowite wentylatora Δp - różnica ciśnień całkowitych natłoczeniu i ssaniu wentylatora
- Moc wewnętrzna Ni - różnica mocy na wale wentylatora (mocy napędowej) oraz strat mocy w elementach konstrukcyjnych, przenoszenie napędu
- Moc użyteczna wentylatora Na - moc przekazana czynnikowi jako iloczyn ciśnień spiętrzenia i wydatku wentylatora
- sprawność wewnętrzna wentylatora ηi - stosunek mocy użytecznej Na do mocy wewnętrznej Ni || ηi = Na/ Ni
- sprawność ogólna wentylatora n= Na / Nw -stosunek mocy użytecznej do mocy na wale (inaczej do mocy napędowej)
9. Zmiana punktu pracy wentylatora
Po przez zmianę parametrów wentylatora wymaga ogólnych znajomości pewnych wielkości charakteryzujących wentylator jako maszynę służącą do wymuszenia przepływu czynnika termodynamicznego.
Przebieg krzywych charakteryzujących wentylator wyznacza się na podstawie danych doświadczalnych ustalonych dla wentylatora modelowego. Mając charakterystykę danego wentylatora zdjętą przy stałe szybkości obrotowej n można drogą obliczeń znaleźć jego charakterystykę przy innej dowolnej szybkości obrotów, a także innych wentylatorów spełniających podobieństwo geometryczne.
Oznaczając i deg. pewnie parametry wentylatora jako:
U - prędkość unoszenia powietrza równa prędkości obrotowej wirnika na jego zewnętrznym promieniu D/z
W - prędkość względna
c- prędkość bezwzględna
10. Paliwa ciekłe
Cechą charakterystyczna paliw ciekłych jest znikową zawartość popiołu ok. 0,05% oraz bardo wysoka wartość opałowa.
W zależności od pochodzenia paliwa ciekłe dzieli się na naturalne i sztuczne.
Paliwa naturalne:
- ropa naftowa jako olej surowy oraz jej pochodne
- oleje łupakowe i smołę łupakową
Paliwa sztuczne obejmują:
- smoły z upłynniania węgla
- smoły z oczyszczania gazu kokosowniczego i generatorowego
- oleje roślinne
Ropa naftowa - jako olej surowy przerabiana jest na ciekłe paliwa silnikowe, oleje opałowe, asfalty w procesach destylacji i termicznej destylacji pialitycznej
Destylacja -rozdzielenie ropy naftowej na frakcje wrzące w różnym zakresie temperatur otrzymuje się:
- gaz płynny
- paliwa silnikowe (benzyny, oleje napędowe)
- oleje opałowe
- stałe węglowodany naftowe
- asfalty drogowe i przemysłowe
- surowce węglowodorowe do syntez organicznych
Alkohole- surowcami do produkcji alkoholu technicznego są gaz ziemny, węgiel, drewno i odpady biologiczne oraz z biomasy przez fermentację i destylacje. Wytwarzane są 2 rodzaje alkoholu
- metanol CH3OH - wartość opałowa 19000 kJ/kg
- etanol C2H5OH - wartość opałowa 27000 kJ/kg
Alkohole charakteryzują się brakiem popiołu i dużą wartością liczby atomowej oraz brakiem tendencji do formowania się sadzy w płomieniach. Jako paliwo silnikowe ma niższą niż przy spalaniu paliw ciekłych emisję HC i NOx do atmosfery. Podczas spalania metanolu w silnikach spalinowych emitowane są aldehydy, a w szczególności trujący fermaldehyd.
11 .Temperatura spalania
Temp. spalania należy traktować jako parametr charakteryzujący rodzaj spalanego paliwa (skład chemiczny, wartość opałowa, warunki procesu spalania: nadmiar i temp powietrza spalania, temp paliwa) oraz cechy konstrukcyjne komory spalania. Praktycznie w każdym punkcie komory spalania zamierzona temp posiadać będzie różne wartości, dlatego obliczenia temperatur spalania dotyczyć będzie jej średniej wielkości dla danej przestrzeni komory spalania. Temp. spalania określa się w oparciu o bilans energii komory spalania. W zależności od przyjętych warunków procesu spalania rozróżnia się:
- kalorymetryczna temp spalania
- teoretyczną temp spalania
- rzeczywistą temp spalania (temp płomienia)
Równanie bilansu:
BpalQi + Bpalcpal|0tpal * tpal + vpcp|0tp *tp = vscs|0ts *ts + Qd + Qstr
ts- temp spalania
Wiedząc, że proces spalania całkowitego i zupełnego, prowadzony izobarycznie z teoretyczną ilością powietrza spalania, bez strat ciepła związanych z transportem ciepła z bilansowej przestrzeni do otoczenia czyli adiabatycznie, wówczas obliczona z bilansu energii temperatura spalania nosi nazwę temp kalorymetrycznej
tk= t1 = ( i0 + iv) / cs|0t1 [oC]
i0 = Q/vos
iv = (cpal|0tpal * tpal + v0cp|0tp *tp) / vos
gdzie:
i0 - entalpia właściwa
vos - objętość spalin teoretycznych
iv - entalpia fizyczna
v0 - objętość substratów spalania do jednostki spalin
Zakładając, że proces spalania całkowitego i zupełnego prowadzony jest izobarycznie i adiabatycznie z odpowiednim nadmiarem powietrza spalania to po uwzględnieniu strat związanych z dysocjacją Co2 i H2O (CO2 = C + O2; H2) = H2 + 0,5O2) temp spalania t2 nazywa się temperatura teoretyczną
tt = t2 = ( iλ + iv - qd) / cs|0t2 [oC]
iλ - entalpię spalin rzeczywistych
qd - ciepło dysocjacji H2O i CO2
Zakładając całkowity i zupełny proces spalania z nadmiarem powietrza spalania i uwzględniając wypromieniowanie ciepła ze spalin w bilansowanym obszarze do przestrzeni komory spalania, obliczona temperatura nosi nazwę temperatury rzeczywistej spalania lub temperatury płomienia
trz = t3 = μ ( iλ + iv - qd) / cs|0t2
μ = η ( 1- δ)
t3 = μt2
gdzie:
μ - pirometryczny współczynnik spalania, zależy d rodzaju pieca
η - sprawność spalania
δ -współczynnik promieniowania Pecleta
Ze względu na zależność wielkości występujących w równaniu bilansu energii (cs, qd) od temperatury spalania jej obliczenie możliwe jest jedynie metodami kolejnych przybliżeń.
12. Wyprowadzić różniczkowe równanie ciągłości Strugi
dq = di + d(0,5w2)
dq = 0
di = - d(0,5w2)
Po rozwinięciu równania i zmianie granic całkowania otrzymuje się:
i1 = i2= 0,5( w22- w12)
i1 + 0,5w12 = i2 + 0,5w22 = ic = const.
ic = i + 0,5w2
Entalpia właściwa całkowita jest to suma entalpii właściwej statycznej i entalpii właściwej dynamicznej.
Jeżeli pominie się tarcie wówczas różnica entalpii równa będzie pracy technicznej
i1 - i2 = It
0,5( w22- w12) = 2∫1 vdp = It
Po zróżniczkowaniu trzymuje się różniczkowe równanie ciągłości Strugi:
wdw = -vdp
ZESTAW V
1.Równanie termiczne stanu gazu wilgotnego
pV=Gg(1+x)RT - przy niezbyt wysokich ciśnieniach gaz wilgotny podlega równaniu Clapeyrona. Stała gazowa R gazu wilgotnego R=(Rg+xRp)/(1+x)
Dla powietrza wilgotnego R=(0,622+x)Rp/1+x
2.Opisać metody wyznaczania wilgotności powietrza
Wyznaczanie wilgotności powietrza na podstawie wskazań psychometru. Metoda ta polega na pośrednim pomiarze ciśnienia składnikowego pary w gazie wilgotnym za pomocą psychometru.
Assmana. Psychometr nie posiadający unormowanego przepływu powietrza nosi nazwę psychometru Augusta. Wilgotność względną można wyznaczyć także za pomocą higrometru wykorzystującego zjawisko zmiany wymiarów liniowych ciał higroskopijnych, wraz ze zmianą wilgotności powietrza.
3.Ciepło właściwe Cp pary przegrzanej nie jest stałe lecz zmienia się w zależności od ciśnienia i temperatury - wzrasta wraz ze wzrostem ciśnienia
Cp= f(P/T) Cp=Cp0 + f(P/T)
Średnie ciepło właściwe pary przegrzanej Cpm=dq/dt=(ip-i'')/(tp-t'')
W pewnym zakresie temperatur średnie ciepło właściwe pary przegrzanej
Cpm=(ip2-ip1)/(tp2-tp1)
4.Dla podanych danych wyznaczyć parametry pracy za pomocą i-s
5.Parametry krytyczne przepływu,ciśnienie,prędkość,strumień krytyczny
p0=p [2/(χ+i)] χ /( χ -1)
Przyjmując założenie β= [2/( χ +i)] χ /( χ -1) jako wielkość stałą zależna tylko do rodzaju gazu oraz zakładając,że ciśnienie końcowe odpowiada ciśnieniu w najmniejszym przekroju kanału p0=p' - ciśnienie krytyczne p'= βp
Ciśnienie krytyczne zależy tylko od ciśnienia początkowego.
Temp.krytyczna
T0/T=(p0/p) κ1/ κ κ 1 (oznacza κ1:)
podstawiamy p0=p[2/( χ +i)] χ /( χ -1)
T0=T'=T*2/(χ +i)
Prędkość krytyczna obliczyć można podstawiając do wzoru na prędkość wypływu w0=w, ciśnienie krytyczne p'=p0=βp
w'=sqrt[p*V*2*χ/(χ+1)]=sqrt[R*T*2*χ/(χ+1)] = sqrt[χ*p'*V'] prędkość krytyczna zależy tylko od początkowego stanu czynnika przy wypływie.
6.Tarcie podczas wypływu. W rzeczywistych warunkach przepływu gazu, pary oraz cieczy, ich cząstki podlegają tarciu pomiędzy sobą oraz sciankami dyszy powodując spadek prędkości. Spadek prędkości spowodowany tarciem wyrazić można tzw. współczynnikiem prędkości φ, jako stosunek prędkości rzeczywistej do teoretycznej φ=w/wt. Stratę energii spowodowanej tarciem wyrazić można (wt^2) /2 - w^2/2 = (w^2 - φ^2wt^2)/2, a miarą straty tej energii jest współczynnik strat energii ξ. ξ(wt^2)/2=[wt^2 - φ^2*wt^2]/2, gdzie ξ=1- φ^2
7.Opisać metodę pomiaru strumienia przepływu medium za Pomocą zwężki pomiarowej. Natężenie przepływu medium przez zwężkę określić można z równania ciągłości strugi
G = F*w/v= F/v sqrt[(2*v*Δp)/(1-m^2)] = F sqrt [(2*ρ*Δp)/(1-m^2)]
G= α*ε*F* sqrt[2ρΔp] kg/s
Uwzględnia się opory wewnętrzne, zewnętrzne oraz stopień ściśliwości medium podczas przepływu przez przewężenie.
α - liczba przepływu uwzględniająca m.in.prędkość czynnika przed przewężeniem, stopień rozwarcia m, własności fizyczne czynnika, tarcie czynnika o ścianki rurociągu
ε - liczba ekspansji zależy od rodzaju medium oraz spiętrzenia Δp
8.Charakterystyka siły wentylacyjnej, równanie, wykres
W celu odpowiedniego doboru sieci rurociągów i wentylatorów konieczna jest znajomość spadku ciśnienia na całej długości sieci. Spadek ciśnienia za leży od oporów tarcia, oporów lokalnych i oporu hydrostatycznego.
Δp=λ(w2 *ρ)/2 * 1/dn + ∑ ξ * (w2 *ρ)/2 + Δp0
Δp0=pk-pp(opór hydrostatyczny)
9.Opisać zmianę punktu pracy wentylatora przez równoczesną zmianę prędkości obrotów wirnika wentylatora i średnicy wirnika
Δpc/ Δp'c = i2n i2D v/v'= in i3D N/N'= i3n i5D
Ciśnienie całkowite natężenie przepływu pobrana moc
10.Omówić paliwa gazowe
Ze względu na pochodzenie gazowe paliwa dzielimy na:
-naturalne : gaz ziemny, wysokometanowy i zaozotowany,
gaz kopalniany z odmetanowania kopalin
-sztuczne: gaz wielkopiecowy(produkt uboczny wielkiego pieca)
gaz konwertorowy(prod. uboczny proc.stalowniczego)
gaz koksowniczy(prod. uboczny proc.koksowania węgla) gaz generatorowy (prod. uboczny zgazowania węgla
Ze względu na wartość energetyczną gazy palne dzielą się na:
-bogate: Qi wartość opałowa powyżej 30 MJ/m3
-ubogie: wartość opałowa poniżej 30 MJ/m3
11.Zależność szybkości reakcji spalania od temperatury
Reakcja chemiczna pomiędzy poszczególnymi cząsteczkami zależy od ich rodzaju, prawdopodobieństwa zdarzeń oraz stanu energetycznego.
Liczba zderzeń według teorii kinetyczno-molekularnej wynosi:
Z0=nA*nB*d2S * sqrt[ (8πRT)/nAG ] nA, nB - liczba cząsteczek A i B
dS=(dA+dB)/2 - średnia efektywna średnica zderzających się cząstek
Reakcja zajdzie tylko dla tych zdarzeń, których energia kinetyczna ruchu względnego jest wyższa lub równa od pewnej krytycznej energii zwanej energią aktywacji.
12. Metody obliczania stosunku nadmiaru powietrza powinno się obliczać po sporządzeniu bilansów pierwiastkowych węgla, wodoru, tlenu i azotu. Można jednak stosować przybliżone wzory, w oparciu o analizy spalin. Dla paliwa zawierającego niewielką ilość azotu przy spalaniu zupełnym można stosować wzór: λ= 1/[1- (79[O2]) / (21[N2]) ] [O2] stężenie
Można posługiwać się także tzw. stosunkiem Molliera oraz wzorem opartym na bilansie substancji procesu spalania
ZESTAW VI
1. Energia wewnętrzna gazu wilgotnego.
i = u + pv || u = i - pv
Objętość gazu wilgotnego v1-x = v(1+X)m3 / 1+Xkg
u1-x = i1-x - pv(1+X)
v- obj. Właściwa gazu wilgotnego obliczona z równania Clapeyrona wykorzystując zastępczą stałą gazową
![]()
|| p - ciśnienie gazu wilgotnego
2. Proces suszenia, model procesu suszenia
W procesie suszenia wilgotny materiał styka się z gazem nienasyconym wilgocią. Intensywność procesu suszenia jest tym większa im mniejsza jest wilgotność suszącego czynnika. Wilgotność gazu φ zmniejsza się przez podgrzanie. Wyróżnia się trzy etapy:
I - powierzchnia zewnętrzna materiału jest nasycona cieczą. Ciśnienie pary wodnej przy pow. Materiału jest równe ciśnieniu nasycenia.
II - na pow. Materiału występuje tylko wilgoć higroskopijna związana z materiałem siłami kapilarnymi. Ciśnienie pary wodnej przy pow. Jest w tym przypadku niższe od ciśnienie nasycenia.
III - powierzchnia parowania przesuwa się w głąb materiału. Wilgoć dyfunduje do powierzchni materiału w postaci pary. Temperatura powierzchni materiału wyraźnie wzrasta
3. Wykres entalpia - ciśnienie
4. Równanie Clausiusa - Clapeyrona dla pary
Równanie wyprowadza się z porównania zjawiska zmiany na parę w układzie pracy i ciepła . Jednostkowa praca w układzie p - v równa jest jednostkowemu ciepłu w układzie T-s czyli
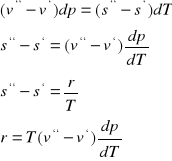
5. Ogólny opis ruchu cieczy elastycznej, ruch stacjonarny i niestacjonarny
w = f(x,y,z) ruch stacjonarny
w = f(x,y,z,t) ruch niestacjonarny
6. Opisać metodę pomiaru strumienia przepływającego medium za pomocą rurek spiętrzających.
Natężenie przepływu można także wyznaczyć za pomocą rurek spiętrzających Pitota lub Prandtla z równością ciągłości struki Bernuliego
![]()
Wykonując pomiar rozkładu ciśnienia statycznego i całkowitego czyli ciśnienia dynamicznego obliczyć można prędkość w każdym punkcie pomiaru ze wzoru:
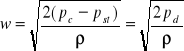
Średnia prędkość w przekroju poprzecznym wyznacza się w zależności:
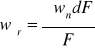
Masowe lub objętościowe natężenie przepływu oblicza się z równania ciągłości strugi:
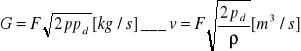
7. Charakterystyki indywidualne wentylatorów; punkt pracy.
Wentylator powinien być dobrany do sieci tak, by sprawność była maksymalna i w punkcie przecięcia charakterystyki przewodu, czyli strat ciśnienia ze względu na opór przepływu w funkcji natężenia przepływu.
Δp=f(V) oraz charakterystyka wentylatora czy ciśnienia całkowitego wentylatora w funkcji
Δpc=f(V) w punkcie tym przy najmniejszym zapotrzebowaniu mocy N przez wentylator η- stosunek mocy użytecznej Nu czyli mocy przekazanej przez wentylator przetłaczanemu czynnikowi do mocy na wale czyli mocy napędowej Nw
![]()
Do oceny stopnia ekonomiczności pracy wentylatora pracującego na wydmuch tj. bez siły tłocznej, gdy całe ciśnienie dynamiczne zostaje tracone, służy statyczna sprawność wentylatora.
![]()
Δps - ciśnienie statyczne wentylatora N/m2
Pkt. Pracy wentylatora - określa on ilość przepływającego czynnika przez siec przy odpowiednim ciśnieniu całkowitym wytworzonym przez wentylator, co powinno nastąpić przy sprawności wentylatora. Zmiana parametrów pracy następuje przy zmianie oporów sieci co można uzyskać poprzez dławienie gazu, wówczas pkt. pracy przesunie się w położenie 2 oraz nastąpi zmniejszenie wydajności z V1 na V2 przy wzroście ciśnienia całkowitego Δpc1 na Δpc2. Zmiana wydajności poprzez dławienie może następować w kierunku jej zmniejszenia.
8. Opisać metody zmiany punktu pracy wentylatora poprzez zmianę oporu jednostkowego sieci.
Punkt pracy wentylatora można zmienić przez zmianę oporu jednostkowego sieci, zmianę prędkości obrotów wentylatora, zmianę parametrów geometrycznych wentylatora. Zmiana oporu jednostkowego sieci poprzez zwiększenie oporu jednostkowego sieci np. przez przymknięcie przepustnicy uczyni charakterystykę sieci bardziej stromą, spowoduje zmniejszenie poboru mocy, lecz także zwiększy wydatek. Natomiast wzrost nieszczelności w sieci zwłaszcza w pobliżu wentylatora spowoduje spadek oporów jednostkowych, znaczny wzrost wydatku a moc pobierana może wzrosnąć tak wysoce, że silnik zostanie przegrzany i ulegnie uszkodzeniu. Silnik może także ulec zniszczeniu jeżeli wentylatory promieniowe z silnikami asynchronicznymi są uruchomione przy całkowicie otwartej zasuwie.
9. Omówić paliwa odnawialne.
Paliwa odnawialne stano biomasa do której zalicza się drewno i słomę oraz odpady zawierające odpady palne min. odpady komunalne, medyczne, przemysłowe. Większość biomasy jest pochodzenia roślinnego powstała w procesie fotosyntezy z wykorzystaniem energii słonecznej.
Fotosynteza - fotochemiczna konwersja energii słonecznej w energię chemiczną węglowodanu. Drewno jest paliwem biologicznym którego ilość odnawia się corocznie. Świeżo ścięte drzewo zawiera 40-50 % wilgoci przy wartości opałowej ok. 8400 kJ/kg. Po wysuszeniu na powietrzu zawiera 15-25% wilgoci i ma wartość opałową 12500 - 14500 kJ/kg.
Słoma i odpady roślinne - są energetycznie mniej wartościowym paliwem jednak ze względu na duży coroczny przyrost ich masy są cennym paliwem odnawialnym.
10. Opóźnienie zapłonu.
W zależności od ciśnienia i składu mieszanki paliwowo powietrznej zapłon nie następuje po uzyskaniu ze źródła zewnętrznego temperatury równej temperaturze zapłonu, lecz dopiero po pewnym czasie zwanym czasem indukcji. Im wyższa temp. źródła zewnętrzno lub ściany pieca oraz ciśnienie mieszanki tym krótszy jest czas indukcji. Dla paliw stałych spalanych w postaci pyłu, opóźnienie zapłonu może być znaczne powodujące spalanie niestabilne np. oderwane płomienia od palnika. Dla paliw ciekłych całkowity czas opóźnienia zapłonu wynosi τ = τg + τp + τch
τp - czas parowania kropli paliwa
τg - czas konieczny do podgrzania kropli paliwa
τch - czas chemicznego opóźnienia zapłonu zależy tylko od struktury chem. paliwa a nie od średnicy kropli.
11. Obliczenia ilości spalin podczas całkowitego i zupełnego spalania.
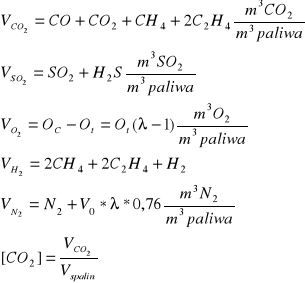
p, w, F
p', w', F'
p0, w0, F0
dyfuzor
konfuzor
dp = 0
Wyszukiwarka
Podobne podstrony:
Egzamin z fizyki, Uczelnia, Metalurgia
egzamin moc, Uczelnia, Metalurgia
Egzamin fizyka, Uczelnia, Metalurgia
PROCESY NIESTACJONARNEJ WYMIANA CIEPŁA, Uczelnia, Metalurgia
terma egzamin
Statyczna próba rozciągania - sprawko, Uczelnia, Metalurgia
Ogólne podstawy projektowania i konstruowania elementów maszyn, Uczelnia, Metalurgia
Materiałznawstwo, Uczelnia, Metalurgia
MOC, Uczelnia, Metalurgia
polityka na egzamin1, Uczelnia, Bezpieczeństwo państwa
Procesy stalownicze, Uczelnia, Metalurgia
Cyna, Uczelnia, Metalurgia
pyt na egzamin, uczelnia
chirurgia egzamin, Uczelnia, giełda chirurgia, gielda
neurologia 2009 egzamin, Uczelnia, Neurologia
algorytmy egzamin, !!!Uczelnia, wsti, materialy, II SEM, algorytmy struktury danych
więcej podobnych podstron