SPRAWOZDANIE Z ĆWICZENIA NR 3 - PRZEWODNICTWO ELEKTROLITÓW
Grupa II :
Michał Październik
Paweł Pietrzykowski
Adam Pośpiech
Grzegorz Wiszowaty
Ćwiczenie 1. Pomiar przewodnictwa równoważnikowego słabych elektrolitów |
||
Data |
Ocena |
Podpis asystenta |
Tabela 1. Wyniki pomiarów
(Temperatura prowadzenia oznaczeń: 298 K).
Stężenie roztworu [mol/l] |
Przewodnictwo roztworu λ [S] |
0,01 KCl |
2,79 x10-3 |
C = 0,03020 C/2 = 0,0151 C/4 = 7,55x10-3 C/8 = 3,77 x10-3 C/16 = 1,89 x10-3 C/32 = 9,44 x10-4 C/64 = 4,72 x10-4
|
638 x10-6 520 x10-6 393 x10-6 286 x10-6 213 x10-6 183 x10-6 156 x10-6 |
Stała naczynka k:
k = ![]()
= ![]()
= 50,645 m-1
Tabela 2. Wyniki obliczeń
Stężenie roztworu [mol/l] |
Przewodnictwo właściwe κ [S/m] |
Przewodnictwo równowaznikowe Λ [Sm2 /mol] |
0,01 KCl |
0,1431 |
1,431 |
C = 0,03020 C/2 = 0,0151 C/4 = 7,55x10-3 C/8 = 3,77 x10-3 C/16 = 1,89 x10-3 C/32 = 9,44 x10-4 C/64 = 4,72 x10-4
|
0,03231 0,02633 0,01990 0,01449 0,01079 9,26x10-3 7,90x x10-3
|
1,07 x10-3 1,74 x10-3 2,63 x10-3 3,84 x10-3 5,71 x10-3 9,81 x10-3 1,67 x10-2 |
Wykres zależności Λ = f( √C) dołączony do sprawozdania.
Obliczenia:
k = ![]()
czyli κ = λ x k
Λ = 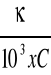
κ C = 50,645 x 638 x10-6 = 0,03231 S/m
ΛC = 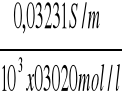
= 1,07 x10-3 Sm2/mol
κ C/2 = 50,645 x 520 x10-6 = 0,02633 S/m
ΛC/2 = 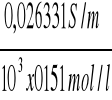
= 1,74 x10-3 Sm2/mol
κ C/4 = 50,645 x 393 x10-6 = 0,01990 S/m
ΛC/4 = 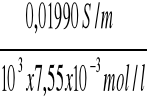
= 2,63 x10-3 Sm2/mol
κ C/8 = 50,645 x 286 x10-6 = 0,01449 S/m
ΛC/8 = 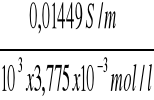
= 3,84 x10-3 Sm2/mol
κ C/16 = 50,645 x 213 x10-6 = 0,01079 S/m
ΛC/16 = 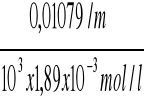
= 5,71 x10-3 Sm2/mol
κ C/32 = 50,645 x 183 x10-6 = 9,26x10-3 S/m
ΛC/32 = 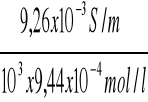
= 9,81 x10-3 Sm2/mol
κ C/64 = 50,645 x 156 x10-6 = 7,90x x10-3 S/m
ΛC/64 = 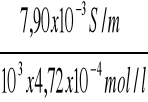
= 1,67 x10-2 Sm2/mol
Ćwiczenie 2. Pomiar przewodnictwa równoważnikowego mocnych elektrolitów |
||
Data |
Ocena |
Podpis asystenta |
Tabela 3. Wyniki pomiarów
(Temperatura prowadzenia oznaczeń: 298 K).
Stężenie roztworu [mol/l] |
Przewodnictwo roztworu λ [S] |
C = 0,02 C/2 = 0,01 C/4 = 0,005 C/8 = 2,5 x10-3 C/16 = 1,25 x10-3
|
296 x10-6 166,3 x10-6 137,6 x10-6 120,0 x10-6 108,5 x10-6 |
Tabela 4. Wyniki obliczeń
Stężenie roztworu [mol/l] |
Przewodnictwo właściwe κ [S/m] |
Przewodnictwo równowaznikowe Λ [Sm2 /mol] |
C = 0,02 C/2 = 0,01 C/4 = 0,005 C/8 = 2,5 x10-3 C/16 = 1,25 x10-3
|
0,01499 8,42 x10-3 6,97 x10-3 6,08 x10-3 5,49 x10-3 |
7,49 x10-4 8,42 x10-4 1,39 x10-3 2,43 x10-3 4,39 x10-3 |
Współczynniki a i b zostały obliczone metodą najmniejszych kwadratów:
a = - 0,0305
b = Λ0 = 0,0043 , a więc równanie ma postać - 0,0305x + 0,0043
Wykres zależności Λ = f( √C) dołączony do sprawozdania.
Obliczenia:
κ C = 50,645 x 296 x10-6 = 0,01499 S/m
ΛC = 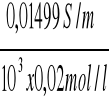
= 7,49 x10-4 Sm2/mol
κ C/2 = 50,645 x 166,3 x10-6 = 8,42 x10-3 S/m
ΛC/2 = 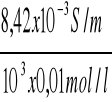
= 8,42 x10-4 Sm2/mol
κ C/4 = 50,645 x 137,6 x10-6 = 6,97 x10-3 S/m
ΛC/4 = 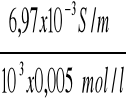
= 1,39 x10-3 Sm2/mol
κ C/8 = 50,645 x 120,0 x10-6 = 6,08 x10-3S/m
ΛC/8 = 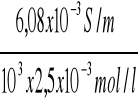
= 2,43 x10-3 Sm2/mol
κ C/16 = 50,645 x 108,5 x10-6= 5,49 x10-3 S/m
ΛC/16 = 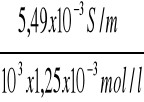
= 4,39 x10-3 Sm2/mol
Ćwiczenie 3. Pomiar iloczynu rozpuszczalności trudno rozpuszczalnej soli |
||
Data |
Ocena |
Podpis asystenta |
Tabela 5. Wyniki pomiarów
(Temperatura prowadzenia oznaczeń: 298 K).
Nr pomiaru |
Przewodnictwo λ [S] |
|
|
Woda |
Roztwór soli |
1 2 3 wartość średnia |
6 x10-6 ---------------- ---------------- 6 x10-6 |
23,4 x10-6 22,4 x10-6 22,8 x10-6 22.87 x10-6 |
Stała naczynka, zgodnie z wcześniejszymi obliczeniami wynosi: k = 50,645 m-1
Tabela 6. Wyniki obliczeń
Λ0sól = 286,9 x10-4 Sm2/mol (wartość podana przez asystenta)
Przewodnictwo właściwe κ [S/m] |
Stężenie soli C [mol/l] |
Iloczyn rozpuszczalności L |
||
Woda κ1 |
R-r soli κ2 |
Sól κ2 - κ1 |
|
|
4,55 x10-4
|
1,16 x10-3 |
7,05 x10-4 |
2,46 x10-5 |
6,04 x10-10 |
Obliczenia:
κ1 = 50,645x6 x10-6 = 4,55 x10-4 Sm2/mol
κ2 = 50,645x22.87 x10-6= 1,16 x10-3 Sm2/mol
κ2 - κ1 =1,16 x10-3 - 4,55 x10-4 = 7,05 x10-4Sm2/mol
Stężenie soli :
Λ= 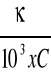
, a więc C = 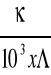
C = 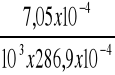
= 2,46 x10-5 mol/l
Iloczyn rozpuszczalności soli :
MeX Me+ + X-
[Me+] = [X- ] = C , a więc L = C2
L = (2,46 x10-5 )2 = 6,04 x10-10
Ćwiczenie 4. Wyznaczanie stałej dysocjacji słabego elektrolitu metodą konduktometryczną i przewodnictwa granicznego |
||
Data |
Ocena |
Podpis asystenta |
Tabela 7. Wyniki pomiarów i obliczeń
(Temperatura prowadzenia oznaczeń: 298 K).
C [mol/dm3] |
λ [S] |
κ [S/m] |
Λ [Sm2/mol] |
|
C |
0,01007 |
442x10-6 |
0,022 |
2,18x10-3 |
C/2 |
5,03x 10-3 |
350x10-6 |
0,018 |
3,51x10-3 |
C/4 |
2,52x10-3 |
275x10-6 |
0,0139 |
5,52x10-3 |
C/8 |
1,26x10-3 |
212x10-6 |
0,0107 |
8,5x10-3 |
C/16 |
6,2910-4 |
173x10-6 |
8,76x10-3 |
0,014 |
Obliczenia:
κ C = 50,645 x 442x10-6= 0,022 S/m
ΛC = 
= 2,18x10-3 Sm2/mol
κ C/2 = 50,645 x 350x10-6 = 0,018 S/m
ΛC/2 = 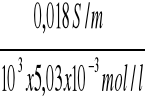
= 3,51x10-3 Sm2/mol
κ C/4 = 50,645 x 275x10-6 = 0,0139 S/m
ΛC/4 = 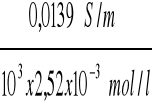
= 5,52x10-3 Sm2/mol
κ C/8 = 50,645 x 212x10-6= 0,0107 S/m
ΛC/8 = 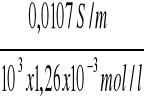
= 8,5x10-3 Sm2/mol
κ C/16 = 50,645 x 173x10-6= 8,76x10-3 S/m
ΛC/16 = 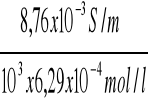
= 0,014 Sm2/mol
Równanie ma postać :
![]()
= ![]()
+ ![]()
Wyznaczone ze wzorów regresji liniowej współczynniki a i b wynoszą:
a = 24561403,51
b = -140,35 , a więc funkcja ma postać y = 24561403,51x -140,35
b = ![]()
, a więc Λ0 = ![]()
= 0,007125 Sm2/mol
a = ![]()
, a więc K = ![]()
= 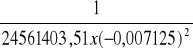
= 8,02 x 10-4
Wykres zależności 1/Λ=f(CxΛ) został dołączony do sprawozdania.
Wyszukiwarka
Podobne podstrony:
sprawko z przewodnictwa poprawione, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawoz
SPRAWOZDANIE Z farmako, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fizy
sprawko z ćwiczenia 11, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fizy
Napiecie powierzchniowe, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fiz
janka, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fizycznej 1, Sprawozd
Wspolczynnik podzialu, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fizyc
SPRAWOZDANIE Z ĆWICZENIA NR 2, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania
inwersja sacharozy, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fizyczne
sprawko z refraktometrii, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fi
sprawozdanie z ćw.7, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fizyczn
SPRAWOZDANIE Z ĆWICZENIA 4, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z
Przewodnictwo elektrolitów, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z
koloidy i emulsje, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fizycznej
Sprawozdanie z cwiczenia 19, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z
SPRAWOZDZANIE Z ĆWICZENIA NR 6, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdani
SPRAWOZDANIE Z farmako, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fizy
sprawko z ćwiczenia 11, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fizy
więcej podobnych podstron