
F
F
IZJOLOGIA
IZJOLOGIA
R
R
OŚLIN
OŚLIN
Pytania na egzamin
Hormony roślinne
wzrost i rozwój roślin
ruchy roślin
s. 2-19
Gospodarka wodna
transpiracja
transport substancji w roślinie
s. 20-33
Gospodarka mineralna
oddziaływania pomiędzy organizmami
s. 35 - 45
Budowa i elementy komórek roślinnych
błony biologiczne
chemosynteza
oddychanie
s. 47 - 65
Fotosynteza
S. 67 -87
Strona 1
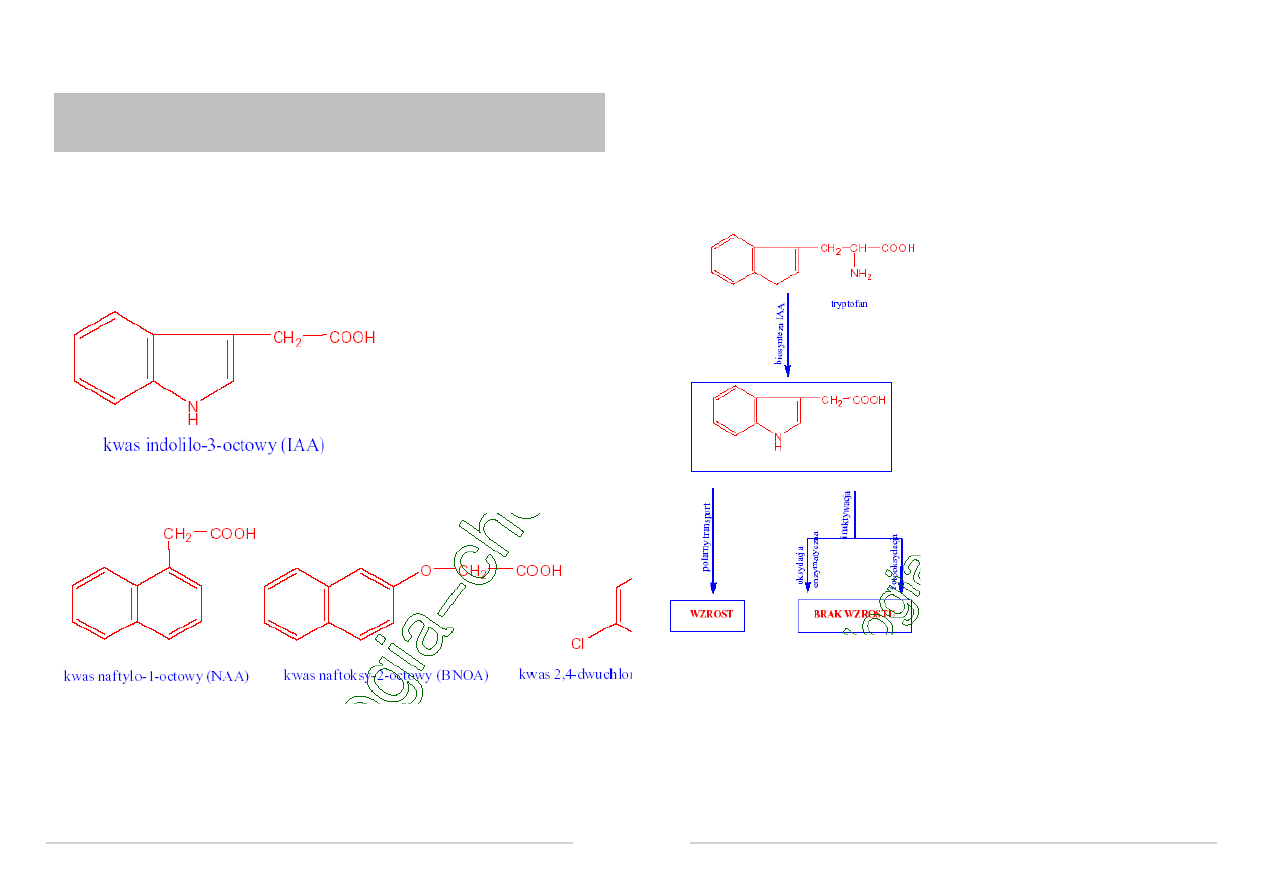
Auksyny - rola w procesach fizjologicznych i
metabolicznych
Auksyny są to związki organiczne, które charakteryzuje zdolność
wywoływania wzrostu elongacyjnego (wydłużeniowego) komórek łodygi w
sposób podobny do kwasu indolilo-3-octowego. Test wygięciowy Avena i
test cylindryczny Avena potwierdzaja i służą do oznaczania i porównywania
ilości auksyn.
Najpospolitszą i
prawdopodobnie jedyną
naturalną auksyną
wszystkich roślin wyższych
jest: kwas indolilo-3-octowy.
Podobne działanie do do
IAA mają auksyny
syntetyczne, stosowane w
różnych celach w rolnictwie
i ogrodnictwie.
AUKSYNY SYNTETYCZNE
Auksyny tworzą się przede wszystkim w pąkach wierzchołkowych oraz w
najmłodszych
liściach i tam zwykle jest ich najwyższe stężenie.
W kierunku od wierzchołka do podstawy rośliny (bazypetalnie), transport
auksyn jest bardzo szybki – prawdopodobnie jest to transport aktywny
wymaga, bowiem obecności cukrów i tlenu a więc energii uwalnianej w
procesie oddychania.
W kierunku przeciwnym natomiast tj. od podstawy łodygi do jej
wierzchołka (akropetalnie),zachodzi wolno, zgodnie z prawami dyfuzji.
SCHEMAT BIOSYNTEZY I INAKTYWACJI
KWASU INDOLILO-3-OCTOWEGO
Kwas indolilo-3-octowy powstaje
najprawdopodobnie z tryptofanu.
nadmiar IAA może wywołać
nadmierny wzrost roślin. Z organów
rośliny, w którym następuje synteza
IAA, jest on szybko i polarnie
odprowadzany do innych części
rośliny. Ponadto IAA może ulegać
inaktywacji drogą utlenianiania:
- pod wpływem specyficznego
enzymu
oksydoredukcyjnego - IAA-
oksydaza
- pod wp³ywem świat³a
Prawdopodobnie energia świetlna
poch³onięta przez ryboflawinę
(witamina B2) przeprowadza IAAw
formę nieaktywną tj.
nieprzyśpieszającą wzrostu.
Zjawisko to nazywamy
fotooksydacją. w ten sposób światło
hamuje wzrost.
A zatem kwas indolilo-3-octowy jest
zarówno produkowany jak i
przemieniany w formę nieaktywną
Strona 2

WPŁYW AUKSYN NA ROŚLINY
Wydłużanie komórek – Auksyny powodują rozluźnienie struktury ściany
komórkowej czyniąc ją bardziej podatną na rozciąganie a równocześnie
zwiększają przenikanie wody do komórki. Proces ten przebiega jedynie w
obecności tlenu,
co świadczy o tym, Se związane sąz oddychaniem.
Podziały komórek – zwłaszcza kambium, czyli w merystemie bocznym
położonym między ksylemem a floemem. Powoduje to przyrost pnia na
grubość. Innym przykładem pobudzania podziałów komórkowych przez
auksyny jest powstawanie kalusu.
Wytwarzanie zawiązków korzeniowych
Wzrost owoców – owoce tworzą się przez rozrost zalążni albo dna
kwiatowego. Czynnikiem, który pobudza rozrost są auksyny, produkowane
przez rozwijające się nasiona. Im większa jest produkcja auksyn tym
intensywniejszy jest wzrost i tym większe są owoce.
Partenokarpia – jeśli zastąpimy naturalne auksyny auksyną syntetyczną
powstaną owoce różniące się jedynie tym, Se nie będą posiadać nasion.
Zjawisko wytwarzania owoców bez zapłodnienia nazywamy partenokarpią.
Hamowanie rozwoju pąków bocznych i dominacja wierzchołkowa –
auksyny wytwarzane są w wierzchołku wzrostu, a następnie są
transportowane polarnie w stronę korzenia. Posuwając się w dół fala
auksyn wprowadza paki boczne w stan spoczynku (uśpienia)
*
. Rozwój
pąka wierzchołkowego.
Zrzucanie liści i owoców – w miarę jak liść się starzeje, zawartość auksyn
zmniejsza się i różnica w stężeniu auksyn pomiędzy blaszką a ogonkiem z
wolna zaciera się. Gdy zniknie zupełnie tzn., gdy stężenie auksyn w
blaszce zrówna się z ogonkiem – wtedy tworzy się warstwa odcinająca i
liść opada (ta sama zasada dotyczy owoców).
Ruchy roślin – mechanizm ruchów roślinnych takich jak fototropizm
(reakcja roślin na jednostronne oświetlenie) i geotropizm (reakcja roślin na
ciążenie związana jest z aktywnością auksyn.
Czynniki warunkujące kwitnienie roślin.
Proces ten nie następuje w dowolnej porze roku, lecz jedynie w
określonych warunkach, wymaga mianowicie okresu obniżonej
temperatury oraz odpowiedniej długości dnia. Dopiero gdy te warunki
zostaną spełnione roślina może zakwitnąć.
Rośliny różnią się w reagowaniu na czas trwania światła i ciemności . Ze
względu na tę reakcję rośliny możemy podzielić na grupy:
-
Rośliny krótkiego dnia (RKD) - kwitną wtedy jeżeli dzienny okres
oświetlania (fotoperiod) jest krótszy od pewnej krytycznej długości .
Jeżeli okres oświetlenia jest dłuższy rośliny nie kwitną , lecz
pozostają w stadium wegetatywnym. Krytyczna długość nie jest
jednakowa dla wszystkich RDK , lecz zależy od gatunku rośliny i
może się wahać od 11 do 15 godzin .
-
Rośliny długiego dnia(RDD) - kwitną wtedy, kiedy dzienny okres
oświetlania jest dłuższy od krytycznego , jeżeli jest krótszy – rośliny
pozostają w stadium wegetatywnym . Długość okresu krytycznego
nie jest stała , lecz podobnie jak RDK zależy od gatunku rośliny i
waha się od 8 do 15 godzin.
-
Rośliny neutralne (czyli niewrażliwe na długość dnia) , rośliny te
zakwitają po osiągnięciu stanu gotowości do kwitnienia niezależnie
od długości dnia.
Substancje wpływające na kwitnienie:
-
giberelina pobudza ona wytwarzanie pędów kwiatowych , może
zastąpić długi dzień u niektórych roślin. Jednak żadna z giberelin
nie wywołuje zakwiatania roślin dnia krótkiego
-
drugą substancją, której dotychczas nie udało się wyodrębnić i
zbadać jest tzw. Antezyna , ma pobudzać wytwarzanie kwiatów.
Zakwitnięcie rośliny wymaga wytworzenia zarówno łodygi jak i kwiatu
zatem hipotetyczny regulator kwitnienia zwany florigenem powinien
składać się z obu wymienionych substancji czyli : Florigen =
giberelina + antezyna
Strona 3

Endogenne inhibitory wzrostu
- morfaktyny,retardanty, herbicydy.
Inhibitory wzrostu są to związki org. które w stężeniach fizjologicznych
hamują takie procesy jak wydłużanie łodygi oraz jej wycinków, wzrost korzeni,
kiełkowanie nasion, otwieranie pąków, i kwitnienie. Hamowanie tych procesów ma
charakter odwracalny, ma wiec obniżenie poziomu inhibitora w roślinie wznawia
zahamowany poprzednio proces. Spośród związków o charakterze inhibitorów
wzrostu najszersze zastosowanie w praktyce rolniczej i ogrodniczej znalazły
retardanty i morfaktyny.
Retardanty: są to syntetyczne inhibitory wzrostu hamujące wzrost
elongacyjny łodyg bez powodowania innych deformacji, a działające przeciwnie niż
gibereliny. Grupa retardantow obejmuje kilkadziesiąt substancji o rożnej strukturze
chemicznej:
A)
chlorek chlorocholiny (chlorek 2-chloroetylotrimetyloaminy ,ccc).
Jest pochodna choliny, która wchodzi w skład lecytyny ,naturalnego składnika
tłuszczowego wszystkich org. żywych.
B) inne retardanty
Odmienna budowę chem, lecz zbliżone działanie fizjologiczne posiadają rożne
substancje produkowane na skalę przemysłową do potrzeb rolnictwa.
Rośliny poddane działaniu retardantów maja charakterystyczny pokrój:
-sa karłowate wskutek silnego skrócenia miedzywiężli,
-łodygi ich są zgrubiale
-liście maja zabarwienie ciemnozielone
Objawy przypominają łączny wpływ działania światła o dużej intensywności oraz
niskiej temp. I są przeciwne objawom wywoływanym przez gibereliny.
Konkurencyjny wpływ giberelin i retaredantow na wzrost roślin wypływa z
przeciwnego działania obu typów regulator na podziały komórkowe w
merystemie podwierzcholkowym ( gibereliny przyspiesza je, a retardanty
hamują powodując w ten sposób skracanie międzywiężli i karlenie roślin).
Prawdopodobnie retardanty blokują niektóre ogniwa biosyntezy giberelin,
wskutek czego po zastosowaniu retardantow poziom giberelin się obniża.
Reatardanty stosuje się w uprawie roślin ozdobnych (azalie, gożdziki iinne)
głownie w celu zapobiegania nadmiernemu wydłużaniu łodyg. Reatardanty
wzrostu maja również uboczne działanie , niekiedy pożądane z punktu
widzenia praktyki, wzmagają odporność roślin na niekorzystne warunki
otoczenia ( niska temp. , susza, nidopowedni odczyn podłoża, smog, i inne ) a
ponadto zwiększają odporność roślin na choroby wywołane
mirkoorganizammi.
Morfaktyny: są syntetycznymi inhibitorami wzrostu , kotre hamują wzrost
elongacyjny łodyg i wywierają głęboki wpływ na organogenze roślin .Pod
względem chemicznym morfaktyny są pochodnymi fluorenu.
Morfaktyny ,wchłonięte przez korzenie albo liście , hamują wzrost i
organogeneze młodych organów , nie wpływając na stan organów starych w
przeciwieństwie do innych regulatorów wzrostu morfaktyny działają powoli, lecz w
sposób długotrwały.
Morfkatyny wywierają silny wpływ morfologiczny na rośliny hamują one podziały
komórkowe w merytsatemach wierzvholkowych , co powoduje skracanie
międzywiężli i ogólnie karlenie rośliny. Powierzchnia blaszek liściowych się
zmniejsza. Morfaktyny zmieniają dominacje wierzchlowkowa- hamują rozwój
paka szczytowego oraz pobudzają rozwój pąków bocznych. Rośliny staja się
wiec silnie rozgałęzione , przy czym pędy boczne często ulęgają deformacji
np. fascjacji (staśmienieu) . Korzenie pod wpływem morkatyn ulęgają
podobnym zmianom morfologicznym ,a ponadto często zaczynają rosnąc w
gore ,zamisat jak normalnie w dol (zaburzenia geotropizmu). Morfaktyny
działają w pewnych procesach antagonistycznych do gibereln, natomiast w
innych antagonistycznie do auksyn lub cytokinin. Nie można jednak uważać
morfaktyn ani za antygibereliny ,ani za auksyny,ani tez za antycytokininy
>Morfaktyny sa raczej wielofunkcyjnymi substancjami zakłócającymi
normalne procesy wzrostu i rozwoju roślin. Hamujące działanie wzrostu roślin
wykorzystuje się w przypadkach w których zależy nam na zachowaniu gęstej
pokrywy roślinnej terenu łatwo ulęgającego erozji wskutek wiatru lub
deszczu., Morkatyny hamują bowiem zbyt bujny wzrost , co pozwala również
zaoszczędzać na koszeniu, lecz nie niszczą całkowicie roślin. Morfaktyny
mogą być również używane do niszczenia chwastów, szczegfl9onie w
połączeniu z niektórymi herbicydami.
Herbicydy:
Nie stanowią grupy inhibitorów wzrostu w sensie fizjologicznym, należą do nich
związki o rożnej budowie chemicznej. O działaniu , a łączy je ze osobna
jedynie podobny sposób stosowania w praktyce .
Herbicydy są to zawiązki fitotoksyczne (trujące dla roślin) używane do niszczenia
nieporządnej roślinności ,a wiec chwastów, roślin rosnących na torowiskach
kolejowych, placach budowanych itp.
Ze względu na sposób stosowania herbicydy można podzielić na:
a)
Totalne - niszczace wszystkie rośliny
b)
Selektywne - niszczące tylko pewne rośliny np. chwasty , lecz nie
działające toksycznie na inne gatunki roślin, np. na rośliny uprawne.
Strona 4

Totalność bądź selektywność zależy od stężenia herbicydów- przy odpowiednio
dużych dawkach każdy prawie herbicyd wykazuje selektywność w stosunku
do kresloych roślin.
Herbicydy można zastosować:
- przedwschodowo – przed wschodami roślin, tak ze wchłaniane są one prze
korzenie lub podziemne części pędu
- powschodowo- wtedy herbicydy działają głownie na liście i pędy.
W zależności od sposobu działania rozróżniamy herbicydy:
•
kontaktowe , czuli działające miejscowo, jedynie na tkankę roślinną, z
która się zetknęły,
•
-układowe – wchłaniane prze rośliny przemieszczające się w jej systemie
przewodzącym w naczyniach lub sitach i działające toksycznie na cały
organizm rośliny. Przy opryskiwaniu nadziemnych części rośliny herbicydy
systematycznie przedostają się szybko do systemu korzeniowego
natomiast przy zastosowaniu doglebowym sa przebrane prze korzenie i
dostają się do części nadziemnych.
Ze względu na budowę chemiczną. Herbicydy dzieli się na :
- nieorganiczne
- organiczne
Fototoksycznosc herbicydów:
Herbicydy działają niszcząco na rośliny w bardzo niskich stężeniach, co wynika z
faktu, ze herbicyd pozostaje w roślinie prze długi okres w postaci
niezmienionej i przez cały czas oddziałuje na nią szkodliwie. Dlatego z
fizjologicznego punktu widzenia herbicydy można określić jako substancje
które dezorganizują równowagę fizjologiczna rośliny na długo przed jej
śmiercią.
Selektywność herbicydów:
Nie jest jedynie cecha herbicydu , lecz wynika z wzajemnych zależności roślin,
herbicydu oraz sposobu jej stosowania. Selektywność może opierać się na
czynnikach fizycznych i biochemicznych:
-selektywność fizyczna (topograficzna) –s tosuje się rożne zabieg i celem
zwiększenia kontaktu herbicydów z chwastami w porównaniu z roślinami
uprawnymi (stosowanie herbicydu przed wysiewem roślin uprawnych lub
przed wschodami) lub zmniejszenie kontaktu herbicydu z roślinami
uprawnymi (stosując spryskiwanie w pasach miedzy roślinami np. w
uprawach okopowych).
Selektywność biochemiczna wykorzystuje różnice w metabolizmie pomiędzy
roślinami wrażliwymi a odpornymi na działanie herbicydów. Selektywność ta
przejawia się w niejednakowym przekształcaniu się herbicydów w roślinach
rożnych gatunków. Istnieją dwie możliwości tych przekształceń: u roślin nie
wrażliwych herbicyd rozkłada się do nietoksycznych związków w roślinach
wrażliwych herbicyd przekształca się na związki toksyczne.
Strona 5
Endogenne regulatory wzrostu roślin
– krotka charakterystyka
Regulatory wzrostu są to związki org. które w bardzo małych ilościach
wykształcających oddziaływanie troficzne(odżywcze) zwiększają,
hamują lub w inny sposób wpływają na procesy wzrostu i rozwoju
roślin. Regulatory wzrostu można uważać za rodzaj chemicznych
sygnałów powstających w niewielkich ilościach w określonych
częściach roślin. Z tych miejsc regulatory wzrostu są przekazywane
przez system prowadzący do innych części, w których kierują
procesami wzrostu i rozwoju roślin. Z tej przyczyny przez analogie z
hormonami występującymi w organizmach zwierzęcych, regulatora
wzrostu roślin są także nazywane hormonami roślinnymi albo
fitohormonami.
Wyróżniamy zasadniczo 5 grup regulatorów wzrostu: auksyny,
gibereliny, cytokininy, inhibitory wzrostu, etylen
Niezależnie od tego podziału, wśród regulatorów wzrostu można wyróżnić
regulatory endogenne(naturalne) wytwarzane przez rośliny oraz
egzogenne- sztucznie wprowadzane do roślin w postaci syntetycznych
preparatów.
Auksyny -to związki, które charakteryzuje zdolność wywoływania wzrostu
elongacyjnego komórek łodyg w sposób podobny do kw. Idolilo – 3
octowego, który jest najpospolitsza i prawdopodobnie jedyna naturalna
auksyna.
Działanie fizjologiczne podobne do IAA maja również auksyny
syntetyczne, stosowane w rożnych kw. 2,4 dichlorofenoksyoctowy(2,4-D)
Auksyny występują we wszystkich roślinach wyższych, a także w
niektórych grzybów. Tworzą się przede wszystkim w pakach
wierzchołkowych oraz w najmłodszych liściach i tam jest zwykle ich
najwyzsze stężenie. Z tkanek tych auksyny są przewodzone do innych
części rośliny przy czym transport ten ma charakter polarny, tzn.
zależy od kierunku. W kierunku od wierzchołka do podstawy
rośliny(bazypetalnie) transport auksyn jest bardzo szybki,
prawdopodobnie jest to transport aktywny wymaga bowiem aktywności
cukrów i tlenu, a wiec energii uwalnianej w procesie oddychania; w
kierunku przeciwnym od podstawy łodygi do wierzchołka (akropetalnie)
zachodzi wolno zgodnie z prawem dyfuzji.
Wpływ auksyn na rośliny:
-
za charakterystyczna cechę auksyn należy uznać ich wielofunkcyjność
polegająca na uczestnictwie w rożnych procesach.
-
Wydłużanie komórek w strefie wzrostu : auksyny rozluźniają strukturę
ściany kom., czyniąc bardziej podatna na rozciąganie a równocześnie
zwiększa przenikanie wody do komórki (następuje wzrost wakuoli oraz
wywołane tym rozciąganie kom.)
-
Podziały komórek zwłaszcza w kambium(merystem boczny położony
pomiędzy ksylenem a floemem)
-
Co można prześledzić u roślin drzewiastych (pierścienie roczne) +
powstawanie kalusa w przypadku zranienia łodygi.
-
Tworzenie zawiązków korzeniowych : im więcej auksyn(w pewnych
granicach) tym korzenie wytwarzają się szybciej i obficiej
+dodatni wpływ auksyn na ukorzenienie
-
Partenokarpia: auksyny , produkowane prze rozwijające się nasiona
pobudzają rozrost zalążka albo dna kwiatowego (partenokarpia
wytwarzanie owoców bez zapłodnienia
-
Hamowanie rozwoju pąków bocznych i dominacja wierzchołkowa
-
Wzmocnienie liści i owoców –auksyny powstrzymują opadanie
owoców i liści
-
fototropizm i geotropizm
Strona 6

Partenokarpia: auksyny , produkowane prze rozwijające się nasiona
pobudzają rozrost zalążka albo dna kwiatowego (partenokarpia
wytwarzanie owoców bez zapłodnienia)
Gibereliny:
- charakterystyczna cecha giberelin jest zwiększanie wzrostu łodyg,
stymulacja podziału kom. Oraz wpływ ba wiele innych procesów
fizjologicznych
- giberelina są to związki org. które maja taki sam szkielet gibam jak kwas
giberelowy i wykazują w testach karłowatych uwfantow (przywracają
karłowatym odmianom kukurydzy lub grochu normalny wzrost) oraz
indukcji
α
amylazy w kiełkujących ziarenkach jęczmienia .
Gibereliny można zaliczyć do terpenoidow tzn. związków których
jednostka budowy jest izopren. Wszystkie gibereliny są kwasami i maja
identyczna konfiguracja oparta na czteropierscioeniwym rdzeniu
giberenowym. Poszczegolne gibereliny oznacza się symbolem GA z
odpowiednia liczba kolejna (GA1 Ga2 itd.). Najlepiej zbadana giberelina
jest kw. Giberelowy (GA3) występujący w wielu roślinach oraz
produkowany fabrycznie. Gibereliny występują powszechnie w roślinach
wyższych , w paprociach , mchach, glonach ,grzybach , bakteriach. Każda
roślina wyższa zawiera zwykle kilka giberelin , które różnią się struktura i
aktywnością fizjologiczna. Nie ma tu zatem analogii z auksyna , która
występuje w roślinach najczęściej w postaci tylko jednego związku –kw.
indolilo- 3- octowego i jego pochodnych .Najwyższe stężenie giberelin
wykazują szybko rosnące i rozwijające się organy a wiec kiełkujące
nasiona , młode liście, wierzchołki łodyg i korzenia, natomiast wyrośnięte w
pełni liście oraz łodygi i korzenie zawierające bardzo niewielki ilości
giberelin.
Gibereliny nie sa transportowane polarnie tak jak auksyny , ich transport
zachodzi przez system prowadzący rośliny , tzn. w naczyniach i sitach
wraz z innymi przewodzącymi substancjami.
Gibereliny podobnie jak auksyny sa związkami wielofunkcyjnymi:
-
wpływ na kwitnienie i pośpiechowatosc :giberelina zwiększa aktywność
merosystemu subapikalnego, od którego zależy wydłużanie
miedzywiązki. Przy malej zawartości giberelin n roślina pozostaje wq
stadium rozety , natomiast przy wyższym poziomie giberelin- strzela w
łodygę i zakwita
-
wpływ na karłowate mutanty giberelin niejako leczy karłowate formy
-
-podziały komórek : gibereliny wyraźnie stymulują podziały komórek
zwłaszcza w merystemach subapikalnych.
-
-gibereliny przyśpieszają kiełkowanie nasion wielu roślin (głownie
przez zwiekszanie hydrolizy związków zapasowych nasienia)
przerywają również stan spoczynku pąków np. oczek w bulwach
ziemniaka.
-
-partenokarpia
-
*ponadto gibereliny mogą podwyższać poziom auksyn dwoma drogami
:
1) przez zmniejszenie rozkładu auksyn
2)przez zwiększenie produkcji auksyn
Cytokininy
W przeciwieństwie do auksyn i giberelin, których najbardziej
charakterystyczna działaniem jest wydłużanie komórek, cytokininuy
przyśpieszają ich podziały. Cytokininy sa to związki org., które
przyśpieszają cytokinezę komórek roślinnych w sposób podobny do
kinetyny , a niezależnie od innej aktywności fizjologicznej. Większość
znanych dzis cytokinin to pochodne 6-aminopiryny. Cząsteczka typowej
cytokininy składa się z poryny , która na węglu 6 posiada grupę aminowa z
dołączonym bocznym łańcuchem lub pierścieniem cytokininy. W
przeciwieństwie do auksyn i giberelin , nie maja charakteru kwasów. Do
najlepiej zbadanych cytokinin zaliczamy syntetyczna kinetaze ( 6-
furfuryloaminopuryne) .
Cytokininy występują w glonach ,mchach paprociach ,a także w roślinach
wyższych, zwłaszcza w tych Czesiach , w kotrych zachodza intensywna
podziały kom ( w kiełkujących nasionach, w mlodych liściach i owocach, w
wierzchołkach pędów i korzeni ) . Cytokininy występują również w
patogenach roślinnych ( np. u owadów minujących, wywołujących
tworzenie się galasow ).
Cytokininy podobnie jak auksyny i gibereliny sa związkami
wielofunkcyjnymi :
-
- stymulacja podziałów kom. I wydłużanie kom.
-
- pobudzanie tkanek hodowanych in vitro do wywarzania rożnych
organów.
Strona 7

-
- cytokininy przyśpieszają kiełkowanie nasion niektórych roślin,
chociaż nie tak wyraźnie jak gibereliny , pobudzają rozwój pąków
bocznych , znoszą zatem hamujący wpływ auksyn w paki, czyli
zmieniają dominacje wierzchołkowa.
-
- cytokininy powstrzymują starzenie się organów i tkanek roślinnych ,
mogą również odmładzać liście, które się już zestarzały i pożółkły,
pobudzając w nich wytwarzanie chlorofili , białek i kw. Nukleinowych
(inhibitory starzenia).
Etylen- jest wysoce aktywnym gazem, wpływającym na procesy
fizjologiczne jako stadnik skomplikowanego systemu endogennych
regulatorów wzrostu. Tworzy się w tkankach roślinnych z rożnych
związków (metioniny, octanu)
-
istnieje wyraźna zależność pomiędzy etylenem a auksynami
(auksyny zwiększają produkcje i działanie etylenu, a etylen hamuje
produkcje
i działanie auksyn, powoduje zaburzenia w ich polarnym
transporcie).
-
etylen w niezwykle niskich stężeniach przyspiesza zrzucanie liści i
owoców., zwiększając w ogonkach liściowych hydrolizie pektyn,
stanowiących lepiszcze łączące komórki
-
etylen zwiększa oddychanie i przyspiesza przez to dojrzewanie
owoców.
Endogenne inhibitory wzrostu - naturalne, wytwarzane przez rośliny
związki organiczne,które w stężeniach fizjologicznych hamują takie
procesy jak wydłużanie łodygi oraz jej wycinków, wzrost korzeni,
kiełkowanie nasion, otwieranie pąków o kwitnienie . Hamowanie tych
procesów na charakter odwracalny, a wiec obnizenie poziomu inhibitora w
roślinie wznawia zahamowany wcześniej proces. Endogenne inhibitory
wzrostu nie stanowią jednorodnej grupy pod względem chemicznym ani
fizjologicznym .
Najlepiej zbadano dwie grupy endogennych inhibitorów wzrostu:
-
-inhibitory fenolowe: wywodzą się z feoli np. kw. Salicylowy, kw.
galusowy, kw. cynamonowy, kw. fenolowy, kumaryna.
-
-kw. absycysynowy (ABA) jest terpenoidem , powstaje z ksantofilu.
Inhibitory wzrostu występują w pakach, liściach , bulwach ,
nasionach i owocach. ABA tworzy się prawdopodobnie w liściach,
stad jest odprowadzany przez wiązki przewodzące.
Inhibitory wzrostu są związkami wielofunkcyjnymi, biorącymi udział w
rożnych procach fizjologicznych:
-
wykazują hamujący wpływ na kiełkowanie ( kumaryna)
-
hamują wzrost elongacyjny indukowany auksyna np. wydłużanie
koleoptyli
-
odpowiadają na stan spoczynku pąków jesienią i zima
ABA jest o wiele bardziej aktywny niż inhibitory fenolowe, dlatego działa w
stężeniach 100-1000 *mniejszych .ABA powstaje głownie w liściach i
owocach zwłaszcza wtedy , kiedy dizen staje się krótszy. Transportowany
jest przez ksylem, floem oraz tkanki parenchymatyczne. Hamuje
wydłużanie i podziały komórki, przyspiesza opadanie liści i owoców
(antagonizm do auksyn) , indukuje stan spoczynku pąków wielu drzew
(odwrotnie niż gibereliny ) oraz przyspiesza starzenie się organów
roślinnych)( antagonistycznie w stosunku do cytokinin).
Strona 8

ROLA AUKSYN W FOTOTROPIZMIE I
GRAWITOTROPIZMIE
FOTOTROPIZM -mechanizm zjawiska fototropizmu tłumaczy się
nierównomiernym rozmieszczeniem auksyn w strefie wzrostu koleoptyla.
Na stronie zaciemnionej występuje większe nagromadzenie tych
fitohormonów. Powodem tego może być poprzeczny transport auksyny na
stronę zacienioną. Wskutek jednostronnego oświetlenia pojawia się
potencjał bioelektryczny między stroną oświetloną i zacienioną koleoptyla,
przy czym strona naświetlona staje się elektroujemna, a więc przypuszcza
się, że poprzecznu transport auksyny zachodzi na skutek
elektroforetycznego przemieszczania się ujemnie naładowanych anionów
IAA- do dodatnio naładowanej strony zacienionej. Pojawienie się może być
jednak tylko skutkiem, a nie przyczyną nierównomiernej dystrybucji IAA.
Powodem większego stężenia auksyny po zacienionej stronie rośliny może
być też hamujący wpływ światła na system enzymatyczny zaangażowany
w syntezie IAA, przez co na stronie zacienionej liścia syntetyzowanej
auksymy jest większa.
Światło może również wpływać na przechodzenie aktywnej formy IAA w
nieaktywne koniugaty (z glukozą, inozytolem, amidami) po oświetlonej
stronie rośliny. Wolny IAA po stronie zacienionej powoduje wtedy
wystąpienie reakcji tropicznej. Istnieją również poglądy, iż przyczyną
wygięcia fototropicznego jest wpływ światła zmniejszający wrażliwość
tkanek na działanie auksyny po stronie oświetlonej. Po stronie zacienionej
więc nawet małe stężenia auksyny mogą być dużo bardziej efektywne
wzrostowo.
GRAWITOTROPIZM (geotropizm) - zjawisko zróżnicowanej szybkości
wzrostu związane jest z nierównomiernym rozmieszczeniem auksyny w
strefie reagującej na bodziec. Auksyna przemieszcza się w roślinie w
kierunku pola przyciągania ziemskiego (ku dołowi), a więc w roślinie
umieszczonej w pozycji poziomej auksyna gromadzi się wzdłuż dolnej
strony łodygi i korzenia. Pomiędzy górną, a dolną stroną organów
powstaje wtedy pewien potencjał geoelektryczny. Różnica potencjałów
między bardziej ujemną stroną górną a bardziej dodatnią stroną dolną
wynosi 5-20 mV. Koleoptyle i pędy ułożone w pozycji poziomej zawierają
więc więcej auksyn po stronie dolnej. Przyczyną tego jest jest poprzeczny
transport auksyny oraz intensywniejsza synteza IAA i większa wrażliwość
na auksynę po stronie dolnej.
Czynniki warunkujące kwitnienie roślin.
Proces ten nie następuje w dowolnej porze roku, lecz jedynie w
określonych warunkach, wymaga mianowicie okresu obniżonej
temperatury oraz odpowiedniej długości dnia. Dopiero gdy te warunki
zostaną spełnione roślina może zakwitnąć.
Rośliny różnią się w reagowaniu na czas trwania światła i ciemności . Ze
względu na tę reakcję rośliny możemy podzielić na grupy:
-
Rośliny krótkiego dnia (RKD) - kwitną wtedy jeżeli dzienny okres
oświetlania (fotoperiod) jest krótszy od pewnej krytycznej długości .
Jeżeli okres oświetlenia jest dłuższy rośliny nie kwitną , lecz
pozostają w stadium wegetatywnym. Krytyczna długość nie jest
jednakowa dla wszystkich RDK , lecz zależy od gatunku rośliny i
może się wahać od 11 do 15 godzin .
-
Rośliny długiego dnia(RDD) - kwitną wtedy, kiedy dzienny okres
oświetlania jest dłuższy od krytycznego , jeżeli jest krótszy – rośliny
pozostają w stadium wegetatywnym . Długość okresu krytycznego
nie jest stała , lecz podobnie jak RDK zależy od gatunku rośliny i
waha się od 8 do 15 godzin.
-
Rośliny neutralne (czyli niewrażliwe na długość dnia) , rośliny te
zakwitają po osiągnięciu stanu gotowości do kwitnienia niezależnie
od długości dnia.
Substancje wpływające na kwitnienie:
-
giberelina pobudza ona wytwarzanie pędów kwiatowych , może
zastąpić długi dzień u niektórych roślin. Jednak żadna z giberelin
nie wywołuje zakwiatania roślin dnia krótkiego
-
drugą substancją, której dotychczas nie udało się wyodrębnić i
zbadać jest tzw. Antezyna , ma pobudzać wytwarzanie kwiatów.
Zakwitnięcie rośliny wymaga wytworzenia zarówno łodygi jak i kwiatu
zatem hipotetyczny regulator kwitnienia zwany florigenem powinien
składać się z obu wymienionych substancji czyli : Florigen = giberelina +
antezyna
Strona 9

Budowa i rola tkanek przewodzących u roślin
wyższych
U roślin wyróżnia się dwie tkanki przewodzące: łyko (floem) i
drewno (ksylem).
W skład łyka wchodzi kilka typów komórek: sitowe, towarzyszące,
miękiszowe i wzmacniające. Komórki sitowe po raz pierwszy opisał Hartig
1838. Są to żywe wydłużone komórki o perforowanych (dziurkowanych)
ścianach poprzecznych. Charakteryzują się brakiem jąder, chloroplastów i
innych struktur występujących w komórkach towarzyszących. Komórki
ułożone są w ciągi i kontaktują się ze sobą przez połączenia plazmatyczne,
o umożliwia swobodny przepływ soku. W komórkach występuje wysokie
ciśnienie turgorowi i wysokie stężenie soku. Sita w komórkach stresowych
zamykają się – kumuluje się ksyloz.
Łyko odgrywa najważniejszą rolę w długodystansowym transporcie
asymilatów od miejsca ich produkcji – liści do miejsca zużycia – korzeń,
tkanek merystematycznych i owoców. Przewodzi sacharozę i aminokwasy.
Ksylem (drewno) zbudowany jest z naczyń i cewek oraz komórek
wzmacniających. Naczynia to martwe, zdrewniałe, pozbawione ścian
poprzecznych. Komórki ustawione w pionowe szeregi, tworzą rury. Tworzą
mikrokapilarne kanały, mają zgrubienia na ścianach oraz liczne jamki.
Cewki przylegają do naczyń, są żywe, znacznie węższe i mają wiele jąder.
Dzięki jamkom w ścianach pobierają wodę i przekazują ją do komórek
miękiszowych na drodze osmotycznej. Naczynia służą do dalekiego
transportu wody i soli mineralnych,
a cewki do krótkiego. Rośliny starsze filogenetycznie (nagozalążkowe)
mają tylko cewki.
Floem i ksylem współpracują w transporcie soli mineralnych,
regulatorów wzrostu i innych substancji.
Fotoperiodyzm – definicja, znaczenie w życiu
roślin,
mechanizm molekularny
Fotoperiodyzm – jest wpływ długości dnia i nocy na zakwitanie
1. RKD – rośliny krótkiego dnia = SDP
Kwitną, gdy fotoperiod (= dzienny okres oświetlenia) jest krótszy od
pewnej krytycznej długości, gdy ten fotoperiod jest dłuższy rośliny
nie kwitną i pozostają w stadium wegetatywnym.
Krytyczna długość dnia: 11-15 godzin
Są to głównie jednoroczne rośliny kwitnące jesienią, tytoń, rzepak,
złocień ogrodowy (=chryzantema), wilczomlecz, soja.
Najważniejszym czynnikiem regulującym zakwitanie tych roślin jest
okres nieprzerwanej ciemności gdyż w ciemności zachodzą w tych
roślinach reakcje chemiczne (wrażliwe na światło) które powoduje
kwitnienie.
Rośliny te mogą zakwitać podczas nieprzerwanej ciemności pod
warunkiem dostarczenia im związków organicznych np. sacharozy
2. RDD – Rośliny długiego dnia = LDP
Kwitną, gdy fotoperiod jest dłuższy od krytycznego (ok. 8 – 15
godzin)
Rośliny roczne, kwitnące w lecie oraz rośliny dwuletnie np. szpinak,
owies, burak pastewny i cukrowy, marchewka.
Najważniejsza różnica między RKD a RDD polega na różnej
wrażliwości na długość okresu kwitnienia!!!
3.ROŚLINY NEUTRALNE – tj. niewrażliwe na d³ugość dnia i nocy
Zakwitają po osiągnięciu stanu gotowości do kwitnienia niezależnie
od długości dnia
Pomidor, ogórek, groch, bób, ryż (odmiany jare)
4. RDKD – rośliny długiego – krótkiego dnia
Strona 10
Ich zakwitanie zależy od tego czy najpierw był dzień długi a potem
krótki
5. RKDD – krótkiego – długiego dnia
Ich zakwitanie zależy od tego czy najpierw był dzień krótki a potem
długi
Miejscem percepcji bodźca fotoperiodycznego są liście zwłaszcza
młode i rozwijające się. Prawdopodobniej powstają w liściu regulatory (lub
hormony) kwitnienia, które przemieszczają się do merystemu
wierzchołkowego, gdzie wywołują wytworzenie zawiązków kwiatowych.
Hipotetyczny regulator kwitnienia to Florigen.
Giberelina – pobudza wytwarzanie pędów kwiatowych (nie kwiatów);
Antezyna - pobudza wytwarzanie kwiatów (nie łodyg).
RKD zawsze wytwarzają giberelinę (normalne łodygi przy
nieodpowiednim fotoperiodzie nie wytwarzają gibereliny (forma rozetowa).
Syntezę regulatorów kwitnienia reguluje system barwników fitochrom.
WYKORZYSTANIE ZJAWISK FOTOPERIODYZMU
1. Zwiększenie produkcji roślinnej
RKD – chryzantemy (skrócenie dnia latem lub przedłużenie zimą);
trzcina cukrowa (przerwanie ciemności krótkim błyskiem światła)
RDD – sałata, szpinak, rzodkiewka
2. Regulacja fotoperiodów w hodowli roślin
Modyfikując odpowiednio długość dnia można zsynchronizować
kwitnienie roślin krzyżowych.
3. Wpływ fotoperiodu na wykształcenie się organów wegetatywnych
(ziemniak, cebula)
GIBERELINY – BUDOWA CHEMICZNA, ZNACZENIE
DLA PROCESÓW FIZJOLOGICZNYCH I
METABOLIZMU
GIBERELINY – związki organiczne które mają taki sam szkielet gibanu jak
kwas giberelinowy i wykazuje aktywność w testach karłowatych mutantów i
indukcji .-amylazy w kiełkujących ziarnach jęczmienia. Odkrycie: na
plantacjach ryżu w Japonii „szalone siewki”
.
zostały zakażone patogennym
grzybem produkującym gibereliny.
BUDOWA CHEMICZNA
Należą do terpenoidów – tj. związków, których jednostką budowy jest
izopren.
Wszystkie są kwasami i mają identyczną konfigurację opartą na
czteropierścieniowym rdzeniu gibanowym
Gibereliny różnią się między sobą strukturą i aktywnością fizjologiczną.
Jedna roślina zawiera zazwyczaj kilka rodzajów giberelin oznaczanych
jako GA1, GA2, GA3 (tj. kwas giberelowy – najlepiej poznana
giberelina), GA4 itd.
WYSTĘPOWANIE
Rośliny wyższe
Paprocie
Mchy
NAJWIĘKSZE STĘŻENIE
Organy szybko rosnące i rozwijające
się
Kiełkujące nasiona
Strona 11

Glony
Grzyby
Bakterie
Młode liście
Wierzchołki łodyg i korzenie
BIOSYNTEZA
Polega na przekształceniu acetylo-CoA w kwas mewalonowy a z kolei jego
przemiany prowadzą do pierścieniowych struktur gibanowych.
Gibereliny w wielu procesach działają pośrednio, poprzez zmianę
stężenia auksyn w tkance roślinnej, zmniejszenie stężenia auksyn,
zwiększenie produkcji auksyn np. tworzenie pośpiechów i roślin
rozetowych (wzrost stężenia giberelin _ 40 krotny wzrost stężenia auksyn _
powstawanie pośpiechów).
Transport ich zachodzi przez system przewodzący rośliny tzn. w
naczyniach i sitach wraz z innymi przewodzonymi substancjami.
FUNKCJE GIBERELIN
Niektóre rośliny np. fasola, groch, kukurydza występują w dwóch
odmianach:
Normalnej (wysokopiennej) *
Karłowatej **
Jeżeli na wierzchołek wzrostu odmiany karłowatej wprowadzić
kroplę gibereliny to wydłuży się do rozmiarów rośliny wysokopiennej
* i ** Różnią się one długością międzywęźli (ich liczna jest taka
sama u obu odmian – różnica tylko w ich długości).
Rośliny rozetowe (krótkopędowe) – np. buraki, sałata mają liście
skupione w rozetę wierzchołkową, ich zakwitanie poprzedza tzw.
szczelanie w źdźbło („pośpiechy”), które polega na 5 – 6 krotnym
wydłużaniu międzywęźli, proces ten wymaga odpowiedniej
temperatury oraz odpowiedniej długości dnia. Gibereliny
przyśpieszają wytwarzanie pośpiechów i zakwitanie, bo zwiększają
aktywność systemu subapikalnego, od którego zależy wydłużanie
międzywęźli.
Stymulują podział komórek
Przyśpieszają kiełkowanie nasion poprzez zwiększenie hydrolizy
związków zapasowych nasienia
Przerywają stan spoczynku pąków np. oczka w bulwach
ziemniaków
Partenokarpia – owoc bez nasiona. Winogron, grusza, wiśnia.
Wspólne działanie auksyn i giberelin – wydłużanie łodyg i wzrost
owoców
INDUKCJA FOTOPERIODYCZNA – MECHANIZM
MOLEKULARNY, ZNACZENIE W ONTOGENEZIE
ROŚLIN
Indukcja fotoperiodyczna – następcze działanie fotoperiodu1. Fotoperiod
wywołuje w roślinie pewne zmiany, które początkowo są niewidoczne, ale
prowadzą do wytworzenia zawiązków kwiatkowych.
Skutki cyklu fotoperiodycznego są trwałe. Rośliny, które zostały
poddane
odpowiedniemu fotoperiodowi i wskutek tego zakwitną po pewnym czasie –
mówimy, że są zaindukowane np. do zaindukowania może wystarczyć
nawet 1 długa noc . (po 2 tygodniach wytwarzają zawiązki kwiatowe).
SCHEMAT PRZEBIEGU FOTOPERIODYCZNEJ INDUKCJI
KWITNIENIA
Strona 12
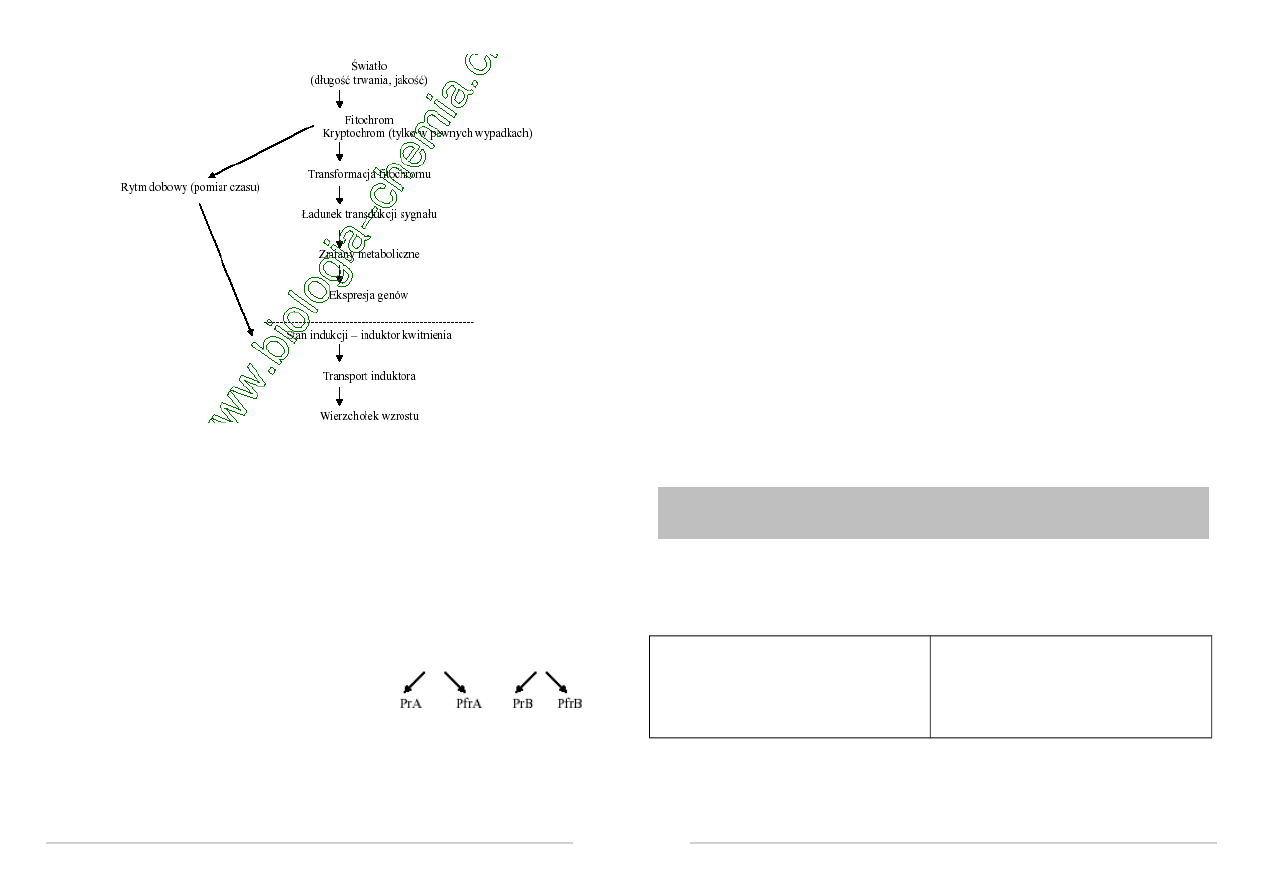
Najefektywniejszym miejscem percepcji bodźca fotoperiodycznego
są młode liście bądź liścienie.
W wyniku indukcji fotoperiodycznej powstaje w liściach induktor
kwitnienia, który jest następnie transportowany do wierzchołków wzrostu
pędu, gdzie zapoczątkowuje przemiany biochemiczne, anatomiczne,
morfologiczne, zakończone wytworzeniem kwiatu.
Główną rolę w indukcji fotoperiodycznej odgrywa okres ciemny,
noc. To jej długość determinuje zakwitanie
MECHANIZM MOLEKULARNY FOTOPERIODYCZNIE
W regulacji tego procesu biorą udział 2 fitochromy: labilny (Phy A) i stabilny (Phy
B)
W liściach roślin dnia krótkiego (SDP):
W ciemności poprzedzającą fazę jasną fotoperiodu zachodzi
synteza fazy PrA
W fazie jasnej zachodzą:
I. Fotokonwersja fazy PrA do PfrA
II. Szybki rozkład czy transformacja PfrA i akumulacja produktu
transformacji, zwanego fitochromem nieodwracalnym zbyt duże
stężenie hamuje indukcję kwitnienia.
III. Synteza formy PrB
IV. Przekształcenie fazy PrB do PfrB
W fazie ciemnej stopniowo zanika Fitochrom nieodwracalny i
pojawia się induktor kwitnienia.
LPD – rośliny dnia długiego - indukcja fotoperiodyczna związana jest z
neutralnym działaniem fitochromu stabilnego (Chyb) a u roślin CPD
fitochromu labilnego (PhyA).
W indukcji fotoperiodycznej oprócz układów fitochromowego
uczestniczą także kryptochromy i światło o długości fali 400 – 500 nm.
stymuluje kwitnienie. Oba układy mogą działać niezależnie lub
synergistycznie lub antagonistycznie
INDUKTOY KWITNIENIA: Floringien – giberelina + antezyna powstaje
w liściach transportowany do wierzchołka wzrostu.
KIEŁKOWANIE NASION – TYPY, PRZEMIANY
METABOLICZNE
Podczas kiełkowania następuje aktywacja układów
enzymatycznych zwykle przy czynnym udziale regulatorów wzrostu, czego
wynikiem jest intensywna przemiana energii.
CZYNNIKI REGULUJĄCE KIEŁKOWANIE
ZEWNĘTRZNE
_ Temperatura
_ Wilgotność
_ Światło
_ Tlen
WEWNĘTRZNE
_ Budowa łupiny
_ Inhibitory
_ Stan zarodka
FIZJOLOGIA KIEŁKOWANIA (na przykładzie ziarniaków
zbóż)
Strona 13

Wnikanie wody do nasion pęcznienie
Cytokininy przełamują działanie inhibitorów wzrostu
Gibereliny indukują wytwarzanie hydrolaz, które uruchamiają
materiały zapasowe białka, produkty hydrolizy dostają się do
zarodka
Cytokininy i auksyny bielma działają na zarodek
Zarodek zaczyna rosnąć przy dostępie wody i produktów hydrolizy
MORFOLOGIA KIEŁKOWANIA
Najpierw pojawia się korzeń zarodkowy a później łodyga zarodkowa
Typy kiełkowania:
1. Kiełkowanie nadziemne (epigeiczne)
Dynia, cebula, fasola, rośliny szpilkowe
Wydłuża się hipokotyl (część podliścieniowa zarodka) który
wynosi liścienie nad powierzchnię gleby
Liścienie są mięsiste, gromadzą materiały zapasowe i po
wydostaniu się na powierzchnię kiełkują i początkowo pełnią
funkcję organu asymilacyjnego.
Następnie z pączka zarodkowego pomiędzy liścieniami rozwija
się łodyga a następnie liście.
2. Kiełkowanie podziemne (hipogeiczne)
Wydłuża się epikotyl (część nadliścieniowa), czerpiący
początkowo materiał zapasowy z liścieni, które pozostają w
łupinach nasiennych.
Rośliny wykazujące ten typ kiełkowania to np. groch, dąb
PRZEMIANY METABOLICZNE
Imbibicja – gwałtowny wzrost oddychania i pobieranie wody, najpierw tlenowe
później beztlenowe. Substancjami oddychania w kiełkujących nasionach są
nagromadzone w nich substancje zapasowe (glukoza, fruktoza).
Faza kataboliczna – mobilizacja rezerwy, hydroliza cukrów, białek
Faza anaboliczna – synteza nowych białek
Spoczynek nasion
Wyróżniamy dwa typy stanu spoczynku
1.
Spoczynek względny- wywołany jedynie brakiem odpowiednich
warunków zew, a więc niedostatkiem wody, tlenu lub nieodpowiednia
temperaturą. Ten typ spoczynku wykazuja nasiona większości roślin
uprawnych. Aby pobudzic je do kiełkowania wystarczy umieścic je w
warunkach odpowiedniej wilgotności i temperatury
2.
Spoczynek bezwzględny- (głęboki), który jest wywołany wewnętrznymi
właściwościami samego nasienia. Nasionom w stanie spoczynku bezwzg
brak jest wewnętrznej gotowości do kiełkowania i normalne czynniki
zewnętrzne nie mogą wywołać kiełkowania.
Regulacja procesu:
Warunki kiełkowania nasion (przerwanie spoczynku względnego) -
podstawowymi czynnikami warunkującymi rozpoczęcie procesu kiełkowania są:
woda, tlen, temperatura, światło.
1)
Woda- rozpoczyna proces kiełkowania nasion. Substancje z których
składa się nasienie, np. białko, celuloza, skrobia itp. maja właściwości
koloidalne (wykazuja zdolności do pęcznienie- imbibicji; nastepuje wtedy
przyciąganie i adsorbowanie wody przez micele koloidów, co powoduje ich
rozsuwanie i zwiekszanie objętości.) Uwodnienie łupiny nasiennej
zwiększa jej zdolność przepuszczania tlenu niezbędnego do oddychania
zarodka, a uwolnienie protoplastów komórek nasienia powoduje aktywacje
układów enzymatycznych, która umożliwia energiczną przemianę materii.
2) Tlen- podczas oddychania zarodek wytwarza niezbędną enerie.
Niedostatek tlenu, wywołany np. całkowitym zalaniem nasion wodą lub
zbyt głębokim siewem zmniejsza natężenie oddychania i może wstrzymać
kiełkowanie. Niektóre nasiona np. ryżu wykorzystuja reakcje biochemiczne
beztlenowe, dzięki czemu nasiona mogą kiełkować w warunkach niemal
beztlenowych.
3) Temperatura- umozliwia ona właściwy przebieg biochemicznych reakcji
metabolizmu. Dla wielu nasion wystarczająca jest dość niska tem, niewiele
wyższa od punktu zamarzania wody. Na ogół optymalna temp dla procesu
kiełkowania jest niższa niż optymalna temp póżniejszego wzrostu.
Poszczególne procesy fizyczne, biochemiczne, fizjologiczne, składające
się na całość procesu kiełkowania, róznia się wymaganiami w stosunku do
temp. Jest to jeden z powodów dla którego w czasie kiełkowania zmiany
temp są korzystniejsze niż stała temp. Kiełkowanie wielu nasion pobudza
zwłaszcza okres obniżonej temp.
4)
Światło- odp w pkt 58
Stan spoczynku bezwzględnego
Uwarunkowany anatomiczną budową nasienia lub też mniej uchwytnymi
przyczynami, np. stanem fizjologicznym zarodka. Nasiona znajdujące się w stanie
spoczynku bezwzgl nie kiełkują, pomimo optymalnych warunków wilgotności, temp
i natlenienia. Może być wiele przyczyn tego stanu:
a) Spoczynek uwarunkowany budową i właściwościami łupiny nasiennej-
łupiny nieprzepuszczalne dla wody, które po długich okresach zanurzenia
wodzie pozostają bez zmiany. Łupina może tez być nieprzepuszczalna
dla gazów przez co powstrzymuje oddychanie rozwijającego się zarodka.
Strona 14

Zbyt twarde łupiny nasienne mogą również hamować kiełkowanie w
sposób czysto mechaniczny, tzn. nie pozwalając a przebicie się kiełka.
Ten typ spoczynku ustepuje po uszkodzeniu łupiny nasiennej.
b) Spoczynek wywołany niewykształceniem się zarodka- w niektórych
roślinach rozwój zarodka jest opóźniony w stosunku do pozostałych
tkanek nasienia. I dopiero po całkowitym dojrzeniu zarodka nasiona takie
mogą kiełkować. (storczyk, kaczeniec, jesion)
c) Spoczynek zarodka- nasiona niektórych roślin nie kiełkuja natychmiast po
zbiorze, pomimo że są w pełni wykształcone- dojrzałe morfologicznie lecz
fizjologicznie nie są gotowe do kiełkowania. Po pewnym czasie
przechowywania takich nasion w normalnej temp i w stanie
powietrznosuchym spoczynek stopniowo ustaje (żyta). Natomiast
Natomiast Natomiast innych nasion spoczynek ustępuje dopiero po
spęcznieniu nasion w wodzie i poddaniu ich działaniu niskiej temp przez
dłuższy czas (stratyfikacja)
d) Spoczynek wywołany inhibitorami chemicznymi- kiełkowanie wielu nasion
hamują zawarte w nich inhibitory. Związki te występują także w owocach i
innych częściach rośliny, powstrzymując kiełkowanie roślin.
e) Nasiona wrażliwe na światło- wywiera wpływ przyśpieszający bądź
opóżniający. Światło lub jego brak może powodować stan spoczynku u
danych nasion.
f)
Nasiona o podwójnym spoczynku (nasiona dwuletnie) – (u drzew,
krzewów, bylin) stan spoczynku wywołany jest równoczesnym działaniem
dwóch przyczyn: „twardością” łupiny oraz spoczynkiem zarodka. Nasiona
takie kiełkuja zazwyczaj na drugą wiosne od czasu ich dojrzewania.
Przerywanie i skracanie stanu spoczynku nasion- znając przyczynę stanu
spoczynku nasion można zastosować określone zabiegi dla jego skrócenia
lub przerwania.
Stratyfikacja i skaryfikacja
– znaczenie dla kiełkowania nasion.
Stratyfikacja – przyczyną spoczynku bezwzględnego nasion jest zbyt twarda
łupina nasienna, która jest nieprzepuszczalna dla wody. Taka łupina nie
dopuszcza do wymiany gazowej i w ten sposób powstrzymuje oddychanie
rozwijającego się zarodka. Zbyt twarde łupiny mogą hamować kiełkowanie w
sposób często mechaniczny – nie pozwalając na przebicie się kiełka. Ten typ
spoczynku ustępuje po mechanicznym uszkodzeniu łupiny nasiennej w procesie
skaryfikacji. Polega on na porysowaniu lub innym mechanicznym uszkodzeniu
łupiny nasiennej , co umożliwia wnikanie wody do wnętrza nasion i w następstwie
pęcznienia oraz wymianę gazową pomiędzy zarodkiem a otoczeniem. W pewnych
przypadkach (np. nasion koniczyny, drzew) stosuje się specjalne maszyny zwany
skaryfikatorami, w których nasiona „twarde” przechodzą pomiędzy wirującymi
tarczami, co powoduje porysowanie skórki , w wyniku czego stają się one zdolne
do kiełkowania. Twardą łupine można uszkodzić traktując nasiona stężonym
kwasem siarkowym. W warunkach naturalnych tę przeszkodę kiełkowania
pokonują bakterie i grzyby glebowe, które rozkładają celulozę, pektyny oraz inne
substancje wchodzące w skład łupiny nasiennej.
Skaryfikacja - jeśli stan spoczynku nasion wywołany jest obecnością inhibitorów
lub spoczynkiem zarodka, podczas którego zarodek, pomimo ze w pełni dojrzały
morfologicznie , fizjologicznie nie jest zdolny do kiełkowania. Stosując skaryfikację
można wywołac kiełkowanie tych nasion . zabieg ten polega na przetrzymaniu
nasion w wilgotnym i przewiewnym środowisku przy stosunkowo niskiej
temperaturze, wynoszącej 1-10℅. Najczęściej warstwy nasion układa się poziomo
na przemian z warstwami wilgotnego piasku, torfu lub mchu. W ten sposób
stwarza się sztucznie warunki istniejące rzeczywiście w przyrodzie, kiedy to
nasiona jesienią padają na glebę i zimują w stanie napęczniałym, przykryte
warstwą liści lub śniegu. Niska temperatura przy jednoczesnym nawilgoceniu oraz
dostępie tlenu wywołuje w nasieniu głębokie zmiany fizjologiczne, w następstwie
których ustępuje stan spoczynku. U wielu gatunków nasion pod wpływem niskiej
temperatury następuje rozkład inhibitorów hamujących kiełkowanie np. podczas
stratyfikacji nasion jabłoni ulega rozkładowi kwas abscysynowy ( ABA) zawarty w
bielmie, które hamuje proces kiełkowania. Im dłużej trwa skaryfikacja , tym mniej
ABA zawierają nasiona i tym łatwiej mogą kiełkować.
FITOCHROM ROLA W REGULACJI PROCESÓW
FIZJOLOGICZNYCH
I METABOLICZNYCH U ROŚLIN WYŻSZYCH.
FITOCHROM - barwnik "dopasowujący" rym wzrostu i rozwoju roślin do
warunków świetlanych, panujących w danej porze roku. Odpowiada on za
wiele zjawisk sezonowych występujących w roślinach, np. zakwitanie w
odpowiednich porach roku, kiełkowanie niektórych nasion itp. Pełni on w
roślinach rolę wewnętrznego "zegara chemicznego", dzięki któremu rośliny
mogą rozpoznawać(niejako "widzieć") nadchodzącą porę roku.
Strona 15

Jest to barwnik błękitny występujący powszechnie w roślinach
wyższych, zwłaszcza w ich częściach merystematycznych. Występuje
także w roślinach niższych, np. glonach.
(cząsteczka) FITOCHROM = CZĘŚĆ BIAŁKOWA + CZĘŚĆ
DROBNOCZĄSTECZKOWA (CHROMOFOR) właściwy barwnik
Fitochrom
=>fitochrom 660 = P660 pochłania światło jasnoczerwone(maksimum
absorpcji 660nm) pod jego wpływem przekształca się w P730. W
ciemności jest trwały, NIEAKTYWNY fizjologicznie
=>fitochrom 730 = P730 pochłania światło ciemnoczerwone(daleka
czerwień), ulegając przekształceniu w P660.
Nietrwały w ciemności powoli wtedy przekształca sie w P660. AKTYWNY
fizjologicznie -zmienia aktywność genów kierujących takimi procesami jak
zakwitanie, kiełkowanie nasion wrażliwych na światło, wydłużenie łodygi,
rozwój chloroplastów, synteza niektórych barwników, np, antocyjanów,
Promienie czerwone i dalekiej czerwieni wchodzą razem w skład
światła słonecznego. W normalnych warunkach oświetlenie dziennego w
roślinach występują więc obie formy fitochromu, z przewagą P730. W
ciemności natomiast ilość P730 zmniejsza się- przekształca on się w P 660
•
rola fitochromu w zjawiskach fotoperiodycznych:
RDK i RDD posiadają taki sam mechanizm fotoperiodyczny, różnica jednak
pomiędzy nimi polega na tym, że reagują na nie odwrotnie:
-RKD- u nich P730 hamuje syntezę regulatorów kwitnienia dlatego
wymagają one zaciemnienia przez odpowiednio długi okres
-RDD- u nich P730 wywołuje kwitnienie-zbyt długa noc(okres ciemności)
wstrzymuje kwitnienie.
•
rola fitochromu w kiełkowaniu nasion:
Niektóre nasiona są wrażliwe na światło. Jest ono niezbędnym warunkiem
kiełkowania nasion wielu gatunków roślin, np. tytoniu, naparstnicy,
wierzbówki, krwawnicy, sałaty i wielu traw. Światło może tez hamować
kiełkowanie niektórych nasiaon(czarnuszki, facelii, szarłatu)-o wiele
rzadziej. Wrażliwość na światło wykazują jedynie nasiona napęczniałe.
Przemiany P660 w P730 zapoczątkowuje łańcuch procesów drogą
regulacji aktywności genów, które prowadzą do kiełkowania.
Zmiany okresów światła i ciemności również wpływają na kiełkowanie
niektórych nasion (nasion krótkiego i długiego dnia).
Wpływ fitochromu na morfogenezę- FOTOMORFOGENEZA
-wydłużanie się pędów jest symulowane przez ciemność i daleką
czerwień(P730), hamowanie natomiast przez światło czerwone-świadczy to
wyraźnie o udziale fitochromu w procesie wydłużania roślin
-rozwój liści i wzrost blaszki liściowej również odbywa sie we
współdzialaniu z fitochromem; różnicowanie i rozwój chloroplastów, nie
może odbywać sie w ciemności; pewne procesy biochemiczne także
zależą fitochromu(synteza protochlorofilidu, karotenoidow, synteza
antocyjanów-czerwonych barwnikow kwiatów itp.)
Światło wywołuje więc za pośrednictwem fitochromu wyraźne zmiany we
wzroście, rozwoju i różnicowaniu się roślin w sposób niezależny od
fotosyntezy.
Zjawisko to nazywa sie FOTOMORFOGENEZĄ, a efekty
wywoływane są przez światło .
Rola światła w kiełkowaniu nasion.
Jednym z czynników który jest istotny w kiełkowaniu nasion jest światło.
Nasiona, których kiełkowanie zależy od warunków świetlnych, nazywamy
fotoblastycznymi . Rozróżniamy 3 rodzaje reakcji nasion na światło:
1)
pozytywnie fotoblastyczne - światło stymuluje kiełkowanie . Występuję u
75% gatunków roślin
2) negatywnie fotoblastyczne – światło hamuje kiełkowanie
3) niefotoblastyczne – nasiona niewrażliwe na światło (światło nie ma wpływu
na kiełkowanie). Wytwarzają je ok.5% gatunków np. zboża, rośliny
motylkowate, len.
Wrażliwość kiełkowania nasion na światło na ogół nie jest cechą warunkującą ich
kiełkowanie. Większość nasion pozytywnie fotoblastycznych kiełkuje również w
ciemności, ale warunki świetlne zwiększają szybkość kiełkowania i liczbę
ostatecznie skiełkowanych nasion. U nasiona np. jemioły , które nie kiełkują w
ogóle w ciemności, naświetlanie jest koniecznym warunkiem ich kiełkowania.
Strona 16

Wymagania nasion w stosunku do warunków świetlnych regulujących kiełkowanie
mogą dotyczyć zarówno czasu ekspozycji i do składu spektralnego światła.
Kiełkowanie krańcowo wrażliwych nasion np. sałaty jest stymulowane w wyniku
kilkuminutowego naświetlania światłem księżyca lub 0,1-sekundowym błyskiem
światła słonecznego
Receptorem światła czynnego w regulacji kiełkowania nasion jest
fitochrom. W stymulacji kiełkowania większości nasion dodatnio fotoblastycznych
najbardziej efektywne jest światło czerwone ( R, max widma czynnościowego
λ=660 nm). Jego efekt jest odwracalny przez naświetlenie światłem dalekiej
czerwieni ( FR λ= 730). Naświetlanie światłem FR jest najbardziej skuteczne w
hamowaniu kiełkowania nasion ujemnie fotoblastycznych . zaobserwowano
również hamowanie kiełkowania przez światło niebieskie i czerwone.
Fitochrom bierze udział w regulacji kiełkowania nie tylko nasion wrażliwych na
światło (fotoblastycznych). Świadczy o tym obecność fitochromu we wszystkich
badanych nasionach oraz obserwacja, że kiełkowanie w ciemności wielu nasion
niefotoblastycznych można zahamować naświetlając je światłem FR oraz że u
nasion niefotoblastycznych poddanych kiełkowaniu w warunkach odbiegających
od optymalnych (zbyt wysoka lub zbyt niska temperatura, stres hydratacyjny )
pojawia się wrażliwość na światło.
Światło działa tylko na nasiona napeczniałe, na suche nie działa.
Strona 17

Wernalizacja - teorie, znaczenie dla rozwoju roślin.
Jarowizacja, jaryzacja, wernalizacja – procesy biochemiczne
zachodzące pod wpływem niskich temperatur u roślin ozimych i
wieloletnich, wpływające na ich zakwitanie lub jego przyspieszenie
( zjawisko indukcyjnego działania obniżonej temperatury na kwitnienie
roślin). Wernalizacji mogą ulegać różne organy roślin, efektywna indukcja
kwitnienia zachodzi w komórkach dzielących się lub zdolnych do podziału.
Miejscem percepcji bodźca termicznego jest merystem wierzchołkowy, w
nasionach części embrionalne (zarodek).Percepcja bodźca termicznego
odbywa się poprzez zmiany fizykochemicznego stanu błon komórkowych,
co pobudza znajdujące się w niej receptory do uruchomienia cyklu
przemian metabolicznych, których końcowym rezultatem jest ekspresja
genów kwiatowych w wierzchołkach wzrostu rośliny. Istnieje specyficzna
substancja- wernalina, tworząca się w roślinach podczas wernalizacji, która
wywołuje kwitnienie. Wernalizacje można zastąpić przedłużonym dniem lub
zwiększeniem intensywności światła. Rośliny rozetowe można pobudzić do
kwitnienia przez potraktowanie giberelina.
SEKWENCJA ZDARZEŃ W PRZEBIEGU WERNALIZACJI:
Wernalizacja
Zjawisko to ma praktyczne
zastosowanie w ogrodnictwie, gdzie
np. aby wytworzyły się pędy cebuli,
rośliny te muszą przejść przez okres
jarowizacji w temperaturze 5-10°C.
Dlatego też cebulę wysadkową
należy przetrzymywać w
temperaturach optymalnych dla
jarowizacji (5-8°C), natomiast
temperatur tych trzeba unikać
przechowując cebulę dymkę.
Jarowizację wykorzystuje się w
produkcji nasion niektórych
gatunków warzyw. Kraje, w których
temperatura zimy jest nieco wyższa
niż 0°C, przeszły na produkcję
nasion buraka cukrowego i
ćwikłowego, stosując tanią
↓ ↓ ↓
Wierzchołek wzrostu
↓
Zmiany stanu błon kom.
↓
przemiany metaboliczne i
hormonalne
↓
jednoroczną uprawę.
Zmiany wrażliwości wierzchołka
wzrostu
↓
Demetylacja genów
↓
Ekspresja genów kwiatowych
↓
Morfogeneza kwiatu
Wzrost elongacyjny komórek roślinnych,
czyli wydłużanie komórek
.
Następuje w strefie wzrostu. Strefa elongacji przesuwa się stale, w
miarę jak dany organ rośnie. Do strefy elongacji wchodzą małe
komórki embrionalne, które przechodzą okres wzrostu i opuszczają
strefę elongacji jako komórki całkowicie wyrośnięte.
Etapy wydłużania komórek:
1. Wzrost plastycznej rozciągliwości ściany wskutek rozluźniania
wiązań pomiędzy makrocząsteczkami materiałów budulcowych.
Dużą rolę pełnią regulatory wzrostu- auksyny, które zwiększają
rozciągliwość ściany komórkowej.
2. W fazie wzrostu do komórek wnika woda na zasadzie osmozy. W
cytoplazmie tworzą się wakuole. W miarę wnikania wody do komórki
wzrasta ciśnienie turgorowe, któro silnie przyciska cytoplazmę do
ściany komórkowej. Jeśli ściana komórkowa jest elastyczna, to
poddaje się ciśnieniu, wskutek czego następuje jej rozciąganie i
wzrost objętości komórki.
Strona 18

3. Rozciągana ściana komórkowa zostaje wzmacniana przez
odkładanie się warstw celulozy w postaci nowych sieci mikrofibryli.
Wzrost komórki jest wynikiem zwiększonego pobierania wody oraz
uelastyczniania ścian komórkowych. Elongacji towarzyszy
odkładanie nowych substancji budulcowych ścian- celulozy i pektyn.
W fazie elongacji ilość komórek pozostaje bez zmian, powiększa się
natomiast wielokrotnie długość i objętość komórek.
Strona 19
RUCHY ROŚLIN - PODZIAŁ, DEFINICJE,
PRZYKŁADY
TYPY RUCHÓW:
I
. ze względu na mechanizm ruchu
•
z udziałem protoplastu
- ruchy turgorowe
- ruchy wzrostowe
- ruchy wzrostowo-
turgorowe
•
bez udziłu protoplastu
- kserochazje
- higrochazje
- ruchy kohezyjne
II. ze względu na bodźce (przyczyne ruchu)
- taksje-bodźce działają kierunkowe
- nastie-bodźce nie działają
kierunkowo
- ruchy szparek opisane w w pkt 9
- tropizmy-wzrostowe, kierunkowe
- ruchy nutacyjne
- ruchy eksplozyjne
NASTIE - ruchy turgorowe wywołane przejściowymi zmianami w
wyspecjalizowanych kom. (poduszeczkach wspierających ogonki liściowe)
ruch niezależnie od kierunku dziłania bodźca, zaś od zmiany jego
natężenia. Impuls elektryczny docierający do kom. poduszeczki powoduje
przenikanie jonów potasowych poza obręb pewnych komórek ruchowych,
następstwem jest utrata wody i zamknięcie np.liścia. Ruchy wywołane
budową organów,a nie kierunkiem działania bodźca.
Fotonastie
- Zmiana natężenia światła. Przykłady: ruchy otwierania i
zamykania kwiatów, m.in. grzybienia białego, goryczek, lepnicy; ruchy
aparatów szparkowych.
Sejsmonastie
- bodźiec mechaniczny dotknięcie lub wstrząśnięcie.
Przykłady: ruchy liści i ogonków liściowych mimozy, ruchy pręcików
berberysu, ruchy liści roślin owadożernych.
Termonastie
- Temperatura, kwiaty otwieraja sie wraz ze wzrostem
temperatury. Przykłady: ruchy otwierania i zamykania kwiatów, m.in.
tulipana i krokusa.
Haptonastie
- Bodziec dotykowy. Przykład: ruchy włosków chwytnych
rosiczki
Hydronastie
- Zmiana wilgotności powietrza. Przykłady: otwieranie lub
zamykanie kwiatów przy zmianie wilgotności powietrza.
Chemonastie
- czynniki natury chemicznej. Przykłady: owadożerne
rosiczki
Występują dwa rodzaje reakcji nastycznych:
-RUCHY WZROSTOWE - wynikają z róźżnicy w szybkości wzrostu
wydłużąniowego przeciwnych stron organu, zachodza w organach młodych
i są bardzo trwałe
-RUCHY TURGOROWE - powodowane różnicami turgoru określonych
komórek, pojawiaja sie po ustaleniu wzrostu wydłuzeniowego i mogą byc
wielkorotnie powtarzane.
TAKSJE - motoryczne reakcje organizmu na bodźce kierunkowe. Polegają
na aktywnym przemieszczaniu się w kierunku bodźca (t. dodatnie) lub w
kierunku przeciwnym (t. ujemne).
W zależności od rodzaju bodźca wyróżnia się następujące rodzaje t.:
a) chemotaksje - występują głównie u heterotroficznych, (saprofity,
pasożyty) umożliwia znajdowanie pokarmu.
b) fonotaksje - występuje u organizmów fotosyntetyzujących, (pewne
bakterie, wiciowce) które dzieki tej właściwości mogą znależć dogodne
warunki świetlne.
RUCHY NUTACYJNE (nutacje autonomiczne, wzrostowe)- jest to zmiana
tempa wzrostu poszczególnych stron młodych pędów lub kwiatostanów.
Przykład mogą stanowić ruchy wahadłowe kwiatostanu cebuli najczęściej
wykonywane przez pędy i liście -ruchy szukające umożliwiają zetknięcie
sie z roślina- żywicielem. Ruch węsów czepnych gwarantuje znalezienie
podpory, owijanie sie
RUCHY EKSPLOZYJNE - występuja w wyniku określonych napięć
tkankowych, zachodzą gdy organ charakteryzuje się dużym turgotm,
natomiast zawierasta stabilną tkankę mechaniczną, która uniemożliwia
dalsze pobieranie wody i wydłużanie się, powstałe napięcie prowadzi do
rozerwania organu np owocników, w odpowiednim do tego miejscu z
równoczesnym wyrzuceniem zawartości.
Strona 20
KSEROCHAZJA - rodzaj ruchów roślin zaliczany do ruchów
higroskopowych. Mechanizm kserochazji polega na nierównomiernym
kurczeniu się i wysychających błon i ścian komórkowych martwych
komórek. Zwilżenie powoduje ruch przeciwny. Wykorzystywany jest przy
otwieraniu się owoców w celu wyrzucenia nasion.
HIGROCHAZJA - wywołany przez pobieranie wody przez komórki, co
powoduje ich odkształcenia. Wykorzystywany przy otwieraniu się owoców
w celu wyrzucenia nasion. W przypadku tzw. róż jerychońskich higrochazji
podlegają większe części, a nawet całe rośliny. Mechanizm higrochazji
polega na nierównomiernym nasiąkaniu i pęcznieniu błon i ścian
komórkowych martwych komóek
RUCHY KOHEZYJNE - ruchy roślin wywoływane działaniem sił kohezji
wody; powstają w efekcie postępującego wysuszania komórek, np.
otwieranie puszek (zarodni) mchów, zarodni paprotników i worków
pyłkowych roślin nasiennych.
TROPIZMY – definicje, mechanizmy, przykłady.
O tropizmach mówimy gdy organ ustawia się w nowym ściśle określonym
położeniu w stosunku do kierunku działania bodźca. Organy roślin wykonują ruchy
wygięcia, skręcania, obrotu i inne.
Paraleotropizm – jeżeli organ reagujący tropicznie ustawia się swą dłuższą osią
równolegle do kierunku bodźca lub spadku jego natężenia, zaś w reakcji na
bodźce grawitacyjne – ortotropizm.
Plagiotropizm – zorientowanie w płaszczyźnie skośnej lub poprzecznej do
kierunku działania bodźca np. ruch ustawiający organ pod kątem 90st. –
diatropizm (tropizm transwersalny).
Klasyfikacja na podstawie bodźca, który je wywołuje:
1)
Fototropizm – powodowany przez światło. Gdy roślina jest
nierównomiernie oświetlona, wiele jej organów zaczyna się tak wyginać,
aby osiągnąć z powrotem pozycję, w której oświetlenie jest równomierne.
Ruch ten jest wynikiem zmiany w sposobie wzrostu indukowanej przez
różnice przestrzennego rozmieszczenia światła podającego na roślinę. Np.
dodatni fototropizm organów roślin wyższych – pędy oraz koleoptyle traw,
zaś u niższych – sporangiofory, a także owocniki wielu grzybów.
2)
Geotropizm (grawitotropizm) – powodowany przez siłę grawitacji. Reakcja
roślin na przyśpieszenie ziemskie. Geotropizm dodatni – wzrost
określonego organu rośliny w kierunku środka Ziemi np. korzenie główne,
chwytniki przedrośli paproci i mchów. Na geotropizm ujemny reagują np.
pędy główne, ulistnione pędy mchów, owocniki i sporangiofory wielu
grzybów. Diageotropizm (geotropizm transwesalny) – gdy oś
jakiegokolwiek organu przybiera położenie pod kątem prostym w stosunku
do pola przyciągania ziemskiego, np. płącza perzu, kokoryczki, stolony
ziemniaka i rozłogi truskawki.
Plagiogeotropizm – gdy organ ustawia się pod kątem pośrednim w
stosunku do pola grawitacji np. boczne gałęzie, korzenie boczne 1go
rzędu, niektóre liście.
Ageotropizm – mała wrażliwość na geotropizm, wykazują np.pędy boczne i
korzenie boczne wyższych rzędów. Percepcja bodźca geotropicznego
zachodzi prawdopodobnie w wyniku działania przyśpieszenia ziemskiego
na pewne cięższe składniki komórkowe – statolity – ulegające
przemieszczaniu w określonych komórkach – które zależnie od
zorientowania organu, wywierają presję na cysterny ER, wyzwalając stany
wzbudzenia.
3)
Chemotropizm – przez czyniki chemiczne. Ruch wywołany różnicami
stężenia jakiegoś czynnika chemicznego w środowisku (kwasy organiczne,
sole, cukry, aminokwasy). Bodziec chemiczny powoduje stymulację, bądź
hamowanie wzrostu komórek, co powoduje wygięcie się organu. Reakcje
chemotropiczne wykazują np. strzępki grzybni, łagiewki pyłkowe, organy
wielokomórkowe, jak korzenie, oraz siewki roślin pasożytniczych.
Chemotropizm dodatni – jeśli strona organu stykająca się z substancją o
większym stężeniu rośnie wolniej, to następuje wygięcie w kierunku
wzrastającego stężenia. Chemotropizm ujemny – jeśli rośnie szybciej to
organ zwraca się w kierunku w kierunku przciwnym do działania bodźca.
4)
Termotropizm – powodowany przez temperaturę (różnica temperatur).
Termotropizm ujemny – następuje wskutek przyśpieszenia wzrostu
ogrzanej strony organu, natomiast, termotropizm dodatni – jest wynikiem
zmniejszenia szybkości wzrostu tej samej strony.
5)
Hydrotropizm – przez różnicę w wilgotności. Wygięcie w kierunku
gradientu potencjału wody.
6)
Tigmotropizm – przez bodźce mechaniczne. (np. dotyk). Tigmotropizm
dodatni wykazują pędy siewek, ogonki liściowe, a także sporangiofory
grzybów. Tigmotropizm ujemny wykazują zwykle korzenie.
7)
Traumotropizm – powodowany przez odpowiedź rośłiny na zranienia.
Dodatnia reakcja – wiąże się z zahamowaniem wzrostu i utratą turgoru po
stronie zranionej. Ujemna – z przyśpieszenie podziałów komórkowych,
Strona 21
wytwarzaniem kalusa i innymi zjawiskami regeneracyjnymi w strefie
zranienia.
Korzenie reagują z reguły ujemnie, natomiast pędy najpierw dodatnio, a
potem z czasem ujemnie.
8)
Elektrotropizm – przez potencjał elektryczny. Wygięcie organów wskutek
działania pola elektromagnetycznego lub poprzecznego przepływu prądu
stałego przez roślinę. Części pędu wyginają się w kierunku anody,
natomiast korzeni w kierunku katody
PODSTAWOWE MECHANIZMY RUCHÓW
ROŚLIN:
- zwiazane ze zdolnością komórek do wzrostu elongacyjnego
- turgorowe
- elementów strukturalnych komórki
- spowodowane pęcznieniem i wysuszeniem
- kohezyjne
- ekspozyjne
Ruchy roślin związane są z wrażliwością tkanek roślinnych na
POBUDZENIE przez określony BODZIEC. Pobudzenie powodują bodźce
zewnętrzne: światło, siła ciążenia, temperatura, substancje chemiczne,
wilgotność powietrza, siły mechaniczne, oraz czynniki wewnętrzne: np.
bodziec pojawiający sie w jednek komórce wywołuje reakcje drugiej, sa to
ruchy autonomiczne mechanizm ten jest bardzo mało poznany.
Pierwszym członem łancucha pobudzenia jest odebranie bodźca czyli
PERCEPCJA- zmiana właściwości fizykochemicznych reagującej komórki.
np jeśli pobudzenie jest wywołane światłem to percepcja bodźca polega na
fitochemicznej zmianie barwnika funkcjonującego jako fotoreceptor. Impuls
wywołany percepcją bodźca zostaje przekazany do protoplazmy i tam
wywołuje pierwszy proces fizjolligiczny czyli POBUDZENIE. Stan
pobudzenia szybko sie ustala, charakteryzuje go zmiana różnych
właściwości fizjologicznych komórki.
Po krótkim spoczynku pojawia sie POTENCJAŁ CZYNNOŚCIOWY-
różnica łądunków elektrycznych między protoplazmą a środowiskiem
zewnętrzynm, wartość powstałych potencjałów nie zależy od siły bodźca a
mianowicie nawet słaby bodziec powoduje powstanie maX potencjału
czynnościowego. Procesowi pobudzenia towarzyszy przejściowy wzrost
przepuszczalności błonykomórkowej, co prowadzi do wurównania róznicy
steżeń jonów między komórka a jej środowsikiem zewnętrznym. Czas
potrzebny do przywrócenia stanu równowagi_ STADIUM REFRAKCYJNE-
zostaje przywrócony potencjał spoczynkowy i komórka odzyskuje pełną
wrażliwość. Równolegle do powstania sie potencjału cztnnościowego
zachodza procesy polegające na bezpośrednim przekazaniu energii
pobudzenia na EFEKTOR- związek wywołujacy reakcję np. wygięcie
fototropoczne koleoptyli owsa.
Gdy miejsce bodźca nie jest miejscem reakcji musi wystąpić przewodzenie
sugnału, odbywa się zazwyczaj ze współudziałem określonych związków
chemicznych pośredniczących w tym procesie tzw transmitery pobudzenia-
substancje wzrostowe- przebudzenie zachodzi wolno Różnice w reagowniu
na bodżce wynikaja z uwarunkowań genetycznych. Stopień wrażliwosci
zależy odwrunków zewnętrznych oraz czynników wewnętrznych- TONUS
ROŚLINY- wrażliwość na bodziec.
Obniżenie lub podwyższenie temperatuty zmiejsza tonus
reagującego organu i powoduje, że maleje zdolnośc ruchu, organ zdolny
do wygiecia fototropicznego jeśli znajduje się w świetle, to słabiej reaguje
na promieniowanie aniżeli taki, który przed zadziałaniem bodźca znajdował
się w ciemności jest to ADAPTACJA. Do wsytąpienia reakcji rośliny o
określonym tonusie potzreba bodźca o minimalnej WARTOŚCI
PROGOWEJ. Jeżeli natężenie bodźca jest zbyt małe by wywołać reakcje
jest nazywane podprogowym. Powtarzające sie bodźce podprogowe
ulregają zazwyczaj sumownaiu. Dolna wartość progowa charakteryzuje
wrażliwość organu, zaś PRÓG ROZRÓŻNIANIA pozwala na percepcję
tego samego bodźca o różnym natężeniu, jest to najmniejsza różnica
natężenia bodźca, która jeszcze warunkuje ruch.
Efekt działania zależy również od czasu działania. CZAS
PREZENCJI- najkrótszy czas działania bodźca niezbędnego do wykonania
ruchu, dlasilniejszych bodźcó jest on silniejszy niż dla słabszych.
Od momentu zadziałania bodźca do rozpoczęcia ruchu upływa pewien
czas- CZAS REAKCJI zależy on od natężęnia bodźca i od czynników
zewnętrznych takich jak temperatura.
Strona 22
GOSPODARKA WODNA
Dostępność wody glebowej dla roślin
wyższych.
W glebie wyróżnia się cztery zasadnicze postacie wody:
1)
Higroskopijna – warstwa molekuł wody, powlekająca cząsteczki glebowe,
utrzymywana przez nie z olbrzymią siłą. Jest niedostępna dla roślin.
2)
Błonkowata – warstwa molekuł wody, następna po higroskopijnej,
przyciągana z siłą coraz mniejszą, jednak zawsze przekraczającą siły
ssące korzenia. Jest niedostępna dla roślin.
3)
Kapilarna – woda wypełniająca włosowate kanaliki w glebie; jest
podtrzymywana siłami napięć powierzchniowych, dzięki czemu nie ulega
sile ciążenia. Jest dostępna dla roślin.
4)
Grawitacyjna – woda wypełniająca okresowo większe przestwory
glebowe. Pod wpływem siły ciążenia spływa na niższe poziomy, a wtedy
przestwory wypełniają się powietrzem. Jest dostępna dla roślin.
Dyfuzja a osmoza – definicje, prawa osmozy.
Dyfuzja jest to proces mieszania się ze sobą cząsteczek, spowodowany ich
przypadkowymi ruchami, wzbudzonymi termicznie. Cząsteczki
przemieszczają się od obszarów o większym stężeniu do obszarów o
mniejszym stężeniu danej substancji – zgodnie z gradientem stężenia
substancji. Dyfuzja zapewnia sprawne przemieszczanie się substancji na
krótkich dystansach.
Szybkośc dyfuzji zależy od:
- rodzaju ośrodka
- temperatury
-pola elektrycznego.
Osmoza jest to niezależne od nakładu energii, spontaniczne
przemieszczanie się wody przez błonę półprzepuszczalną zgodne z
gradientem stężenia wody po obu stronach błony.
Prawa osmozy:
•
Ciśnienie osmotyczne jest wprost proporcjonalne do stężenia roztworu
(analogia z prawem Boyla-Mariotta)
•
Ciśnienie osmotyczne jest wprost proporcjonalne do temperatury
bezwzględnej, czyli inaczej podniesienie temperatury o 1 stopień
powyżej 0 stopni powoduje wzrost ciśnienia o 1/273 (analogia z
prawem Gay – Lussaca)
•
Jednomolarny roztwór dowolnej substancji (lecz nie elektrolitu) ma
ciśnienie osmotyczne 22,4 atmosfery w temperaturze 0 stopni
Celsjusza. Substancje, które ulegają dysocjacji (elektrolity) wykazują
wyższe ciśnienie, gdyż częśc ich cząsteczek rozpada się na jony, w
rezultacie czego stężenie się zwiększa. Odpowiednio zwiększa się
również ciśnienie osmotyczne takiego roztworu.
Stosunki osmotyczne w komórce roślinnej –
podstawowe prawa, definicje, wykres Thodaya.
Każda żywa komórka roślinna ma zdolność do pobierania i oddawania
wody. U
podstaw tych zjawisk leżą takie procesy fizyczne jak dyfuzja, osmoza
i pęcznienie. Dyfuzja jest to przemieszczanie się cząsteczek z stężenia
większego do stężenia mniejszego wywołane naturalnym ruchem cieplnym
cząsteczek. Wszystkie cząsteczki występujące na ziemi są w nieustannym
ruchu. Ruch ten jest uwarunkowany ich energią kinetyczną, która zależy do
temperatury danej substancji. W miarę podwyższania temperatury rośnie
ich energia kinetyczna, a przez to szybkość dyfuzji.
Osmoza jest to przepływ wody z roztworu hipotonicznego do roztworu
hipertonicznego, w którym następuje zwiększenie objętości i wzrost
ciśnienia hydrostatycznego. Układ osmotyczny stanowi dwa roztwory o
niejednakowym stężeniu substancji, podzielone błoną półprzepuszczalną.
Na skutek intensywnej dyfuzji wody przez błonę z roztworu hipotonicznego
Strona 23

do roztworu hipertonicznego (osmoza), w tym ostatnim następuje
zwiększenie objętości i wzrost ciśnienia hydrostatycznego.
Osmoza:
- to dyfuzja (przemieszczanie się) wody przez błonę półprzepuszczalną
(selektywną) oddzielającą 2 roztwory o różnych stężeniach bądź czystą
wodę od roztworu, zgodnie z gradientem stężeń roztworów po obu
stronach błony, w stronę roztworu o większym stężeniu.
- jest spontaniczna i niezależna od nakładu energii.
- odgrywa bardzo ważną rolę w procesach pobierania i oddawania wody
przez komórkę.
Pęcznieniem nazywamy absorpcję wody połączonej ze zwiększeniem
objętości
substancji koloidalnych. Cząsteczki wody dyfundując pomiędzy micele
koloidów, rozsuwają je, przez co zwiększają ich masę i objętość (tym różni
się od kapilarnego wchłaniania wody np. przez kredę.
Pomiar potencjału osmotycznego (ciśnienia osmotycznego) – możliwy jest
dzięki przyrządowi zwanemu osmometrem Pfeffera. Składa się on z
cylindra z porowatej glinki, nasyconej roztworami K4Fe(CN)6 i CuSO4
(tworzącymi idealną półprzepuszczalną membranę), połączonego z
manometrem rtęciowym. Przyrząd wypełnia się badanym roztworem i
zanurza w naczyniu z czystą wodą. Miarą ciśnienia osmotycznego będzie
różnica poziomów rtęci w ramionach manometru.
Ciśnienie osmotyczne (potencjał osmotyczny) - ciśnienie, które
równoważy osmotyczne przenikanie wody; wyraża się w atmosferach i jest
miarą siły z jaką roztwór ssie wodę.
Podstawowe prawa osmotyczne (są zbliżone do praw o ciśnieniu gazów):
1. Ciśnienie osmotyczne jest wprost proporcjonalne do stężenia
roztworu (analogia z prawem Boyla-Mariotta)
2. Cisnienie osmotyczne jest wprost proporcjonalne do temperatury
bezwzględnej, czyli inaczej podniesienie temperatury o 1 stopień powyżej 0
stopni powoduje wzrost ciśnienia o 1/273 (analogia z prawem Gay-
Lussaca)
3. Jednomolarny roztwór dowolnej substancji (lecz nie elektrolitu)
ma ciśnienie osmotyczne 22,4 atmosfery w temp. 0 stopni C (analogia z
prawem Avogadro)
Substancje, które ulegają dysocjacji (elektrolity) wykazują wyższe
ciśnienie, gdyż część ich cząsteczek rozpada się na jony, w rezultacie
czego stężenie się zwiększa. Odpowiednio zwiększa się również ciśnienie
osmotyczne takiego roztworu.
Ciśnienie(potencjał) osmotyczne roztworu można wyrażać w atmosferach
albo w molach na litr. Zależność między molarnym stężeniem roztworu a
jego ciśnieniem osmotycznym przedstawia równanie van’t Hoffa:
Po = i * C * R * T
Po – ciśnienie osmotyczne
I – współczynnik izotoniczny
C – stężenie roztworu ( w molach na decymetr sześcienny)
R – stała gazowa
T – temperatura bezwzględna
Dodatkowe pojęcia (oprócz tych dotyczących osmozy):
Dyfuzja – przypadkowy, bezładny ruch cząsteczek danej substancji
(ruchy Browna) z jednego punktu przestrzeni od drugiego, uwarunkowany
ich energią kinetyczną (wprost proporcjonalną do temperatury). Dążenie do
maksymalnej entropii zmusza cząsteczki do bezładnego przemieszczania
się w całej powierzchni.
Prawo Steffana (do dyfuzji) – prawo dotyczące dyfuzji pary wodnej
i innych gazów przez szparki. Mówi ono że wymiana gazowa i parowanie z
powierzchni bardzo małych odbywa się proporcjonalnie do średnicy, a nie
do ich powierzchni.
Siła ssąca - siła odpowiedzialna za wnikanie wody do komórki
roślinnej podczas osmozy. Powstaje jako różnica między potencjałem
osmotycznym (P
O
) roztworu zewnętrznego a ciśnieniem turgorowym
komórki (cT):
S = P
O
- cT
Strona 24
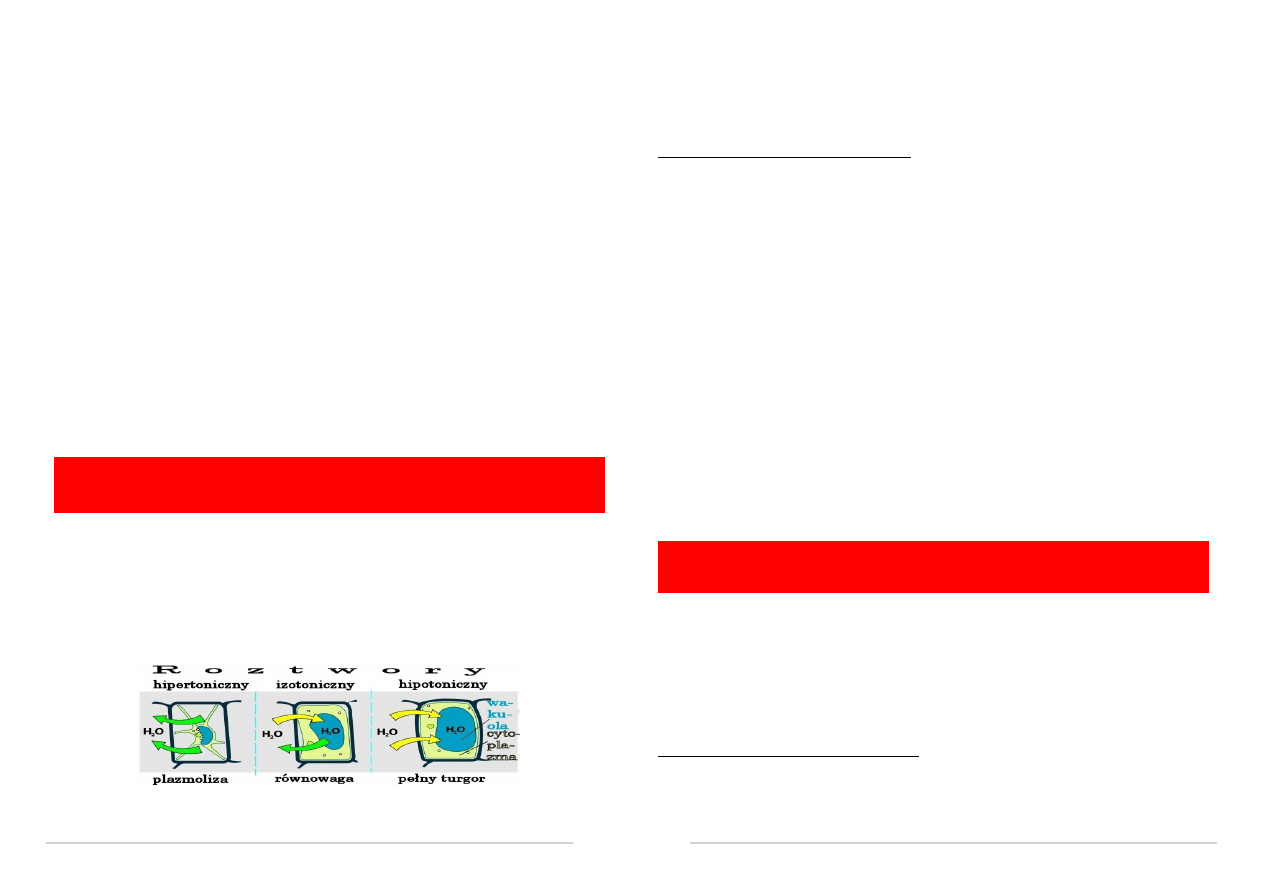
Siła ssąca osiąga tym większą wartość, im większy niedobór wody w
komórce, wywołany np. intensywną transpiracją. Wyrażamy ją w
atmosferach.
Turgor –stan napięcia komórki, usztywnienia tkanek, który jest jednym z
czynników nadającym roślinom określony kształt.
Susza fizjologiczna - susza wywołana nie brakiem wody, lecz czynnikami
utrudniającymi jej pobieranie
Bilans wodny – różnica między ilością wody pobranej przez roślinę i
ilością wody wytranspirowanej. Wskazuje on na kierunek i wielkość
odchyleń od stanu równowagi. Wykazuje stale pewne oscylacje w czasie.
Można go wyznaczyć określając zmiany zawartości wody w roślinie. O
bilansie wodnym decydują: parowanie wody z roślin (transpiracja),
pobieranie wody z gleby i przewodzenie wody z korzeni do tkanek.
Wykres Thodaya – wykres między siłą ssącą (obecną w wakuoli) a
potencjałem osmotycznym komórki i ciśnieniem turgorowym. (rysunek
schematyczny w wykładzie II z fizj. roś)
Zjawiska osmotyczne i ich znaczenie dla komórki
roślinnej.
Osmoza – dyfuzja rozpuszczalnika przez błonę półprzepuszczalną z
roztworu hipotonicznego do hipertonicznego.
Komórki organizmów żywych w kontakcie z roztworem hipotonicznym
ulegają powiększeniu. Jeśli komórka nie ma ściany komórkowej, może
nawet ulec rozsadzeniu. Trafiając do roztworu hipertonicznego, komórki
kurczą się, podlegając różnego stopnia plazmolizie.
Plazmoliza - proces tracenia wody w komórce w roztworze hipertonicznym.
W wyniku tego następuje obkurczenie cytoplazmy od ścian komórki.
Dotyczy ona wyłącznie komórek roślinnych.
Wyróżnia się 4 rodzaje plazmolizy:
•
kątowa
•
wklęsła
•
wypukła
•
graniczna
Procesem odwrotnym do plazmolizy jest deplazmoliza.
Deplazmoliza - proces odwrotny do plazmolizy, polegający na pobieraniu
wody przez komórkę przeniesioną z roztworu hipertonicznego (niezbyt
silnie) i zanurzoną w roztworze hipotonicznym. W wyniku deplazmolizy
komórka odzyskuje turgor, a błona komórkowa w komórkach roślinnych,
ponownie w pełni przylega do ściany komórkowej. Deplazmoliza zachodzi
tylko jeżeli białka błony komórkowej nie uległy denaturacji, a błona jest nie
rozerwana dzięki czemu wciąż cechuje ją półprzepuszczalność.
Rośliny wykorzystują zjawiska osmotyczne do transportu wody od
korzeni do liści. Zjawiska osmotyczne zapewniają sztywność liści i łodyg
(we współdziałaniu z niektórymi tkankami), są też podstawą działania
aparatu szparkowego.
Krótko dystansowy transport wody w roślinach
wyższych
Droga wody od gleby aż do liścia składa się z trzech etapów:
Pobieranie wody oraz jej przewodzenie w poprzek tkanek korzenia
do walca osiowego
Daleki transport wody elementami ksylemu (naczynia) do liścia
Transport wody poprzez tkani liścia zakończony wyparowaniem
(transpiracją) do atmosfery.
Transport wody w poprzek korzenia
Strona 25

Woda wnika do korzenia przez cienka ścianę włośnika lub skórki w strefie
włośnikowej, a następnie migruje przez warstwy komórek kory pierwotnej
do walca osiowego. Ruchy wody przez korę pierwotną:
A. Wędrówka na drodze imbibicyjnej w tzw. kanale apoplastycznym
(czyli w kapilarnych przestrzeniach ścian komórkowych
celulozowych lub celulozowo-pektynowych, z pominięciem
cytoplazmy i wakuoli)
B. Wędrówka prze tzw. kanał symplistyczny (czyli przez cytoplazmę
komórki z pominięciem wakuoli, a następnie przez plazmodesmy do
cytoplazmy komórki następnej.
C. Ruch wody na drodze osmotycznej od wakuoli do wakuoli.
Zachodzi ona, gdyż siła ssąca komórek wzrasta w miarę posuwania
się w głąb korzenia, co jest warunkiem koniecznym
przemieszczania się wody z komórki do komórki.
Droga wody jest „kombinowana” tzn. że transport wody nie
zachodzi w jednym określonym kanale lecz różnymi drogami. Woda
migruje częściowo ścianami komórkowymi, przedostaje się do
cytoplazmy, a z niej albo z powrotem do ściany, albo do wakuoli i
dalej na zmianę do cytoplazmy, ścianami lub wakuolami, w
zależności od oporu, różnic sił ssących i stopnia nasycenia wodą
danych elementów komórkowych.
Transport wody przez tkanki liścia
Transport zachodzi od cewek i naczyń do komórek miękiszu gąbczastego i
palisadowego. Migracja wody następuje przede wszystkim kanałem
apoplastycznym, a więc ścianami komórkowymi. Z powierzchni komórek
mezofilu woda wyparowuje na drodze transpiracji.
Mechanizm pobierania i przewodzenia wody.
Pobieranie wody w roślinach naczyniowych odbywa się dzięki działaniu
mechanizmu biernego i aktywnego.
Mechanizm bierny opiera się na sile ssącej liści powstającej na skutek
transpiracji, czyli parowania wody z liści. Wyparowywanie wody z powierzchniowej
warstwy komórek liści powoduje zmniejszenie ich potencjału wody i turgoru, a tym
samym wzrost siły ssącej. Na miejsce wytranspirowanej wody podciągane są
następne cząsteczki. Komórki powierzchni liści odbierają zatem wodę komórkom
sąsiednim, a te następnym itd. - aż do naczyń i cewek. Ubytek wody w naczyniach
i cewkach (spowodowany ssącym działaniem transpiracji) wywołuje podciśnienie
hydrostatyczne sięgające przez łodygę do korzenia, na skutek czego woda
przechodzi z komórek walca osiowego korzenia do naczyń i cewek, a z gleby do
włośników. W takim układzie każda komórka, która oddaje wodę komórce
sąsiadującej z nią z jednej strony, pobiera ją od komórki sąsiadującej z drugiej
strony. Ruch wody odbywa się na drodze najmniejszego oporu i następuje albo
ścianami komórkowymi (kanał apoplastyczny), albo przez cytoplazmę i
plazmodesmy (kanał symplastyczny), bądź też od wakuoli do wakuoli (na zasadzie
osmozy). Niski potencjał wody występujący w liściach zapewnia możliwość
dostarczenia wody do wierzchołka korony najwyższych drzew. W mechanizmie
biernym nie korzenie, a liście są sprawcą pobierania i transportu wody przez
roślinę (korzenie pełnią funkcję bierną, a woda sama wnika do korzeni, ponieważ
wartość -w jest w nich niższa od-w w glebie). Oprócz siły ssącej liści na ruch wody
w naczyniach ma wpływ działanie siły kohezji (spójności) wody, zapobiegającej
rozerwaniu się słupów wody w kapilarach. Mechanizm bierny, choć korzystny,
ponieważ nie wymaga dostarczania energii (poza energią słoneczną niezbędną do
transpiracji), ma tę wadę, że jest skuteczny w warunkach sprawnej transpiracji.
Wiosną, kiedy jeszcze nie ma liści, bądź rozwinęły się dopiero pączki, a ich
transpiracja jest bardzo słaba, względnie w nocy, gdy w porównaniu z dniem
transpiracja wielokrotnie maleje, pobieranie, transport i wydalanie wody przez
roślinę odbywa się jedynie lub głównie dzięki mechanizmowi aktywnemu, który
tłoczy wodę w górę rośliny. Miejscem działania mechanizmu aktywnego pobierania
i transportu wody jest korzeń. Zachodzący w komórkach korzeni aktywny
mechanizm pobierania wody przez korzeń wymaga dopływu energii z przemian
metabolicznych (ATP). Woda przenika z gleby do komórek ryzodermy i dalej, w
poprzek korzenia, aż do naczyń i cewek, powodując wzrost ciśnienia w
elementach przewodzących, które podnosi w nich poziom wody. Powstające w
naczyniach i cewkach ciśnienie nazywa się parciem korzeniowym, a jego wartość
jest niższa od siły ssącej transpirujących liści. O istnieniu zjawiska parcia
korzeniowego można się łatwo przekonać, jeśli zetnie się młodą siewkę, np. fasoli,
przy szyjce korzeniowej. Po kilku minutach na powierzchni przecięcia pojawią się
krople wody, które świadczą o tym, że korzeń aktywnie pompuje wodę do góry. W
naturalnych warunkach parcie korzeniowe powoduje gutację lub wyciekanie soku
ze zranionych części rośliny.
Oba mechanizmy transportu wody, bierny i aktywny, uzupełniają się wzajemnie.
Polepszanie warunków transpiracji i towarzyszący temu wzrost siły ssącej liści
Strona 26

powoduje obniżenie wartości parcia korzeniowego. W sytuacji odwrotnej przeważa
mechanizm aktywny. Z ekonomicznego punktu widzenia lepszy jest mechanizm
bierny, ponieważ nie przynosi roślinie strat w postaci "zużytego" w oddychaniu
cukru w celu uzyskania ATP, koniecznego do aktywnego transportu. Mechanizm
bierny wykazuje również większą skuteczność, ponieważ siła ssąca liści osiąga
wyższe wartości niż parcie korzeniowe.
Pobieranie i transport wody w roślinach
wyższych
Roślina lądowa pobiera wodę systemem korzeniowym, a rozprowadza
wiązkami sitowo –naczyniowymi.
System korzeniowy jest częścią rośliny, która bezpośrednio kontaktuje się
z glebą i zaopatruje roślinę w wodę i sole mineralne. Dzięki obecności włośników
powierzchnia systemu korzeniowego jest wielokrotnie większa od powierzchni
części nadziemnej. Włośniki wnikając między cząsteczki gleby zapewniają
bezpośredni kontakt korzenia z wodą zaadsorbowaną na powierzchni tych cząstek
lub z roztworem wody w kapilarach gleby. Adsorpcja wody przez korzeń zachodzi
głównie w strefie położonej blisko wierzchołka wzrostu, gdzie komórki skórki mają
cienkie ściany i liczne włośniki.
Transport wody w poprzek korzenia:
Woda wnika do korzenia przez cienką ścianę włośnika lub skórki w strefie
włośnikowej, a następnie migruje przez warstwy komórek kory pierwotnej do walca
osiowego. Bierze się pod uwagę trzy drogi przemieszczania się wody przez te
tkanki: może się ona przemieszczać w apoplaście- w obrębie ścian i przestworów
komórkowych, w symplaście – przez cytoplazmę poszczególnych komórek,
połączonych plazmodesmami oraz ruch wody na drodze osmotycznej od wakuoli
do wakuoli.
Transport wody elementami ksylemu
Ksylem jest zbudowany z wielu typów komórek, z których najbardziej istotne
funkcje pełnią cewki (u paprotników i większości nagozalążkowych) i naczynia (u
okryto-zalążkowych). Naczynia są wydłużonymi, martwymi komórkami o
zgrubiałych ścianach komórkowych wysyconych ligniną. Cewki mają skośne
poprzeczne ściany komórkowe, podczas gdy w naczyniach uległy one zanikowi.
Transport wody w ksylemie jest transportem biernym - nie wymaga nakładów
energetycznych, a jedynie drożnych kanałów, w których może sprawnie
przebiegać; dlatego też cewki i naczynia są pozbawione protoplastów. Ksylem
składa się głównie z komórek zdrewniałych, dlatego pełni także funkcje tkanki
wzmacniającej. Jest tkanką bardzo niejednorodną, zbudowaną z wielu typów
komórek. Cewki są wydłużonymi komórkami o końcach zwężonych bądź
zakończonych ukośnymi ścianami komórkowymi. Dojrzałe cewki są martwymi
komórkami pozbawionymi protoplastów. W ich ścianach znajdują się jamki, przez
które woda może bez przeszkód przemieszczać się między komórkami i dzięki
temu jest sprawnie rozprowadzana po roślinie. Naczynia budujące ksylem roślin
okrytozalążkowych są długimi rurami, które powstały dzięki zanikowi ścian
poprzecznych składających się na nie komórek. Komórki te, zwane członami
naczyniowymi, są martwe, a budową przypominają cewki. Ich podłużne ściany
komórkowe są nierównomiernie zgrubiałe, są też zaopatrzone w jamki. Ustawione
pionowo w szeregi, tworzą system nieprzerwanych kanałów ciągnących się na
znacznych odcinkach. Dzięki zanikowi ścian pomiędzy poszczególnymi członami
rury woda przepływa bez żadnych przeszkód. Woda w ksylemie przemieszcza się
do wyżej położonych części rośliny pod wpływem parcia korzeniowego i
transpiracji.
Transport wody przez tkanki liścia
Ruch wody od cewek i naczyń do komórek miękiszu gąbczastego i palisadowego.
Migracja wody przez tkanki liścia następuje przede wszystkim kanałem
apoplastycznym, a więc ścianami komórkowymi. Z powierzchni komórek mezofilu
woda wyparowuje, co stanowi istotę transpiracji.
Pasywne i aktywne mechanizmy pobierania
jonów przez rośliny wyższe
Proces biernego przenikania jonów przez błony może przebiegać przez
dyfuzję prostą, złożoną lub ułatwioną. Dyfuzja prosta zachodzi w kierunku od
stężenia większego do mniejszego i ustaje w wyniku wyrównania się stężeń
związku po obu stronach błony. W przypadku dyfuzji złożonej poza gradientem
stężeń szybkość przenikania substratu przez błony zależy również od gradientu
potencjału elektrycznego lub gradientu ciśnienia osmotycznego. W procesie dyfuzji
ułatwionej uczestniczą nośniki, które wiążą określoną cząsteczkę o jednej stronie
błony i przenoszą na stronę przeciwną.
Transport aktywny wymaga stałego dopływu energii metabolicznej.
Energia ta wykorzystywana jest do wytwarzania siły transportowej. Uważa się, że
Strona 27

transport aktywny zachodzi dwóch etapach. W pierwszym (transport pierwotny) na
skutek aktywności pompy protonowej dochodzi do powstania elektrochemicznego
gradientu protonów. W drugim etapie (transport wtórny) protony powracają do
komórki czemu towarzyszy transport różnych jonów.
Przemieszczanie jonów polega na sprzężonym ruchu H+ oraz
transportowanej cząsteczki z udziałem specyficznych nośników białkowych.
Wyróżniamy symport i antysport protonowy. W przypadku symportu zarówno
protony jak i transportowane jony są przenoszone ze środowiska
zewnątrzkomórkowego do cytoplazmy. Gdy przemieszczaniu protonów ze
środowiska do wnętrza komórki towarzyszy odwrotnie ukierunkowany transport
jonów mamy do czynienia z antyportem.
Pasywne i aktywne mechanizmy transportu
wody.
Mechanizm bierny opiera się na sile ssącej liści powstającej na
skutek transpiracji, czyli parowania wody z liści (sama transpiracja
jest wynikiem dużego spadku potencjału między liściem i atmosferą).
Wyparowywanie wody z powierzchniowej warstwy komórek liści
powoduje zmniejszenie ich potencjału wody i turgoru, a tym samym
wzrost siły ssącej. Na miejsce wytranspirowanej wody podciągane
są następne cząsteczki. Komórki powierzchni liści odbierają zatem
wodę komórkom sąsiednim, a te następnym itd. - aż do naczyń i
cewek. Ubytek wody w naczyniach i cewkach (spowodowany
ssącym działaniem transpiracji) wywołuje podciśnienie
hydrostatyczne sięgające przez łodygę do korzenia, na skutek czego
woda przechodzi z komórek walca osiowego korzenia do naczyń i
cewek, a z gleby do włośników. W takim układzie każda komórka,
która oddaje wodę komórce sąsiadującej z nią z jednej strony,
pobiera ją od komórki sąsiadującej z drugiej strony. Ruch wody
odbywa się na drodze najmniejszego oporu i następuje albo
ścianami komórkowymi (a - kanał apoplastyczny), albo przez
cytoplazmę i plazmodesmy (b - kanał symplastyczny), bądź też od
wakuoli do wakuoli (c - na zasadzie osmozy). Niski potencjał wody
występujący w liściach zapewnia możliwość dostarczenia wody do
wierzchołka korony najwyższych drzew.
W mechanizmie biernym nie korzenie, a liście są sprawcą
pobierania i transportu wody przez roślinę (korzenie pełnią funkcję
bierną, a woda sama wnika do korzeni). Zniszczenie korzeni nie
zmniejsza, a nawet niekiedy zwiększa bierne pobieranie wody.
Oprócz siły ssącej liści na ruch wody w naczyniach ma wpływ
działanie siły kohezji (spójności) wody, zapobiegającej rozerwaniu
się słupów wody w kapilarach. Jeśli zanurzymy rurkę szklaną w
pojemniku z wodą, to dzięki kohezji woda w rurce podniesie się
ponad poziom wody w pojemniku. Wysokość podniesienia słupa
wody w kapilarze zależy od jej średnicy (im mniejsza średnica, tym
wyżej podnosi się woda), a naczynia roślin są bardzo cienkimi
rurkami. Mechanizm bierny, choć korzystny, ponieważ nie wymaga
dostarczania energii (poza energią słoneczną niezbędną do
transpiracji), ma tę wadę, że jest skuteczny w warunkach sprawnej
transpiracji.
Mechanizm aktywny – u większości roślin pobieranie wody
zachodzi przez włośniki korzeniowe (w strefie różnicowania się
komórek), które wnikają głęboko między cząsteczki gleby i
powiększają powierzchnię absorbcyjną korzenia. W tym
mechanizmie woda wraz z jonami pierwiastków przenika na drodze
transportu aktywnego (przy użyciu ATP) do cytoplazmy komórek
włośnikowych. W wyniku aktywnego pobierania jonów między
cytoplazmą a roztworem glebowym powstaje gradient stężenia, który
powoduje bierne, aczkolwiek niezależne od transpiracji, pobieranie
wody. Woda przepływa w poprzek korzenia przez przestwory
międzykomórkowe i ściany komórkowe – apoplast – lub przez
wnętrza komórek – symplast. Woda z solami przechodzi kolejno
przez: skórkę (włośnik), warstwę kory pierwotnej, śródskórnię (w jej
ścianach znajdują się pasemka Caspary’ego – pasma
impregnowane suberyną, które blokują translokację wody przez
apoplast endodermy), komórki perycyklu i ostatecznie dociera do
naczyń lub cewek w walcu osiowym. Ciągły napływ wody powoduje
wzrost ciśnienia w elementach przewodzących i podnoszenie się
poziomu wody. Powstające w cewkach i naczyniach ciśnienie zwane
jest parciem korzeniowym. Woda pobierana jest przez korzenie tylko
wtedy, gdy roztwór glebowy jest roztworem hipotonicznym.
Strona 28
Trochę innymi słowami;)Wiosną, kiedy jeszcze nie ma liści, bądź rozwinęły się
dopiero pączki, a ich transpiracja jest bardzo słaba, względnie w nocy, gdy w
porównaniu z dniem transpiracja wielokrotnie maleje, pobieranie, transport i
wydalanie wody przez roślinę odbywa się jedynie lub głównie dzięki
mechanizmowi aktywnemu, który tłoczy wodę w górę rośliny. Miejscem działania
mechanizmu aktywnego pobierania i transportu wody jest korzeń. Zachodzący w
komórkach korzeni aktywny mechanizm pobierania wody przez korzeń, oparty na
aktywnym transporcie jonów przez błonę komórkową, wymaga dopływu energii z
przemian metabolicznych (ATP). W wyniku aktywnego pobierania jonów przez
komórki powstaje gradient stężeń i nieustannie utrzymywane są wysokie siły
ssące, które powodują bierne, aczkolwiek niezależne od transpiracji, pobieranie
wody. Woda przenika z gleby do komórek ryzodermy i dalej, w poprzek korzenia,
aż do naczyń i cewek, powodując wzrost ciśnienia w elementach przewodzących,
które podnosi w nich poziom wody. Powstające w naczyniach i cewkach ciśnienie
nazywa się parciem korzeniowym, a jego wartośc jest niższa od siły ssącej
transpirujących liści.
Plazmoliza i deplazmoliza- związki ze zjawiskami
osmotycznymi w komórkach roślinnych.
Plazmoliza - proces tracenia wody w komórce w roztworze
hipertonicznym. W wyniku tego następuje obkurczenie cytoplazmy od ścian
komórki. Dotyczy ona wyłącznie komórek roślinnych.
Inaczej jest to zjawisko odstawania protoplastu od ściany komórkowej.
Plazmolizę można zaobserwować w komórkach roślinnych po
umieszczeniu ich w roztworze hipertonicznym. Zgodnie z prawami osmozy
woda przenika przez plazmalemmę z komórki do roztworu, co powoduje
odwodnienie komórki i kurczenie się cytoplazmy podstawowej. W
zależności od stopnia utraty wody wyróżnia się plazmolizę kątową, wklęsłą
i wypukłą (graniczną). Umieszczenie splazmolizowanej komórki w
roztworze hipotonicznym spowoduje napływ wody do komórki i odzyskanie
turgoru - deplazmolizę.
Plazmoliza – zjawisko odwracalne, polegające na kurczeniu się protoplastu
i jego odstawaniu od ścian komórkowych, wskutek umieszczenia komórki
w roztworze hipertonicznym.
Wyróżnia się 4 rodzaje plazmolizy:
•
kątowa
•
wklęsła (skurczony protoplast ma wyraźne wklęśnięcia)
•
wypukła (skurczony protoplast odstaje od ściany komórkowej w
postaci uwypuklonej)
•
graniczna (początkowe stadium plazmolizy, w którym protoplast
odstaje od ściany jedynie w narożach komórki)
Deplazmoliza - proces odwrotny do
, polegający na pobieraniu
wody przez
przeniesioną z roztworu hipertonicznego (niezbyt
. W wyniku deplazmolizy
, a
. Deplazmoliza zachodzi
tylko jeżeli białka błony komórkowej nie uległy denaturacji, a błona jest nie
rozerwana dzięki czemu wciąż cechuje ją półprzepuszczalność.
(Znaczenie zjawisk osmotycznych w życiu roślin: )
Zjawiska osmotyczne odgrywają zasadnicza rolę w procesie
wnikania wody do komórki. Również takie procesy, jak pobieranie
wody przez włośniki, przekazywanie jej z jednej komórki do drugiej i
rozprowadzanie wody po roślinie są w znacznej mierze –
zjawiskami osmotycznymi.
Dzięki procesom osmotycznym roślina posiada turgor, czyli stan
usztywnienia tkanek, który jest jednym z czynników nadających
roślinom określony kształt (obok tkanek mechanicznych, jak
kolenchyma i sklerenchyma). Wystarczy porównać roślinę
zwiędniętą z roślina w stanie pełnego turgoru, aby zrozumieć jakie
znaczenie mają procesy osmotyczne.
Dzięki procesom osmotycznym rosnące tkanki mogą wywierać
znaczne siły, których przykładem może być siła z jaką młody korzeń
lub kiełek przebija się przez glebę.
-Stężenie osmotyczne soku komórkowego stanowi ważny czynnik
odporności roślin na niskie temperatury i suszę. Komórki o
wyższym stężeniu osmotycznym wykazują zwykle większą
odpornośc na mróz.
WŁAŚCIWOŚCI OSMOTYCZNE KOMÓRKI
ROŚLINNEJ
Dojrzała komórka roślinna składa się ze ściany komórkowej oraz
cienkiej warstwy cytoplazmy która otacza centralna wakuolę wypełnioną
sokiem komórkowym.
Strona 29

•
Ściana komórkowa zbudowana jest z celulozy z dodatkiem
hemicelulozy. Posiada liczne submikroskopowe przestwory o
wymiarach przekraczających wymiary przenikających cząsteczek.
Jest ona zatem przegroda w pełni przepuszczalną, nie posiada
właściwości selektywnych i nie odgrywa roli membrany selektywnej.
•
Cytoplazma, a przede wszystkim jej membrany plazmatyczne
(plazmolemma i tonoplast) są selektywnie przepuszczalne.
Cytoplazma jest więc membraną selektywną, nie spełnia jednak
wszystkich warunków które spełnia idealna membrana
półprzepuszczalna. Mogą przez nią przenikać zarówno związki
niedysocjujące jak i dysocjujące.
•
Sok komórkowy – wypełnia wakuole – jest wodnym roztworem
rozmaitych soli, cukrów i innych związków. W zależności od
stężenia soku wykazuje określony, ale zmienny potencjał
osmotyczny.
Strona 30

Jeżeli komórkę umieścimy w czystej wodzie, to zachodzić będzie osmoza,
czyli dyfuzja wody poprzez selektywną warstwę cytoplazmy, do wakuoli.
Siłę z jaką woda będzie wnikać do komórki nazywamy siłą ssącą
komórki. W miarę wnikania wody wakuola powiększa się, czemu
towarzyszy rozciąganie woreczka cytoplazmatycznego, a także ścian
komórkowych.
W rozciąganej ścianie komórkowej pojawiają się siły sprężyste
przeciwdziałające dalszemu rozciąganiu. W końcu dochodzi do stanu
równowagi, w którym siły osmotyczne są równoważne sprężystością ścian
komórkowych. Komórka taka znajduje się w stanie pełnej turgoscencji, a
ciśnienie wywierane przez zawartość komórki na jej ściany nazywamy
ciśnieniem turgorowym.
Siła ssąca komórki równa się różnicy pomiędzy potencjałem
osmotycznym soku komórkowego a ciśnieniem turgorowym.
W komórce roślinnej umieszczonej w czystej wodzie zachodzi osmoza,
przy czym w miarę wnikania wody:
Ciśnienie turgorowi będzie wzrastać,
Objętość komórki będzie wzrastać,
Potencjał osmotyczny soku będzie maleć (gdyż maleć będzie
stężenie soku z powodu wnikania wody)
WODA JAKO ŚRODOWISKO ŻYCIA
– WŁASNOŚCI FIZYKOCHEMICZNE
Życie powstało w wodzie i woda w organizmach roślin i zwierząt jest elementem
absolutnie niezbędnym do życia. Cząsteczka wody składa się z atomu tlenu
związanego kowalencyjnie z dwoma atomami wodoru1. Ładunki wody równoważą
się wzajemnie w wyniku, czego nie posiada ona żadnego ładunku netto. Woda jest
cząsteczką spolaryzowaną (dipolem). Cząsteczki wody przyciągają się wzajemnie
na zasadzie oddziaływania elektrostatycznego (wiązań wodorowych). Wiązania te
sprawiają, że 80% wolnej wody w komórce tworzy pseudokrystaliczną sieć
zbudowaną z szybko powstających i znikających agregatów ich wielkość zależy od
temperatury; wzrost temperatury powoduje zmniejszenie. Polarne właściwości
wody sprawiają, że: jest ona doskonałym rozpuszczalnikiem, szczególnie dla
substancji obdarzonych ładunkiem elektrycznym gdyż cząsteczki wody wiążą
siłami elektrostatycznymi z
powierzchnią jonów (otoczki wodne) lub z polarnymi grupami białek
i polisacharydów (powłoki hydratacyjne).
Ma duże ciepło właściwe trzeba dostarczyć bardzo dużą ilość energii cieplnej, aby
podnieść jej temperaturę o 1º) oraz duże ciepło topnienia i ciepło parowania (te
zmiany stanu skupienia wody wymagają dostarczenia dużej ilości energii cieplnej).
Właściwości te umożliwiają roślinie utrzymanie temperatury „ciała” na stosunkowo
stałym poziomie.
S
ą
podstaw
ą
takich zjawisk jak:
o Kohezja (wzajemnie przyciąganie się cząsteczek wody), która
zapewnia
dużą wytrzymałość słupa wody na rozciąganie.
o Adhezja (przyciąganie wody przez naładowane elektrycznie
powierzchnie
np. ściany komórkowe)
o Napięcie powierzchniowe (przyciąganie się cząsteczek na styku
fazy
wodnej i gazowej, jest większe w obrębie fazy wodnej niż gazowej
o Kapilarność (powierzchnie ścian komórkowych bezpośrednio
wystawione
na działanie powietrza np. ściany Komorek mezofilu liścia pozostają
wilgotne i nie wysychają).
WODA W ORGANIZMIE ROŚLINNYM PEŁNI WIELORAKIE FUNKCJE:
W komórkach jest rozpuszczalnikiem substancji biologicznie czynnych, stanowi
środowisko wielu reakcji chemicznych. Bierze bezpośredni udział w wielu
reakcjach chemicznych jako substrat (np. donor wodoru w fotosyntezie) lub jako
produkt reakcji (np. końcowy produkt oddychania).
Woda hydratacyjna odpowiada za strukturę makromolekuł (np. białek, kwasów
nukleinowych, lipidów błon) i decyduje o ich aktywności metabolicznej
Wypełniając wakuole podtrzymuje turgor komórek i całej rośliny. W wyniku zmiany
turgoru zachodzi wiele ruchów roślinnych w odpowiedzi na działanie niektórych
bodźców środowiskowych. Jest czynnikiem umożliwiającym wzrost szybki tzw.
elongacyjny komórek i tkanek. Bierze udział w przemieszczaniu się substancji w
organizmach roślinnych: związków mineralnych i niektórych metabolitów w
Strona 31

ksylemie oraz produktów asymilacji i substancji czynnych biologicznie we floemie.
Jest, więc czynnikiem umożliwiającym integrację procesów polegających w
różnych organach rośliny W niektórych sytuacjach pozwala obniżyć temperaturę
nadziemnych organów o parę stopni. Wszystkie te funkcje wody w roślinie
związane są z jej strukturą i właściwościami fizycznymi.
Akwaporyny roślinne
– charakterystyka, rola w komórce
Woda będąc podstawowym składnikiem wszystkich żywych organizmów,
musi być dostarczana do komórek w odpowiedniej ilości. Jednak woda w
transporcie do wnętrza komórki musi pokonywać barierę plazmolemmy
gdyż jej wnętrze jest hydrofobowe. Dobry i szybki transport wody
zapewniają akwaporyny - które odkryto w latach 90- tych. Są to integralne
białka błonowe, które tworzą kanał dla przepływu wody. Akwaporyny
umożliwiają przemieszczanie się w poprzek błony wyłącznie cząsteczek
wody.
Białka te:
-
Mają konserwatywną sekwencję aminokwasów
-
Ich masa wynosi 26-30 kDa. Ich łańcuch polipeptydowy przenika
sześciokrotnie prze błonę a końce N- i C- wystają po
cytoplazmatycznej stronie błony.
-
Światło poru kanału wodnego ma 0,15 nm – 0,2 nm
-
Duża wrażliwość na działanie soli rtęci
-
U roślin stwierdzono 2 rodzaje białek akwaporynowych:
1. W tonoplaście – γ-TIP – białka syntetyzowane konstytutywnie
przez cały okres życia rośliny
2. W plazmolemmie – RD28 – białka indukcyjne syntetyzowane
tylko w odpowiedzi na odwodnienie komórki.
Funkcja Akwaporyny:
-
Regulacja przepływu wody
-
Hydratacja ziaren pyłku
-
Pęcznienie i kiełkowanie nasion
Transpiracja- rodzaje, czynniki wpływające na
natężenie transpiracji
Transpiracja to wyprowadzanie wody przez żywe organizmy. Jest to
proces
fizjologiczny, czyli czynnie regulowany przez roślinę. Rozmiary transpiracji można
podawać w różnych jednostkach. Do najczęściej spotykanych należą
intensywność i współczynnik transpiracji. Intensywność wyrażamy w gramach
wyparowanej wody na jednostkę powierzchni liścia (1 dm3) i na jednostkę czasu
(1h). Zależy ona od gatunku rośliny, jej wieku oraz od czynników zewnętrznych.
Współczynnik transpiracji – jest ilość wyparowanej wody (wyrażona w
gramach)
na 1 gram przyrostu suchej masy roślin w okresie wegetacji. Wykazuje, więc
zależność pomiędzy wyparowaną wodą a wytworzoną w tym samym czasie masę
organiczną. Jest on, zatem miarą efektywności wykorzystywania wody. Zależy on
nie tylko od czynników, które wpływają na transpirację, lecz również od czynników,
które wpływają na wzrost roślin (pH gleby itp.)
W zwi
ą
zku z ró
ż norodn
ą
budow
ą
li ś cia i łodygi wyró
ż niamy kilka typów transpiracji:
•
Kutikularną
•
Szparkową
•
Przedchlinkową (perydermalną)
Transpiracja kutikularna jest to parowanie wprost z zewnętrznej powierzchni
liścia, czyli ze skórki zakrytej kutikulą. W skład kutikuli wchodzą: celuloza oraz
woski i
kutyna – wykształcona w postaci płytek ułożonych obok siebie lub nad sobą.
Kutikula jest wsadzie nieprzenikliwa dla gazów i wody, jednak wykazują pewną
ograniczoną zdolność pęcznienia głównie ze względu na hydrofilowe właściwości
celulozy. Napęczniała kutikula oddaje część wody do atmosfery w postaci pary i
wysysa jednocześnie nowe ilości wody z komórki skórki. Natężenie transpiracji
kutykularnej zależy przede wszystkim od grubości kutikuli. U roślin środowisk
wilgotnych mających cienką warstwę kutikuli transpiracja kutikularna nie ustępuje
szparkowej a czasem nawet ją przewyższa. U sukulentów i innych typów roślin
miejsc suchych transpiracja kutikularna praktycznie nie istnieje. Młode liście mają
stosunkowo wysoką transpirację, która w miarę ich starzenia się ulega
Strona 32

zmniejszeniu. Liście rosnące w pełnym świetle mają grubszą kutikulę a zatem
niższą transpirację kutikularną niż liście rosnące w cieniu.
Strona 33

Transpiracja perydermalną – parowanie wody z powierzchni przesyconej
suberyną. Transpiracja z powierzchni wewnętrznej liścia – tzn. z powierzchni
ściany komórkowej otaczającej przestwory międzykomórkowe. Przestwory
międzykomórkowe są zwykle prawie wysycane parą wodną. Ich RH wynosi prawie
100%. Jeśli RH jest stałe to bezwzględne stężenie pary wodne zwiększa się wraz
ze wzrostem temperatury.
W temperaturze 20º powietrze o RH = 100% zawiera prawie dwa razy więcej pary
wodnej niż w temperaturze 10º. Ogrzewanie liścia powoduje, więc wzrost ciśnienia
pary wodnej w liściu, a więc zwiększa się gradient prężności pary wodnej między
powierzchnią liścia a powietrzem. Czynnikiem, który ogrzewa powierzchnię liścia
jest promieniowanie słoneczne. Podwyższenie temperatury liścia umożliwia
transpirację (i zarazem przepływ wody przez roślinę) w warunkach dużej, nawet
100% wilgotności względnej atmosfery zewnętrznej.
Transpiracja szparkowa – dyfuzja przez szparki jest bardzo efektywnym
sposobem
wymiany gazowej w roślinie. Osiąga znacznie wyższą wartość, niż gdyby
odbywała się jedną dużą powierzchnią równą sumie powierzchni szparek. Jest to
spowodowane przez zjawisko zwane efektem brzeżnym dyfuzji, wyrażanym przez
prawo Stephana mówiące, że parowanie przez małe otwory nie jest
proporcjonalne do ich powierzchni, lecz średnicy. Dyfuzja jest, bowiem większa
przy brzegach otworu niż w jego środku. W środku otworu możliwe są dla wielu
cząsteczek tylko tory dyfuzyjne prostopadłe do powierzchni otworu natomiast na
jego brzegach cząsteczki mogą również dyfundować na boki, po torach ukośnych
do powierzchni. Stąd np. zgodnie z prawem Stephena dyfuzja przez dwa otwory
mniejsze jest taka sama jak przez otwór większy, którego średnica jest sumą
średnic otworów mniejszych, lecz powierzchnia znacznie większa. Toteż w liściu,
chociaż otwarte szparki zajmują przeciętnie 1% jego powierzchni, wyparowuje
przez nie 50% tej ilości wody, jaka wyparowałaby z powierzchni swobodnej równej
całej powierzchni liścia. Szparki są efektywnymi urządzeniami nie tylko dla dyfuzji
pary wodnej, lecz także do wymiany innych gazów, jak CO2 i O2 między rośliną a
środowiskiem. Reasumując przy zamkniętych szparkach dyfuzja gazów ulega
silnemu lub nawet całkowitemu ograniczeniu przy otwartych zaś jest bardzo
znaczna.Podczas parowania wody z powierzchni komórek otaczających
przestwory międzykomórkowe zachodzi najpierw do zmiany fazy wodnej
z płynnej w gazową i dopiero wówczas para wodna ucieka przez otwory aparatów
szparkowych. Z powierzchni rośliny woda przemieszcza się do przyległej warstwy
powietrza (warstwa graniczna) i dopiero stąd – do otwartego powietrza. Wiatr,
powodując wymianę powietrza, usuwa parę wodną z warstwy graniczne i
przyśpiesza parowanie.
CZYNNIKI ZEWNĘTRZNE WPŁYWAJĄCE NA NATĘŻENIE TRANSPIRACJI
Światło – czynnik inicjujący otwieranie się szparek i tym samy uruchamiający
proces
transpiracji szparkowej ok. 70% energii świetlnej ulega zmianie na energię cieplną
i
stymuluje transpirację, liście nasłonecznione transpirują lepiej niż ocienione.
Temperatura – wpływa na intensywność transpiracji, oddziałuje na stopień
otwierania się szparek i na proces parowania wody, dostarcza niezbędnej energii
do oderwania się cząsteczki wody z fazy ciekłej i przejście w fazę gazową.
Niedosyt wilgotności powietrza – czynnik warunkujący transpirację. Wzrostowi
suchości powietrza towarzyszy wzrost intensywności transpiracji. W powietrzu
wilgotnym transpiracja maleje a przy braku niedosytu wilgotności powietrza, ustaje.
Dostępność wody glebowej – warunkiem normalnego przebiegu transpiracji, dla
większości roślin optymalna wilgotność glebowa waha się od 60 do 80% gdy ilość
wody w glebie jest ograniczona następuje zahamowanie procesu transpiracji.
Ruch mas powietrza – zazwyczaj nad powierzchnią parującą się zwiększa.
Natężenie transpiracji się zwiększa w miarę wzrostu szybkości wiatru, najszybszy
wzrost transpiracji ma miejsce przy stosunkowo słabym wietrze.
Stężenie CO2 – wpływa pośrednio na transpirację, oddziałuje na stopień otwarcia
szparek, nadmierne stężenie powoduje zamykanie się szparek.
CZYNNIKI ROŚLINNE MAJĄCE WPŁYW NA TRANSPIRACJĘ
Opór dyfuzyjny warstwy granicznej – w dużym stopniu zależy od wielkości,
kształtu i właściwości powierzchni liścia. Dla małych liści (np. igieł roślin iglastych)
opór ten jest rzadko większy niż 1s · cm-1 natomiast dla wielkich liści (np. banana)
może osiągnąć 3s · cm-1 a nawet więcej. Gdy szybkość wiatru wynosi, co najmniej
ok. 2m · s-1 opór warstwy granicznej maleje i przestaje odgrywać większą rolę w
regulacji transpiracji.
Opór dyfuzji kutikuli – jest zazwyczaj duży, choć różny u różnych gatunków.
Zależy
od struktury, gęstości i liczby warstw kutyny i wosków występujących w ścianach
zewnętrznych epidermy a także od grubości kutikuli kiściach higromorficznych
opór
dyfuzyjny kutikuli wynosi 40-100 s · cm-1 natomiast w liściach igłach
charakteryzujących się dobrą ochroną przed transpiracją opór ten wynosi około
Strona 34

400 s · cm-1. w warunkach, których epiderma wysycha i kurczy się, następuje
zbliżenie warstw hydrofobowych, co może podwoić wartość tego oporu.
Opór dyfuzyjny szparek – zależy od stopnia rozwarcia aparatów szparkowych.
Minimalny opór dyfuzyjny szparek jest różna dla różnych gatunków i zależy od
takich
cech anatomicznych jak wydajność, struktura, usytuowanie i liczba aparatów
szparkowych na powierzchni. Wielkość tego oporu może decydować o zdolności
(pojemności) transpiracyjnej liścia.
Transpiracja wody przez aparaty szparkowe – mechanizmy:
Są 2 ale żaden nie działa oddzielnie.
1. Mechanizm glukozowy - fotosyntetyczny
* Niskie pH(ok. 5) spowodowane pobieraniem CO2 do komórek mezofilu i
akumulacja kwasu węglowego - intensywna fotosynteza - akumulacja skrobi
fotosyntetycznej - niedobór osmotycznie czynnej glukozy -spadek turgoru-
zamykanie aparatów szparkowych.
* Niedobór CO2 zużytego przez fotosyntezę - pH wzrasta do 7 – aktywacja
fosfatazy skrobiowej -przemiana skrobi asymilacyjnej do glukozy – wzrost
potencjału osmotycznego i turgoru - otwieranie aparatów szparkowych
2. Mechanizm jonowy (jony K+)
* Deficyt wody stymuluje syntezę kwasu abscysynowego1 (ABA) w liściach - ABA
zwiększa przepuszczalność błon komórek aparatów szparkowych dla jonów
potasowych, jony potasowe wypływają z komórki, spada turgor - zamykanie
aparatów szparkowych.
Żaden z tych mechanizmów nie działa niezależnie, a w cyklu dobowym następują
sprzężone zmiany ich intensywności. Szparki otwierają się na ogół na świetle, co
w warunkach dobrego zaopatrzenia rośliny w wodę i małego stężenia CO2 w
przestworach międzykomórkowych. Ciemność, niedostatek wody, zwiększone
stężenie CO2 w tkance
(w wyniku oddychania) powoduje zamykanie szparek. Jedynie rośliny CAM
otwierają szparki w nocy, gdy maleje transpiracja. Otwieranie się szparek
spowodowane jest wzrostem ciśnienia turgorowego w komórkach szparkowych, do
których wnika woda
a więc jest przykładem ruchu turgorowego. Pobieranie wody przez komórki
szparkowe spowodowane jest obniżeniem ich potencjału wody a skutek
nagromadzenia się w wakuoli jonów potasu i chloru (transportowanych z apoplastu
i/lub z sąsiednich komórek) oraz jabłczanu (powstającego w cytoplazmie).
Transport potasu do wakuoli zachodzi w wyniku aktywacji pompy elektrogenicznej.
Światło niebieskie absorbowane przez karotenoidy zeaksantynę, znajdującą się w
tylakoidach Gan chloroplastu,aktywuje H+ - ATP-azę w plazmolemmie komórek
szparkowych. H+-ATP-aza produkowana przez chloroplasty i mitochondria,
wytwarza gradient protonów przez błonę, co umożliwia transport K+ przez
specyficzne kanały potasowe i akumulację tego kationu w wakuoli. Podobne
znaczenie ma akumulacja w wakuoli innego anionu – jabłczanu. Jest on
syntetyzowany w cytoplazmie w wyniku przemian glukozy, pochodzącej z hydrolizy
skrobi.
Zamykanie się szparek jest wywołane zmniejszeniem turgoru w komórkach
szparkowych spowodowanym utratą wody do atmosfery (zamykanie
hydropasywne) lub reakcjami metabolicznymi (zamykanie hydroaktywne),
indukowanym przez otwieranie całego liścia i/lub zwiększoną podaż kwasu
abscysynowego(ABA). Reakcje te są w zasadzie odwrotne do procesów
powodujących otwieranie się szparki: na skutek depolaryzacji błony zostają
otwarte kanały jonowe dla potasu i zachodzi wypływ jonów potasu
z komórek szparkowych zgodnie z gradientem stężeń tego jonu, a jabłczan zostaje
wykorzystany w resyntezie skrobi w ciemności. Powolna synteza kwasu
abscysynowego zachodzi stale w komórkach mezofilu gdzie hormon ten gromadzi
się w stromie chloroplastów, gdyż na świetle pH stromy jest wyższe niż pH
cytozolu. Pod wpływem odwodnienia obniża się pH stromy, co prowadzi do
przemieszczenia się ABA
z chloroplastu do apoplastu, skąd hormon ten dociera do komórek szparkowych
(w stężeniu transpiracji). Ponadto zwiększa się szybkość syntezy ABA; zarówno
w komórkach liścia jak i w korzeniach. Z Komórek korzeni ABA przemieszcza się
do liści
w soku ksylemu oraz z prądem transpiracji. Kwas abscysynowy może powodować
zamykanie się szparek nawet wtedy, gdy nie wystąpiły jeszcze zmiany potencjału
wody
w komórkach liścia. Jest, więc przekaźnikiem informacji o pogarszaniu się
stosunków wodnych w komórkach.
Budowa anatomiczna liści roślin wyższych
jako wyraz pełnionych funkcji.
a ) Liść jest organem przystosowanym do fotosyntezy:
o - Blaszka liściowa jest spłaszczona, dzięki czemu ma dużą
powierzchnię w stosunku do objętości. Umożliwia to nie tylko
Strona 35

doskonałe wykorzystanie energii świetlnej padającej na liść, lecz
także zwiększa powierzchnię absorpcyjną dla CO2.
o - Skórka liścia jest zwykle przezroczysta a wiec nie hamuje dostępu
światła do mezofilu złożonego z jednej lub kilku warstw miękiszu
palisadowego (u światłolubnych ta warstwa jest grubsza) oraz z luźno
rozłożonych komórek miękiszu gąbczastego.
o - Elementy przewodzące liścia rozmieszczone w nerwach liścia
doprowadzają do komórek wodę i sole mineralne odprowadzają zaś
produkty wytwarzane w procesie fotosyntezy. Wiązki przewodzące w
liściu są bardzo duże.
b ) Li
ść
jako miejsce transpiracji:
o Woda paruje z całej powierzchni rośliny przeważa jednak parowanie z
powierzchni liści, ponieważ ich powierzchnia jest nieporównywalnie
większa w porównaniu z innymi częściami rośliny. Ale liść nie jest
organem służącym specjalnie do transpiracji, ponieważ jego główna
funkcja związana jest z fotosyntezą.
o Liść od zewnątrz osłonięty jest przez skórkę, która pokryta jest kutikulą
mało przepuszczalna dla gazów i wody. W skórce zwłaszcza w dolnej
znajdują się aparaty szparkowe, przez które odbywa się wymiana
gazów pomiędzy wnętrzem liścia a atmosferą, oraz zachodzi
transpiracja. (Transpiracja
to wyprowadzanie wody przez żywe
organizmy. Jest to proces fizjologiczny, czyli czynnie regulowany przez
roślinę).
o Wśród wewnętrznych tkanek liścia zwanych mezofilem lub miękiszem
zieleniowym wyróżnić można: miękisz palisadowy (od górnej strony
liścia) i miękisz gąbczasty od dolnej strony liścia. W miękiszu
zieleniowym znajdują się duże przestwory międzykomórkowe,
zajmujące nawet 30% objętości liścia. Są one większe w miękiszu
gąbczastym, ale występują również w miękiszu palisadowym. Nie
wszystkie komórki stykają się ze sobą bokami. Podobne przestwory
znajdują się również w łodygach i korzeniu tworząc ciągły system
przewietrzający, który magazynuje substancje gazowe. Umożliwia
wymianę gazów między komórką a atmosferą.
o W liściu można wyróżnić dwie powierzchnie parowania: zewnętrzną
(górna i dolna skórka pokryta warstwą kutikuli) oraz wewnętrzną
(komórki miękiszu gąbczastego i palisadowego które graniczą z
przestworami międzykomórkowymi).
o W komórkach mezofilu znajdują się duże ilości chloroplastów a w nich
barwnik chlorofil, który jest niezbędny w procesie fotosyntezy.
o Skórka liścia zawiera aparaty szparkowe, które regulują m.in. turgor
komórki. Aparaty szparkowe są niezbędnym elementem budowy roślin,
gdyż dzięki nim para wodna może dyfundować na zewnątrz w procesie
transpiracji szparkowej. A także mogą tą transpirację ograniczać (w
niesprzyjających warunkach). Przez szparki zachodzi również dyfuzja
CO2 i O2. Mogą one występować zarówno w dolnej jak i w górnej części
skórki. Gęstość rozmieszczenia zależy od gatunku rośliny (liść średniej
wielkości może mieć kilka milionów szparek). (Budowa aparatów
szparkowych: 2 komórki szparkowe, pomiędzy którymi znajduje się
otwór – szparka prowadząca do umieszczonej niżej komory szparkowej;
zawierają chloroplasty - mogą, więc wytwarzać związki organiczne w
przeciwieństwie do innych komórek epidermy).
BUDOWA I DZIAŁANIE APARATÓW
SZPARKOWYCH
Aparaty szparkowe są niezbędnym elementem budowy roślin, gdyż
dzięki nim para wodna może dyfundować na zewnątrz w procesie
transpiracji szparkowej. A także mogą tą transpirację ograniczać (w
niesprzyjających warunkach). Przez szparki zachodzi również dyfuzja CO
2
i
O
2
. Mogą one występować zarówno w dolnej jak i w górnej części skórki.
Gęstość rozmieszczenia zależy od gatunku rośliny (liść średniej wielkości
może mieć kilka milionów szparek).
ROZMIESZCZENIE APARATÓW SZPARKWYCH W LIŚCIACH
Liście hypostomatyczne – aparaty szparkowe wyłącznie w dolnej
epidermie (w większości roślin).
Liście amfistomatyczne – aparaty liściowe po obu stronach blaszki
liściowej
Liście epistomatyczne – aparaty szparkowe w górnej epidermie (u roślin
wodnych, których liście pływają po powierzchni wody).
BUDOWA APARATÓW SZPARKWOYCH
2 komórki szparkowe, pomiędzy którymi znajduje się otwór – szparka
prowadząca do umieszczonej niżej komory szparkowej. Zawierają
chloroplasty (mogą, więc wytwarzać związki organiczne w przeciwieństwie
do innych komórek epidermy).
RODZAJE APARATÓW SZPARKOWYCH
Strona 36
1. Typ gramineae – występuje u traw. Mają kształt hantli. Komórki
zamykające są wydłużone, przy czym partie środkowe są wąskie i silnie
zdrewniałe, podczas gdy ich końce są pęcherzykowato rozszerzone i
cienkościenne. Wzrost turgoru powoduje zwiększenie średnicy
pęcherzykowatych zakończeń, wskutek czego środkowe zdrewniałe partie
odchylają się od siebie, poszerzając w ten sposób otwór. Przy
zmniejszaniu turgoru zbliżają się one do siebie i szparka zamyka się.
Komórki szparkowe otoczone są innymi komórkami epidermy, określanymi
jako przyszparkowe, które wspomagają komórki przyszparkowe np. w
regulacji rozwarcia szparki. W pęcherzykowatych zakończeniach
mikrofibryle celulozowe ułożone są promieniście, dzięki czemu przy
wzroście turgoru zakończenia komórek szparkowych mogą zwiększyć
swoją średnicę, wskutek czego wąskie zdrewniałe partie odchylają się od
siebie, poszerzając w ten sposób otwór. W przypadku spadku turgoru
dzieje się odwrotnie.
2. Typ Amaryllis – występuje u dwuliściennych. Komórki szparkowe mają
kształt nerkowaty, ich ściany graniczące ze szparką są grubsze, ściany zaś
znajdujące się po przeciwnej stronie – cieńsze. Przy wzroście turgoru
ściany cienkie rozdymają się, wskutek czego kształt komórek staje się
bardziej wygięty i szparka powiększa się. W razie zmniejszenia turgoru –
przeciwnie – komórki szparkowe wyprostowują się i ich ściany schodzą się
razem zamykając szparkę
TURGOROWE MECHANIZMY DZIAŁANIA APARATÓW SZPARKOWYCH
1. Mechanizm glukozowy
•
Niskie pH spowodowane (ok. 5) spowodowane pobieraniem CO
2
do
komórek mezofilu i akumulacja kwasu węglowego
intensywna
fotosynteza
akumulacja skrobi fotosyntetycznej
niedobór
osmotycznie czynnej glukozy
spadek turgoru
zamykanie
aparatów szparkowych.
•
Niedobór CO
2
zużytego przez fotosyntezę
pH wzrasta do 7
aktywacja fosfatazy skrobiowej
przemiana skrobi asymilacyjnej do
glukozy
wzrost potencjału osmotycznego i turgoru
otwieranie
aparatów szparkowych
2. Mechanizm jonowy (jony K
+
)
Deficyt wody stymuluje syntezę
kwasu abscysynowego
1
(ABA) w liściach
ABA zwiększa
przepuszczalność błon komórek aparatów szparkowych dla jonów
potasowych, jony potasowe wypływają z komórki, spada turgor
zamykanie aparatów szparkowych.
Ż
aden z tych mechanizmów nie działa niezale
ż nie, a w cyklu dobowym
nast
ę
puj
ą
sprz
ęż
one zmiany ich intensywności.
Światło
Podwyższona temperatura
Dodatni bilans wodny
Deficyt prężności pary w powietrzu
Niskie stężenie CO2 w komórkach mezofilu liści
Ujemny bilans wodny
Wysoka prężność pary wodnej w powietrzu
Podwyższona temperatura
Siła ssąca transpiracji, a parcie korzeniowe.
Siła ssąca transpiracji polega na podciąganiu wody w górę rośliny
przez całą długośc ksylemu. Ssanie to następuje gdy w liściach zaczyna
brakowac wody z powodu wyparowywania. Cząsteczki wody silnie się
przyciągają, więc gdy jedna zaczyna się poruszac, ciągnie za sobą kolejne
cząsteczki – jest to zjawisko kohezji.
Parcie korzeniowe jest to fizjologiczne zjawisko u roślin polegające na
tłoczeniu wody przez korzenie do łodyg i liści. Jest ono procesem
zużywającym energię metaboliczną, związanym z aktywnym transportem
jonów. Parcie korzeniowe widoczne jest szczególnie u drzew na wiosnę,
umożliwia ono wtedy transport wody i substancji odżywczych do
rozwijających się pąków liściowych. Po tym czasie nie odgrywa ono
większej roli, przejmuje ją działanie siły ssącej transpiracji.
Parcie korzeniowe można zaobserwowac uszkadzając roślinę. Przez
pewien czas z miejsca nacięcia wydziela się sok (sok płaczu). Skutkiem
parcia korzeniowego jest również gutacja – wydzielanie się kropli płynu na
Strona 37
brzegach liści, gdy roślina znajduje się w atmosferze dobrze wysyconej
para wodną.
Gutacja i płacz roślin wywołane są aktywnym pobieraniem wody przez
korzenie.
Budowa i rola tkanek przewodzących u roślin
wyższych.
Tkanka przewodząca – tkanka roślinna, w której odbywa się transport
wody wraz z rozpuszczonymi w niej substancjami do wszystkich części
roślin, zbudowana jest z niejednorodnych komórek.
Dzieli się ją na:
(drewno), przewodzący wodę i rozpuszczone w
niej sole mineralne z korzeni do innych części rośliny. W funkcji tej
wyspecjalizowały się dwa rodzaje elementów drewna:
(tracheidy), charakterystyczne dla paprotników i roślin
nagonasiennych, i
okrytonasiennych.
U roślin wyższych występują naczynia:
o
protoksylem - składa się z naczyń o umocnieniach
pierścieniowych i spiralnych;
o
metaksylem - (drabinkowate) 90% transportu wody (jeśli
roślina nie ma przyrostu wtórnego)
o
ksylem wtórny - mają ściany jajkowate (w roślinie, która
posiada przyrost wtórny)
(łyko), przewodzący rozpuszczone produkty asymilacji
z liści w głąb rośliny, zbudowany z bezjądrowych komórek sitowych
tworzących
(sitowe elementy roślin), a także z komórek
i włókien wzmacniających. U roślin okrytonasiennych
występują ponadto wyspecjalizowane tzw.
pełniące rolę pomocniczą w przewodzeniu substancji pokarmowych
przez rurki sitowe.
U roślin wyróżnia się dwie tkanki przewodzące: drewno (ksylem) i łyko
(floem).
Ksylem (drewno) zbudowany jest z naczyń i cewek oraz komórek
wzmacniających.
Naczynia to martwe, zdrewniałe, pozbawione ścian poprzecznych. Komórki
ustawione w pionowe szeregi, tworzą rury. Tworzą mikrokapilarne kanały,
mają zgrubienia na ścianach oraz liczne jamki. Cewki przylegają do
naczyń, są żywe, znacznie węższe i mają wiele jąder. Dzięki jamkom w
ścianach pobierają wodę i przekazują ją do komórek miękiszowych na
drodze osmotycznej. Naczynia służą do dalekiego transportu wody i soli
mineralnych a cewki do krótkiego. Rośliny starsze filogenetycznie
(nagozalążkowe) mają tylko cewki.
Floem i ksylem współpracują w transporcie soli mineralnych,
regulatorów wzrostu i innych substancji.
Ksylem:
Przewodzi wodę, zw. nieorganiczne (~30%), + aminokwasy, amidy,
aminy, trochę cukrów, kwasy, hormony (np. stresowe)
woda: korzeń → pęd (ogólnie: reszta rośliny)
brak protoplastu – komórki są martwe
nierównomiernie zgrubiała ściana wzmocniona ligniną
cewki (tracheidy): wydłużone, wrzecionowate woda przemieszcza
się między komórkami przez jamki w zdrewniałych ścianach
komórkowych
naczynia (tracheje): szereg komórek („stos”)
uszkodzenie ksylemu jest śmiertelne
transport pod ujemnym ciśnieniem (transpiracja)
Strona 38
ŁYKO (FLOEM) W skład łyka wchodzi kilka typów komórek: sitowe,
towarzyszące, miękiszowe i wzmacniające. Komórki sitowe po raz
pierwszy opisał Hartig 1838. Są to żywe wydłużone komórki o
perforowanych (dziurkowanych) ścianach poprzecznych. Charakteryzują
się brakiem jąder, chloroplastów i innych struktur występujących w
komórkach towarzyszących. Komórki ułożone są w ciągi i kontaktują się ze
sobą przez połączenia plazmatyczne, o umożliwia swobodny przepływ
soku. W komórkach występuje wysokie ciśnienie turgorowe i wysokie
stężenie soku. Sita w komórkach stresowych zamykają się – kumuluje się
ksyloz.
Łyko odgrywa najważniejszą rolę w długodystansowym transporcie
asymilatów od
miejsca ich produkcji – liści do miejsca zużycia – korzeń, tkanek
merystematycznych i owoców. Przewodzi sacharozę i aminokwasy.
Floem (łyko):
Przewodzi roztwory (cukry, poliole, kwasy: jabł. i cytr., hormony,
jony, polimery – nie polisacharydy)
donory – miejsca [produkcji | magazynowania] → akceptory –
miejsca [zużywania | magazynowania] → pęd
żywe komórki (ale nie mają jąder, rybosomów ani tonoplastu)
komórki sitowe – są zakończone sitami (Φ sit – od ułamków μm do
kilkunastu μm, sita zajmują do 50% powierzchni ściany)
wnętrze wyścielone kalozą (funkcja LEPISZCZA) – zmniejsza
światło otworów, żeby zmniejszyć transport (np. przed zimą)
białko floemowe (P-protein) – zakleja uszkodzenia, pełni funkcję
transportową
roztwór we floemie bardziej stężony (gł. sacharoza) i alkaliczny niż
w ksylemie
komórki towarzyszące są połączone z sitowymi plazmodesmami
(plazmodesmy nie służą tu do transportu masowego)
uszkodzenie floemu nie musi być śmiertelne
Transport we floemie – cechy:
dwukierunkowy
różna prędkość różnych składników
pod dodatnim ciśnieniem (odwrotnie niż w ksylemie
Meatloporfiryny roślinne – budowa, znaczenie w
metabolizmie
metaloporfiryny, pochodne porfiryn; zawierają atom metalu (żelazo,
miedź, magnez), centralnie wbudowane w układ porfirynowy za
pośrednictwem atomów azotu; np. hem, heminy, chlorofil.
Cząsteczka każdego chlorofilu zbudowana jest z pochodnej porfiryny
określanej feoporofiryną. Feoporofiryna to pięciopierścieniowa porfiryna z
różnymi podstawnikami. Cztery z pierścieni to pierścienie pirolowe, a piąty
pierścień tworzą same atomy węgla. Wiązania pomiędzy atomami
Strona 39

tworzącymi pierścienie to następujące po sobie wiązania pojedyncze i
podwójne składające się na układ wiązań sprzężonych. Centralne miejsce
w układzie porfiryny zajmuje atom magnezu łączący się z atomami azotu
każdego z pierścieni. U większości chlorofili (poza chlorofilami c)
feoporfiryna łączy się poprzez wiązanie estrowe z alkoholem o 20 atomach
węgla – fitolem. Porfiryna tworząca kompleks z magnezem posiada
zdolność do absorpcji promieniowania elektromagnetycznego w zakresie
widzialnym.
Dzięki chlorofilom możliwy jest proces fotosyntezy, która jest jednym z
podstawowych procesów biologicznych. Warunkuje ona życie na Ziemi,
dzięki niemu możliwa jest przemiana materii nieorganicznej w organiczną.
Związki organiczne, które zostają wytworzone w trakcie tego procesu są
czynnikiem budującym oraz pokarmowym. Poprzez proces wiązania
dwutlenku węgla i uwalnianie tlenu możliwe jest zachowanie stabilnej
sytuacji gazowej.
Strona 40
GOSPODARKA MINERALNA :
Strategie pobierania Fe przez rośliny wyższe
Rośliny mogą pobierać Fe w postaci:
- jonu żelazawego (Fe2+)
- jonu żelazowego (Fe3+)
- związków chelatowych
Wyróżnia się obecnie dwie strategie pobierania Fe.
Strategia I: polega na redukcji Fe3+ do Fe2+ przed pobraniem do
wnętrza komórek korzenia. Jest ona charakterystyczna dla roślin
dwuliściennych i jednoliściennych oprócz traw. Obejmuje przystosowania
morfologiczne (zwiększone wytwarzanie korzeni bocznych i
wyróżnicowanie specjalnych komórek transferowych) oraz fizjologiczne,
polegające na wytworzeniu trzystopniowego procesu pobierania Fe, a
obejmujące wydzielanie protonów, kwasów organicznych i związków
fenolowych do podłoża. Powodowane w ten sposób zakwaszenie prowadzi
do uwolnienia Fe3+ z cząstek glebowych, a chelatowanie ułatwia
utrzymanie go w roztworze. Drugim etapem jest tu redukcja przez
reduktazy błonowe, których aktywność w warunkach deficytu Fe wzrasta
kilkakrotnie. Rośliny wykorzystujące tę strategię pobierania Fe redukują
zarówno Fe3+ jonowe, jak i związane w chylaty wydzielane przez korzenie.
Niektóre rośliny tej strategii wydzielają do podłoża – po obniżeniu jego pH
poniżej 4,5 – związki redukujące Fe3+ do Fe2+ w roztworze glebowym.
Ostatnim etapem jest przeniesienie zredukowanego Fe przez błonę
komórkową do wnętrza korzenia.
Strategia II
to przenoszenie przez błonę komórkową
schelatowanego Fe 3+ i jego redukcja wewnątrz komórek korzenia.
Strategia ta jest charakterystyczna tylko dla traw. Wykorzystywane są tu
specyficzne związki chelatujące, zwane fitosideroforami. Rośliny tej
strategii są mniej wrażliwe na deficyt Fe niż rośliny strategii I
Symbioza –definicja, przykłady, znaczenie w świecie roślin
wyższych
Symbioza - zjawisko ścisłego współżycia przynajmniej dwóch gatunków,
które przynosi korzyść każdej ze stron (mutualizm) lub jednej, a drugiej nie
szkodzi (komensalizm). Powszechnie spotykanym rodzajem symbiozy jest
mikoryza - współżycie korzeni roślin i grzybów, gdzie grzyb wspomaga
pobieranie wody i soli mineralnych stanowiąc "przedłużenie" systemu
korzeniowego rośliny, a sam pobiera substancje odżywcze z korzenia
powstające w drodze fotosyntezy.
U niektórych gatunków, np. storczykowatych i wrzosowatych, symbioza
mikorytyczna jest bardzo ścisła. Grzyby rozkładające celulozę i pektyny
umożliwiają storczykom kiełkowanie nasion i wzrost na martwym podłożu
organicznym, np. próchniejącym drewnie.
Mikoryzę dzielimy na ektotroficzną i endotroficzną w zależności od
rozmieszczenia nitek grzybni w układzie grzyb - roślina. Mikoryza
ektotroficzna występuje na krótkich korzeniach wielu gatunków roślin
dwuliściennych (Pinaceae, Betulaceae, Fagaceae, Rosaceae). Korzenie
nie mają wówczas włośników i często są pozbawione czapeczki. Grzybnia
występuje głównie na powierzchni korzeni, tworząc gęstą sieć splątanych
nitek, zwanych płaszczem lub siatką Hartiga. W przypadku mikoryzy
endotroficznej grzybnia wnika do wnętrz komórek korzenia i ma znacznie
mniejszą masę w porównaniu z grzybnią ektomikorytyczną. Ten rodzaj
mikoryzy występuje powszechnie u wielu drzew oraz licznych gatunków
roślin zielnych, np. lucerny.
Grzyby mikorytyczne syntetyzują hormony typu auksyn, giberelin i
cytokinin, które wydzielają do komórek gospodarza oraz antybiotyki
przenikające do środowiska i zmniejszające w ryzosferze liczebność
patogenów. Zwarty płaszcz grzybni w przypadku mikoryzy egzotroficznej
mechanicznie utrudnia wnikanie różnych patogenów do korzenni.
Strona 41
Rośliny mikorytyczne są na ogół odporniejsze na niektóre warunki
stresowe: skrajne temperatury gleby, niekorzystne pH lub na obecność
substancji toksycznych.
Mikoryza jako szczególny przykład symbiozy.
Mikoryza to rodzaj symbiozy korzeni drzew z grzybami w której obaj partnerzy
czerpią pewne korzyści. Grzybom mikoryza ułatwia zaopatrzenie w organiczne
substancje odżywcze (produkty fotosyntezy) wytwarzane przez rośliny w zamian
za przekazywane im związki mineralne Np. fosforowe lub azotowe często
występujące w podłożu w formie trudno dostępnej dla roślin. Grzyby
ułatwiają również pobieranie cynku i miedzi. Dla korzeni związek ze strzępkami
grzybni oznacza zwiększenie powierzchni chłonnej, co ułatwia pobieranie wody i
jonów. Grzyb rozkładając próchnicę glebową tworzy w otoczeniu korzenia strefę
bogatą w proste związki odżywcze. Prócz tego, grzyby wytwarzają substancje
witaminowe i hormonalne, pobudzające wzrost i przemianę materii komórek
korzenia. Grzyby syntetyzują hormony typu auksyn, giberelin i cytokinin, które
wydzielają do komórek gospodarza oraz antybiotyki przenikające do środowiska i
zmniejszające w ryzosferze ilość patogenów. Płaszcz grzybni utrudnia wnikanie
różnych patogenów do korzeni niestety nie chroni rośliny przed nicieniami i
infekcjami wirusowymi. Rośliny mikorytyczne są odporniejsze na niekorzystne
warunki: nieoptymalna temperaturę gleby, niekorzystne ph lub na obecność
substancji toksycznych.
Rozróżnia się dwa podstawowe rodzaje mikoryzy: zewnętrzną
(ektotroficzną) i wewnętrzną (endotroficzną):
o
W mikoryzie zewnętrznej strzępki grzyba oplatają krótkie korzenie
boczne, tworząc gęstą sieć splatanych nitek zwanych płaszczem lub siatką
Hartiga. Strzępki wnikają także do kory pierwotnej, ale rozrastają się tylko w
przestworach międzykomórkowych i nie wnikają do wnętrza komórek. Wzrost
korzenia na długość zostaje zahamowany, ale tworzy za to charakterystyczne
rozgałęzienia. Włośniki zanikają, a ich funkcje przejmują strzępki grzyba. Korzenie
często są pozbawione czapeczki. Mikoryza zewnętrzna jest charakterystyczna dla
wielu drzew i dla wielu z nich stanowi czynnik niezbędny do normalnego rozwoju.
o
W mikoryzie wewnętrznej strzępki grzyba nie tworzą płaszcza dlatego
włośniki na korzeniach zostają zachowane. Strzępki grzyba nie ograniczają się do
przestworów międzykomórkowych lecz wnikają do wnętrza komórek. Mikoryza
endotroficzna występuje u niektórych drzew i wielu roślin zielnych, m.in. u roślin
zbożowych.
U niektórych gatunków np. storczykowatych symbioza mikorytyczna jest bardzo
ścisła. Grzyby rozkładające celulozę i pektyny umożliwiają storczykom kiełkowanie
i wzrost na martwym podłożu organicznym np. próchniejącym drewnie.
Istnieje tez forma pośrednia pomiędzy ekto i endomikoryzą, w której występuje
dobrze rozwinięta grzybnia zewnętrzna, równocześnie strzępki wrastają do
wnętrza komórek korzenia.
Wykorzystywanie nieorganicznych form azotu
przez rośliny wyższe.
W glebie zachodzą liczne procesy umożliwiające roślinom pobieranie azotu w
odpowiedniej dla nich formie. Są to procesy nitryfikacji, mineralizacji,
immobilizacji .
Rośliny pobierają azot przez system korzeniowy głównie w formie amonowej
(NH4+) oraz azotanowej (NO3-). Minimalne ilości mogą być pobierane w postaci
jonu NO2- , lecz w większych ilościach jest on toksyczny dla rośliny. Forma
azotanowa i amonowa są równorzędne w żywieni rośliny a to jaką formę pobiorą
zależy od wielu czynników tj. od gatunku rośliny, jej stanu fizjologicznego, formy
azotu w nawozach. Duży wpływ na pobieraną formę ma także pH gleby. W
warunkach zbliżonych do pH obojętnego lepszy jest azot w formie amonowej. Im
wyższe pH tzn. im gleba jest kwaśniejsza tym zwiększa się pobieranie azotu w
formie azotanowej. Pobrany w ten sposób azot jest włączany w strukturę
roślinnych związków organicznych i bezpośrednio wykorzystywany w roślinie. W
roślinie azot występuje głównie w postaci związków organicznych, tylko niewielkie
jego części występują w formie mineralnej (NH4+ , NO3-). Produktami syntezy
azotu mineralnego pobieranego przez rośliny są organiczne związki azotowe.
Zalicza się do nich: aminokwasy, białka, peptydy, amidy, kwasy nukleinowe i
nukleotydy, związki wchodzące w skład chlorofilu, witamin i wiele innych. Bez
wątpienia najważniejszą grupą związków azotowych są białka. To one stanowią
budulec dla innych związków i substancji. Znaczne ilości azotu znajdują się w
białkach zapasowych w nasionach i ziarniakach zbóż (zawartość azotu w nich
może dochodzić do 8-15% suchej masy, a u niektórych gatunków nawet do 50%).
Białka pełnią wiele ważnych funkcji gdyż są odpowiedzialne za przeprowadzanie i
regulowanie prawie wszystkich procesów biochemicznych zachodzących w
roślinie. Związki azotowe są także niezastąpione w procesie fotosyntezy,
najważniejszego procesu w roślinie. Inną ważną grupą związków azotowych są
nukleotydy i kwasy nukleinowe. Stanowią one materiał genetyczny wszystkich
organizmów żywych. Azot wchodzi w skład białek, które następnie wchodzą w
Strona 42
skład łańcuchów budujących DNA i RNA. Azot bierze udział w stymulowaniu
syntezy i obiegu regulatorów wzrostu i rozwoju roślin tj. auksyn, giberelin i kwasu
abscysynowego. Także niektóre alkaloidy i naturalne substancje ochronne w
roślinie syntetyzowane są przy pomocy azotu.
Nikotianamina
– rola w pobieraniu i transporcie floemowym
żelaza.
Nikotianamina to niebiałkowy aminokwas , występujący w roślinach
obydwu strategii pobierania żelaza( strategia I- proces polegający na
redukcji żelaza (III) do żelaza (II) przed pobraniem do wnętrza komórek
korzenia, charakterystyczny dla roślin dwuliściennych i jednoliściennych,
oprócz traw, natomiast strategia II – to proces przenoszenia przez błonę
komórkową schelatowanego żelaza (III) i jego redukcji wewnątrz komórek
korzenia, charakterystyczny dla traw).
Nikotianamina u roślin strategii I pełni funkcje związku chelatującego
dwuwartościowe jony metali i chelatuje Fe2+ transportowane zarówno w
ksylemie jak i floemie, oraz reguluje metabolizm Fe w roślinie poprzez
regulację dostępności tego pierwiastka . Istotną rola nikotianaminy w
metabolizmie roślin strategii I potwierdziły badania Herbik i in., w których
wykazano, iż mutant Lycopersicon esculentum Mill. Nie zawierający
nikotianaminy jest fenotypowo rośliną chlorotyczną, wykazującą objawy
ostrego deficytu Fe pomimo akumulacji Fe w liściach.
Nitryfikacja i denitryfikacja – udział w obiegu
azotu.
Azot w przyrodzie występuje w solach mineralnych. Bardzo ważne
jest występowanie azotu w organizmach żywych w postaci białek.
Zdecydowanie najwięcej, bo aż 78% azotu ma powietrze. Obieg azotu w
przyrodzie opiera się na pięciu podstawowych procesach: pobieraniu
nieorganicznych związków z podłoża, rozkładzie martwych szczątków
organicznych z uwolnieniem amoniaku, wiązaniu azotu cząsteczkowego,
nitryfikacji i denitryfikacji.
W krążeniu azotu w przyrodzie biorą udział bakterie. Bakterie gnilne
rozkładają obumarłe szczątki roślin i zwierząt. Powstaje wtedy amoniak
(NH3).
W przyrodzie żyją bakterie, które mogą pobierać azot z powietrza. Są nimi
bakterie tlenowe z rodzaju Azotobakter i beztlenowe z rodzaju Clostridium.
Bakterie z rodzaju Rhizobium żyją w symbiozie z korzeniami roślin
motylkowych i mogą przetwarzać azot atmosferyczny na aminokwasy oraz
białka.
Znajdujące się w glebie sole azotowe, które pobierają rośliny i obracają na
budowę cząsteczek białka, stanowią podstawowy element ciała roślin i
zwierząt.
Powstają sole azotowe w wyniku utleniania amoniaku i jego związków
przez bakterie nitryfikacyjne na tlenki azotu, które z innymi związkami
mineralnymi tworzą znów azotowe związki glebowe. Nazwa „nitryfikatory”
pochodzi od łacińskich słów „nitrum”, czyli soda i „facio”, czyli czynię.
Nitryfikacja jest procesem realizowanym głównie przez bakterie
Nitrosomonas i Nitrobacter. Są to mikroorganizmy, które jako budulec
własnego ciała wykorzystują podobnie jak rośliny proste związki
nieorganiczne: wodę i dwutlenek węgla. Niezbędną do życia energię
uzyskują natomiast w wyniku chemicznej reakcji utleniania azotu
amonowego do azotynów, a następnie azotynów do azotanów.
W uproszczeniu bakterie Nitrosomonas przeprowadzają reakcję:
NH
4
+
+ 1,5 O
2
-> NO
2
-
+ 2H
+
+ H
2
O + 352 kJ
zaś bakterie Nitrobacter:
NO
2
- + 0,5 O
2
-> NO
3
-
+ 73kJ
W wyniku działalności tych pożytecznych mikroorganizmów następuje
przekształcenie stosunkowo toksycznego azotu amonowego (NH4+ i NH3)
w znacznie mniej szkodliwy azot azotanowy (NO3-). Drugi etap nitryfikacji
przeprowadzany przez Nitrobacter przebiega znacznie szybciej i cały
wytworzony azot azotanowy (NO2-) jest praktycznie natychmiast
przetwarzany. Bakterie nitryfikacyjne bytują głównie w glebie, wzbogacając
ją w azotany, najchętniej wykorzystywaną przez rośliny formę azotu. Zbyt
intensywna nitryfikacja nie jest pożądana, gdyż azotany są znacznie łatwiej
Strona 43

wypłukiwane z gleby niż jony amonowe.
Inaczej mówiąc, bakterie nitryfikacyjne utleniają amoniak wytwarzany
podczas procesów gnilnych (w rozkładzie białek). Są bardzo ważnym
czynnikiem obiegu związków azotowych w przyrodzie. Azotany stanowią
źródło pokarmu azotowego dla roślin wyższych.
Warunki nitryfikacji autotroficznej:
•
pH od 5,5 do 9 (optymalne 7,5)
•
zawartość tlenu rozpuszczonego minimum 2mgO2/dm3 oraz
teoretycznie 4mgO2/mgNH4+
•
obecność mikroelementów Ca, Fe, Cu, Mg, P
•
gazowy NH3 poniżej 1mg/dm3 (jest toksyczny dla nitryfikatorów)
•
brak innych toksycznych związków (fenoli, antybiotyków itp.)
•
obecność CO2 lub węglanów jako źródła węgla dla autotrofów
•
neutralizacja powstającego kwasu azotowego (III) który hamuje
obie fazy nitryfikacji, można to zrobić przez dodatek kredy.
Azotany mogą być bezpośrednio wykorzystywane jako źródło azotu przez rośliny,
mogą gromadzić się w glebie (np. złoża saletry chilijskiej) lub ulegać rozkładowi
przez bakterie denitryfikacyjne. Denitryfikacja lub oddychanie azotanowe zachodzi
przede wszystkim wtedy, kiedy stworzone są warunki beztlenowe, czyli takie, w
których tlen nie występuje w formie cząsteczkowej (O2), ale jest obecny w formie
związanej chemicznie np. w postaci azotanów (NO3-). W takiej sytuacji bakterie
nie mogą używać do oddychania tlenu cząsteczkowego i muszą wykorzystywać
ten związany chemicznie. Następuje wykorzystanie tlenu zawartego w azotanach
w myśl uproszczonej reakcji:
NO
3
-
+ 0,5 H
2
O -> 0,5 N
2
+ 2,5 O + OH
-
W wyniku aktywności życiowej mikroorganizmów następuje przekształcenie azotu
azotanowego w formę cząsteczkową N2, który jest gazem i ulatnia się z wody w
powietrze. Liczne denitryfikatory żyją w glebie i wodzie, przyczyniając się do
lokalnych strat azotu glebowego, zwłaszcza w glebach słabo przewietrzanych.
Przykładem bakterii denitryfikujących , żyjących w wodzie to bakterie
Pseudomonas fluorescens.
Znaczenie denitryfikacji:
•
zmniejszenie ilości przyswajalnego azotu,
•
usuwa nadmiar NO
i NO
•
zamyka obieg azotu.
Bezsprzecznie rola bakterii nitryfikacyjnych i denitryfikacyjnych jest bardzo
duża. Bez ich obecności niemożliwy byłby prawidłowy obieg azotu w
przyrodzie. Spowodowałoby to zaburzenie cykli biogeochemicznych i
równocześnie nastąpiłoby całkowite zachwianie równowagi w środowisku
naturalnym.
Makro- i mikroelementy
- znaczenie składników mineralnych dla roślin.
W roślinach oprócz wody i związków organicznych występują związki
mineralne, które po spaleniu pozostają jako popiół. Zawiera on pierwiastki
pobrane z podłoża oprócz azotu i części siarki, które w czasie spalania
utleniają się do tlenków i ulatniają do atmosfery. Procentowy skład
poszczególnych pierwiastków może wahać się w szerokich granicach.
Zależy on często od gatunku rośliny, jej organu, wieku lub okresu rozwoju.
Może również zależeć od zasobności gleby w składniki mineralne oraz od
ich dostępności dla rośliny. Jednocześnie skład pierwiastków w suchej
masie niezależnie od gatunku jest stały pod względem jakościowym.
Oznacza to, że spośród głównych pierwiastków zwykle te same występują
u wszystkich gatunków roślin, a różnice dotyczą zmian ilościowych.
Wszystkie niezbędne dla roślin pierwiastki dzieli się na dwie grupy:
makroelementy i mikroelementy.
Makroelementy- pierwiastki występujące w roślinach w ilości powyżej
0.1% suchej masy(K, Ca, Mg, P, S, N)
Mikroelementy – pierwiastki występujące w bardzo małych ilościach,
niezbędne dla roślin w stężeniach 100 – 1000 razy mniejszych niż
makroelementy. (Fe, Cu, Co, Cl, Mo, Mn, Zn, Ni, B)
Strona 44
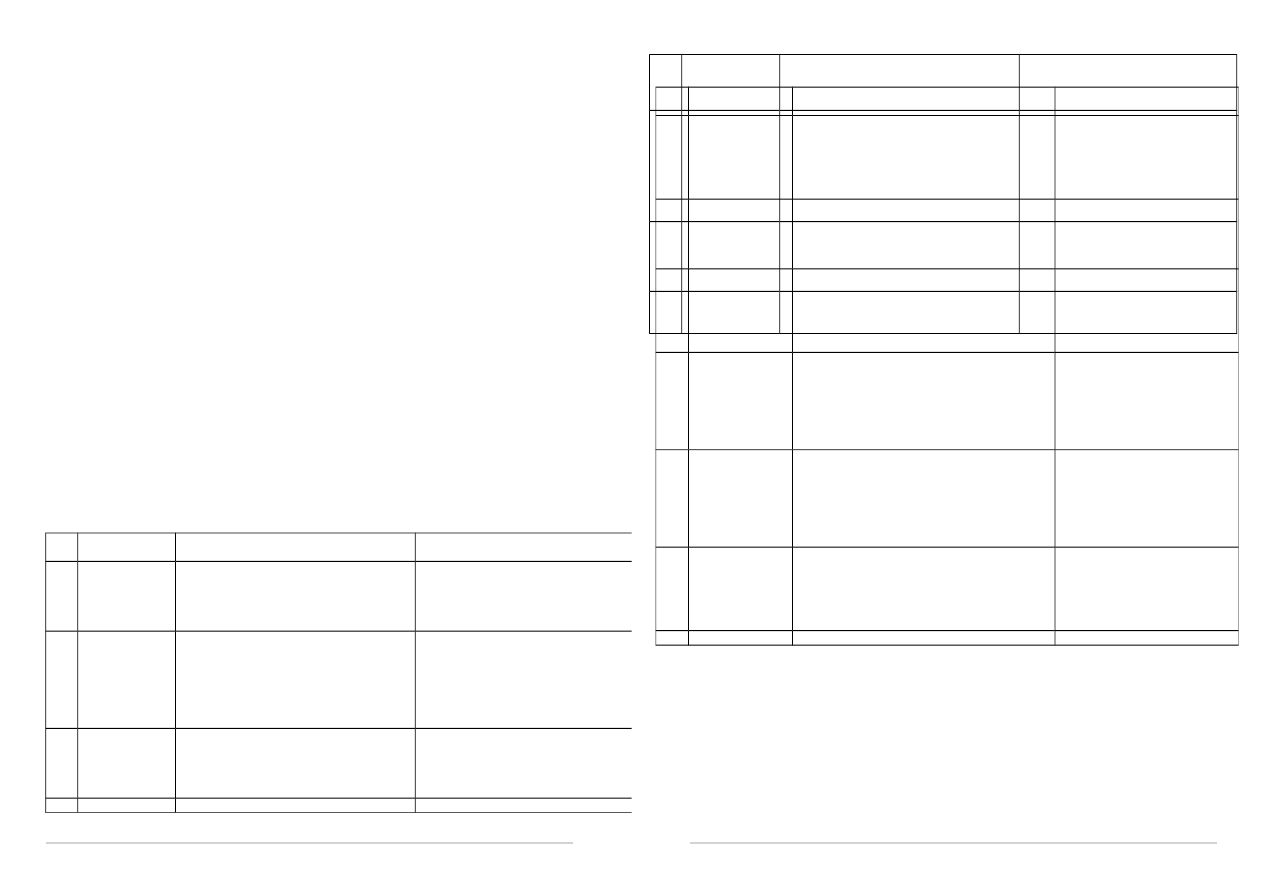
W roślinach występują również pierwiastki które nie są niezbędne,
ale ich obecność może wywierać korzystny wpływ na przebieg procesów
życiowych. Są to pierwiastki korzystne dla roślin.
Na- może zastępować u większości roślin funkcje potasu.
Si- zmniejsza parowanie wody z powierzchni liści oraz zawartość fosforu.
Co- uczestniczy w procesie wiązania azotu atmosferycznego przez
Rhizobium.
Al- dla większości roślin jest pierwiastkiem niekorzystnym, w przypadku
dużych ilości manganu lub miedzi w podłożu chroni rośliny przed ich
toksycznym działaniem.
Pierwiastki organogeniczne- trzy zasadnicze pierwiastki, które
wchodzą w skład wszystkich roślin: węgiel, wodór i tlen, pobierane w
formie gazowej jako CO
2
O
2
i H
2
0
Zróżnicowanie zawartości mikro i makroelementów waha się w bardzo
szerokich granicach. Różnice te wynikają między innymi z występowania
tych organizmów na różnych podłożach.
Kationy jednowartościowe pobierane są tym szybciej im większy jest ich
promień, a mniejsza otoczka hydratacyjna: Cs+ > Rb+ > K+ > Na+ > Li+.
Kationy jednowartościowe pobierane są szybciej niż dwuwartościowe i
trójwartościowe.
Funkcja i objawy niedoboru makroelementów.
Forma
pobierania
Funkcja
Objawy niedoboru
N
NO3
-
NH4+
mocznik
Składnik:aminokwasów,
amidów, białek, kwasów
nukleinowych, nukleotydów,
koenzymów, chlorofilu,
cytokinin.
Hamowanie wzrostu,
szczególnie liści małe
krzewienie, chloroza liści
starszych
P
H2PO4
-
HPO4
2-
Składnik: kwasów
nukleinowych, nukleotydów,
koenzymów, fosfolipidów. Występuje
jako Pi (wykorzystywany w reakcjach
syntezy ATP) i PPi (nośnik energii),
kluczowa rola w transporcie związków
org.
Zahamowanie wzrostu, liście
ciemnozielone, często od
dolnej strony fioletowo
purpurowe (np. pomidory)
S
SO4
2-
Składnik: cystyny, cysteiny,
metioniny, białek, sulfolipidów,
różnych koenzymów. Występuje w
związkach smakowych i zapachowych
chrzanu, cebuli i czosnku.
Chloroza całych liści, żyłki
czerwonawe. Czasem brak
turgoru liści. Objawy zbliżone
do braku azotu.
K
K
+
Występuje w postaci jonowej,
Plamy chloretyczne i nekrotyczne na
aktywator ponad 50 enzymów.
Uczestniczy w osmoregulacji
(np. aparatu szparkowego) i w
równowadze jonowej.
liściach starszych (dolnych).
Zahamowany wzrost organów
spichrzowych.
Ca
Ca
2+
Chelaty
Kofaktor enzymów np. fosfolipazy,
amylazy, ATP-azy, stabilizator kilku
receptorów, składnik pektyn i ściany
komórkowej. Stabilizator błon
komórkowych. Wtórny przekaźnik
informacji w regulacji metabolizmu.
Zahamowanie wzrostu. Zamieranie
wierzchołków pędu, śluzowacenie
korzeni, nietypowe chlorozy.
Deformacja liści. Zasychanie
wierzchołków liści, szczególnie
kapustnych, sucha zgnilizna
owoców,: pomidora i papryk, gorzka
plamistość jabłek.
M
g
Mg
2+
Składnik chlorofilu, aktywator wielu
enzymów, głównie uczestniczących w
przenoszeniu reszt fosforanowych,
reguluje ph w komórce Występuje
głównie w chloroplastach.
Chlorozy przechodzące w
nekrozy (na liściach dolnych
pięter plamy między żyłkami)
w skrajnych przypadkach nekrozy
brzegów liści.
Cl
Cl
-
Konieczny w reakcjach uwalniania tlenu
(w chloroplastach) podczas
rozkładu wody.
Prawie niespotykane.
Funkcja i objawy niedoboru mikroelementów.
Forma
pobierania
Funkcje
Objawy niedoboru
Fe
Fe
2+
Fe
3+
Chelaty
Składnik: cytochromów, ferredoksyny,
dysmutazy ponadtlenkowej (SOD)
katalazy, peroksydazy, reduktazy
azotanowej. 80% Fe – w
chloroplastach.
Stymulator syntezy chlorofilu.
Chloroza całych liści młodych
Mn
Mn2+
Mn3+
Chelaty
Aktywator dekarboksylaz, dehydrogenaz,
występuje kompleksie PSII – białko, w
dysmutazie ponadtlenkowej (SOD). Kwaśnej
fosfatazie. Uczestniczy w reakcjach
wydzielania tlenu w fotosyntezie.
Mozaikowa chloroza, nekroza
międzyżyłkowa. Niekiedy
smugowate plamy (u
zbóż)Zahamowanie wzrostu.
Opadanie liści.
B
H2BO3
B4O7
2-
Uczestniczy w tworzeniu struktur ścian
komórkowych i w procesie wzrostu (podziały
komórkowe, wzrost łagiewki pyłkowej i in.).
pośrednio uczestniczy w metabolizmie
cukrowców.
Nekroza wierzchołków
wzrostu pędu i korzeni. Liście
kruche, zamieranie kwiatów,
brak zawiązywania owoców,
owoce niewyrośnięte,
skołowaciałe, spękane.
Cu
Cu
2+
Cu
+
Chelaty
Składnik: plastocyjanina, oksydazy
cytochromowej i askorbinianowej. Występuje
w SOD (z Cu i Zn) i reduktazie azotanowej. W
komórce głównie w chloroplastach.
Nekrotyczne plamy,
niebieskozielona barwa liści.
Czasem brak turgoru.
Zaburzenia w formowaniu
organów generatywnych.
Zahamowanie wypełniania
ziarniaków zbóż.
Zn
Zn
2+
Chelaty
Składnik: dehydrogenazy
alkoholowej, anhydrazy węglanowej,
SOD (z Cu) polimerazy RNA, palców
cynkowych, aktywator enzymów metabolizmu
cukrowców i białek.
Regulacja ekspresji genów.
Stabilizacja struktur białkowych.
Zahamowanie wydłużania
międzywęźli (u drzew),
redukcja powierzchni blaszek
liściowych. Przebarwienia
jasnozielone liści starszych.
Mo
MoO4
2-
Składnik nitrogenazy (z Fe) i
reduktazy azotanowej (z Fe).
Redukcja rozwoju blaszki
liściowej. Chloroza liści
młodych. Zahamowanie
brodawkowania i wzrostu
roślin motylkowych.
Deformacja pędu.
Ni
Ni
3+
Składnik ureazy i hydrogenaz.
Brak danych
Strona 45
Wiązanie wolnego azotu.
Wiązaniem azotu nazywamy przemianę gazowego N
2
w amoniak. Proces
ten przeprowadzany jest przez niewiele mikroorganizmów, nazywanych
diazotrofami. Są nimi wolno żyjące bakterie glebowe jak Azotobacter,
Kiebsiella, Clostridium, cyjanobakterie (sinice) i bakterie symbiotyczne z
rodzaju Rhizobium, które dokonują inwazji korzeni roślin motylkowych
( groch, fasola, koniczyna) i tworzą brodawki korzeniowe, w których
zachodzi wiązanie azotu. Bakterie wiążące azot dostarczają gospodarzowi
NH
3
lub glutaminę, roślina dostarcza natomiast związki węgla oraz
zapewnia warunki do rozwoju – niszę ekologiczną. Rhizobia żyją w glebie
jako saprofity i w tym czasie tracą zdolność do wiązania azotu. Uzyskują ją
dopiero po wniknięciu przez włośniki do kory pierwotnej korzenia rośliny
motylkowej i rozpoczęciu kooperacji z gospodarzem. Bakterie dzielą się
wówczas intensywnie pobudzając komórki rośliny do szybkiego wzrostu w
skutek którego na korzeniu tworzą się brodawki. Najintensywniejsze
wiązanie N
2
występuje przed kwitnięciem rośliny. Po kwitnieniu natężenie
wiązania słabnie, brodawki rozpadają się a przedostające się do gleby
bakterie mogą zainfekować nowe rośliny.
Interesującym autotrofami CO
2
i N
2
są sinice np. Nostoc. W niciach,
cyjanobakterii rosnących na podłożu pozbawionym azotu tworzą się w
regularnych odstępach heterocysty. Są to duże grubościenne,
wyspecjalizowane komórki pozbawione niektórych składników PSII. W
heterocystach zachodzi wiązanie azotu z udziałem ATP i związków
redukujących, powstających w wyniku fotosyntetycznego transportu
elektronów. Sinice wiążą N
2
jako organizmy wolnożyjące, ale mogą tez
wchodzić w symbiozę z różnymi np. mchami, paprociami i roślinami
wyższymi.
Mechanizm wiązania N
2
jest podobny u różnych mikroorganizmów.
Proces ten katalizuje specjalny kompleks enzymatyczny – nitrogenaza,
który składa się z 2 współpracujących ze sobą białek. Większe z nich –
dinitrogenaza
zwana też białkiem MoFe zawiera miejsce redukcji N
2
. Jest
heterotetramerem zbudowanym z 2 podjednostek α i 2 podjednostek β.
Nitrogenaza bakterii symbiotycznych zawiera zawsze molibden, dlatego
jest on mikroelementem koniecznym do symbiotycznego wiązania N2.
Bakterie w razie braku molibdenu w podłożu zastępują go w kompleksach
Mo-Fe-S wanadem lub żelazem. Mniejsze białko zbudowana jest z dwóch
identycznych podjednostek. Jego funkcją jest wiązanie ATP i dostarczanie
elektronów dinitrogenazie. Do działania nitrogenazy konieczna jest
obecność ATP i Mg
2+.
Mała podjednostka nitrogenazy ulega redukcji i
tworzy kompleks Fe- białko- Mg- ATP. W tej postaci łączy się z dużą
podjednostką zawierającą Mo i oddaje jej swoje elektrony. W ten sposób
powstaje aktywny enzym zdolny do redukcji N
2.
Sumaryczna reakcja biologicznego wiązania azotu:
8 H
+
+ N
2
+ 8 e
-
+ 16 ATP + 16 H
2
O = 2 NH
3
+ H
2
+ 16 ADP + 16 Pi
Ukazuje, ze jest to proces bardzo kosztowny pod względem
energetycznym.
Leghemoglobina -kompleks nitrogenazy jest niezwykle wrażliwy na
inaktywacje przez O
2
, enzym ten musi więc być chroniony przed tym
reaktywnym gazem. W brodawkach korzeniowych ochronę te zapewnia
leghemoglobina. Część globinową tego monomerycznego białka
wiążącego jest syntetyzowana przez roślinę, zaś hem jest wytwarzany
przez Rhizobium. Leghemoglobina ma duże powinowactwo do O
2
utrzymuje więc wystarczająco małe jego stężenie, chroniąc nitrogenazę.
Wpływ składników mineralnych na wysokość
plonów roślin-prawa żywienia mineralnego.
1.Prawo zwrotu składników mineralnych - mówi, że aby utrzymać
żyzność gleby trzeba zwracać jej substancje pokarmowe pobrane przez
rośliny oraz te , które zostały uwstecznione na skutek stosowania
nawozów. Rośliny pobierają z gleby duże ilości składników pokarmowych
w tym: azotu, potasu, fosforu i wapnia. Składniki te są wyprowadzane z
gleby wraz z plonami, wskutek czego zmniejsza się ich zawartość w
glebie, dlatego należy je uzupełniać. Wprowadzanie do gleby określonego
składnika mineralnego może zmniejszać przyswajalność innego. Duże
Strona 46
dawki nawozów potasowych wypierają z gleby magnez, a nadmierne
wapnowanie gleby powoduje zanik przyswajalnego manganu, duże dawki
nawozów azotowych zmniejszają przyswajalność miedzi.
2.Prawo minimum ( prawo Liebiga)-mówi, że wysokość plonów
określa ten składnik pokarmowy, który występuje w glebie w ilościach
najniższej w stosunku do potrzeb rośliny. Wynika z niego, że niedobór
któregokolwiek ze składników pokarmowych ogranicza działanie
pozostałych składników i w rezultacie jest przyczyną niskich plonów. Niska
zawartość azotu jest czynnikiem ograniczającym i pomimo, że pozostałe
składniki( P, K, Ca) są obecne w ilościach wystarczających, plony nie
mogą być wyższe niż na to pozwala zawartość azotu. Prawo to odnosi się
także do czynników od których zależy wzrost i plonowanie roślin np. :
temperatura, woda, światło, CO
2
itp. Do koncepcji tego prawa należy
zasada współdziałania czynników, duże stężenie któregoś z czynników
może modyfikować działanie czynnika będącego w minimum.
3. Prawo Mitscherlicha ( prawo nadwyżek mniej niż
proporcjonalnych)- mówi, że plon roślin zwiększa się wraz ze wzrostem
dawek składnika pokarmowego proporcjonalnie do różnicy pomiędzy
plonem maksymalnym a plonem rzeczywiście przez dawkę tego składnika
osiągniętym. Przyrost plonu otrzymany po dodaniu do gleby jednostkowej
dawki składnika pokarmowego jest tym mniejszy, im więcej tego składnika
było przedtem w glebie.
4.Prawo maksimum- mówi, że nadmiar składnika pokarmowego w
glebie ogranicza skuteczność działania innych składników i w następstwie
powoduje obniżkę plonów.
5. Prawo pierwszeństwa- mówi, że stosowanie nawozów ma na
celu przede wszystkim poprawę wartości biologicznej plonów, która ma
większe znaczenie aniżeli wysokość plonów.
Pasywne i aktywne mechanizmy pobierania
jonów przez rośliny wyższe.
Adsorpcja wymienna (faza niemetaboliczna ): jony, które wniknęły do
wolnej przestrzeni korzenia AFS, ulegają w niej adsorpcji
elektrostatycznej. Protoplasty ściany komórkowej i najbardziej zewnętrzna
warstwa plazma lemmy mają określone centra o ładunku ujemnym .
Ujemne centra adsorbują dodatnie kationy ; takie związanie nie jest
stabilne ( kationy mogą ulegać wymianie na inne). Adsorpcja ma charakter
wymienny ( najczęściej wymianie ulegają protony). Adsorpcji mogą ulegać
też aniony ( w mniejszym stopniu bo w wolnej przestrzeni korzenia i ich
adsorpcji w ścianach kom. I na zewnętrznej powierzchni plazma lemmy .
Jest to proces fizyczny nie związany bezpośrednio z aktywnością
metaboliczną protoplastu- faza niemetaboliczna.
Aktywny transport( Faza metaboliczna). Przenikanie jonów przez plazma
lemmę do cytoplazmy (symplastu ) wymaga nakładu energii.
HIPOTEZY
1.nośników jonowych ( w plazmalemmie są organiczne cząstki, są
specyficzne dla danych jonów). Mają zdolność wykonywania ruchów w
plazmalemmie (obrotowe, wahadłowe) . Cząstka nośnika związuje dany
jon a następnie przenosi go na drugą stronę plazma lemmy. Jon zostaje
uwolniony a pusty nośnik wraca z powrotem.
Ruch nośników i transport jonów wymaga nakładu energii, jej źródłem jest
ATP . Ze względu na bezpośredni związek transportu jonów z
metabolizmem oddechowym tę część procesu pobierania substancji
mineralnych nazywa się fazą metaboliczną.
2. Pinocytoza- zewnętrzna powierzchnia plazma lemmy wraz z
zaabsorbowanymi jonami pukla się do wnętrza komórki, tworząc zamknięty
pęcherzyk, który znajduje się wewnątrz cytoplazmy, ale zawiera w sobie
roztwór zewnętrzny. Pęcherzyk dzieli się na mniejsze pęcherzyki ,
poruszające się swobodnie w masie cytoplazmy. Zawartość tych
pęcherzyków zostaje powoli włączona w metabolizm komórki.
3. Fagocytoza – polega na pochłanianiu przez protoplast drobnych
cząst. ciał ( zachodzi tylko w zewnętrznych kom. Korzenia np. we
włośnikach). W jej wyniku w cytoplazmie gromadzą się kationy . Powstaje
różnica potencjałów między cytoplazmą a środowiskiem zewnętrznym .
Jest przyczyną wciągania do cytoplazmy ujemnych anionów dla
zobojętnienia tej różnicy. Dla zrealizowania pobierania jonów wystarczy
metaboliczny transport jednego typu jonów, transport drugiego typu jonów
Strona 47

jest wynikiem różnicy potencjałów między cytoplazmą a środowiskiem .
Jony wciągane do wnętrza kom. przez wypełnione wodą pory w
plazmalemmie w sposób bierny.
Przemiany azotu nieorganicznego u roślin
- rola reduktazy azotanowej i azotynowej.
Reduktaza azotanowa- to enzym, który katalizuje pierwszy etap
asymilacyjnej redukcji azotanów ściślej reakcję redukcji azotanów do
azotynów zachodzącą w cytoplazmie. Typowym donorem elektronów dla
reduktazy azotanowej jest NADH. Organizmy roślinne mogą zawierać
więcej niż jedną reduktazę azotanową. W glonach eukariotycznych i w
korzeniach traw obok enzymu specyficznego względem NADH występuje
także niespecyficzna reduktaza, korzystająca z NADH lub NADPH. Główne
cechy reduktaz azotanowych pochodzących z roślin wyższych i glonów są
bardzo podobne. Enzym ten jest homotetramerem zawiera po 1 cząst.
FAD, hemu i molibdipteryny w każdej z 4 podjednostek białkowych.
Kofaktory te pośredniczą w przeniesieniu elektronów na cząst. NO
3
-
jako
źródła azotu. Reduktaza azotanowa jest jednym z niewielu enzymów
roślinnych, których syntezę reguluje egzogenny substrat na poziomie
ekspresji genu. Azotan musi być stale obecny, aby utrzymać stacjonarny
poziom enzymu w komórce, ponieważ białko reduktazy ulega szybkiej
degradacji. Aktywność reduktazy azotanowej reguluje światło. Aktywność
enzymu można stwierdzić w częściach nadziemnych jak i podziemnych
roślin, a także wyłącznie w korzeniach lub w pędach. Rośliny cieniolubne
mają tendencję do redukcji azotanu w korzeniach, a światłolubne w
liściach.
Reduktaza azotynowa-to enzym, który katalizuje drugi etap
asymilacyjnej redukcji azotanów z udziałem zredukowanej ferredoksyny
( Fd) jako donora elektronów. Reduktaza azotynowa ma bardzo duże
powinowactw odo substratu znacznie większe od reduktazy azotanowej.
Dzięki temu azotyny nie mogą nagromadzać się w dużych stężeniach. Jest
to bardzo istotne dla organizmu, gdyż azotyny są toksyczne z powodu
zdolności do reakcji z hemem, gr. –NH
2
aminokwasów oraz zasad
organicznych. W tkankach fotosyntetyzujących reduktaza azotynowa
występuje w chloroplastach. Redukcja ferredoksyny związana jest z
fotosyntetycznym transportem elektronów, dlatego redukcja azotynów
zależy od światła. W niefotosyntetyzującychtkankach roslin reduktaza
azotynowa jest związana z plastydami, a ferredoksyna zostaje
zredukowana przez NADPH wytworzony w szlaku pentozo fosforanowym.
Rola żelaza w procesach fizjologicznych
i metabolicznych roślin wyższych.
Zawartość żelaza w roślinach jest duża w porównaniu z innymi mikroelementami.
Ze względu na funkcje katalityczne Fe jest obecnie powszechnie zaliczane do
mikroelementów. Występuje w wielu enzymach oksydoredukcyjnych oraz aktywuje
liczne enzymy. W roślinach Fe przemieszcza się przez ksylem w równowadze z
cytrynianami lub innymi anionami. Podstawowym warunkiem utrzymania jonów
żelaza w roztworze, umożliwiającym pobieranie go przez system korzeniowy, jest
niskie pH. Żelazo uczestniczy w reakcjach oksydoredukcyjnych jako przenośnik
elektronów lub tworząc podobnie jak Mn i Mg mostek jonowy między enzymem a
substratem. Szczególlnie ważna jest funkcja Fe jako aktywatora w syntezie
chlorofilu i niektórych białek. Białkowe związki Fe uczestniczą w przekształcaniu
energii świetlnej w chemiczną , potrzebną do fotolizy wody w procesie fotosyntezy.
Żelazo uczestniczy w redukcji azotanów i wiązania wolnego azotu oraz
metabolizmie kwasów nukleinowych. U roślin duża część Fe związana jest z
porfirynami do których należą enzymy: ferredoksyna( bierze udział w powstawaniu
NADPH) i cytochromy( odpowiadają za magazynowanie energii w postaci
ATP),a więc enzymy te biorą udział w procesach fotochemicznych, warunkują
powolne uwalnianie energii świetlnej i wytwarzanie wysokoenergetycznych
związków chemicznych.
Antagonizm jonów
Antagonizm jonów– zjawisko osłabienia określonych właściwości
fizjologicznych pewnych jonów przez obecność innych. Roztwory
pojedynczych soli wpływają zwykle szkodliwie na rośliny, dodatek innej soli
może zmniejszyć toksyczne działanie soli pojedynczej. Roztwór
zawierający różne sole w takiej proporcji , przy której nie jest on toksyczny,
nazywamy roztworem zrównoważonym. Jony potasowe zwiększają
hydratację i przepuszczalność cytoplazmy. Wprowadzenie jonów Ca
2+
do
środowiska, wypiera z cytoplazmy część jonów K
+
i przywraca właściwą
Strona 48
równowagę. Podobny antagonizm występuje między parami Na
+
i Mg
2+
;
NH
4
+
i Ca
2+
. Do zjawisk antagonistycznych można zaliczyć wpływ
wywierany przez jeden jon na pobieranie innych jonów, np. zwiększona
ilość potasu obniża zawartość wapnia w liściach, nadmiar wapnia
zmniejsza zdolność wykrywania magnezu. Jony Al
3+
hamują pobieranie
Cu
2+
.
Obieg azotu w przyrodzie.
Duża ilość azotu znajduje się w atmosferze ziemskiej w postaci wolnej N
2
, jest ona jednak niedostępna dla zwierząt i większości roślin. Zdolność
wiązania azotu cząsteczkowego mają niektóre bakterie żyjące w glebie
wolno albo w symbiozie z roślinami motylkowatymi. Również zakłady
przemysłowe wiążą w procesach technologicznych wielkie ilości azotu,
który w postaci nawozów znajduje powszechne zastosowanie w
rolnictwie . Azot roślin, głównie w postaci białek i aminokwasów, jest
wykorzystywany przez zwierzęta roślinożerne. Azot wszystkich żywych
organizmów, zarówno roślinnych jak i zwierzęcych zostaje po ich śmierci
przekształcony przez reducentów ( bakterie gnilne) na amoniak. Jest on
albo pobierany przez rośliny, albo pobierany przez rośliny, albo ulega
utlenieniu przy udziale bakterii nitryfikacyjnych na azotany i w tej dopiero
postaci jest pobierany przez rośliny. Część azotanów rozkładają do
wolnego azotu bakterie denitryfikacyjne i w ten sposób zamyka się cykl
krążenia azotu.
Gospodarka azotowa roślin - przyswajalne formy
azotu nieorganicznego, przemiany w organiźmie.
Rośliny nie mogą bezpośrednio korzystać z azotu atmosferycznego,
chociaż jego zawartość w powietrzu sięga około 78%. Głównymi formami
dostępnymi dla roślin są NO
3
-
i
NH
4
+
.Z energetycznego punktu widzenia
jony NH
4
+
są korzystniejszym źródłem azotu, ponieważ azotan wymaga
kosztownej energetycznie redukcji przed wbudowaniem do amoniaku.
Źródła azotu:
o Organiczne: białka, kwasy nukleinowe, próchnica, mocznik,
aminy, amidy, aminokwasy;
o Nieorganiczne: sole amonowe i azotanowe;
o Azot atmosferyczny (cząsteczkowy).
Asymilacyjna redukcja azotanów:
Pobrane jony amonowe są bezpośrednio wykorzystywane do syntezy
związków organicznych, natomiast jony azotanowe po wniknięciu do
rośliny ulegają najpierw redukcji do amoniaku. Jest to redukcja NO
3
-
do
NH
4
+
. Wymaga ona dużej ilości energii( 8e-).Przebiega dwustopniowo:
•
Pierwszy etap
- Redukcja azotanów do azotynów katalizowana
przez reduktazę azotanową ( zachodzi w cytoplazmie):
NO
3
-
+ NAD(P)H + H
+
-> NO
2
-
+ NAD(PH
2
) + H
2
O
Reduktaza azotanowa- zbudowana jest z czterech podjednostek
białkowych, zawiera molibden ( Mo), dlatego rośliny pozbawione Mo nie
mogą korzystać z NO
3
-
jako źródła azotu. Reduktaza azotanowa powstaje
w tkankach tylko w obecności jonów NO
3
-
. Jej aktywność zależy od
światła, jej syntezę reguluje egzogenny substrat na poziomie ekspresji
genów. Organizmy roślinne mogą zawierać więcej niż jedną reduktazę
azotanową . W glonach eukariotycznych, korzeniach traw występuje
niespecyficzna reduktaza mogąca korzystać z NADH lub NADPH.
Rośliny cieniolubne mają tendencję do redukcji NO
3
-
w korzeniach, a
światłolubne w liściach.
•
Drugi etap
asymilacji katalizuje reduktaza azotynowa z udziałem
zredukowanej ferredoksyny (Fd) jako donora elektronów:
NO
2
-
+ 6Fd
red
+ 8 H
+
-> NH
4
+
+ 6Fd
ox
+ 2H
2
O
Asymilacja właściwa: W biosyntezie wszystkich aminokwsów zasadniczą
rolę odgrywają reakcje aminacji , czyli przyłączenia do łańcucha
węglowego grup aminowych z NH
3
oraz reakcje transaminacji, polegające
na przenoszeniu grup aminowych z określonych aminokwasów na keto
kwasy.
Aminacja- jest to powszechnie występujące w komórkach roślin wyższych
oraz u mikroorganizmów redukcyjne przyłączenie grupy aminowej z
Strona 49
amoniaku do α- ketoglutaranu, w wyniku czego tworzy się glutaminian oraz
woda:
α – ketoglutaran + NH
3
+ NADH + H
+
-> glutaminian + NAD
+
+ H
2
O
Reakcja ta katalizowana jest przez dehydrogenazę glutaminianowa
występująca w mitochondriach, enzym ten jest nieaktywny w stosunku do
innych keto kwasów tj. pirogronian.
Amoniak może być także wykorzystywany bezpośrednio do syntezy
glutaminy. Przyłączenie amoniaku do glutaminy zachodzi przy udziale
syntetazy glutaminianowej: Glutaminian + NH
3
+ ATP -> glutamina +
ADP + P
Transaminacja – polega na przeniesieniu grupy aminowej z aminokwasu
na określony ketokwas. Stwierdzono, że grupy aminowe przynajmniej
takich aminokwasów jak waliny, leucyny, izoleucyny, fenyloalaniny,
tyrozyny, asparaginianu, alaniny i seryny, pochodzą bezpośrednio z grupy
aminowej glutaminianu. Oznaczałoby to, że glutaminian pełni funkcje
pośrednika pomiędzy azotem nieorganicznym a azotem zawartym w
aminokwasach. Enzymem uczestniczącym w procesie transamincji jest
aminotransferaza asparaginianowa, katalizuje głównie reakcję:
Glutaminian + szczawiooctan -> α – ketoglutaran + asparaginian
Inna aminotransferaza, otrzymywana z siewek fasoli, katalizuje
transaminację aminokwasów aromatycznych z wytworzeniem
pirogronianu.
Dawcą grup aminowych w procesach transaminacji może być także
glutamina, która ponadto jest dawcą azotu w syntezie innych związków
azotowych.
Pobieranie i przekształcanie związków azotowych
przez rośliny wyższe
Rośliny pobierają azot przez system korzeniowy głównie w formie
jonów amonowych (NH4+) oraz azotanowych (NO3-). Minimalne ilości
mogą być pobierane w postaci jonu NO
2
⁻
, lecz w większych ilościach jest
on toksyczny dla rośliny.
Związki organiczne: mocznik, białka, aminokwasy, kwasy
nukleinowe, próchnica. Z wymienionych związków organicznych
łatwo dostępny jest jedynie mocznik. Występuje on dość często w
glebie, jako produkt rozpadu białka lub odchodów zwierzęcych.
Mocznik jest w dużych ilościach wprowadzany do gleby, jako nawóz.
Dla olbrzymiej większości roślin stanowi on doskonałe źródło azotu.
Rośliny wykorzystują mocznik przy udziale enzymu zwanego ureazą.
Enzym ten występuje stale w roślinach, lub może być produkowany
indukcyjnie wtedy, kiedy roślina pobiera mocznik. Pod wpływem tego
enzymu następuje hydrolityczny rozpad mocznika w komórkach
roślinnych lub bezpośrednio w glebie.
Mocznik → amoniak + dwutlenek węgla
Wytworzony amoniak jest silnie sorbowany przez glebę, co
zabezpiecza przed większymi stratami azotu, nie utrudnia jednak
pobierania przez rośliny.
•
Związki nieorganiczne: sole azotanowe i sole amonowe.
Związki azotanowe gleby pochodzą z nitryfikacji, z biologicznego
utleniania amoniaku, przeprowadzanego przez bakterie
nitryfikacyjne. Związki te nie są sorbowane przez koloidy glebowe i
dlatego łatwiej ulegają wypłukaniu z gleby.
Związki amonowe pochodzą z amonifikacji, tzn. z biologicznego
rozkładu szczątków zwierzęcych i roślinnych. W wyniku hydrolizy
enzymatycznej związki azotu o skomplikowanej budowie przechodzą
w związki prostsze. Amonifikację przeprowadzają: grzyby, bakterie,
promieniowce, śluzowce oraz rośliny wyższe i zwierzęta.
Najważniejszym produktem końcowym jest amoniak, który ulega
sorpcji przez koloidy glebowe.
•
Azot atmosferyczny, cząsteczkowy
Azot atmosferyczny jest niedostępny dla roślin.
Większość azotu z
atmosfery trafia do biosfery poprzez wolno żyjące bakterie azotowe.
Należy do nich m.in. rodzaj Rhizobium. Bakterie te posiadają enzym
nitrogenazę, katalizujący reakcję gazowego azotu z wodorem
Strona 50
pochodzącym z reakcji biochemicznych w wyniku czego powstaje
amoniak, a także aminokwas glutamina. Tego rodzaju bakterie żyją
samodzielnie lub w symbiozie z roślinami. Szczególnie dużo
występuje ich w roślinach motylkowych, gdzie oddają one amoniak
lub glutaminę.
Pobieranie i transport substancji mineralnych
przez rośliny
System korzeniowy pobiera z gleby wodę i sole mineralne . Można w
nim wyróżnic 5 stref, różniących się budową i właściwościami
fizjologicznymi. Komórki wszystkich tych stref mogą pobierać
substancje mineralne. Zasadniczą rolę w zaopatrywaniu organów
nadziemnych rośliny w substancje mineralne odgrywa strefa
włośnikowa.
Oprócz korzeni także liście mogą pobiera substancje mineralne.
Pozwala to na zastosowanie tzw. nawożenia dolistnego
polegającego na skraplaniu roślin rozcieńczonym roztworem soli
mineralnych.
Pobieranie substancji jest procesem niezwykle skomplikowanym,
który przebiega z udziałem sił fizykochemicznych i metabolicznych.
Korzenie mogą pobierać zarówno jony jak i całe niezdysocjowane
cząsteczki mineralne oraz organiczne.
Bliski transport jonów: Następuje on od środowiska zewnętrznego
do naczyń korzenia dwoma kanałami:
•
Kanałem apoplastycznym- jony migrują w wolnej przestrzeni
korzenia, a szczególnie łatwo w blaszce środkowej, wchodzące,
bowiem w jej skład pektyny mają bardzo luźną strukturę. Przeszkodę
w tym transporcie stanowi endoderma, ponieważ jej skorkowaciałe
ściany ( pasemka Caspary’ego) uniemożliwiają dalszą dyfuzję w
ścianach komórkowych. Pokonanie tej przeszkody zachodzi w
sposób metaboliczny, przy udziale energii metabolicznej.
•
Kanałem symplistycznym- jony, które dostały się do symplastu
w fazie metabolicznej, migrują poprzez cytoplazmę z komórki do
komórki.
Końcowym etapem transportu jonów w obu kanałach jest
metaboliczne wymagające energii wydzielanie jonów do wnętrza
naczyń.
Daleki transport jonów: Transport od korzeni do liści następuje od
korzeni do liści wraz z prądem transpiracyjnym, przy czym
substancją pośredniczącą jest woda. Jony płyną wraz z nią wzdłuż
łodygi a dalej przez ogonki liściowe do silnie rozgałęziającego się
systemu żyłek w liściu.
Strona 51

Biogeneza chloroplastów:
Komórki roślinne posiadają wiele specyficznych tylko dla nich
organelli. Wśród nich możemy wyróżnić plastydy, z których najważniejsze
są chloroplasty – zawierające barwnik fotosyntetyczny (chlorofil).
Chloroplasty powstają właśnie z plastydów, już w tkankach merystema
tycznych można wyróżnić proplastydy, czyli podwójnie obłonione
pęcherzyki (błony białkowo – lipidowe otaczające stromę). Ich namnażanie
zachodzi wraz z podziałami komórkowymi.
Jeżeli nowo powstałe komórki będą rozwijać się w ciemności to
zajdzie tzw. etiolacja i w proplastydach zaczną gromadzić się związki
cukrowe lub tłuszcze (powstaną leukoplasty, bądź amyloplasty –
skupiające ziarna skrobi). Z czasem w leukoplastach nastąpi inwaginacja
wewnętrznej błony białkowo – lipidowej, aż zaczną odrywać się od niej
pęcherzyki. Utworzą one nieregularne skupienia błon w kształcie rurek (w
jednym biegunie komórki) – twór ten nazywamy ciałem prolameralnym.
Ciało prolameralne zawiera w sobie żółty barwnik – protochlorofilid, a
plastyd z ciałem prolameralnym (w kształcie plastru miodu) nazywamy
etioplastem. Wystarczy wystawić etiolowane komórki na światło, a
rozpocznie się w nich synteza chlorofilu z protochlorofilidu, chlorofil idu a i z
kwasu aminolewulinowego (deetiolacja). Pęcherzyki zaczną się rozpadać i
spłaszczać – powstaną grana. Poza tym nastąpi synteza białka wiążącego
chlorofil a/b, które łącząc się z chlorofilem i zakotwiczając w błonie
tylakoidów utworzy antenę fotosystemu II. Zajdzie także synteza
podjednostek enzymu: karboksylazy rybulozo – 1,5 – bisfosforylowej
(RuBisCO) – niezbędnego do asymilacji CO
2
. Proces syntezy chlorofilu,
białka wiążącego chlorofil i RuBisCO kontrolowany jest przez system
fitochromowy – główny fotoreceptor.
Jeżeli komórki będą rozwijać się przy pełnym dostępie światła, to
wówczas z plastydów od razu zaczną formować się spłaszczone
pęcherzyki tylakoidów gran i wydłużone połączenia pomiędzy nimi –
tylakoidy stromy. Rozpocznie się także synteza chlorofilu.
Z czasem chloroplasty zaczną przekształcać się w chromoplasty –
organella z takimi barwnikami jak: karotenoidy i fikobiliny, będzie to
oznaczać, że zachodzi w nich proces starzenia.
Skład chemiczny chloroplastów:
W błonach chloroplastów dominującym składnikiem są białka – ok.
60%. Lipidy stanowią ok.: 20 – 35% i są to przede wszystkim galaktolipidy -
85% wszystkich lipidów (ich obecność świadczy o pochodzeniu
chloroplastów od bakterii, są to: monogalaktozylodiacyloglicerol i
digalaktozylodiacyloglicerol, sulfolipid) , które posiadają w swych
strukturach wiele kwasów nienasyconych (linolowy, linolenowy). W
błonach chloroplastów niewielki procent stanowią fosfolipidy(ok.15%
lipidów), a wśród nich głównie fosfatydyloglicerol, fosfatydylocholina.
Oprócz białek i lipidów w błony chloroplastów wbudowane są liczne
barwniki fotosyntetyczne:
o chlorofil a i b oraz c i d (absorbują światło w zakresie widzialnym o
barwie niebieskiej ok. 400nm i czerwonej ok 600nm), składają się one z
układów pirolowych z centralnie położonym atomem Mg
2+
oraz
dwudziestowęglowego łańcucha alkoholu – fitolu (służy do
zakotwiczenia w błonie tylakoidu)
o bakteriochlorofile: a,b,c,d,e,g, u bakterii fotosynetycznych np.: sinic
o barwniki pomocnicze: karotenoidy (karoteny – zbudowane z dwóch
pierścieni połączonych długim łańcuchem węglowodorowym ze
sprzężonym układem wiązań, np.: ß – karoten i ksantofile – podobne w
swej budowie do karotenów ale z atomami tlenu przy pierścieniach np.:
zeaksantyna, wiolaksantyna) oraz fikobiliny – barwniki krasnorostów i
sinic, zbudowane z 4 pierścieni pirolowych ale w układzie liniowym i bez
fitolu np. fikocyjanina, fikoerytryna
o w błonach spotkamy także specyficzne chinony (przekaźniki
elektronów): plastochinon, hydrochinon, plastohydrochinon, filochinon –
witamina K, α – tokoferol – witamina E (ich obecność potwierdza teorię
endosymbiozy)
Strona 52

W Stromie chloroplastów znajdują się cząsteczki autonomicznego,
kulistego DNA, które stanowią ok. 7% składników chloroplastów i
cząsteczki RNA: 1,7 – 3,5 %. Występują tu rybosomy o stałej
sedymentacji: 70S – co świadczy o prokariotycznym pochodzeniu
chloroplastów (teoria endosymbiozy).
Strona 53

Fosforylacje – rodzaje, mechanizmy, znaczenie:
Fosforylacja – jest to proces syntezy ATP z ADP i nieorganicznej reszty
fosforanowej, wyróżniamy trzy rodzaje fosforylacji:
1) Fosforylacja fotosyntetyczna (fotofosforylacja).
2) Mitochondrialna fosforylacja oksydacyjna.
3) Fosforylacja substratowa.
Ad do 1): Mechanizm fotofosforylacji:
a) według chemiosmotycznej teorii Mitchella siłą napędową fosforylacji
jest gradient stężeń protonów – H
+
, pojawiający się w poprzek błony
tylakoidu podczas transportu elektronów przez układ przenośników w
fotosystemach: I i II, aż do zredukowania NADP
+
.
b) We wnętrzu tylakoidy tworzy się nadmiar jonów H
+
, które powstają z
rozpadu wody: 2H
2
O -> 4H
+
+ 4e
-
+ O
2
; z procesu utleniania
plastochinolu
c) przez kompleks cytochromowy b
6
f
d) Na zewnątrz tylakoidy (w stromie chloroplastu) zaczyna brakować
protonów, ponieważ są one pobierane do redukcji NADP
+
: 2e
-
+ 2 H
+
+
2NADP
+
-> NADPH + H
+
; są pobierane również do redukcji
plastochinonu w miejscu Q
B
e) Synteza ATP zachodzi przy udziale kompleksu SYNTAZY ATP
zwanego czynnikiem sprzęgającym. Jest ona zbudowana z dwóch
podjednostek: CF
0
i CF
1
. CF
0
stanowi zakotwiczenie kompleksu w
błonie tylakoidu i umożliwia przepływ jonów H
+
przez błonę. CF
1
o
złożonej strukturze (wiele podjednostek białkowych) posiada dużo
miejsc katalitycznych i regulatorowych, w których zachodzi
spontaniczna synteza ATP: ADP + Pi -> ATP. Energia przepływających
przez podjednostkę CF
0
protonów pozwala na zmianę konformacji
elementów podjednostki CF
1
i w wyniku tego następuje uwolnienie
zsyntetyzowanego ATP.
f) Fotofosforylację dzielimy na cykliczną i niecykliczną:
•
Fosforylacja niecykliczna polega na wytworzeniu ATP z ADP i Pi
dzięki gradientowi stężeń jonów H
+
, jaki tworzy się podczas
przepływu elektronów pochodzących z rozpadu wody na NADP
+
przez przenośniki fotosystemu I (PSI) i fotosystemu II (PSII), dzięki
tej fosforylacji zyskujemy tzw. Siłę asymilacyjną fotosyntezy, czyli:
ATP oraz zredukowany NADPH + H
+
- znaczenie.
•
Fosforylacja cykliczna zachodzi tylko w obrębie PSI i elektrony
wybite z PS – 700 trafiają na przenośniki błony tylakoidu,
przechodząc przez kompleks cytochromów b
6
f wytwarzają gradient
stężeń jonów H
+
(wykorzystywany do syntezy ATP), po przejściu na
ferredoksynę nie trafiają na cząsteczkę NADP
+
, ale znów
przechodzą na kompleks cytochromów b
6
f (ponowne wytworzenie
gradientu) i przez plastocyjaninę trafiają znowu na P – 700
+
. W tym
procesie nie tworzy się NADPH + H
+
, powstaje natomiast znaczna
ilość ATP – znaczenie .
Ad. Do 2) Mechanizm fosforylacji oksydacyjnej:
a) W wewnętrznej błonie mitochondrialnej wbudowany jest łańcuch
przenośników elektronów – są to cztery kompleksy przenośników,
których elementy rozmieszczone są nieregularnie po obu stronach
błony – tworzy się gradient elektryczny.
b) Przykładami asymetrycznego rozmieszczenia składników łańcucha
mitochondrialnego są: występowanie utleniania NADPH + H
+
oraz
redukcja tlenu – O2 odbywa się po stronie matrix, mobilny cytochrom
c funkcjonuje po przeciwnej stronie błony – zwrócony do cytoplazmy,
w kompleksie III: centra Fe – S i cytochrom c1 jest po str cytoplazmy,
a cytochromy b po stronie matrix.
c) Oprócz gradientu elektrycznego występuje tu również gradient
chemiczny związany z nierównomiernym stężeniem jonów H
+
, które
podczas transportu elektronów prze łańcuch mitochondrialny na tlen,
zostają usunięte z matrix do przestrzeni międzybłonowej, a ich powrót
do wnętrza mitochondrium związany jest z funkcjonowaniem
kompleksu SYNTAZY ATP (ponieważ wewnętrzna błona nie jest
przepuszczalna dla H
+
); kompleks ten zbudowany jest analogicznie do
SYNTAZY ATP występującej w chloroplastach i składa się z dwóch
Strona 54

podjednostek: F
0
i F
1
; F
0
– odpowiada za przepływ H
+
przez błonę, a
F
1
posiada miejsca katalityczne, na których syntezowany jest ATP i
następnie uwalniany, dzięki energii przepływu protonów.
d) Ten rodzaj fosforylacji stanowi główne źródło energii dla wszystkich
organizmów! – znaczenie
Ad do 3): Mechanizm fosforylacji substratowej:
a) Jej mechanizm opiera się na syntezie ATP przez bezpośrednie
przeniesienie reszty fosforanowej ( Pi ) z wysokoenergetycznego
substratu na ADP.
b) Zachodzi ona przede wszystkim w pierwszym etapie oddychania,
czyli w glikolizie, podczas przekształcania 1,3 – bisfosfoglicerynianu
w fosfoglicerynian oraz fosfoenolopirogronianu w pirogronian.
c) Fosforylacja substratowa zachodzi także podczas drugiego etapu
oddychania – Cyklu Krebsa, kiedy to bursztynylo – Co
Przekształcany jest w bursztynian za pośrednictwem enzymu:
syntetazy bursztynylo – Co A.
d) Jej znaczenie w produkcji ATP jest niewielkie. Uzupełnia ona ATP,
które zostało pobrane do początkowych reakcji glikolizy.
Budowa błon biologicznych
– rola błon w funkcjonowaniu komórki roślinnej.
Podstawowymi składnikami wszystkich błon biologicznych są lipidy,
steroidy i białka. Błony zbudowane są z dwóch warstw lipidów. Do lipidów
błonowych należą: fosfolipidy (fosfolipidy cholinowe i aminowe),glikolipidy ,
lipidy obojętne. Zrąb błony tworzą amfofilowe fosfolipidy, których cząsteczki
zbudowane są z hydrofilowych grup funkcyjnych i hydrofobowych
łańcuchów węglowodorowych. W podwójnej warstwie błonowej polarne
grupy skierowane są do środowiska wodnego, a ich hydrofobowe części
skierowane do środka błony. W zewnętrznej warstwie roślinnej błony
komórkowej występują silnie kwaśne fosfolipidy(kwas fosfaty dylowy,
fosfatydyloglicerol oraz niektóre glikolipidy). W błonie komórkowej
występują kwasy tłuszczowe, najliczniej kwas palmitynowy, linolowy i
linolenowy. Stałym jej składnikiem są wolne sterole (sito sterol,
kampesterol i stigmasterol). Błony biologiczne to struktury dynamiczne,
cząsteczki fosfolipidów mogą się obracać wokół własnej osi lub
przemieszczać w płaszczyźnie błony. Błony biologiczne mogą mieć różną
płynność zależną od występujących w niej wolnych steroli, temperatury,
rodzaju kwasów tłuszczowych.
Wchodzące w skład błon komórkowych białka błonowe dzielimy na
powierzchniowe i integralne. Białka powierzchniowe luźno związane są z
warstwą lipidową . Zazwyczaj wiązane są siłami elektrostatycznymi z
polarnymi grupami fosfolipidów lub białek integralnych. Białka integralne
mogą wystawać na jedną ze stron błony lub przenikać przez dwuwarstwę
lipidową i przenikać ponad obie powierzchnie, przez co dają się usunąć z
błony jedynie po jej zniszczeniu. Zbudowane są z 15-28 aminokwasów
hydrofobowych, N-końcowy fragment polipeptydu występuje po
zewnętrznej stronie błony, a fragment C-końcowy po stronie wewnętrznej,
mogą również być zbudowane z kilku polipeptydów.
Błony biologiczne oddzielają komórkę od środowiska zewnętrznego i chroni
ją. Zapewnia również komplementarność komórkom, dzięki temu w
komórce mogą zachodzić procesy wzajemnie się wykluczające. Dzięki
temu mogą zachodzić procesy syntezy i rozkładu jednocześnie. Błony
otaczają także wiele organelli wewnątrzkomórkowych. Pozwalają na
selektywny, wybiórczy, dwukierunkowy transport jonów i cząsteczek do
otoczenia, a także odbieranie bodźce ze środowiska i przekazy wanie je
innym komórkom.
Liść jako miejsce transpiracji
- funkcjonowanie aparatów szparkowych
Transpiracja jest to czynne parowanie wody z nadziemnych części
rośliny. Głównym narządem transpiracji liść. Liście transpirują przez
aparaty szparkowe i przez skórkę. Mają do tego szereg przystosowań:
•
Powierzchnia liścia jest znacznie większa od pozostałych
części rośliny.
Strona 55

•
Rzeczywista powierzchnia parowania jest wielokrotnie
większa od powierzchni liścia. Spowodowane jest to budową
anatomiczną liścia, który zbudowany jest z wewnętrznych
komórek mezofilu (miękisz palisadowy i gąbczasty), w których
znajdują się przestwory międzykomórkowe tworzące system
przewietrzający. Umożliwia to wymianę gazów.
•
Liść osłonięty przez skórkę. W dolnej jej części znajdują się
aparaty szparkowe, przez które odbywa się wymiana gazów
pomiędzy wnętrzem liścia a atmosferą, zachodzi także
transpiracja.
•
Liść pokryty jest kutykulą, która jest mało przepuszczalna dla
gazów i wody. Kutykula jednak pęcznieje, a napęczniała
oddaje część wody do atmosfery.
Transpiracja wody zachodzi przez aparaty szparkowe według
dwóch mechanizmów:
Mechanizm glukozowy
o
Niskie pH (około 5) spowodowane pobieraniem CO
2
do
komórek mezofilu i akumulacja kwasu węglowego =>
intensywna fotosynteza => akumulacja skrobi
fotosyntetycznej => niedobór osmotycznie czynnej
glukozy => spadek turgoru =>zamykanie aparatów
szparkowych.
o
Niedobór CO
2
zużytego do fotosyntezy => pH wzrasta
o 7 => aktywacja fosfatazy skrobiowej => przemiana
skrobi asymilacyjnej do glukozy => wzrost potencjału
osmotycznego i turgoru => otwarcie aparatów
szparkowych.
Mechanizm jonowy (jony K
+
)
o
Deficyt wody stymuluje syntezę kwasu abscysynowego
(ABA) w liściach => ABA zwiększa przepuszczalność
błon komórkowych aparatów szparkowych dla jonów
potasowych; jony K
+
wypływają z komórki, spada turgor
=> zamykanie aparatów szparkowych.
CHEMOSYNTEZA
Chemosyntez - proces przekształcania CO
2
w związki organicze, w którym w
odróżnieniu od fotosyntezy wykorzystywana jest nie energia świetlna, ale energia
pochodząca z utleniania różnych związków nieorganicznych lub prostych
jednowęglowych organicznych.
Chemosyntezę można podzielić na dwa etapy:
1. utlenianie związku chemicznego (odpowiednik fazy jasnej fotosyntezy, w
którym dany organizm wytwarza energię użyteczną biologicznie (ATP oraz
powstaje czynnik redukujący w postaci NADPH)
2.
związanie CO
2
i produkcja glukozy (na tej samej zasadzie co faza ciemna
fotosyntezy. Dwutlenek węgla jest związany przez 1,5-bisfosforybulozę.
Reakcję tę katalizuje karboksylaza 1,5- bisfosforybulozy. Produkty tej
karboksylacji są następnie redukowane do poziomu związków
organicznych przy udziale NADPH i ATP).
Chemolitotrofy- bakterie wykorzystujące jako źródło energii takie substraty
nieorganiczne jak związki siarki (bakterie siarkowe), wodór (bakterie wodorowe),
związki azotu (bakterie nitryfikacyjne), żelaza (bakterie żelaziste).
Bakterie siarkowe:
( występują w zbiornikach wody słodkiej i morskiej
obfitujących w niektóre związki siarki, środowiskach z rozkładającą się materią
organiczną- osady denne, ścieki kanalizacyjne). Do substratów najczęściej
wykorzystywanych przez bakterie siarkowe należą:
•
siarkowodór
•
tiosiarczan
•
siarka pierwiastkowa
Najwięcej energii uzyskują bakterie utleniające siarkowodór zgodnie z reakcją:
H
2
S + 2O
2
→ 2H
+
+ SO
4
2-
Nieco mniej energii uwalnia się przy utlenianiu siarki pierwiastkowej:
S
0
+ H2O + 1
2
1
O
2
→2H
+
+
SO
4
2-
Najmniej energii dostarcza utlenianie tiosiarczanu:
Na
2
S
2
O
3
+ H
2
O + 2O
2
→ 2H
+
+ 2Na
+
+ 2 SO
4
2-
Strona 56

Bakterie wykorzystujące siarkowodór (np. Thiothrix nivea, Beggiatoa) często
utleniają ten związek najpierw do pierwiastkowej siarki:
H
2
S +
2
1
O
2
→H
2
O + S
0
Siarka ta odkłada się w komórce jako energetyczny materiał zapasowy i kiedy H
2
S
w środowisku ulegnie wyczerpaniu, ona z kolei dostarcza energii ulegając
przekształceniu do siarczanu. Bakterie siarkowe wykazują duże zróżnicowanie
metaboliczne:
-gatunki autotroficzne, asymilujące CO
2
w cyklu Calvina-Bensona ( np.Thiobacillus
thiooxidans, T. thioparus
Bakterie siarkowe anaerobowe np. Thiobacillus denitrificans
wykorzystuje jako akceptor elektronów azotany zamiast tlenu:
6HNO
3
+5S+2H
2
O→5H
2
SO
4
+3N
2
Thiobacillus acidophilai i T.novellus wykazują mikotroficzny sposób życia tj.
czerpią energię z utleniania nieorganicznych związków siarki, natomiast jako
źródło węgla wykorzystują związki organiczne. Thiobacillus thiocyanooxidads
czerpie energię z utleniania rodanków – produktami utleniania rodanku są jon
siarczanowy, dwutlenek węgla i amoniak.
Bakterie wodorowe:
(występują zazwyczaj w glebie) mają zdolność
wykorzystywania wodoru do uzyskiwania energii. Zaliczane rodzaje:
Hydrogenomonas, Mycobacterium, Nocardia (akceptorem elektronów jest tlen).
Bakterie wodorowe mają enzym hydrogenazę, który uczestniczy w przeniesieniu
elektronów z wodoru na NAD
+
lub chinon. Dalej elektrony przenoszone są przez
łańcuch oddechowy na tlen, generując siłę protomotoryczną i syntezę ATP.
Równanie reakcji utleniania wodoru:
H
2
+
2
1
O
2
→H
2
O
Bakterie żyjące w warunkach beztlenowych, np. Micrococcus denitrificans
wykorzystuje azotany jako akceptory elektronów.
Gatunek ten może uczestniczyć w procesie denitryfikacji.
Bakterie żelaziste:
Czerpią energię z utleniania jonu Fe
2+
do Fe
3+
4FeCO
3
+O
2
+6H
2
O→4Fe(OH)
3
+4CO
2
Jon Fe
2+
jest trwały w obecności tlenu tylko w pH kwaśnym. Ilość energii
uzyskiwanej przez utlenienie Fe
2+
do Fe
3+
jest stosunkowo niewielka w porównaniu
z ilością energii uzyskiwanej przez bakterię siarkowe czy wodorowe. Bakterie
żelaziste wykorzystują do syntezy ATP naturalny gradient stężenia jonów
wodorowych, jaki istnieję pomiędzy zakwaszonym środowiskiem zewnętrznym( pH
ok. 2), a wnętrzem komórki(odczyn zbliżony do obojętnego ).
Thiobacillus ferrooxidans może utleniać także zredukowane związki siarki
uzyskując w ten sposób energię – prowadzi autotroficzny tryb życia .
Bakterię nitryfikacyjne
(występują pospolicie w glebie i zbiornikach wodnych)
energię potrzebną do przeprowadzenia procesów życiowych czerpią z utlenienia
takich form azotu jak NH
3
i NO
2
-
Bakterie z rodzaju Nitrosomonas, Nitrosocystis utleniają amoniak do azotynu
zgodnie z reakcją NH
3
+1
2
1
O
2
→ NO
2
-
+H
+
+H
2
O
Bakterie z grupy Nitrobacter czy Nitrococcous utleniają powstały azotyn do
azotanu :
NO
2
-
+
2
1
O
2
→NO
3
-
Bakterie nitryfikacyjne oprócz utleniania azotynów, mogą w większości
przypadków wykorzystywać energie pochodzącą z rozkładu niektórych związków
organicznych, przez co można j zaliczyć do chemoorganortofów.
Chemoorganotrofy - w grupie tej umieszcza się bakterie które czerpią energię z
utleniania prostych, jednowęglowych związków organicznych takich jak: metan,
metanol, mrówczan tzw. metylotrofy i zalicza się do nich takie rodzaje jak:
Methylobacter, Methylocystis, Methanomonas i inne.
Metylotrofy występują w środowiskach, gdzie dostępne są zarówno wymienione
związki węgla, jak i tlen (gleba, zbiorniki wodne), są obligatoryjnymi aerobami.
Jedną z grup są metylotrofów są metanotrofy, które przeprowadzają reakcję
utleniania metanu do dwutlenku węgla.
CH
4
+
2
1
O
2
→CH
3
OH→CHOH + 2H
CHOH+ H
2
O→HCOOH + 2H
HCOOH→CO
2
+ 2H
Metylotrofy nie mogą asymilować CO
2
. Jako źródło węgla wykorzystują takie
związki jak metanol czy aldehyd mrówkowy. Są tu jednak wyjątki np.
Pseudomonas oxalaticus, bakteria utleniająca kwas mrówkowy. Organizm ten
można zaliczyć do autotrofów, gdyż produkt utlenienia mrówczanu - CO
2
może być
wykorzystywany jako źródło węgla do syntezy własnych związków organicznych.
Strona 57
Współczynnik oddechowy
(zwany również ilorazem oddechowym)
Współczynnik oddechowy
-
stosunek liczby moli produkowanego CO
2
do
zużywanego O
2
w procesie oddychania lub stosunek objętości wydalonego
w procesie oddychania dwutlenku węgla do objętości pobranego tlenu.
RQ = CO
2
/ O
2
Wielkość współczynnika oddechowego zależy od rodzaju
substratu oddechowego oraz od charakteru procesu oddechowego:
Jeśli całkowitemu utlenieniu ulega glukoza lub inny cukier to
RQ=1(6CO
2
/6 O
2
, zgodnie z podanym równaniem).
C
6
H
12
O
6
+ 6O
2
→6CO
2
+ 6H
2
O
Gdy substratem oddechowym jest związek bardziej
utleniony, kwas organiczny, wówczas RQ > 1.
Podczas utleniania bardziej zredukowanych związków, takich
jak kwasy tłuszczowe (w porównaniu z cukrami uboższe w tlen, a
bogatsze w wodór –wymagają dodatkowego utlenienia) lub białka
RQ< 1. Współczynnik oddechowy wielu lipidów wynosi 0,7; a białek
0,8.
Mniejsza od jedności wartość współczynnika oddechowego
nie zawsze oznacza, że substratem oddechowym jest związek silnie
zredukowany. Taką wartość może również przybierać RQ podczas
niecałkowitego utlenienia cukru:
2C
6
H
12
O
6
+ 11O
2
→2(COOH)
2
+ 8CO
2
+ 10 H
2
O RQ=0,73 (8
CO
2
/ 11O
2
) Niezupełne utlenienie cukru
może wystąpić np. w mięsistych owocach, wskutek czego
nagromadzają się w nich kwasy organiczne. Bardzo małe wartości
RQ (ok. 0,2) są charakterystyczne dla sukulentów z powodu
ponownego włączania CO
2
, który powstaje w procesie oddechowym
do kwasów organicznych. Jeśli natomiast oddychanie odbywa się w
warunkach ograniczonego dostępu tlenu, to dominującym procesem
staje się fermentacja i stosunek CO
2
/ O
2
osiąga duże wartości, gdy
całkowicie brak tlenu pojęcie RQ traci sens.
ODDYCHANIE TLENOWE
Oddychanie tlenowe- jest wielostopniowym procesem utleniania
substratu związanym z wytwarzaniem energii użytecznie
metabolicznej.
Chociaż substratem w reakcji oddychania mogą być wszystkie
związki organiczne obecne w komórkach, najczęściej ogólną reakcję
oddychania komórkowego zapisuje się dla utleniania cukru – glukozy
w obecności tlenu:
C
6
H
12
O
6
+ 6O
2
→ 6CO
2
+ 6H
2
O
Energia uwolniona w procesie utleniania związków organicznych pojawia
się częściowo w postaci związku wysokoenergetycznego – ATP, który
może być wykorzystany do przeprowadzania reakcji chemicznych
zachodzących w komórce lub do poruszania organizmu np. w tkance
mięśniowej. Proces produkcji ATP nie przebiega ze 100% sprawnością i
część energii uwalniana jest w postaci ciepła.
Poza węglowodanami organizmy w procesie oddychania mogą
utleniać tłuszcze oraz białka, a po bardziej złożonych modyfikacjach
także pozostałe związki organiczne.
W przypadku najczęściej występującego substratu - glukozy,
oddychanie można podzielić na trzy główne etapy:
1) Glikoliza- przebiega w cytoplazmie ( polega na częściowym
utlenieniu glukozy do pirogroninu)
2) Cykl kwasów tri karboksylowych - odbywa się w
mitochondrialnej matriks (tylko jeden enzym dehydrogenaza
bursztynianowa jest związana z wewnętrzną błoną
mitochondrialną).polega na całkowitym utlenieniu pirogronianu do
dwutlenku węgla.
3) Łańcuch oddechowy - mitochondrium (wewnętrzna błona
mitochondrialna) polega na utlenieniu nukleotydów (NADH, FADH
2
)
pochodzących z glikolizy i cyklu Krebsa.
Strona 58

Glikoliza nazywana także szlakiem Embedena-Meyerhofa-
Parnasa, jest główną drogą katabolizmu heksoz pochodzących z rozkładu
materiałów zapasowych. Proces ten zachodzi zarówno w warunkach
beztlenowych jak i tlenowych, ale tlen nie bierze w nim udziału.
W pierwszym etapie glikolizy glukoza lub inna heksoza ulega fosforylacji.
Reakcję tę przeprowadza enzym – heksokinaza , zużywając cząsteczkę ATP(w
postaci kompleksu z jonem dwuwartościowym, zazwyczaj magnezem)- reakcja
nieodwracalna. Powstała cząsteczka glukozo-6-fosforanu przekształcana jest
do fruktozo-6-fosforanu przez izomerazę heksozofosforanową . Reakcja ta
jest odwracalna. W podobny sposób do fruktozo-6-fosforanu mogą być
przekształcane inne fosfoheksozy. Fruktoza, która jest produktem rozkładu często
występującego u roślin cukru zapasowego, sacharozy, jest przekształcana
bezpośrednio do fruktozo-6-fosforanu poprzez przyłączenie reszty fosforanowej z
ATP przez fruktokinazę. Wytworzony fruktozo-6-fosforanu ulega fosforylacji w
pozycji 1 katalizowanej przez 1-fosfofruktokinazę (ATP-fosfofruktokinazę) ,
co prowadzi do powstania fruktozo-1,6-bisfosforanu. Podobnie jak przy
fosforylacji glukozy zużywana jest cząsteczką ATP, a reakcja jest
nieodwracalna. W komórkach roślinnych przekształcenie fruktozo-6-fosforanu do
fruktozo-1,6-bisfosforanu może być także przeprowadzane przez 1-
fosfotransferazę pirofosforan – fruktozo-6-fosforan (PPi-fosfofruktodikinaza). W
tym przypadku reszta fosforanowa pochodzi z pirofosforanu, a reakcja jest
odwracalna. Aktywność PP-fosfofruktodikinazy jest większa w tkankach
intensywnie rosnących. W komórkach o stosunkowo wolnym metabolizmie
przeważa aktywność ATP-fosfofruktokinazy. Utworzenie 1 cząsteczki fruktozo-1,6-
bisfosforanu z glukozy lub fruktozy wymaga zużycia dwóch cząsteczek ATP, jeśli
odbywa się z udziałem ATP-fosfofruktokinazy i jednej cząsteczki ATP jeśli
zaangażowany jest szlak PPi-fosfofruktokinazy.
Powstały fruktozo-1,6-bifosforan jest rozszczepiony na dwie cząsteczki: aldehyd
3-fosfoglicerynowy i fosfodihydroksyaceton. Reakcję katalizuje aldolaza
fruktozobisfosforanowa . Ufosforylowane triozy łatwo przechodzą jedna w drugą
pod działaniem izomerazy triozofosforanowej. Powstanie dwóch trioz jest
końcem pierwszego etapu glikolizy.
Drugi etap glikolizy dostarcza użytecznej energii w postaci NADH i ATP.W
drugim etapie aldehyd 3-fosfoglicerynowy zostaje utleniony do 1,3-
bisfosfoglicerynianu. Reakcję tę katalizuje dehydrogenaza aldehydu 3-
fosfoglicerynowego . Energia wyzwolona podczas utleniania aldehydu 3-
fosfoglicerynowego wystarcza do zredukowania cząsteczki NAD
+
do NADH oraz
ufosforylowania powstającego kwasu 1,3-bisfosfoglicerynowego przez
przyłączenie fosforanu nieorganicznego. Fosfodihydroksyaceton także wchodzi w
opisaną reakcję, po odwracalnym przekształceniu do aldehydu 3-
fosfoglicerynowego przez izomerazę triozofosforanową . Kwas 1,3-
bisfosfoglicerynowy ma dużą energię swobodna wiązania fosforanowego i jest
dobrym donorem fosforu. Kwas ten traci jedną z grup fosforanowych, przekazując
ją na ADP. Reakcję przeniesienia fosforanu na ADP przeprowadza kinaza
fosfoglicerynianowa, co prowadzi do powstania cząsteczki ATP (fosforylacja
substratowa) oraz 3-fosfoglicerynianu. Związek ten może być łatwo
przekształcony do 2-fosfoglicerynianu w odwracalnej reakcji katalizowanej przez
mutazę fosfoglicerynianu. 2-fosfoglicerynian w kolejnej odwracalnej reakcji
zostaje przekształcony w fosfoenolopirogronian (PEP) przez enolazę , która
odłącza cząsteczkę wody. Energia zawarta w fosfoenolopirogronianie zostaje
wykorzystana do syntezy kolejnej cząsteczki ATP (fosforylacja substratowa)w
ostatniej reakcji nieodwracalnej glikolizy katalizowanej przez enzym, kinazę
pirogronianow, której efektem działania jest powstanie ostatecznego produktu
glikolizy: pirogronianu.(W efekcie zachodzenia szlaku glikolitycznego jedna
cząsteczka glukozy przekształcana jest do dwóch cząsteczek pirogronianu,
zużywane są dwie cząsteczki ATP, a powstają 2 cząsteczki NADH oraz 4
cząsteczki ATP. Powstające w procesie glikolizy ATP jest efektem przenoszenia
reszty fosforanowej z substratu na ADP przez odpowiednie enzymy i nosi nazwę
fosforylacji substratowej.)
Strona 59
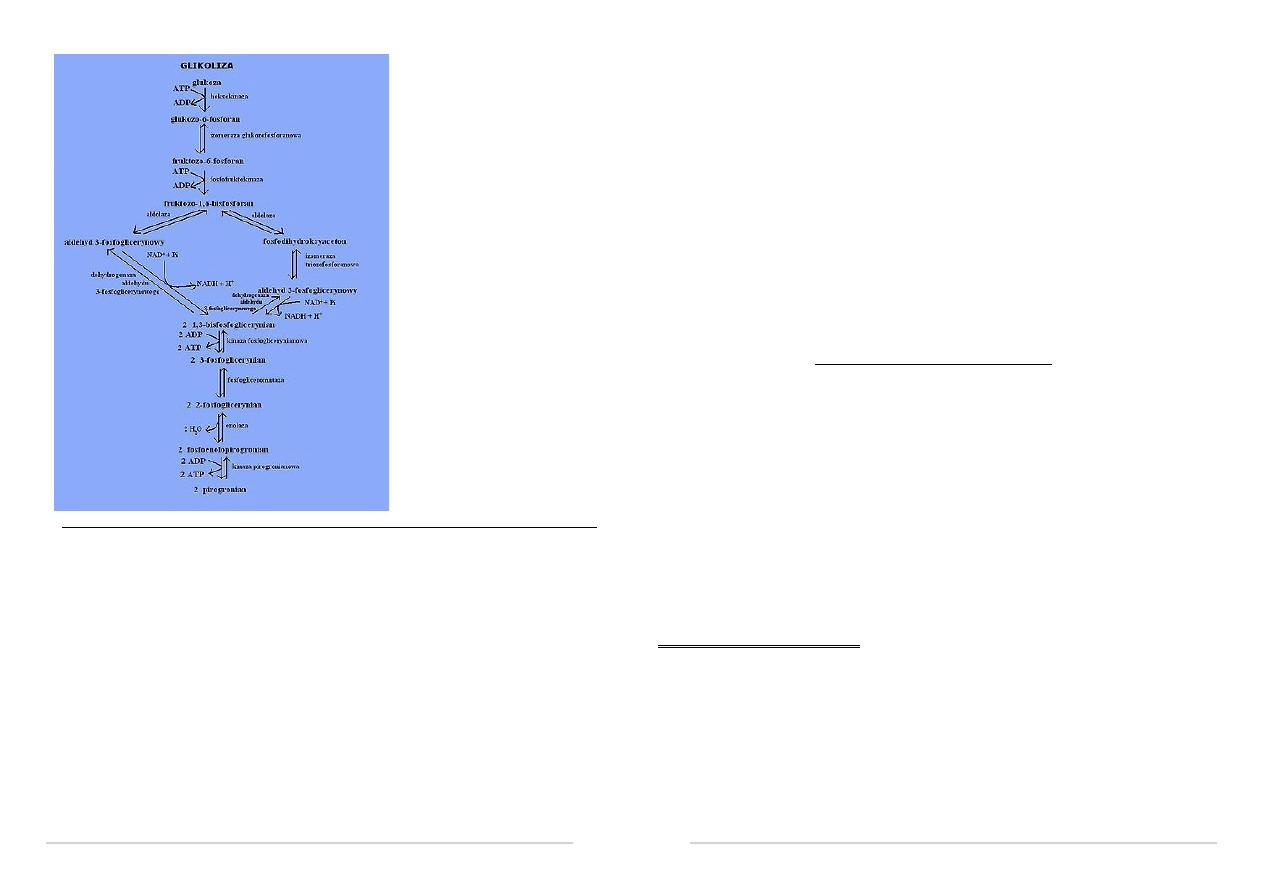
Oksydacyjny szlak pentozofosforanowy i jego powiązania z glikolizą
Glukoza może zostać utleniona także inną drogą niż opisana wyżej
glikoliza. W cytozolu komórki glukoza może zostać przekszatłcona w rybulozo-5-
fosforan w oksydacyjnym szlaku pentozofosforanowym. Metabolity tego szlaku są
wspólne z metabolitami glikolizy, dzięki czemu zwiększa się ilość glukozy
utlenianej w ogólnym metabolizmie oddechowym.
Podobnie jak w glikolizie, pierwsza reakcja polega na ufosforylowaniu
glukozy w pozycji 6. Powstały glukozo-6-fosforan przekształcany jest do 6-
fosfoglukonolaktonu przez dehydrogenazę glukozo-6-fosforanu . W reakcji tej
redukcji ulega cząsteczka NADP
+
i powstaje NADPH. 6-fosfoglukonolakton
przekształcany jest do 6-fosfoglukonianu poprzez przyłączenie cząsteczki H
2
O
przez laktonazę 6-fosfoglukonianu . Powstały 6-fosfoglukonian zostaje
przekształcony do związku pięciowęglowego poprzez dekarboksylację przy
jednoczesnej redukcji kolejnej cząsteczki NADP
+
do NADPH. Reakcję
przeprowadza dehydrogenaza 6-fosfoglukonianu , a powstaje w niej rybulozo-5-
fosforan. Opisany szereg reakcji określany jest jako faza oksydacyjna szlaku
pentozofosforanowego.
W kolejnych reakcjach rybulozo-5-fosforan może zostać przekształcony do
związków włączanych w glikolizę. Z rybulozo-5-fosforanu powstaje rybozo-5-
fosforan, w reakcji katalizowanej przez izomerazę rybozo-5-fosforanu , lub
ksylulozo-5-fosforan w reakcji katalizowanej przez epimerazę rybulozo-5-fosforanu
. Poprzez przenoszenie fragmentów łańcucha węglowego pomiędzy rybozo-5-
fosforanem a ksylulozo-5-fosforanem powstaje sedoheptulozo-7-fosforan oraz
aldehyd 3-fosfoglicerynowy. Reakcje przeprowadza transketolaza , enzym
przenoszący dwuwęglowy fragment z ketozy na aldozę. Aldehyd 3-
fosfoglicerynowy oraz sedoheptulozo-7-fosforan biorą udział w kolejnej reakcji
przeprowadzanej przez transaldolazę , w wyniku której powstają fruktozo-6-
fosforan i erytrozo-4-fosforan. Oba wytworzone związki mogą zostać
przekształcone przez transketolazę do aldehydu 3-fosfoglicerynowego i ksylulozo-
5-fosforanu.
Dwa spośród metabolitów opisanych przekształceń są jednocześnie
związkami biorącymi udział w glikolizie i mogą być w nią włączane. Są to aldehyd
3-fosfoglicerynowy oraz fruktozo-6-fosforan.
Dekarboksylacja pirogronianu
Powstały w glikolizie pirogronian w komórkach eukariotycznych jest
transportowany do matriks mitochondrialnej przez przenośnik znajdujący się w
błonie mitochondrialnej. W matriks mitochondrialnej pirogronian jest oksydacyjnie
dekarboksylowany przez kompleks enzymatyczny dehydrogenazy
pirogronianowej. W jego skład wchodzi wiele kopii pięciu różnych enzymów. Są to
dehydrogenaza pirogronianowa (PDH) , acetylotransferaza dihydrolipoamidowa i
dehydrogenaza dihydrolipoamidowa przekształcające pirogronian do acetylo-CoA
oraz kinaza dehydrogenazy pirogronianowej i fosfataza P-PDH, które poprzez
odwracalną fosforylację dehydrogenazy pirogronianowej regulują aktywność
całego kompleksu. Cała reakcja przebiega wg równania:
pirogronian + CoA + NAD
+
→ Acetylo-CoA + NADH + CO
2
+ H
+
Jednocześnie z dekarboksylacją, która prowadzi do powstania cząsteczki
CO
2
, redukcji ulega jedna cząsteczka NAD
+
, a dwuwęglowy fragment łańcucha
pirogronianu przenoszony jest na koenzym A.
Cykl kwasu cytrynowego:
Powstały na skutek dekarboksylacji pirogronianu acetylo-CoA
jest substratem dla kolejnego etapu oddychania: cyklu Krebsa –
szeregu reakcji biochemicznych zachodzących w matriks
mitochondrialnej. W reakcjach tych ze związków organicznych
wytwarzany jest CO
2
oraz związki wysokoenergetyczne w postaci
NADH, FADH
2
oraz GTP lub ATP.
W pierwszej reakcji reszta acylowa z acetylo-CoA
przyłączana jest do cząsteczki szczawiooctanu przez enzym
Strona 60

syntazę cytrynianową . W wyniku tej reakcji powstaje cząsteczka
cytrynianu oraz odtwarzany jest koenzym A. Cytrynian
przekształcany jest do izocytrynianu przez akonitazę. Reakcja ta
jest odwracalna, a jej produktem pośrednim jest
cis-akonitan – związany z cząsteczka enzymu. Izocytrynian
zawierający sześć atomów węgla ulega kolejno utlenieniu i
dekarboksylacji przeprowadzanej przez dehydrogenazę
izocytrynianową . W wyniku tej reakcji powstaje cząsteczka α-
ketoglutaranu, określanego także 2-oksoglutaranem, cząsteczka
CO
2
oraz NAD
+
jest redukowany do NADH. Pięciowęglowy α-
ketoglutaran (2-oksoglutaran) ulega kolejnej dekarboksylacji
przeprowadzanej przez kompleks enzymatyczny dehydrogenazy
α-ketoglutaranowej . W tej reakcji również powstaje CO
2
i ulega redukcji kolejna cząsteczka NAD
+
, a czterowęglowy produkt
zostaje przeniesiony na koenzym A, tworząc bursztynylo-CoA.
Powstały bursztynylo-CoA rozkładany jest na bursztynian i
cząsteczkę koenzymu A, w wyniku reakcji hydrolizy. Reakcję tę
katalizuje syntetaza bursztynylo-CoA, a energia wyzwalana
podczas reakcji pozwala ufosforylować cząsteczkę GDP do GTP w
mitochondriach cześci zwierząt lub ADP do ATP w mitochondriach
pozostałych organizmów . Podobnie jak w glikolizie, GTP lub ATP
powstaje na drodze fosforylacji substratowej. W kolejnej
(odwracalnej) reakcji bursztynian ulega dehydrogenacji
przeprowadzanej przez dehydrogenazę bursztynianową – jedyny
enzym cyklu, który nie jest białkiem rozpuszczalnym, lecz
osadzonym w wewnętrznej błonie mitochondrialnej, zawierającym
grupę prostetyczną w postaci FAD. Podczas przekształcania
bursztynianu do fumaranu dinukleotyd flawinoadeninowy ulega
redukcji, przechodząc w FADH
2
. Fumaran ulega przekształceniu do
jabłczanu poprzez przyłączenie cząsteczki H
2
O katalizowane przez
fumarazę . Z jabłczanu odtwarzany jest pierwszy związek cyklu
– szczawiooctan. Reakcję katalizuje dehydrogenaza
jabłczanowa . Powstaje w niej ostatnia, trzecia, cząsteczka NADH
wytwarzana w jednym obrocie cyklu. Dwie ostanie reakcje są
odwracalne, a powstały szczawiooctan może przyłączyć kolejną
resztę acylową.
Szczególne cechy cyklu kwasu cytrynowego w roślinach:
•
fosforylacja substratowa dostarczająca ATP w reakcji
syntetazy bursztynylo- CoA
•
oksydacyjna dekarboksylacja jabłczanu, reakcja ta zachodzi
pod wpływem specyficznego enzymu dehydrogenazy
jabłczanowej dekarboksylującej zależnej od NAD
+
.
Sumaryczny wzór cyklu Krebsa to:
acetylo-CoA + GDP + P
i
+ 3NAD
+
+ FAD + 2H
2
0 → koenzym-A + GTP + 3NADH + 3H
+
+
FADH
2
+ 2CO
2
Podczas jednego, pełnego obrotu cyklu Krebsa powstają 3
cząsteczki NADH, jedna cząsteczka FADH
2
i jedna cząsteczka GTP.
Najbardziej wszechstronnym nośnikiem energii w komórce jest ATP. GTP
jest łatwo zamieniany na ATP przez odpowiedni enzym. Natomiast NADH i
FADH
2
biorą udział w mitochondrialnym łańcuchu oddechowym -
przemianie, która zamienia energię tych zredukowanych związków na
energię wiązań ATP. Niezbędnym uczestnikiem łańcucha oddechowego
jest tlen.
Jedna cząsteczka NADH pozwala wyprodukować 3 cząsteczki ATP,
a jedna cząsteczka FADH
2
- 2 cząsteczki ATP. Nietrudno więc obliczyć, że
jeden pełny obrót cyklu Krebsa pozwala wytworzyć 12 cząsteczek ATP -
uniwersalnego nośnika energii dla komórki (3 x 3 + 1 x 2 + 1 = 12).
Strona 61

Łańcuch oddechowy:
NADH wytworzony podczas glikolizy oraz NADH i FADH
2
powstające w cyklu kwasu cytrynowego zostają w warunkach tlenowych
ostatecznie utlenione przez O
2
.Proces ten jest związany z dużą zmianą
energii swobodnej, której część zostaje zużyta do produkcji ATP z ADP i Pi
w procesie fosforylacji oksydacyjnej zredukowane nukleotydy redukują tlen
cząsteczkowy do wody za pośrednictwem przenośników elektronów i
protonów uszeregowanych w mitochondrialny łańcuch transportu
elektronów. Składniki tego łańcucha są umiejscowione w wewnętrznej
błonie mitochondrialnej i zgrupowane w cztery kompleksy białkowe z
których pierwszy odbiera elektrony z NADH, drugi z FADH
2,
zaś dwa
następne uczestniczą w dalszym przekazywaniu elektronów na tlen.
Oprócz wielopodjednostkowych kompleksów, w łańcuchu funkcjonują dwa
niskocząsteczkowe przenośniki elektronów: ubichinon (UQ), który może
przemieszczać się w błonie, oraz cytochrom c, poruszający się w fazie
wodnej, przestrzeni międzybłonowej (ubichinon jest 1,4-benzochinonem z
poliprenylowym łańcuchem bocznym zawierającym 9-10 jednostek
izoprenoidowych, który może odwracalnie przechodzić z formy utlenionej w
zredukowaną - ubichinol: UQ+2e
-
+2H
+
↔UQH
2
Strona 62

Ubichinon podobnie jak plastochinon jest związkiem hydrofobowym
rozpuszczalnym w lipidach skutkiem czego może dyfundować wewnątrz
błony tworząc pulę nie związaną z żadnym konkretnym białkiem, i-
podobnie jak plastochinon w błonie tylakoidu – działać jako ruchomy
przenośnik redoks między białkowymi kompleksami łańcucha transportu
elektronów.
Budowa kompleksów łańcucha oddechowego u roślin
•
Kompleks I.
Dehydrogenaza NADH utlenia NADH i redukuje ubichinon
miejsce wiązania NADH znajduje się po stronie matrix dlatego utleniany
jest tylko NADH powstały w cyklu kwasy cytrynowego . W skład
kompleksu wchodzą FMN oraz 3-4 białka zawierające centra Fe-S.
Dehydrogenaza NADH składa się z dwóch mniejszych kompleksów
dających się łatwo rozdzielić: hydrofobowego wbudowanego w błonę i
hydrofilowe sterczącego z błony po stronie matrix.
•
KompleksII.
występuje również flawina FAD i 3 centra Fe-S, na
cząsteczkę białka przypada większa ilość atomów żelaza i siarki.
Częścią tego kompleksu jest enzym cyklu Krebsa dehydrogenaza
bursztynianowa. Elektrony z utlenionego bursztynianu kolejno redukują
FAD i centra Fe-S aby ostatecznie przejść na ubichinon. UQH
2
przekazuje elektrony z pierwszych dwóch kompleksów na 3 kompleks,
który jest oksydoreduktazą ubichinon :cytochromu c.Cytochromy są
białkami zawierającymi żelazo w pierścieniu porfirytowym.
•
Kompleks III
- jest dimerem. Każdy z tworzących go monomerów
zbudowany jest z wielu podjednostek : dwóch cytochromów typu b i
jednego typu c
1,
białka zawierającego centrum Fe-S i kilku innych
polipeptydów. Jeden elektron z UQH
2
zostaje przekazany na cytochrom
c przez białko zawierające Fe-S i cytochrom c
1,
zaś drugi przeniesiony
zostaje przez dwa cytochromy typu b, do centrum redukującego UQ.
Cytochrom c redukowany przez kompleks III jest jedynym białkiem
mitochondrialnego łańcucha transportu , nie wbudowanym w błonę.
Jest to małe, ruchliwe, hydrofilowe białko poruszające się po
zewnętrznej powierzchni wewnętrznej błony mitochondrialnej i
przenoszące elektrony między kompleksami III i IV.
•
Kompleks IV.
Oksydaza cytochromowa tzw. oksydaza końcowa
(terminalna) redukuje cząsteczkę tlenu do dwóch cząsteczek wody w
procesie czteroelektronowym. Kompleks IV zbudowany jest z7- 9
polipeptydów, a jego cztery centra redukcji leżą w obrębie podjednostek
kodowanych w genomie mitochondrialnym. Elektrony do redukcji
pobierane są do cytochromu c po cytozolowej stronie błony wewnętrznej i
przekazywane na cząsteczkę tlenu znajdującą się po stronie matriks. W
redukcji tej pośredniczą dwa centra miedziowe oraz dwa cytochromy typu
a.W tym miejscu łańcucha transporty elektronów działają znane inhibitory
oddychania mitochondrialnego: azydek, cyjanek i tlenek węgla, które
konkurują z tlenem o elektrony.
•
Dodatkowe kompleksy:
Zewnętrzne dehydrogenazy NAD(P)H umiejscowione na zewnętrznej
powierzchni wewnętrznej błony mitochondrialnej.
Utleniają one NADH i NADPH pochodzące z cytozolu.
Po stronie matriks, oprócz miejsca wiązania NADH w kompleksie I
występuje dodatkowa dehydrogenaza NADH, nie wrażliwa na inhibitory
kompleksu pierwszego.
Oksydaza alternatywna.
Wewnątrz błony mitochondrialnej (u eukariontów) lub w błonie
komórkowej (u bakterii) następuje utlenianie NADH do NAD
+
.
Uwolnione elektrony uczestniczą w łańcuchu oddechowym, aby
napędzić przeniesienie protonów w poprzek błony przez składające
się na ten łańcuch odpowiednie przenośniki (pompy). W
chloroplastach i błonach fotosyntetyzujących organizmów
prokariotycznych protony przenoszone są dzięki energii uzyskanej
poprzez pochłonięcie kwantów światła przez odpowiednie
kompleksy.
ATP wytwarzane jest z ADP i P
i
(reszty ortofosforanowej) w
wyniku działania syntazy ATP. Rotacja jej odpowiedniego segmentu
umożliwia syntezę ATP. Energia niezbędna do syntezy dostarczana
jest przez gradient elektrochemiczny.
Strona 63
Znaczenie oddychania: dostarcza energii potrzebnej do normalnego
funkcjonowania komórki dostarcza materiałów wyjściowych do syntezy
podstawowych składników komórkowych, na przykład acetylo-CoA
Budowa i działanie aparatów szparkowych.
Aparaty szparkowe składają się z dwóch komórek
szparkowych(zamykających), które zawierają chloroplasty i różnią się
znacznie od pozostałych komórek skórki. Pomiędzy komórkami
szparkowymi istnieje przestwór między komórkowy- por szparki- łączący
system wentylacyjny liścia z atmosferą.
Komórki szparkowe oglądane z góry mają najczęściej kształt nerkowaty ich
ściany graniczące ze szparką są grubsze, ściany zaś znajdujące się po
przeciwnej stronie – cieńsze. Przy wzroście turgoru w komórce ściany
cieńsze „rozdymają się”, wskutek czego kształt komórek staje się bardziej
„wygięty” i szparka powiększa się. W razie zmniejszania turgoru
przeciwnie- komórki szparkowe wyprostowują się ich ściany schodzą się
razem zamykając szparkę.
Aparaty szparkowe u traw mają odmienną budowę. Komórki zamykające
są wydłużone, przy czym partie środkowe są wąskie i silnie zdrętwiałe,
podczas gdy ich końce są pęcherzykowato rozszerzone i cienkościenne.
Wzrost turgoru powoduje zwiększenie średnicy pęcherzykowatych
zakończeń, wskutek czego środkowe zdrewniałe partie odchylają się od
siebie, poruszając w ten sposób otwór. Przy zmniejszaniu turgoru zbliżają
się one do siebie i szparka się zamyka.
Pomimo różnic w budowie zasada działania aparatów szparkowych jest taka
sama: komórki mają nierównomiernie zgrubiałe ściany i dzięki temu zmiana
turgoru wywołuje zmianę ich kształtu. Jest wiele czynników wpływających na stan
aparatów szparkowych. Stopień rozwarcia aparatów szparkowych zależy od
warunków zewnętrznych. Głównym czynnikiem, który wywołuje otwieranie
szparek jest światło. Reakcje ta można uznać za celową ponieważ otwarcie
szparek umożliwia wnikanie do wnętrza liścia CO2, niezbędnego w procesie
fotosyntezy przebiegającego jedynie na świetle. W ciemności kiedy fotosynteza nie
zachodzi szparki zamykają się, chroniąc roślinę przed nadmierną utratą wody.
Ponadto na stan aparatów szparkowych wpływa stężenie CO2,zawartość wody w
liściach , temperatura i regulatory wzrostu.
Hipoteza wyjaśniająca ruch aparatów szparkowych
-Pod wpływem światła CO2 zostaje zużyty w procesie fotosyntezy. Zmniejsza się
więc ilość kwasu węglowego, co powoduje zmianę odczynu komórki z kwaśnego
pH=5 w ciemności, na obojętny na świetle. Odczy obojętny jest optymalny dla
enzymu fosforylazy, który przeprowadza rozpad skrobi na glukozę. Zatem na
świetle skrobia rozpada się na glukozę, przy czym z jednej cząsteczki skrobi
powstają tysiące cząsteczek glukozy. Pociąga to za sobą wzrost potencjału
osmatycznego komórek, a tym samym wzrost turgoru. Podwyższenie turgoru
powoduje zaś, jak wspomniano, otwieranie się aparatów szparkowych. W
ciemności natomiast, wskutek procesów oddechowych, zwiększa się stężenie
CO2 . Wyniku procesów karboksylacyjnych, tworzą się grupy kwasowe(-COOH).
Komórka zakwasza się , a w następstwie glukoza przekształca się na skrobię,
wskutek czego turgor maleje i szparka zamyka się. Nie jest to jedyna hipoteza
starająca wyjaśnić ruch aparatów szparkowych.
Według innych poglądów ruchy te są związane z kationami K, mianowicie
podwyższenie turgoru w komórkach szparkowych i , co za tym idzie , otwieranie
się aparatów szparkowych ma być, zgodne z nową hipotezą , następstwem
pobieraniu a przez te komórki dużych ilości jonów potasu z otoczenia.; wszystkie
czynniki powodują otwieranie aparatów szparkowych (światło, obniżenie stężenia
CO2, kwas abscynowy.) prowadzą jednocześnie do znacznego nagromadzenia
potasu w komórkach szparkowych. I odwrotnie wszystkie czyniki powodujące
zamykanie szparek(ciemność, wzrost ztężenia CO2, kwas abscynowy) prowadza
jednocześnie do obniżenia zawartości potasu w komórkach szparkowych.
Zmniejsz się w tedy turgor i szparka się zamyka. Żadna z tych hipotez nie zgadza
się jednak ze wszystkimi obserwowanymi faktami. Zagadnienie mechanizmu ruchu
aparatów szparkowych nie jest więc rozwiązane.
Inne czyniki wpływające na ruch aparatów szparkowych;
•
-zawartość wody w liściach- w słoneczne, ciepłe dni często występuje w
liściach deficyt wody. Prowadzi tp do utraty turgoru w komórkach
szparkowych, co powoduje zamykanie się szparek.
•
-temperatura- w tem. Bliskiej 0C szparki pozostają zamknięte. Wzrost
temperatury, przy nie nie zmieniających się pozostałych czynnikach ,
powoduje otwieranie szparek. Dalszy wzrost temperatury ponad 25-30C
prowadzi dz zamykania szparek.
Strona 64
•
-regulatory wzrostu-w więdnących roślinach zwiększa się natężenie kwasu
abscynowego jest on przyczyną zamykania aparatów szparkowych
zapobiega w ten sposób dalszym stratą wody.
(Czerwiński str.79)
Aparaty szparkowe
- rola, rodzaj, budowa i działanie aparatów
szparkowych
.
Aparaty szparkowe składają się z dwóch komórek
szparkowych(zamykających), które zawierają chloroplasty i różnią się
znacznie od pozostałych komórek skórki. Pomiędzy komórkami
szparkowymi istnieje przestwór między komórkowy- por szparki- łączący
system wentylacyjny liścia z atmosferą.
Komórki szparkowe oglądane z góry mają najczęściej kształt nerkowaty ich
ściany graniczące ze szparką są grubsze, ściany zaś znajdujące się po
przeciwnej stronie – cieńsze.
U roślin wyższych wyróżniamy dwa typy komórek szparkowych. U traw i
kilku innych roślin jednoliściennych , np. u palm, komórki szparkowe mają
charakterystyczny kształt gimnastycznych ciężarów , zakończonych
bulwkami. Otwór szparkowy stanowi długą szczelinę, ulokowaną między
dwoma „drążkami”. Takie komórki szparkowe otoczone są paroma innymi
komórkami epidermy, określanymi jako komórki przyszparkowe, które
wymagają komórki szparkowe w regulacji rozwarcia szparki.
U roślin dwuliściennych i tych jednoliściennych, które nie należą do rodziny
traw, a także u mchów , paproci i roślin nagozalążkowych, komórki
szparkowe mają kształt nerkowatya otwór znajdujący się między nimi ma
przekrój owalny. U tych roślin często nie występują komórki przy
szparkowe i wówczas komórki otoczone są zwykłymi komórkami
epidermy. Charakterystyczna cechą budowy komórek szparkowych jest
nierównomierna grubość i specyficzna struktura ich ścian, związana z
układem mikrofibryli celulozowych. W zwykłych komórkach cylindrycznych
ułożone są poprzecznie w stosunku do głównej osi komórki, co umożliwia
rozciąganie komórki wzdłuż jej podłużnej osi. W nerkowatych komórkach
szparkowych mikrofibryle celulozowe rozchodzą się promieniście od
otworu szparkowego. W związku z tym obwód szparki zostaje
wzmocniony, a sama komórka wygina się na zewnątrz w trakcie
rozwierania szparki. U traw środkowe części komórek szparkowych
rozciągają się wówczas, gdy wzrasta objętość ich bulwkowatych
zakończeń, zddolnych do rozciągania się, co pozwala na rozszerzanie
leżącej miedzy nimi szczeliny.
Komórki szparkowe funkcjonują jako wielo czujnikowe zastawki hydrauliczne .
Reagują na zmiany czujników środowiska, takich jak natężenie i jakość światła,
temperaturę wilgotność względna powietrza, wewnętrzno komórkowe stężenie
CO2 oraz na zmiany stężenia hormonu- kwasu abscynowego. Rozwieranie się
aparatów szparkowych spowodowane jest spadkiem potencjału wody w
komórkach szparkowych na skutek reakcji związanych z fotosyntetycznym
metabolizmem węgla, transportem niektórych produktów fotosyntezy oraz jonów
potasu. W wyniku zmniejszania się potencjału wody w komórkach szparkowych
zaczyna się do nich przemieszczac woda z innych komórek epidermy. W miarę
dopływu wody wzrasta ciśnienie turgorowi w komórkach szparkowych.
Zróżnicowana grubość ich ścian sprawia, że otwór między nimi zaczyna się
rozwierać. Zamykanie się szparki zachodzi w wyniku utraty wody przez komórki
szparkowe do atmosfery(zamykanie hydropasywne) Reakcje te, indukowane np.
przez odwodnienie całego liścia i / lub zwiększoną podaż kwasu abscynowego
prowadzą do utraty turgoru w komórkach szparkowych, co jest bezpośrednia
przyczyną zamykania się szparki. Kwas abscynowy(ABA) jest stale syntezowany
w komórkach mezofilu i gromadzony w chloroplastach, a także wytwarzany w
komórkach korzenia. Pod wpływem słabego nawet odwodnienia liści lub korzeni
następuje wzmożenie syntezy ABA w tych organach, a także zachodzi
redystrybucja. W liściach ABA zostaje uwolniony z komórek mezofilu do apoplastu,
skąd przemieszcza się do komórek szparkowych. Z komórek korzenia
przemieszcza się do liści wraz z prądem transpiracji w soku ksylemu. Kwas
abscynowy może powodować zamykanie się szparek nawet wówczas, gdy nie
wystąpiły jeszcze zmiany potencjału wody w komórkach liścia. Hormon ten jest
więc przekaźnikem informacji o pogorszeniu się stosunków wodnych w korzeniu.
Zmiany transpiracji wywołane pogarszającym się w ciagu dnia uwodnieniem liści
powodują iż transpiracja zachodzi najszybciej gdy szparki są całkowicie rozwarte,
i najwolniej, gdy szparki są zamknięte. Podczas pełnego zamknięcia szparek
Strona 65
zachodzi tylko transpiracja kutykularna. W sytuacji częściowego rozwarcia szparek
inne czynniki mogą wpływać na intensywność transpiracji. Jeżeli np. warunki
atmosferyczne nie sprzyjają parowaniu wody, to transpiracja osiąga maksimum
wówczas, gdy szparki są tylko częściowo rozwarte. Jeśli jednak czynniki
zewnętrzne są dla parowania korzystne, to intensywność transpiracji rośnie wraz z
rozwarciem aparatów.
(Lewak str.179)
Organizacja strukturalna komórki roślinnej- cechy charakterystyczne.
Budowa błony komórkowej, cytoplazma podstawowa i struktury
cytoplazmatyczne, siateczka śródplazmatyczna ,aparaty Golgiego,
mikrociała –peroksysomy i giloksysomy, plastydy, mitochondria, jądro
komórkowe, wakuola, ściana komórkowa. Znajduje się to w Lewaku str.
21-50.
Akwaporyny roślinne- charakterystyka, rola w
komórce.
Woda w transporcie do wnętrza komórki musi pokonywać barierę
plazmolemmy, której wnętrze jest hydrofobowe. Dlatego też dobry i
szybki transport wody zapewniają kanały wodne zwane
akwaporynami- specjalne, integralne białka błonowe stanowiące
kanał dla przepływu wyłącznie cząsteczek wody w poprzek błony.
Obecność tych białek stwierdzono w plazmolemmie, a także w
tonoplaście.
Białka te:
Należą do rodziny konserwatywnych białek błonowych MIP
Mają konserwatywną sekwencję aminokwasów
Ich masa wynosi 26-30 kDa
Ich łańcuch polipeptydowy przenika sześciokrotnie prze błonę a
końce N- i C- wystają po cytoplazmatycznej stronie błony.
Światło poru kanału wodnego ma 0,15 nm – 0,2 nm
Nie przewodzą protonów, gdyż ich zwiększone stężenie zmniejsza
pH powodując zahamowanie kanałów akwaporynowych
(przylepienie się jonu hydroniowego do ściany kanału);
Duża wrażliwość na działanie soli rtęci i srebra
U roślin stwierdzono 2 rodzaje białek akwaporynowych:
1. W tonoplaście – γ- TIP – białka syntetyzowane konstytutywnie
przez cały okres życia rośliny;
2. W plazmolemmie – RD28 – białka indukcyjne syntetyzowane
tylko w odpowiedzi na odwodnienie komórki.
Funkcja Akwaporyny:
Transport i regulacja przepływu wody przez błonę;
Hydratacja ziaren pyłku;
Pęcznienie i kiełkowanie nasion.
Mechanizm wpływu fitochromu na
przepuszczalność błon komórkowych.
Fitochrom to barwnik o właściwościach absorpcji światła czerwonego.
W roślinach występuje on w dwóch formach molekularnych różniących się
między sobą pod względem ich własności spektralnych. P
r
pochłania
światło z pasma o długości 660 nm. (jasnoczerwone) i pod wpływem jego
działania przekształca się w formę P
fr
. Ta z kolei reaguje już na światło o
długości 730 nm. (daleka czerwień) i cechuje ją mała trwałość oraz
niewielka aktywność fizjologiczna, a właściwie to całkowitym jej brak. P
fr
może ulegać degradacji bądź ponownej konwersji do P
r
. Forma ta
odgrywa ważną rolę w kontroli kwitnienia zarówno roślin dnia krótkiego jak i
długiego - odpowiedni stosunek P
r
do P
fr
stanowi sygnał dla roślin do
syntezy odpowiednich czynników powodujących zakwitanie roślin.
Kwitnienie roślin polega na ich przejściu od fazy wegetatywnej do
generatywnej. Fitochrom sprawują kontrolę nad takimi procesami jak
Strona 66
kiełkowanie roślin, rozwojem ich łodyg oraz liści, syntezą antocyjanów itd.
Oprócz dwóch różnych form fitochrom ma także dwie postaci (phyA i
phyB), które różnią się pod względem wrażliwości na światło, tj. krytycznej
dawki powodującej przejście ich formy P
r
w P
fr
Pod względem
strukturalnym P
r
i P
fr
posiadają odmienną budowę strukturalną. Ogólnie
białko fitochromowe posiada dwa obszary: N-terminalny, który tworzy tzw.
"kieszeń" dla chromatoforu oraz C-terminalny w obrębie, którego to właśnie
dochodzi do zmian konformacyjnych w wyniku absorpcji odpowiedniej
dawki światła. Poza tym to właśnie C-koniec odpowiada za dimeryzację
fitochromu, który w takiej postaci ( dimeru) znajduję się kiedy nie jest
aktywny. Podczas fotokonwersji dochodzi do zmian w organizacji
przestrzennej fragmentu z chromatoforem, które następnie rzutują na
konformację części białkowej.
Fitochrom: fotokonwersja – proces
niskoenergetyczny, odwracaln
Synteza w ciemności
światło białe lub czerwone
660 nm (86%)
P
r
———————→
P
fr
660nm
←———————
730nm
daleka czerwień 730 nm (96%)
powolny rozpad
powolna przemiana
w ciemności
Rośliny SDP i LDP wykazują określone rytmy wrażliwości na światło
czerwone i daleką czerwień. Przy zakwitaniu są też ważne okresy nocy.
Reakcja fotoperiodyczna zależy od fitochrom, od tego jak następują
periodyczne okresy światła i ciemności w cyklu dobowym i od ich ilości.
MECHANIZM DZIAŁANIA
fitochromu
:
Hipotezy na temat mechanizmu funkcjonowania fitochromu wiążą jego
aktywność z wpływem funkcjonowania błon, na zlokalizowane w nich
pompy jonowe oraz na ekspresję genów. Mogą one działać na dwóch
różnych drogach biorąc udział w reakcjach typu:
szybkiego- przykładem takiej odpowiedzi rośliny na światło za sprawą
fitochromów jest ruch turgorowy w poduszkach liściowych Minosa pudica.
Efekt ten ma ścisły związek z aktywnością kanałów jonowych lub np.
hamujący wpływ światła czerwonego na wzrost wydłużeniowy łodygi
odbywający się w następujący sposób: P
fr
powoduje wypływ jonów
wapnia Ca
2+
np. z wodniczki i przejściowy wzrost ich stężenia w cytosolu;
Ca
2+
tworzy kompleks z kalmoduliną, ten stymuluje pompę
wapniową (Ca
2+
-ATPazę) w plazmolemie, wypływ Ca
2+
powoduje wzrost
jego stężenia w ścianie komórkowej, następuje zmniejszenie
elastyczności ściany i zahamowanie wydłużania się komórek w
międzywęźlach.
wolnego- wiąże się z regulatorowym wpływem fitochromów na
proces transkrypcji, gdyż jak wykazano fitochromy po połączeniu z
odpowiednimi białkami mogą dostawać się do jądra komórkowego.
Zatem fitochrom może powodować zmiany jedynie chwilowe (jak zmiana
przepuszczalności błon) oraz długotrwałe, do których zaliczamy m.in.
wydłużanie międzywęźli, kiełkowanie, kwitnienie czy tworzenie bulw oraz
cebul.
Liść jako organ fotosyntezy
- przystosowania anatomiczne i molekularne
•
Blaszka liściowa jest spłaszczona, dzięki czemu ma dużą powierzchnię
w stosunku do objętości. Umożliwia to nie tylko doskonałe
wykorzystanie padającej energii świetlnej lecz także zwiększa
powierzchnię absorpcyjną dla CO
2
•
Większość roślin lądowych wykształca liście o symetrii
grzbietobrzusznej, tzn. że górna część blaszki różni się budową
anatomiczną od części dolnej. Liście ekwifacjalne(nie wykazujące
symetrii grzbietobrzusznej) występują między innymi u roślin wodnych
zanurzonych, wielu drzew iglastych.
•
Od strony górnej i dolnej blaszka pokryta jest warstwa komórek
epidermalnych: jednowarstwowa epiderma (skórka) występuje u
większości mezofitów i higrofitów, natomiast epiderma kilkuwarstwowa
u kserofitów.
•
Skórka liścia jest zwykle przezroczysta dzięki czemu nie hamuje
dostępu światła do mezofilu złożonego z jednej lub kilku warstw
miękiszu palisadowego( u roślin światłolubnych warstwa ta jest
grubsza) oraz z luźno rozłożonych komórek miękiszu palisadowego.
Komórki miękiszu palisadowego mają kształt cylindryczny i zawierają
znaczną liczbę chloroplastów a rozbudowanie warstwy palisadowej
Strona 67

zależy w dużym stopniu od warunków świetlnych środowiska, np. u
roślin światłolubnych warstwa ta jest dużo grubsza niż u roślin
cieniolubnych.
•
Elementy przewodzące liścia rozmieszczone w nerwach liścia
doprowadzają do komórek wodę i sole mineralne a odprowadzają
wytworzone w procesie fotosyntezy produkty.
Strona 68
•
Komórki roślinne zawierają plastydy, z których tylko chloroplasty mają
zdolność do przeprowadzania procesu fotosyntezy. W chloroplastach
zawarte są barwniki takie jak karotenoidy (karoteny i ksantofile) oraz
fikobiliny pełniące funkcję barwników pomocniczych. Ważnymi
barwnikami są chlorofile należące do karotenoidów w tym chlorofil a i b.
Funkcją chlorofili (syntetyzowanych w plastydach) które
przeprowadzają fotosyntezę jest wychwytywanie kwantów światła i
przekazywanie energii wzbudzenia do centrum reakcji fotoukładu skąd
wybijane są elektrony, spożytkowane następnie w dalszych etapach
fotosyntezy. U roślin wyższych chlorofil występuje w dwóch odmianach:
niebieskozielony chlorofil a, absorbujący głównie światło fioletowe i
czerwone, oraz żółtozielony chlorofil b, absorbujący głównie światło
niebieskie i pomarańczowe.
•
Specyficzną budowę anatomiczną mają liście roślin, u których zachodzi
fotosynteza C4. U roślin tych, w związku z przestrzennym
rozdzieleniem wiązania dwutlenku węgla i syntezy węglowodanów,
wykształca się mezofil wieńcowy i mezofil C4. Ten pierwszy tworzy
pochwy okołowiązkowe, gdzie stężenie CO
2
przekracza 10–20 razy
stężenie tego gazu w innych komórkach mezofilu. W chloroplastach
komórek budujących te pochwy zachodzi cykl Calvina. Z kolei mezofil
C4 wypełnia pozostałą przestrzeń wewnątrz liścia i w jego komórkach
następuje wiązanie dwutlenku węgla.
•
Powierzchnia blaszki liściowej rzadko jest gładka, najczęściej pokrywa
ją warstwa włośników lub nalot woskowy.
•
Najczęściej na dolnej stronie blaszki położone są aparaty szparkowe
których które również zawierają chloroplasty
•
Do przystosowań liści do funkcji asymilacyjnej należy także ich
zdolność do wykonywania ruchów tropicznych - uzależnionych od
kierunku działania bodźca, którym jest światło. Zdolność tę określa się
mianem fototropizmu.
•
U roślin, u których blaszka uległa redukcji lub pełni inną funkcję niż
asymilacyjna, funkcję tę może przejąć spłaszczony ogonek liściowy,
nazywany wówczas liściakiem (fyllodium).
Budowa anatomiczna liści roślin wyższych
jako wyraz pełnionych funkcji
•
Liście asymilacyjne są zwykle spłaszczone grzbieto-brzusznie.
Do wyjątków należą liście spłaszczone bocznie (np. u kosaćca
Iris) lub cylindryczne (np. u wielu gatunków z rodzaju czosnek
Allium). Dolna strona liścia zwana jest odosiową lub grzbietową
(w pąku kwiatowym znajduje się na górze). Górna strona liścia
zwana jest doosiową lub brzuszną
•
Ze względu na kształt liście dzielą się na: nitkowate,
szczeciniaste, igłowate, równowąskie, lancetowate, klinowate,
trójkątne, rombowate, łopatkowate, jajowate, eliptyczne, okrągłe
(ogonek osadzony bocznie), tarczowate (ogonek osadzony
centralnie wobec blaszki). Ze względu na kształt i rodzaj nasady
blaszki liściowej wyróżnia się liście nerkowate, sercowate,
strzałkowate i oszczepowate. Do określeń kształtu dodaje się
często przedrostki precyzujące proporcję długości do szerokości
liścia, np. szeroko-, wąsko-, podłużnie- (lancetowaty, jajowaty)
lub odwrotnie jajowaty.
Liść asymilacyjny roślin okrytonasiennych tworzą najczęściej trzy
rodzaje tkanek:
Epiderma - okrywa górną (doosiową) i dolną (odosiową)
powierzchnię liścia. Zewnętrzne jej ściany pokryte są kutykulą, której
budowa, grubość, ilość wosków i pektyn jest zróżnicowana u
poszczególnych gatunków i w obrębie samej rośliny. Stałym
elementem budowy epidermy liści są szparki (lub aparaty
szparkowe). Jeżeli występują tylko po dolnej (grzbietowej) stronie
liścia – co u roślin zdarza się najczęściej - liść taki nazywany jest
hipsostomatycznym. U roślin jednoliściennych i w liściach
pływających szparki znajdują się na górnej powierzchni, a liść taki
nazywany jest epistomatycznym. Zagęszczenie szparek w epidermie
liścia jest bardzo zróżnicowane, wyższe u roślin światłolubnych,
niższe u cieniolubnych. Epiderma blaszki liściowej wykształca często
włoski, zwłaszcza na młodych liściach. Chronią one przed
żerowaniem drobnych roślinożerców mechanicznie lub chemicznie
Strona 69
jeśli zawierają wydzieliny. Komórki epidermy liści mają często falisty
zarys, co za sprawą turgoru i większej grubości ścian tych komórek w
stosunku położonych pod nimi, powoduje, że właśnie epiderma
nadaje odpowiednią sztywność liściom (o ile nie zawierają tkanek
wzmacniających). U niektórych roślin (rodziny morwowate,
pieprzowate, begoniowate) epiderma liścia może być
wielowarstwowa i zwykle pełni wówczas funkcję magazynującą wodę
lub ochronną, działając jak filtr świetlny. U roślin wodnych komórki
epidermy liści zawierają chloroplasty i pełnią funkcje asymilacyjne.
Zróżnicowane komórki epidermy liści występują u traw.
Mezofil - Składa się z miękiszu, u większości roślin podzielonego
na miękisz gąbczasty w dolnej części liścia i palisadowy w górnej.
Obejmuje zieloną tkankę liścia (chlorenchyma) wraz z pochwami
wiązkowymi otaczającymi wiązki przewodzące, sklereidy oraz
komórki układu wydzielniczego nie związane z epidermą). Liście nie
mające grzbieto-brzusznej budowy (jednakopowierzchniowe) mają
miękisz niezróżnicowany lub brak go w ogóle. Na przykład u
hydrofitów występuje tylko miękisz gąbczasty, zwykle w formie
aerenchymy. U kserofitów nierzadko miękisz palisadowy występuje
po obu stronach liścia, a miękiszu gąbczastego brak. Jednorodna
tkanka miękiszowa występuje także zazwyczaj w liściach traw i
iglastych. Specyficzną budowę anatomiczną mają liście roślin, u
których zachodzi fotosynteza C4. U roślin tych, w związku z
przestrzennym rozdzieleniem wiązania dwutlenku węgla i syntezy
węglowodanów, wykształca się mezofil wieńcowy i mezofil C4. Ten
pierwszy tworzy pochwy okołowiązkowe, gdzie stężenie CO
2
przekracza 10–20 razy stężenie tego gazu w innych komórkach
mezofilu. W chloroplastach komórek budujących te pochwy zachodzi
cykl Calvina. Z kolei mezofil C4 wypełnia pozostałą przestrzeń
wewnątrz liścia i w jego komórkach następuje wiązanie dwutlenku
węgla.
Wiązki przewodzące tworzą nerwację liścia. Liście mogą być
jednożyłkowe (np. u skrzypów i iglastych) lub wielożyłkowe. U roślin
okrytonasiennych wiązki tworzą użyłkowanie zamknięte. Dzięki temu
uszkodzenie (przecięcie) części wiązek powoduje zwykle obumarcie
tylko niewielkiej części liścia. Żyłki wychodzące od nasady blaszki
nazywane są pierwszorzędowymi i do nich należy też żyłka
centralna, zwykle najgrubsza. Pozostałe odgałęzienia stanowią żyłki
odpowiednio drugo- i trzeciorzędowe. Najdrobniejsze wiązki
zamykające sieć zwane są areolami.
Modyfikacje funkcjonalne liści
Liście jako organ fotosyntezujący
Najczęściej spotykana i determinująca budowę liści funkcja związana jest z
ich rolą w wykorzystywaniu energii świetlnej w procesie fotosyntezy. W tym
celu liść pochłania energię świetlną, pobiera dwutlenek węgla i
odprowadza asymilaty. Zwiększenie efektywności pochłaniania światła
zapewnia zwiększenie stosunku powierzchni do objętości liścia.
Liście jako organ obronny
Liście roślin zagrożonych żerowaniem roślinożerców wykształcają często
przystosowania chroniące roślinę przed zgryzaniem. Poza obroną
chemiczną, skutecznym sposobem utrudnienia dostępu drobnym
bezkręgowcom do miękkich tkanek jest pokrycie liścia gęstymi włoskami
(częste zwłaszcza na młodych liściach) lub grubą warstwą kutykuli. Na
krawędzi blaszki wykształcać się mogą kolce lub całe liście mogą ulegać
przekształceniu w ciernie. Specyficzny mechanizm obronny wykształciła
mimoza Mimosa. Po dotknięciu jej liści w ciągu 0,1 s podrażniony
(dotknięty) odcinek liścia stula listki, a ogonek liściowy zwiesza się. Ruch
ten (sejsmonastia) powodowany jest gwałtowną utratą turgoru w tzw.
poduszeczkach stawowych znajdujących się u nasady wszystkich członów
liścia. Przystosowanie to ma zrazić roślinożercę i zmniejszyć atrakcyjność
rośliny jako źródła pożywienia.
Liście biorące udział w rozmnażaniu
Zmodyfikowane liście odgrywają kluczową rolę w rozmnażaniu
generatywnym roślin, bowiem to właśnie one tworzą kwiat (listki okwiatu,
pręciki i słupki). U niektórych gatunków (np. wilczomleczy, w szczególności
u gwiazdy betlejemskiej) rolę powabni dla zwierząt zapylających pełnią
liście przykwiatowe (twory takie nazywane są liśćmi wabiącymi). Także
liście asymilacyjne mogą brać udział w rozmnażaniu, w ich wypadku
zawsze wegetatywnym. Roślina u nas uprawiana jako doniczkowa -
płodnolist (żyworódka) Bryophyllum tworzy na brzegu liścia łatwo
odpadające rozmnóżki. U rzeżuchy Cardamine diasporą może stać się
listek, który u nasady tworzy pączki i korzonki, po czym łatwo może odpaść
od reszty liścia. W okresie wiosennym można nierzadko obserwować takie
listki-diaspory rzeżuchy łąkowej pływające w rowach na łąkach
. W rodzaju
Strona 70
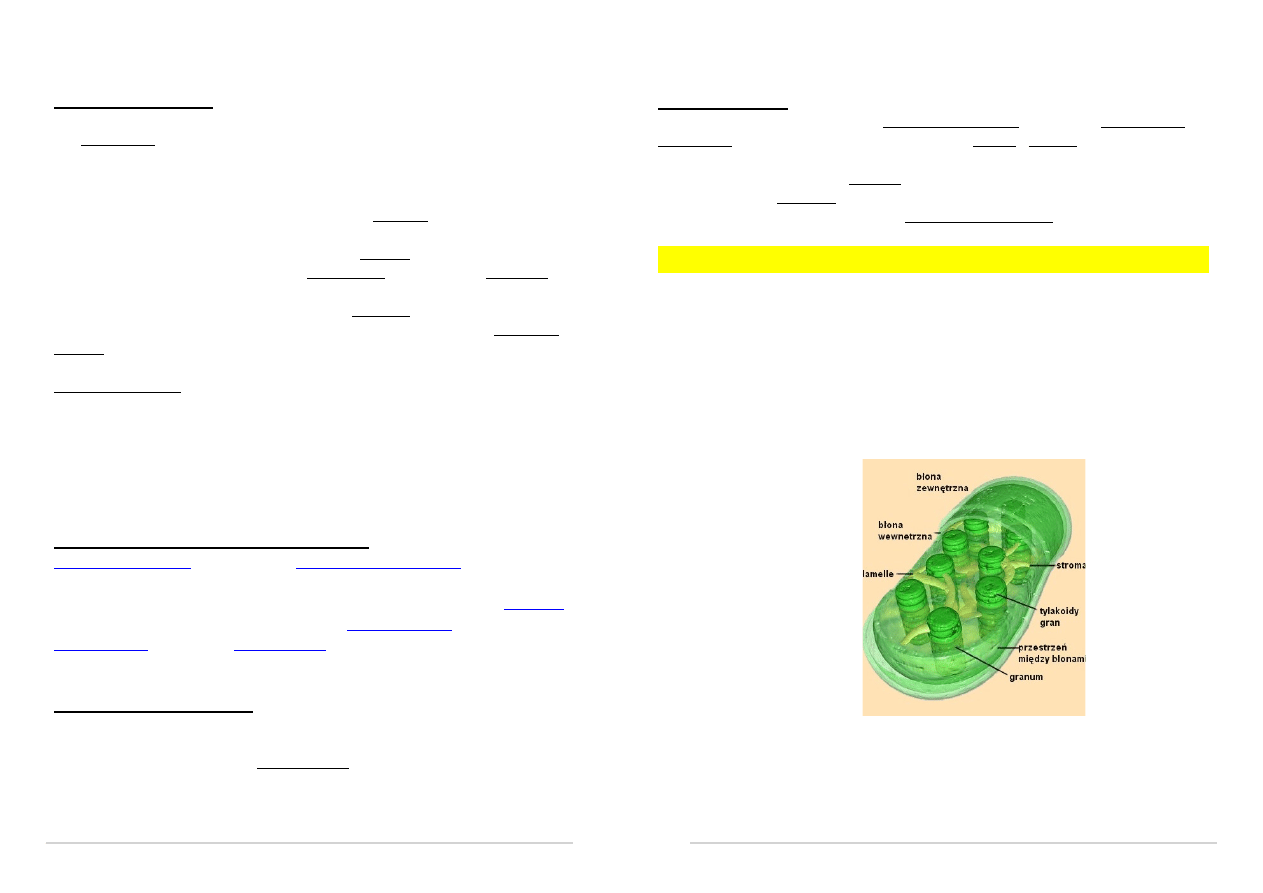
Liście kseromorficzne
Liście przystosowane do zminimalizowania transpiracji wodnej są typowe
dla kserofitów i innych roślin narażonych na szybką utratę wody.
Najbardziej wyraźną cechą liści kseromorficznych jest zmniejszenie
powierzchni liści w stosunku do ich objętości. Inne elementy budowy liści
kseromorficznych wynikające z przystosowania do specyficznych
warunków siedliskowych to: gruba warstwa kutykuli utrudniająca
transpirację na powierzchni epidermy, pełniąca taką samą funkcję warstwa
śluzu zasychająca w postaci błonki (np. u rezedy Reseda arabica) i często
spotykane gęste owłosienie (np. u dziewanny Verbascum i kocanek
Helichrysum). Inne przystosowania wiążą się z dodatkowym
wspomaganiem regulowanej transpiracji szparek. W sytuacjach niedoboru
wody u niektórych roślin dochodzi do zaczopowania szparki woskami lub
żywicą. U kserofitów szparki często są dodatkowo zagłębione w
powierzchni liścia, co zmniejsza transpirację nie wpływając istotnie na
wymianę gazową. W końcu cały liść ulega przekształceniom
zapobiegającym utracie wody poprzez zwijanie, składanie blaszki liściowej
lub wykształcanie liści o niewielkich rozmiarach. Liście zmniejszają także
transpirację chroniąc się przed nadmiernym nagrzaniem, co osiągają
odpowiednio zmieniając ustawienie względem światła słonecznego lub
okrywając powierzchnię liścia substancjami nabłyszczającymi ją (gł.
woskami), powodującymi odbijanie światła.
Liście chwytające i trawiące pożywienie
chwytania i trawienia pokarmu zwierzęcego. W reakcji na bodziec
mechaniczny włoski gruczołowate na liściu pułapkowym
naginają się ku źródłu podrażnienia (
). Liście pułapkowe
sejsmonastyczne umożliwiające schwytanie drobnych zwierząt.
Liście stanowiące podporę
U niektórych pnączy liście pełnią ważną funkcję mechaniczną umożliwiając
wspinanie się po innych roślinach. Ogonki liściowe lub liście częściowo lub
w całości przekształcone w wąs czepny owijają się wokół podpór
ułatwiając roślinie wyścig o dostęp do światła.
Liście spichrzowe
Najczęściej wyspecjalizowane liście spichrzowe gromadzą substancje
zapasowe lub wodę (tak jest na przykład u cebuli i aloesu). Specyficzny
spichlerz tworzą liście rośliny Dischidia rafflesiana – wyrastają one na
kształt worków, w których mrówki tworzą swe gniazda. Zgromadzony z
czasem w liściu detrytus odżywia roślinę, bowiem przez otwór na szczycie
worka roślina wpuszcza do niego korzeń przybyszowy.
Budowa chloroplastu:
o
chloroplast otoczony jest podwójną błoną biologiczną
o
błona wewnętrzna wpukla się tworząc lamelle
o
pęcherzyki utworzone z rozszerzeń lamelli to tylakoidy, tylakoidy zebrane są
w grana (l. pojedyncza - granum)
o
w błony gran wbudowany jest chlorofil
o
chloroplast wypełnia stroma - substancja składem i konsystencją
przypominająca cytoplazmę
o
w stromie zanurzone są: naga, kolista cząsteczka DNA i rybosomy o cechach
przypominających DNA i rybosomy Procaryota
Strona 72
Funkcje chloroplastów:
W chloroplastach zachodzi fotosynteza. Fotosynteza jest formą autotroficznego
odżywiania się organizmów. W dużym uproszczeniu polega na syntezie związków
organicznych ze związków nieorganicznych przy udziale energii świetlnej.
6CO
2
+ 6H
2
O + energia świetlna --> C
6
H
12
O
6
+ 6O
2
Fotosynteza przebiega w dwóch fazach:
•
faza jasna, = zależna od światła
o
przebiega w błonach gran, tam znajduje się chlorofil niezbędny do
przeprowadzenia tej fazy
o
polega na transformacji energii - energia świetlna, zaabsorbowana przez
chlorofile, zamieniona zostaje w energię wiązań chemicznych (ATP)
o
jej produktami są ATP i NADPH
2
- tzw. siła asymilacyjna - potrzebne do fazy
niezależnej od światła oraz tlen, który wydzielany jest do atmosfery, gdyż jest
produktem ubocznym fotosyntezy
•
faza ciemna, = niezależna od światła, = cykl Calvina
o
przebiega w stromie chloroplastu
o
polega na transformacji materii - związki nieorganiczne (H
2
O i CO
2
) pobrane z
otoczenia zostają zamienione w cukry proste (glukoza), czyli proste związki
organiczne, przy udziale energii zmagazynowanej w fazie jasnej w postaci
ATP
Budowa mitochondriów
Mitochondria to organella o kształcie zwykle owalnym, mogą też być kuliste lub
nieregularne. Ich wnętrze wypełnia macierz mitochondrialna (matriks). Otoczka
mitochondriów jest dwuwarstwowa. Zewnętrzna błona jest gładka i łatwo
przepuszcza wiele substancji na zasadzie transportu biernego. Błona wewnętrzna
stanowi barierę, przepuszczającą jedynie wybrane związki. Pomiędzy błoną
zewnętrzną a wewnętrzną znajduje się przestrzeń międzybłonowa. Błona
wewnętrzna tworzy uwypuklenia, tworzące w matriks mitochondrialnej tzw.
grzebienie. Na tych grzebieniach znajdują się buławkowate wypukłości.
Funkcja mitochondriów
Mitochondria to organella silnie wyspecjalizowane. Stanowią miejsca produkcji
energii dla komórki i są przystosowaniem do przemian oddechowych z udziałem
tlenu. Energia wytwarzana w mitochondriach magazynowana jest w postaci
wysokoenergetycznych wiązań w związku zwanym ATP. Podstawą procesów
zachodzących w mitochondrium jest pirogronian, powstający w wyniku
beztlenowego rozkładu glikolizy w cytoplazmie komórki i dostający się do matriks
mitochondrialnej. Tutaj ulega przekształceniu do acetylokoenzymu A przy udziale
obecnych w matriks enzymów. Następnie acetylokoenzym A ulega utlenianiu w
cyklu przemian zwanym cyklem Krebsa, w wyniku czego wydziela się dwutlenek
węgla oraz powstaje zredukowana forma dinukleotydu nikotynoamidoadeninowego
- NADH. Na grzebieniach mitochondrialnych następuje szereg reakcji utleniających
NADH, co wiąże się z oddawaniem elektronów i protonów. Cząstki te są
przenoszone na cząsteczkowy tlen, w wyniku czego powstaje cząsteczka wody.
Przenoszenie elektronów i protonów z NADH na tlen nosi nazwę łańcucha
oddechowego. Biorą w nim udział specyficzne enzymy, zlokalizowane na błonach
mitochondrium. Reakcje łańcucha oddechowego napędzają pracę syntaz ATP. Są
to enzymy znajdujące się w buławkowatych wypukłościach błony wewnętrznej.
Funkcją syntaz ATP jest produkcja wysokoenergetycznych wiązań w ATP.
Pochodzenie mitochondriów - teoria endosymbiozy
Mitochondria występują jedynie w komórkach eukariotycznych. Budową jednak
bardzo przypominają organizmy prokariotyczne - posiadają własny materiał
genetyczny w postaci podwójnej nici DNA, koliście zwiniętej w matriks, zawierają
również rybosomy typu 70S. Oprócz DNA w matriks występują też enzymy
potrzebne do jego replikacji oraz syntezy białek. Dzięki temu mitochondria są
organellami półautonomicznymi - posiadają wprawdzie cały aparat niezbędny do
produkcji własnych białek, ale większość z nich powstaje w cytoplazmie komórki
na matrycy genów jądrowych. Podobieństwa do budowy prokariotycznej
przyczyniły się do powstania teorii o pochodzeniu tych organelli. Uważa się
mianowicie, że jakiś czas temu pewne prokariotyczne komórki, oddychające
tlenowo, wniknęły do komórek eukariotycznych i żyły w nich na zasadzie
symbiozy. W toku ewolucji związek ten uległ tak silnej specjalizacji, że
endosymbiont przekształcił się w półautonomiczne organellum, będące
integralnym składnikiem komórki eukariotycznej. Zgodnie z ta teorią wewnętrzna
Strona 73
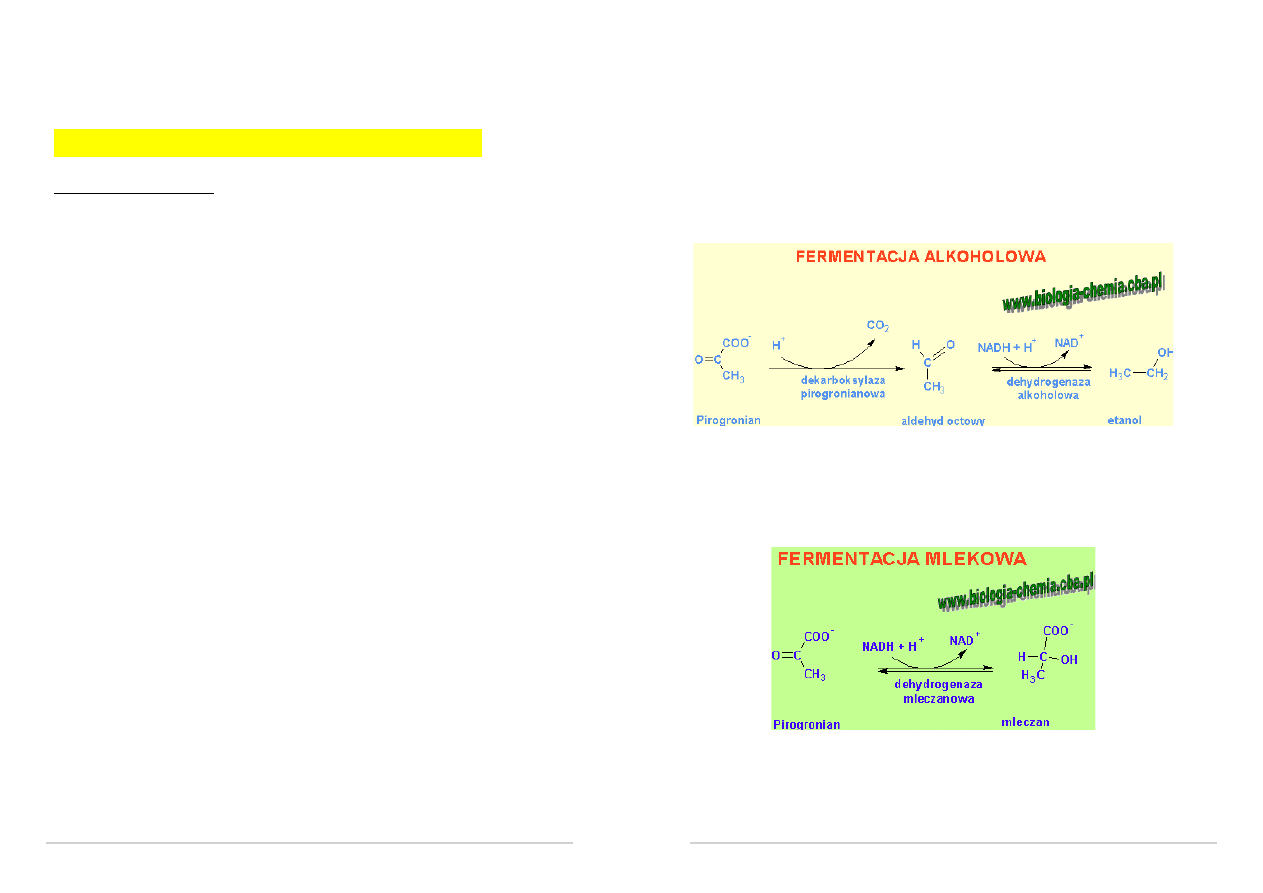
błona mitochondrium byłaby pierwotną błoną endosymbionta, a błona zewnętrzna -
błoną eukarionta, porwaną podczas wnikania symbionta do komórki.
Oddychanie beztlenowe. Fermentacja
Oddychanie beztlenowe jest procesem występującym głównie u mikroorganizmów
i zachodzi w cytoplazmie komórek. Początkowe etapy procesu polegają na
uaktywnieniu substratu oddechowego-glukozy która ulega przemianie w
ufosforylowaną glukozę. Następnie sześciowęglowy związek rozpada się na dwa
łańcuchy trójwęglowe, które dalej są przekształcane do kwasu pirogronowego. W
czasie tych przemian powstaje zredukowany przenośnik wodorowy NADH
2
a
następnie wydzielona energia jest akumulowana w ATP podczas fosforylacji
substratowej. Kwas pirogronowy ulega przemianom w różne związki, przy czym
zawsze gra rolę akceptora wodoru. Końcowy etap-wiązanie wodoru-nie uwalnia
energii. Nazwa fermentacji pochodzi od końcowego jej produktu. Drożdże
przeprowadzają przemianę kwasu pirogronowego do alkoholu (fermentacja
alkoholowa) z wydzielaniem CO
2
: C
6
H
12
O
6
+2ADP+2Pi→2C
2
H
5
OH+2CO
2
+2ATP,
a w komórkach bakterii mlekowych tworzy się kwas mlekowy-produkt fermentacji
mleczanowej: C
6
H
12
O
6
+2ADP+2Pi→2CH
3
CHOHCOOH+2ATP.
Homofermentacja proces prowadzący od substratu do wytworzenia produktów
końcowych określonych ogólnym równaniem chemicznym przy czym ilość tych
produktów odpowaida stosunkom stechiometrycznym w danym równaniu. W
rzeczywistość wynik odbiega od teoretycznych zalożeń ze względu na tworzenie
produktów ubocznych np. glukoza-kw.mlekowy
Heterofermentacja- powstaja rózne produkty końcowe których wzajemny
stosunek zależy od warunków w jakich odbywa się fermentacja. np. fermentacja
mlekowa, acetonowo butanolowa; glukoza-kw. mlekowy+was octowy; glukoza-
kw.mlekowy +etanol+CO
Bilans oddychania beztlenowego
Oddychanie beztlenowe zachodzi u niektórych organizmów np. bakterii,
grzybów, a także zwierzęcych pasożytów wewnętrznych.
Substratem oddychania beztl. Jest najczęściej glukoza. I etapem tego
oddychania jest glikoliza, która prowadzi do utworzenia kw. pirogronowego , 2
cząst. ATP i 2 cząst. NADH2/ Przy braku tlenu nie może zajść utlenianie NADH2 w
łańcuchu oddechowym.
Kw. pirogronowy nie może być dalej utleniany, ponieważ powodowałoby to
dalsze gromadzenie NADH2. Dlatego też kwas pirogronowy podlega
bezpośredniej lub pośredniej redukcji, której towarzyszy utlenianie NADH2 do
NAF. Końcowym produktem oddychania beztlenowego mogą więc być rożne zw.
organiczne np. alkohol etylowy, kw. mlekowy, masłowy.
Fermentacja alkoholowa
Przebiega w kom. Drożdży w mięsistych dużych owocach, nasionach pokrytych
twarda łupiną, w korzeniach, jeżeli jest duzo wody w glebie. Powstający w glikolizie
kwas. Pirogronowy ulega dekarboksylacji do aldehydu octowego a ten redukcji do
etanolu.
Fermentacja mlekowa
Zachodzi w komp. Bakterii mlekowych, w mięśniach szkieletowych w warunkach
deficytu tlenu. Kw. pirogronowy wytworzony w procesie glikolizy ulega
bezpośredniej redukcji do kw. mlekowego. Fermentacja przeprowadzona przez
bakterie odgrywa istotna role w życiu człowieka ponieważ np. powoduje kwaszenie
mleka, kapusty
Strona 74

Fotosynteza
Chloroplasty
Chloroplast (ciałko zieleni) – otoczone podwójną błoną białkowo-
lipidową organellum komórkowe występujące u roślin i glonów
eukariotycznych. Są rodzajem plastydów. Zawierają zielone barwniki
chlorofile pochłaniające energię światła słonecznego potrzebną do
fotosyntezy. W nich zachodzi przemiana dwutlenku węgla oraz wody z
wykorzystaniem energii świetlnej w glukozę oraz tlen.
Chloroplasty są otoczone dwiema błonami o różnej
przepuszczalności, otaczającymi stromę wypełniającą wnętrze
chloroplastu. Błona zewnętrzna dobrze przepuszcza jony. Wewnętrzna
błona jest natomiast słabo przepuszczalna i tworzy liczne woreczki (zwane
tylakoidami). W chloroplastach granalnych ułożone są one w płaskie stosy
zwane tylakoidami gran. U chloroplastów bezgranalnych natomiast
występują jedynie lamelle – tylakoidy stromy, czyli tylakoidy rozciągnięte
wzdłuż całego chloroplastu (w komórkach pochew okołowiązkowych
niektórych roślin przeprowadzających fotosyntezę C
57)
Wnętrze chloroplastu wypełnia białkowa substancja – stroma –
koloid białkowy. W jej skład wchodzą m.in. niewielkie ilości DNA, enzymy
biorące udział w fotosyntezie oraz rybosomy typu prokariotycznego (tzw.
rybosomy małe, o stałej sedymentacji 70s), które biorą udział w produkcji
białek, są one jednak mniejsze od rybosomów eukariotycznych o stałej
sedymentacji 80s, znajdujących się w cytoplazmie.
Błona tylakoidów jest zbudowana głównie z galaktolipidów:
monogalaktozylodiacyloglicerolu i digalaktozylodiacyloglicerolu, które
stanowią 75% wszystkich lipidów chloroplastowych. Zawierają one dużo
wiele nienasyconych kw. Tłuszczowych, takich jak kw. Linolowy i
linolenowy. Błony tylakoidów zawierają stosunkowo niewiele fosfolipidów
ich głównym przedstawicielem jest fosfatydyloglicerol – jego zawartość nie
przekracza 15% wszystkich lipidów chloroplastowych. Wszystkie lipidy
łącznie stanowią 35-40% zawartości błony tylakoidów. Dominującym
składnikiem błon tylakoidów są białka. Oprócz białek i lipidów istotnym
elementem, charakterystycznym jedynie dla błon transformujących energię
świetlną, jest występowanie barwników fotosyntetycznych. Główne
barwniki to chlorofile. Wszystkie organizmy fotosyntetyzujące, które
produkują tlen zawierają chlorofil a. w chloroplastach roślin wyższych
występuje ponadto chlorofil b, stanowiący ok. 1/3 ilości chlorofilu a.
cząsteczka chlorofilu zbudowana jest z 5-pierścieniowej pochodnej
porfiryny, zwanej feoporfiryną, oraz reszty 20-węglowego alkoholu – fitolu,
dołączonej wiązaniem estrowym do reszty kw. Propionowego, która jest
jednym z podstawników IV pierścienia pirogowego feoporfiryny. Fragmenty
4 połączonych pierścieni pirogowych oraz dodatkowego piątego pierścienia
niepirolowego tworzą układ następujących po sobie kolejno wiązań
pojedynczych i podwójnych. Nosi on nazwę układu wiązań sprzężonych i
charakteryzuje się zdolnością absorpcji promieniowania świetlnego.
Centralne miejsce w pierścieniu porfirytowym zajmuje atom magnezu,
połączony z atomami azotu pierścieni pirogowych. Obok chlorofili w
błonach fotosyntetycznych występują także inne barwniki np. karotenoidy i
fikobiliny – są to barwniki pomocnicze. Karotenoidy są barwnikami
pochodnymi izoprenu dzielą się na pomarańczowoczerwone karoteny,
zbudowane wyłącznie z węgla i wodoru, oraz żółte i żółtopomarańczowe
ksantofile zawierające również tlen. W związkach tych występują 2
pierścienie jonowe połączone długim łańcuchem węglowodorowym, w
którym występujące na przemian wiązania pojedyncze i podwójne tworzą
układ wiązań sprzężonych. Specyficzną grupą barwników pomocniczych
są fikobiliny. Zbudowanie są z 4 pierścieni pirogowych połączonych w
układ liniowy i nie zawierają magnezu ani fitolu. Fikobiliny w połączeniu z
odpowiednimi białkami tworzą struktury antenowe zwane fikobilisomami,
dostarczające energię wzbudzenia do chlorofili fotoskładu II
Chloroplasty zaliczamy do organelli samoreplikujących się
(obecność chloroplastowego DNA oraz zdolność do samoreplikacji
Błona tylakoidu jest miejscem gdzie zachodzą reakcje świetlnej fazy
fotosyntezy.
Reakcje ciemnej fazy fotosyntezy zachodzą w stromie chloroplastu, gdzie
znajdują się wszystkie enzymy uczestniczące w tym procesie.(pytanie 8)
Strona 75

Biogeneza chloroplastów:
Komórki roślinne posiadają wiele specyficznych tylko dla nich
organelli. Wśród nich możemy wyróżnić plastydy, z których najważniejsze
są chloroplasty – zawierające barwnik fotosyntetyczny (chlorofil).
Chloroplasty powstają właśnie z plastydów, już w tkankach merystema
tycznych można wyróżnić proplastydy, czyli podwójnie obłonione
pęcherzyki (błony białkowo – lipidowe otaczające stromę). Ich namnażanie
zachodzi wraz z podziałami komórkowymi.
Jeżeli nowo powstałe komórki będą rozwijać się w ciemności to
zajdzie tzw. etiolacja i w proplastydach zaczną gromadzić się związki
cukrowe lub tłuszcze (powstaną leukoplasty, bądź amyloplasty –
skupiające ziarna skrobi). Z czasem w leukoplastach nastąpi inwaginacja
wewnętrznej błony białkowo – lipidowej, aż zaczną odrywać się od niej
pęcherzyki. Utworzą one nieregularne skupienia błon w kształcie rurek (w
jednym biegunie komórki) – twór ten nazywamy ciałem prolameralnym.
Ciało prolameralne zawiera w sobie żółty barwnik – protochlorofilid, a
plastyd z ciałem prolameralnym (w kształcie plastru miodu) nazywamy
etioplastem. Wystarczy wystawić etiolowane komórki na światło, a
rozpocznie się w nich synteza chlorofilu z protochlorofilidu, chlorofil idu a i z
kwasu aminolewulinowego (deetiolacja). Pęcherzyki zaczną się rozpadać i
spłaszczać – powstaną grana. Poza tym nastąpi synteza białka wiążącego
chlorofil a/b, które łącząc się z chlorofilem i zakotwiczając w błonie
tylakoidów utworzy antenę fotosystemu II. Zajdzie także synteza
podjednostek enzymu: karboksylazy rybulozo – 1,5 – bisfosforylowej
(RuBisCO) – niezbędnego do asymilacji CO
2
. Proces syntezy chlorofilu,
białka wiążącego chlorofil i RuBisCO kontrolowany jest przez system
fitochromowy – główny fotoreceptor.
Jeżeli komórki będą rozwijać się przy pełnym dostępie światła, to
wówczas z plastydów od razu zaczną formować się spłaszczone
pęcherzyki tylakoidów gran i wydłużone połączenia pomiędzy nimi –
tylakoidy stromy. Rozpocznie się także synteza chlorofilu.
Z czasem chloroplasty zaczną przekształcać się w chromoplasty –
organella z takimi barwnikami jak: karotenoidy i fikobiliny, będzie to
oznaczać, że zachodzi w nich proces starzenia.
BUDOWA I DZIAŁANIE APARATÓW
SZPARKOWYCH
Aparaty szparkowe są niezbędnym elementem budowy roślin, gdyż
dzięki nim para wodna może dyfundować na zewnątrz w procesie
transpiracji szparkowej. A także mogą tą transpirację ograniczać (w
niesprzyjających warunkach). Przez szparki zachodzi również dyfuzja CO
2
i
O
2
. Mogą one występować zarówno w dolnej jak i w górnej części skórki.
Gęstość rozmieszczenia zależy od gatunku rośliny (liść średniej wielkości
może mieć kilka milionów szparek).
ROZMIESZCZENIE APARATÓW SZPARKWYCH W LIŚCIACH
Liście hypostomatyczne – aparaty szparkowe wyłącznie w dolnej
epidermie (w większości roślin).
Liście amfistomatyczne – aparaty liściowe po obu stronach blaszki
liściowej
Liście epistomatyczne – aparaty szparkowe w górnej epidermie (u roślin
wodnych, których liście pływają po powierzchni wody).
BUDOWA APARATÓW SZPARKWOYCH
2 komórki szparkowe, pomiędzy którymi znajduje się otwór – szparka
prowadząca do umieszczonej niżej komory szparkowej. Zawierają
chloroplasty (mogą, więc wytwarzać związki organiczne w przeciwieństwie
do innych komórek epidermy).
RODZAJE APARATÓW SZPARKOWYCH
1. Typ gramineae – występuje u traw. Mają kształt hantli. Komórki
zamykające są wydłużone, przy czym partie środkowe są wąskie i silnie
zdrewniałe, podczas gdy ich końce są pęcherzykowato rozszerzone i
cienkościenne. Wzrost turgoru powoduje zwiększenie średnicy
pęcherzykowatych zakończeń, wskutek czego środkowe zdrewniałe partie
odchylają się od siebie, poszerzając w ten sposób otwór. Przy
zmniejszaniu turgoru zbliżają się one do siebie i szparka zamyka się.
Komórki szparkowe otoczone są innymi komórkami epidermy, określanymi
jako przyszparkowe, które wspomagają komórki przyszparkowe np. w
regulacji rozwarcia szparki. W pęcherzykowatych zakończeniach
mikrofibryle celulozowe ułożone są promieniście, dzięki czemu przy
Strona 76
wzroście turgoru zakończenia komórek szparkowych mogą zwiększyć
swoją średnicę, wskutek czego wąskie zdrewniałe partie odchylają się od
siebie, poszerzając w ten sposób otwór. W przypadku spadku turgoru
dzieje się odwrotnie.
Aparaty szparkowe
- rola, rodzaj, budowa i działanie aparatów
szparkowych
.
Aparaty szparkowe składają się z dwóch komórek
szparkowych(zamykających), które zawierają chloroplasty i różnią się
znacznie od pozostałych komórek skórki. Pomiędzy komórkami
szparkowymi istnieje przestwór między komórkowy- por szparki- łączący
system wentylacyjny liścia z atmosferą.
Komórki szparkowe oglądane z góry mają najczęściej kształt nerkowaty ich
ściany graniczące ze szparką są grubsze, ściany zaś znajdujące się po
przeciwnej stronie – cieńsze.
U roślin wyższych wyróżniamy dwa typy komórek szparkowych. U traw i
kilku innych roślin jednoliściennych , np. u palm, komórki szparkowe mają
charakterystyczny kształt gimnastycznych ciężarów , zakończonych
bulwkami. Otwór szparkowy stanowi długą szczelinę, ulokowaną między
dwoma „drążkami”. Takie komórki szparkowe otoczone są paroma innymi
komórkami epidermy, określanymi jako komórki przyszparkowe, które
wymagają komórki szparkowe w regulacji rozwarcia szparki.
U roślin dwuliściennych i tych jednoliściennych, które nie należą do rodziny
traw, a także u mchów , paproci i roślin nagozalążkowych, komórki
szparkowe mają kształt nerkowatya otwór znajdujący się między nimi ma
przekrój owalny. U tych roślin często nie występują komórki przy
szparkowe i wówczas komórki otoczone są zwykłymi komórkami
epidermy. Charakterystyczna cechą budowy komórek szparkowych jest
nierównomierna grubość i specyficzna struktura ich ścian, związana z
układem mikrofibryli celulozowych. W zwykłych komórkach cylindrycznych
ułożone są poprzecznie w stosunku do głównej osi komórki, co umożliwia
rozciąganie komórki wzdłuż jej podłużnej osi. W nerkowatych komórkach
szparkowych mikrofibryle celulozowe rozchodzą się promieniście od
otworu szparkowego. W związku z tym obwód szparki zostaje
wzmocniony, a sama komórka wygina się na zewnątrz w trakcie
rozwierania szparki. U traw środkowe części komórek szparkowych
rozciągają się wówczas, gdy wzrasta objętość ich bulwkowatych
zakończeń, zddolnych do rozciągania się, co pozwala na rozszerzanie
leżącej miedzy nimi szczeliny.
Komórki szparkowe funkcjonują jako wielo czujnikowe zastawki hydrauliczne .
Reagują na zmiany czujników środowiska, takich jak natężenie i jakość światła,
temperaturę wilgotność względna powietrza, wewnętrzno komórkowe stężenie
CO2 oraz na zmiany stężenia hormonu- kwasu abscynowego. Rozwieranie się
aparatów szparkowych spowodowane jest spadkiem potencjału wody w
komórkach szparkowych na skutek reakcji związanych z fotosyntetycznym
metabolizmem węgla, transportem niektórych produktów fotosyntezy oraz jonów
potasu. W wyniku zmniejszania się potencjału wody w komórkach szparkowych
zaczyna się do nich przemieszczac woda z innych komórek epidermy. W miarę
dopływu wody wzrasta ciśnienie turgorowi w komórkach szparkowych.
Zróżnicowana grubość ich ścian sprawia, że otwór między nimi zaczyna się
rozwierać. Zamykanie się szparki zachodzi w wyniku utraty wody przez komórki
szparkowe do atmosfery(zamykanie hydropasywne) Reakcje te, indukowane np.
przez odwodnienie całego liścia i / lub zwiększoną podaż kwasu abscynowego
prowadzą do utraty turgoru w komórkach szparkowych, co jest bezpośrednia
przyczyną zamykania się szparki. Kwas abscynowy(ABA) jest stale syntezowany
w komórkach mezofilu i gromadzony w chloroplastach, a także wytwarzany w
komórkach korzenia. Pod wpływem słabego nawet odwodnienia liści lub korzeni
następuje wzmożenie syntezy ABA w tych organach, a także zachodzi
redystrybucja. W liściach ABA zostaje uwolniony z komórek mezofilu do apoplastu,
skąd przemieszcza się do komórek szparkowych. Z komórek korzenia
przemieszcza się do liści wraz z prądem transpiracji w soku ksylemu. Kwas
abscynowy może powodować zamykanie się szparek nawet wówczas, gdy nie
wystąpiły jeszcze zmiany potencjału wody w komórkach liścia. Hormon ten jest
więc przekaźnikem informacji o pogorszeniu się stosunków wodnych w korzeniu.
Zmiany transpiracji wywołane pogarszającym się w ciagu dnia uwodnieniem liści
powodują iż transpiracja zachodzi najszybciej gdy szparki są całkowicie rozwarte,
Strona 77
i najwolniej, gdy szparki są zamknięte. Podczas pełnego zamknięcia szparek
zachodzi tylko transpiracja kutykularna. W sytuacji częściowego rozwarcia szparek
inne czynniki mogą wpływać na intensywność transpiracji. Jeżeli np. warunki
atmosferyczne nie sprzyjają parowaniu wody, to transpiracja osiąga maksimum
wówczas, gdy szparki są tylko częściowo rozwarte. Jeśli jednak czynniki
zewnętrzne są dla parowania korzystne, to intensywność transpiracji rośnie wraz z
rozwarciem aparatów.
Budowa anatomiczna liści roślin wyższych jako
wyraz pełnionych funkcji
•
Liść jest organem specjalnie przystosowanym do fotosyntezy.
Blaszka liściowa jest spłaszczona, dzięki czemu ma dużą powierzchnię w
stosunku do objętości. Umożliwia to nie tylko doskonałe wykorzystanie
energii świetlnej padającej na liść, lecz także zwiększa powierzchnię
absorpcyjną dla CO
2
Skórka liścia jest zwykle przezroczysta a wiec nie hamuje dostępu światła
do mezofilu złożonego z jednej lub kilku warstw miękiszu palisadowego (u
światłolubnych ta warstwa jest grubsza) oraz z luźno rozłożonych komórek
miękiszu gąbczastego. Elementy przewodzące liścia rozmieszczone w
nerwach liścia doprowadzają do komórek wodę i sole mineralne
odprowadzają zaś produkty wytwarzane w procesie fotosyntezy. Wiązki
przewodzące w liściu są bardzo duże.
•
Liść jako miejsce transpiracji
Woda paruje z całej powierzchni rośliny przeważa jednak parowanie z
powierzchni liści, ponieważ ich powierzchnia jest nieporównywalnie
większa w porównaniu z innymi częściami rośliny. Ale liść nie jest organem
służącym specjalnie do transpiracji, ponieważ jego główna funkcja
związana jest z fotosyntezą. Liść od zewnątrz osłonięty jest przez skórkę,
która pokryta jest kutikulą mało przepuszczalna dla gazów i wody. W
skórce zwłaszcza w dolnej znajdują się aparaty szparkowe, przez które
odbywa się wymiana gazów pomiędzy wnętrzem liścia a atmosferą, oraz
zachodzi transpiracja.
Wśród wewnętrznych tkanek liścia zwanych mezofilem lub
miękiszem zieleniowy wyróżnić można: miękisz palisadowy (od górnej
strony liścia) i miękisz gąbczasty od dolnej strony liścia. W miękiszu
zieleniowym znajdują się duże przestwory międzykomórkowe, zajmujące
nawet 30% objętości liścia. Są one większe w miękiszu gąbczastym, ale
występują również w miękiszu palisadowym. Nie wszystkie komórki stykają
się ze sobą bokami. Podobne przestwory znajdują się również w łodygach i
korzeniu tworząc ciągły system przewietrzający, który magazynuje
substancje gazowe. Umożliwia wymianę gazów komórką
a atmosferą. W liściu można wyróżnić dwie powierzchnie parowania:
zewnętrzną (górna i dolna skórka pokryta warstwą kutikuli) oraz
wewnętrzną (komórki miękiszu gąbczastego i palisadowego) które graniczą
z przestworami międzykomórkowymi. W komórkach mezofilu znajdują się
duże ilości chloroplastów a w nich barwnik chlorofil, który jest niezbędny w
procesie fotosyntezy. Skórka liścia zawiera aparaty szparkowe, które
regulują m.in. turgor komórki.
Liść jako organ fotosyntezy
– przystosowanie anatomiczne i molekularne.
Chloroplasty zawierają zielony barwnik chlorofil, który nadaje liściom
zielone zabarwienie i spełnia podstawową funkcję w fotosyntezie pochłaniając
energię promieniowania słonecznego. Chloroplasty mają zwykle kształt deskowaty
i skomplikowaną strukturę wewnętrzną. W komórce występują w liczbie od 20 do
100. Mają średnicę ok. 5μm i grubość 1μm.
Zdolność do przeprowadzania fotosyntezy wykazują wszystkie zielone
części rośliny jednak 95% związków pokarmowych powstaje w liściach. Jest to
bowiem organ specjalnie przystosowany do przeprowadzania tego procesu.
Świadczy o tym duża powierzchnia spłaszczonej blaszki liściowej w porównaniu z
jej objętością. Umożliwia ona w pełni wykorzystanie energii
świetlnej
, a także
zwiększa powierzchnię absorpcyjną dla dwutlenku węgla. Kolejną cechą liścia jako
głównego organu przeprowadzającego fotosyntezę jest przezroczysta skórka,
przez którą światło bez trudu dociera do bogatych w chloroplasty komórek
miękiszu liściowego. Dzięki silnie rozwiniętym przestworom międzykomórkowym
każda zielona komórka bezpośrednio kontaktuje się zarówno z wewnętrzną, jak
i zewnętrzną atmosferą liścia. Gęsta siatka wiązek sitowo – naczyniowych
Strona 78
doprowadza wodę i składniki mineralne do liścia oraz odprowadza związki
organiczne powstałe w procesie fotosyntezy do wszystkich komórek rośliny.
Warstwa wosku pokrywająca liść chroni przed nadmierną utratą wody, a szparki –
otworki na powierzchni liścia pozwalają gazom krążyć między wnętrzem liścia, a
środowiskiem.
Chemosynteza- definicja, organizmy
chemosyntetyczne.
Chemosynteza to proces polegający na przekształcaniu CO
2
w związki
organiczne, w którym wykorzystywana jest energia pochodząca z
utleniania różnych związków nieorganicznych lub prostych jedno-
węglowych związków organicznych.
Zjawisko chemosyntezy występuje w świecie drobnoustrojów. Bakterie
chemosyntetyczne dzielimy na dwie grupy:
a) chemolitotrofy - zalicz się do nich bakterie wykorzystujące jako
źródło energii takie substraty nieorganiczne jak związki siarki(bakterie
siarkowe), wodór (bakterie wodorowe), związki azotu(bakterie
nitryfikacyjne), żelazo(bakterie żelaziste)
Bakterie te są jedynymi organizmami poza organizmami
przeprowadzającymi fotosyntezę, które mogą rosnąć w warunkach
zupełnego braku substancji organicznych w środowisku.
c) chemoorganotrofy - zalicza się do nich bakterie, które czerpią
energię z utleniania prostych, jedno-węglowych związków
organicznych, takich jak metan, metanol, mrówczan
*Bakterie siarkowe
Bakterie siarkowe występują w zbiornikach wody słodkiej i morskiej obfitujących w
niektóre związki siarki. Do substratów wykorzystywanych przez bakterie siarkowe
należą: siarkowodór, tiosiarczan, siarka pierwiastkowa. Najwięcej energii uzyskują
bakterie utleniające siarkowodór zgodnie z reakcją:
H
2
S +2O
2
2H
+
+SO
4
2-
Nieco mniej energii uwalnia się przy utlenianiu siarki pierwiastkowej:
S
0
+H
2
O
+1
1
/
2
O
2
2H
+
+SO
4
2-
Stosunkowo najmniej energii dostarcza utlenianie tiosiarczanu:
Na
2
S
2
O
3
+ H
2
O + 2O
2
2H
+
+2Na +2SO
4
2-
Bakterie wykorzystujące siarkowodór np.Thiothrix nivea , często utleniają ten
związek najpierw do pierwiastkowej siarki, która odkłada się w komórce jako
energetyczny materiał zapasowy i kiedy siarkowodór środowisku ulegnie
wyczerpaniu, ona z kolei dostarcza energii ulegając przekształceniu do siarczanu,
który jest ostatecznym produktem utleniania. Do bakterii siarkowych należą
gatunki autotroficzne, asymilujące CO
2
w cyklu Calvina-Bensona.
Bakterie te muszą wytwarzać zarówno ATP jak i NADPH, niezbędne do
przeprowadzenia tego cyklu. ATP powstaje zgodnie z mechanizmem
chemiosmotycznym, w którym siłą napędową fosforylacji jest gradient stężenia
protonów w poprzek błony powstający w czasie przepływu elektronów z
utlenionego związku siarki na tlen. Elektrony pochodzące z utleniania H
2
S
przekazywane są na flawoproteinę łańcucha oddechowego, zaś kiedy substratami
jest tiosiarczan lub siarka pierwiastkowa, elektrony włączają się w łańcuch
transportu elektronów na poziomie cytochromu c. Redukcja NADP
+
do NADPH
zachodzi natomiast wskutek stymulowanego przez potencjał błonowy odwrotnego
przepływu elektronów z cytochromów poprzez chinony i reduktazę NADP-chinon.
*Bakterie wodorowe
Bakterie wodorowe występują zazwyczaj w glebie i mają zdolność do
wykorzystywania wodoru obecnego w środowisku do uzyskania energii potrzebnej
do przeprowadzenia procesów życiowych. Wśród bakterii wodorowych
wyróżniamy gatunki, w których ostatecznym akceptorem elektronów jest tlen a
więc końcowym produktem utleniania wodoru jest woda oraz gatunki, w których
ostatecznym akceptorem elektronów są inne związki niż tlen, bakterie te żyją w
warunkach anaerobowych. Bakterie wodorowe żyjące w warunkach tlenowych
mają enzym- hydrogenazę, który uczestniczy w przeniesieniu elektronów z H
2
na
NAD
+
lub chinon. Dalej elektrony przenoszone są przez łańcuch oddechowy na
tlen, generując siłę protomotoryczną i syntezę ATP. Natomiast bakterie żyjące w
warunkach beztlenowych, których przykładem jest Microccocus denitrificans
wykorzystuje azotany jako akceptory elektronów. Bakterie wodorowe wykazują
zróżnicowany metabolizm. Wiele gatunków jako źródło energii wykorzystuje wodór
kiedy jest on obecny w środowisku ale mogą również czerpać energię z utleniania
związków organicznych są więc chemolitotrofami fakultatywnymi. Zróżnicowanie
obserwuje się również w odniesieniu do formy węgla, która może być przyswajana
przez te organizmy. Kiedy w środowisku obecny jest CO
2
jako jedyne źródło węgla
to te bakterie rosną autotroficznie przyswajając CO
2
w cyklu Calvina-Bensona.
Strona 79

Jednak jeśli w środowisku znajdują się substancje organiczne wówczas bakterie
odżywiają się w sposób heterotroficzny. Istnieją również bakterie, które energie
czerpią z utleniania H
2
a jako źródła węgla wykorzystują wyłącznie związki
organiczne.
Strona 80

*Bakterie żelaziste
Bakterie żelaziste przekształcają związki żelazawe w żelazowe, czerpiąc z
utleniania jonu Fe
2+
do Fe
3+
energię niezbędną do przeprowadzania swoich
procesów życiowych. Reakcja przebiega wg następującego schematu:
4FeCO
3
+ H
2
O + 6H
2
O4Fe(OH)
3
+4CO
2
Jon Fe
2+
jest trwały w obecności tlenu tylko w środowisku kwaśnym. W pH
obojętnym ulega szybkiemu samorzutnemu utlenieniu do Fe
3+
, który wytrąca się z
roztworu jako wodorotlenek żelazowy. Dlatego też większość bakterii żelazistych
występuje w środowiskach zakwaszonych, gdzie jony Fe
2+
wykazują większą
stabilność.
Ilość energii uzyskiwanej przez utlenienie Fe
2+
do Fe
3+
stosunkowo niewielka w
porównaniu z ilością energii uzyskiwanej przez bakterie siarkowe czy wodorowe podczas
utleniania związków siarki lub cząsteczek wodoru. Mała ilość energii wyzwalanej
podczas przejścia elektronu z Fe
2+
na tlen wiąże się z stosunkowo elektrododatnim,
wynoszącym +0,77 V, potencjałem oksydoredukcyjnym pary Fe
2+
/Fe
3+
. Zatem elektrony
włączane są w łańcuch transportu elektronów dopiero na jego ostatnim odcinku,
bezpośrednio poprzedzającym tlen. Pośredniczy w tym rustycyjanina - białko zawierające
miedź oraz cytochromy c i a
1
Ilość wyzwolonej energii jest zbyt mała aby mogła być wykorzystana do trans-
portu protonów, co jest warunkiem wytworzenia siły protonomotorycznej i syntezy ATP.
Dlatego też bakterie żelaziste wykorzystują do syntezy ATP naturalny gradient stężenia
jonów wodorowych, jaki istnieje pomiędzy zakwaszonym środowiskiem zewnętrznym
(pH ok.2) a wnętrzem komórki (odczyn zbliżony do obojętnego). Protony wnikając do
komórki przez kompleks syntazy ATP powodują syntezę ATP zgodnie z koncepcją
Mitchella. Następnie, już wewnątrz komórki, protony te łączą się z tlenem
zredukowanym elektronami przeniesionymi z Fe
2+
i powstaje woda. W ten sposób
komórka pozbywa się nadmiaru wnikających protonów, co pozwala jej na utrzymanie
obojętnego pH cytoplazmy.
Niektóre bakterie żelaziste, np. Thiobacillus ferrooxidans, mogą utleniać także zredu-
kowane związki siarki, uzyskując w ten sposób energie. Th. ferrooxidans prowadzi
autotroficzny tryb życia. Acydofilne bakterie żelaziste występują zazwyczaj w glebach
zakwaszonych i środowiskach zanieczyszczonych, Istnieje także grupa bakterii
żelazistych, które żyją w strefie ograniczonej dostępności tlenu Fe
2+
jest stabilny
nawet w pH obojętnym, co stwarza możliwość wykorzystania go jako substratu
energetycznego. W środowiskach tego typu występują np. bakterie z rodzaju
Gallionella, u których stwierdzono występowanie autotrofii.
*Bakterie nitryfikacyjne
Bakterie nitryfikacyjne występują pospolicie w glebie i w zbiornikach wodnych, a energię
potrzebną do przeprowadzania procesów życiowych czerpią z utleniania takich form
azotu jak NH
3
i NO
-
2
. Bakterie z rodzajów Nitrosomonas i Nitrosocystis i inne utleniają
amoniak do azotynu zgodnie z reakcją:
NH
3
+1
1/
2
O
2
- NO
2
+ H
+
+ H
2
O
Etapem pośrednim jest tu wytworzenie hydroksylaminy (NH
2
OH)
Z kolei bakterie z grupy Nitrobacter czy Nitrococcus utleniają powstały azotyn do
azotanu:
NO
2
-
+
1
/
2
O
2
NO
3
-
Jak wynika z przytoczonych reakcji, bakterie z rodzaju Nitrobacter uzależnione są
metabolicznie od substratu wytworzonego przez Nitrosomonas i w rzeczywistości te
dwie grupy bakterii występują wspólnie. Potencjał redoks obu substratów tj. amoniaku i
azotynu, jest stosunkowo wysoki, dlatego też elektrony odłączane od tych związków
włączają się dopiero w ostatnie ogniwa łańcucha transportu elektronów, dostarczając w
związku z tym niewielkich ilości energii. Amoniak przekształcany jest najpierw przez
enzym błonowy - monooksygenazę amoniakową do hydroksylaminy, która jest
następnie utleniana przez oksydoreduktazę hydroksylaminową do azotynu. Elektrony
odłączone w tym procesie przerzucane są przez cytochrom typu c. Jon NO
2
-
utleniany
jest przez enzym błonowy - oksydazę azotynową, a odłączane elektrony są
przekazywane na cytochrom c łańcucha oddechowego.
*Chemoorganotrofy
W odróżnieniu od chemolitotrofów, które czerpią energię z utleniania substratów nie-
organicznych, chemoorganotrofy uzyskują energię niezbędną do przemian metabolicz-
nych przez utlenianie związków organicznych. Na szczególne wyróżnienie zasługuje
tu grupa bakterii utleniająca związki jedno-węglowe, takie jak metan, metanol czy
mrówczan z użyciem tlenu atmosferycznego jako akceptora elektronów. Bakterie te określa
się nazwą metylotrofy i zalicza się do nich takie rodzaje jak Methylobacter.
Metylotrofy występują w środowiskach, gdzie dostępne są zarówno wymienione związki
węgla, jak i tlen (gleba, zbiorniki wodne),są bowiem obligatoryjnymi aerobami. Jedną z
grup metylotrofów są metanotrofy, które przeprowadzają reakcję utlenienia
metanu do dwutlenku węgla poprzez kilka stadiów pośrednich, według poniższych
reakcji:
CH
4
+ 1
1
/
2
O
2
CH
3
OH CHOH + 2 H
CHOH + H
2
0 HCOOH + 2 H
HCOOH CO
2
+ 2 H
Strona 81

Metylotrofy nie mogą asymilować CO
2
. Jako źródło węgla wykorzystują takie związki,
jak metanol czy aldehyd mrówkowy, w których węgiel jest na niższym stopniu
utlenienia niż dwutlenek węgla. Organizmy te nie spełniają zatem klasycznej definicji
autotrofii nie zalicza się ich zatem do organizmów samożywnych. Są tu jednak wyjątki,
np. Pseudomonas oxalaticus, bakteria utleniająca kwas mrówkowy. Organizm ten
można zaliczyć do grupy autotrofów, gdyż produkt utlenienia mrówczanu – dwutlenek
węgla może być wykorzystany jako źródło węgla do syntezy własnych związków or-
ganicznych.
Cykl CAM i C4 - podobieństwa i różnice.
Obie grupy tych roślin wykształciły dodatkowy mechanizm wiązania
dwutlenku węgla poprzedzający cykl Calvina-Bensona. Do grupy roślin
określanych jako C4 zaliczamy rośliny strefy zwrotnikowej np. kukurydza..
Liście tych roślin mają charakterystyczną Budowę anatomiczną, w której
można wyróżnić komórki miękiszu (mezofilu) liścia oraz specjalną grupę
komórek otaczających wiązki przewodzące, zwaną pochwą okołowiązkową. W
cytozolu komórek
miękiszu występuje enzym
karboksylaza
fosfoenolopirogronianowa , który katalizuje przyłączenie CO
2
do wysokoener-
getycznego związku - fosfoenolopirogronianu. Pierwszym produktem
przyłączenia dwutlenku węgla do fosfoenoopirogronianu jest szczawiooctan.
Utworzony szczawiooctan ulega przekształceniu w jabłczan. który specjalnymi
kanałami plasmodesma jest transportowany do komórek pochwy
okołowiązkowej. W komórkach tych następuje dekarboksylacja jabczanu z
udziałem tzw. enzymu jabłczanowego (dehydrogenaza jabłczanowa
dekarboksylująca), a uwolniony CO
2
jest ponownie wiązany przez obecną w
chloroplastach komórek pochwy okołowiązkowej karboksylazę l,5
bisfoforybulozy i następnie przekształcany zgodnie z reakcjami cyklu Calvina-
Bensona. Tworzący się w procesie dekarboksylacji pirogronian przemieszcza
się z powrotem do komórek mezofilu, gdzie ulega fosforylacji do
fosfoenolopirogronianu . Reakcja jest katalizowana jest przez dikinazę
pirogronian-fosforan, która fosforyluje nie tylko pirogronian, lecz także
cząsteczkę fosforanu nieorganicznego, zużywane są zatem dwa
wysokoenergetyczne wiązania ATP. Natomiast do roślin określanych mianem
CAM zaliczamy rośliny strefy pustynnej i półpustynnej Rośliny te ze względu na
warunki środowiska muszą prowadzić oszczędną gospodarkę wodną i aby
zapobiec nadmiernej utracie wody, otwierają szparki tylko w nocy kiedy
temperatura znacznie się obniża. Otwarcie szparek umożliwia dopływ
dwutlenku węgla do wnętrza rośliny, ale z powodu braku światła nie
przebiegają procesy świetlnej fazy fotosyntezy, dostarczające ATP i NADPH.
Dwutlenek węgla jest więc wstępnie przyłączany przez znajdującą się w
cytozolu komórek karboksylazę do fosfoenolopirogronianu i powstaje
szczawioctan. Fosfoenolpirogronian jest dostarczany przez glikolizę i
pochodzi z rozkład skrobi lub innych cukrów. Szczawiooctan ulega redukcji do
jabłczanu, który jest transportowany do wakuoli i tam gromadzony w dużych
ilościach, powodując jej zakwaszenie. W czasie dnia, kiedy szparki są
zamknięte, jabłczan jest przenoszony na powrót do cytozolu i tam ulega
dekarboksylacji przez enzym jabłczanowy, dostarczając dwutlenku węgla.
Ponieważ w tym czasie zachodzą reakcje świetlnej fazy fotosyntezy i stają się
dostępne jej produkty - ATP i NADPH, uruchamia się cykl Calvina-Bensona i
zachodzi asymilacja uwolnionego dwutlenku węgla. W tym czasie następuje też
regeneracja zapasów skrobi asymilacyjnej. Zamknięte w ciągu dnia szparki nie
tylko chronią przed transpiracją, ale i nie dopuszczają do utraty uwolnionego CO
2
do atmosfery. Rośliny typu CAM podobne są pod pewnymi względami do
roślin C4. W obu tych grupach występuje wstępne wiązanie CO
2
poprzedzające cykl Calvina-Bensona. W obu przypadkach pierwotnym
akceptorem dwutlenku węgla jest fosfoenolopirogronian i tworzone są
przejściowe związki, które ulegając następnie dekarboksylacji dostarczają
odpowiednio dużego stężenia CO
2
, tak aby cykl Calvina-Bensona mógł
przebiegać z odpowiednią wydajnością. Różnicy między tymi dwoma grupami
roślin dotyczą natomiast umiejscowienia zależności czasowych procesów
wstępnej karboksylacji i dekarboksylacji. W roślinach C
4
procesy karboksylacji
fosfoenolopirogronianu do szczawiooctanu i dekarboksylacji jabłczanu
zachodzą równocześnie, ale w różnych typach
komórek, są więc oddzielone
przestrzennie.
W roślinach C AM oba procesy przebiegają w tych samych
komórkach, są jednak rozdzielone w czasie karboksylacja odbywa się w nocy,
zaś dekarboksylacja w ciągu dnia.
Strona 82

Porównanie zasadniczych cech szlaków asymilacji CO
2
- C
3,
C
4,
CAM.
*Asymilacja CO
2
przez rośliny C
3.
Produkty świetlnej fazy fotosyntezy - ATP i NADPH są zużywane do
wbudowania dwutlenku węgla w związki organiczne w procesie
określanym jako ciemna faza fotosyntezy. Rośliny u których pierwszym
produktem asymilacji dwutlenku węgla jest kwas 3-fosfoglicerynowy
oznacza się mianem roślin C
3.
Rośliny C
3
wiążą dwutlenek węgla w
procesie fotosyntezy za pomocą cyklu Calvina-Bensona. Akceptorem
dwutlenku węgla u tych roślin jest 1,5-bifosorybuloza zaś enzymem
katalizującym tą reakcję-karboksylaza 1,5bifosforybuzozy(inna nazwa rubisco).
Karboksylaza l ,5-bisfosforybulozy jest kluczowym enzymem cyklu Calvina-
Bensona, determinującym szybkość przyswajania dwutlenku węgla. Przyłącza
ona dwutlenek węgla 1,5 bisfosforybulozy dając nietrwały związek 6-węglowy,
który natychmiast rozpada się na dwie cząsteczki kwasu 3-
fosfoglicerynowego. Związany dwutlenek węgla stanowi grupę karboksylową
jednej z tych cząsteczek. Kwas 3-fosfoglicerynowy jest następnie
fosforylowany na koszt ATP do do kwasu 1,3 -bisfosfoglicerynowego, który
udziałem NADPH ulega redukcji do poziomu cukrów tj. do aldehydu 3-
fosfoglicerynowego.
W cyklu Calvina-Bensona wyróżnia się trzy fazy: karboksylacyjną, redukcyjną
regeneracyjną
.
o faza karboksylacyjna jest związana z aktywnością karboksylazy l ,5-bisfos-
forybulozy i utworzeniem 2 cząsteczek kwasu 3-fosfoglicerynowego. Reakcja
karboksylacji przebiega ze znacznym spadkiem energii swobodnej co
powoduje jej nieodwracalność, nawet gdy stężenie CO
2
jest małe.
o faza regeneracyjna polega na wytworzeniu aldehydu 3-fosfoglicerynowego w
którym uczestniczą takie enzymy jak kinaza fosfoglicerynianowa
dehydrogenaza aldehydu 3-fosfoglicerynowego.
o faza regeneracyjna polegająca na odtworzeniu 1,5 bisfosforybulozy, która
wymaga udziału takich enzymów, jak odpowiednie aldolazy, transketolazy, fos-
fatazy, izomerazy oraz epimeraza i kinaza.
*Wiązanie dwutlenku węgla w roślinach typu C
4
i CAM
Obie grupy tych roślin róznią się od roślin C
3
tym że wykształciły dodatkowy
mechanizm wiązania dwutlenku węgla poprzedzający cykl Calvina-Bensona.
Do grupy roślin określanych jako C4 zaliczamy rośliny strefy zwrotnikowej np.
kukurydza.. Liście tych roślin mają charakterystyczną Budowę anatomiczną,
w której można wyróżnić komórki miękiszu (mezofilu) liścia oraz specjalną
grupę komórek otaczających wiązki przewodzące, zwaną pochwą
okołowiązkową. W cytozolu komórek miękiszu występuje enzym
karboksylaza fosfoenolopirogronianowa , który katalizuje przyłączenie CO
2
do
wysokoenergetycznego związku - fosfoenolopirogronianu. Pierwszym
produktem przyłączenia dwutlenku węgla do fosfoenoopirogronianu jest
szczawiooctan. Utworzony szczawiooctan ulega przekształceniu w jabłczan.
który specjalnymi kanałami plasmodesma jest transportowany do komórek
pochwy okołowiązkowej. W komórkach tych następuje dekarboksylacja
jabczanu z udziałem tzw. enzymu jabłczanowego (dehydrogenaza
jabłczanowa dekarboksylująca), a uwolniony CO
2
jest ponownie wiązany przez
obecną w chloroplastach komórek pochwy okołowiązkowej karboksylazę l,5
bisfoforybulozy i następnie przekształcany zgodnie z reakcjami cyklu Calvina-
Bensona. Tworzący się w procesie dekarboksylacji pirogronian przemieszcza
się z powrotem do komórek mezofilu, gdzie ulega fosforylacji do
fosfoenolopirogronianu . Reakcja jest katalizowana jest przez dikinazę
pirogronian-fosforan, która fosforyluje nie tylko pirogronian, lecz także
cząsteczkę fosforanu nieorganicznego, zużywane są zatem dwa
wysokoenergetyczne wiązania ATP. Natomiast do roślin określanych mianem
CAM zaliczamy rośliny strefy pustynnej i półpustynnej Rośliny te ze względu na
warunki środowiska muszą prowadzić oszczędną gospodarkę wodną i aby
zapobiec nadmiernej utracie wody, otwierają szparki tylko w nocy kiedy
temperatura znacznie się obniża. Otwarcie szparek umożliwia dopływ
dwutlenku węgla do wnętrza rośliny, ale z powodu braku światła nie
przebiegają procesy świetlnej fazy fotosyntezy, dostarczające ATP i NADPH.
Dwutlenek węgla jest więc wstępnie przyłączany przez znajdującą się w
cytozolu komórek karboksylazę do fosfoenolopirogronianu i powstaje
szczawioctan. Fosfoenolpirogronian jest dostarczany przez glikolizę i
pochodzi z rozkład skrobi lub innych cukrów. Szczawiooctan ulega redukcji do
jabłczanu, który jest transportowany do wakuoli i tam gromadzony w dużych
ilościach, powodując jej zakwaszenie. W czasie dnia, kiedy szparki są
zamknięte, jabłczan jest przenoszony na powrót do cytozolu i tam ulega
dekarboksylacji przez enzym jabłczanowy, dostarczając dwutlenku węgla.
Ponieważ w tym czasie zachodzą reakcje świetlnej fazy fotosyntezy i stają się
dostępne jej produkty - ATP i NADPH, uruchamia się cykl Calvina-Bensona i
Strona 83
zachodzi asymilacja uwolnionego dwutlenku węgla. W tym czasie następuje też
regeneracja zapasów skrobi asymilacyjnej. Zamknięte w ciągu dnia szparki nie
tylko chronią przed transpiracją, ale i nie dopuszczają do utraty uwolnionego CO
2
do atmosfery. Rośliny typu CAM podobne są pod pewnymi względami do
roślin C4. W obu tych grupach występuje wstępne wiązanie CO
2
poprzedzające cykl Calvina-Bensona. W obu przypadkach pierwotnym
akceptorem dwutlenku węgla jest fosfoenolopirogronian i tworzone są
przejściowe związki, które ulegając następnie dekarboksylacji dostarczają
odpowiednio dużego stężenia CO
2
, tak aby cykl Calvina-Bensona mógł
przebiegać z odpowiednią wydajnością. Różnicy między tymi dwoma grupami
roślin dotyczą natomiast umiejscowienia zależności czasowych procesów
wstępnej karboksylacji i dekarboksylacji. W roślinach C
4
procesy karboksylacji
fosfoenolopirogronianu do szczawiooctanu i dekarboksylacji jabłczanu
zachodzą równocześnie, ale w różnych typach komórek, są więc oddzielone
przestrzennie. W roślinach C AM oba procesy przebiegają w tych samych
komórkach, są jednak rozdzielone w czasie karboksylacja odbywa się w nocy,
zaś dekarboksylacja w ciągu dnia.
Cykl Calvina – charakterystyka poszczególnych faz
Jest to tzw. ciemna faza fotosyntezy, zachodzi bez udziału światła, jednak
ma miejsce w dzień, ponieważ jest uzależniona od produktów fazy jasnej
(ATP i NADPH). Ma ona miejsce w stromie chloroplastu, gdzie znajdują się
enzymy uczestniczące w tym procesie. Cykl ten zachodzi u roślin typu C
3.
ATP i NADPH są zużywane do wbudowania CO
2
w związki organiczne.
FAZA I KARBKSYLACJA. Akceptorem dwutlenku węgla jest 1,5-
bisfosforybuloza, a reakcje katalizuje karboksylaza 1,5-bisfosforybulozy. Po
połączeniu 1,5-bisfosforybulozy i dwutlenku węgla powstaje nietrwały
związane 6-węglowy, który natychmiast się rozpada na dwie cząsteczki
kwasu 3-fosfoglicerynowego.
Karboksylaza 1,5-bisfosforybulozy (Rubisco) determinuje szybkość
przyswajania dwutlenku węgla. Aktywowana jest przez Mg
+
. Jest to jeden z
najbardziej rozpowszechnionych enzymów w świecie roślin). Jego
aktywność i pozostałych enzymów regulują też:
•
-alkalizacja stromy
•
-światło (utrzymuje w stanie zredukowanym grupy sulfhydrylowe)
Szybkość wiązania CO
2
zależy od:
•
-stężenia metabolitów pośrednich cyklu
•
-dostępności nieorganicznego fosforanu w stromie (wytwarzanie
ATP)
FAZA II
REDUKCJA
Powstały kwas 3-fosfoglicerynowy fosforylowany jest
kosztem ATP do kwasu 1,3-bisfosfoglicerynowego (enzym: kinaza
fosfoglicerynianowa), który z udziałem NADPH ulega redukcji do aldehydu
3-fosfoglicerynowego (enzym: dehydrogenaza aldehydu 3-
fosfoglicerynowego). Powstały aldehyd jest fosfotriozą, monosacharydem.
Jego część służy do syntezy dalszych sacharydów (np. glukoza,
sacharozy), a część jest skierowana na szlak prowadzący do regeneracji
akceptora dwutlenku węgla.
FAZA III
REGENERACJA
Polega na odtworzeniu 1,5-bisfosforybulozy.
Następuję to w serii zachodzących po sobie reakcji, poprzez metabolity
trój-, cztero-, pięcio- i siedmiowęglowe. (enzymy: aldolaza, fosfataza,
izomeraza, transketolaza, epimeraza pentozofosforanowa, kinaza
pentozofosforanowa).
Fosforylacje – rodzaje, mechanizmy, znaczenie.
Siłą napędową procesu fosforylacji jest gradient stężenia protonów w
poprzek błony tylakoidu. Towarzyszy on transportowi elektronów z cząst.
wody na NADP
+
. Wewnątrz pęcherzyka tylakoidy gromadzą się protony
pochodzące z rozkładu wody i uwalniane w procesie utlenienia
plastochinolu przez kompleks cytochromowy. Z kolei w stromie maleje
stężenie protonów na skutek protonacji zredukowanych cząsteczek
plastochinonu w miejscu Q
B
, aktywności cyklu Q i przekształcania
cząsteczek NADP
+
w NADPH. Ponieważ błona tylakoidy jest
nieprzepuszczalna dla protonów dochodzi do zakwaszenia wnętrza
Strona 84
tylakoidy i alkalizacji stromy. Gdy gradient protonów osiągnie pewną
wielkość a ich przepływ powoduje powstawanią ATP z ADP i fosforanu
nieorg. to proces ten to fosforylacja fotosyntetyczna.
Fosforylacja cykliczna. A tym wypadku fotosystem I działa niezależnie od
fotosystemu II. Elektrony wzbudzone przez światło przemieszczają się z
chlorofilu a – centrum reakcji fotochemicznej PSI, na łańcuch
transportumelektronów, kolejno przez ferrodoksynę, plastochinon,
kompleks cytochromowi b
6
f, plastocyjaninę i powracają na pierwotnie
wzbudzony chlorofil P700. Elektrony nie docierają do reduktazy
ferrodoksyna-NADP stąd nie powstaje NADPH. Fosforylacja ta nie jest
podstawą fotosyntezy, w przypadku ograniczonej dostępności wody lub
zwiększonego zapotrzebowania na ATP względem NADPH luz zbyt małej
ilości NADP przyjmującego elektrony, może pomagać utrzymać żywotność
i wytwarzane jest samo ATP.
Fosforylacja niecykliczna. Przepływ elektronów angażuje PSII i PSI, a
jego produktami końcowymi jest tlen, NADPH i ATP. Elektron wybity z
chlorofilu nie powraca do niego, lecz zostaje przechwycony przez
nukleotyd. Wysokoenergetyczne elektrony z PSII przechodzą przez
akceptory łańcucha transportu elektronów, zlokalizowane w błonie
tylakoidu. Elektrony przekazywane są z chlorofilu a na feofitynę, następnie
na plastochinon Q
A
, Q
B
, cytochrom b
6
f i na plastocyjaninę, poprzez którą
elektrony trafiają do centrum rekacji PSI. Aby nastąpił taki przepływ e, z
cząst. chlorofilu P700 musi zostać usunięty wcześniej elektron na skutek
wzbudzenia przez światło. Pierwszym akceptorem w PSI jest cząsteczka
chlorofilu a (A
0
), następnym A
1
(Wit. K
1
). Następnie elektrony przenoszone
są poprzez białka żelazo-siarkowe typu Fe
4
S
4
(F
0,
F
1,
F) na ferredoksynę
(zewnętrzna powierzchnia błon tylakoidów) Ostatnim etapem transferu
elektronów jest ich przeniesienie z ferredoksyny na NADP
+
. W wyniku
redukcji z udziałem reduktazy feeredoksyny-NADP
+
powstaje NADPH
(wymaga 2e pochodzących ze wzbudzenia chlorofilu i 2 protonów z
rozkładu wody).
Świetlna faza fotosyntezy – lokalizacja, przebieg,
znaczenie.
Faza świetlna polega na wykorzystaniu energii świetlnej do
wytworzenia związków bogatych w energię: ATP i NADPH (tzw. siła
asymilacyjna niezbędna do zajścia fazy ciemnej). Jest zależna od światła i
zachodzi w dzień. Ma miejsce w tylakoidach i jest związana z absorpcją
światła przez barwniki fotosyntetyczne.
Jej istotą jest oderwanie elektronów od cząsteczki wody i
przeniesienie ich na utlenioną formę NADP.
W transporcie elektronu biorą udział dwa fotoukłady (zawierają
barwniki antenowe-chlorofile i karotenoidy oraz centra reakcji
fotochemicznej) oraz przenośniki elektronów. Chlorofil a w centrum reakcji
PSII (chlorofil P680 ma max absorpcji przy 680nm ) przechodząc w stan
wzbudzony (w wyniku absorpcji światła) staje się silnym reduktorem.
Wzbudzony elektron przekazywany jest na feofitynę ( pierwotny akceptor
elektronów ). Dochodzi do separacji ładunków (oddzielenie e od barwnika).
Feofityna przekazuje elektron na przenośnik elektronów – chinon Q
A
(pierwszy stabilny akceptor elektronu ). Bezpośrednim akceptorem
elektronu w tym przenośniku jest plastochinon, który może przyjąć jeden e.
Kolejnym akceptorem jest przenośnik Q
B
( także plastochinon, ale w innym
otoczeniu białkowym ). Przyjmuje on 2 elektrony, ulega protonacji i
przechodzi w plastochinol.
Plastochinol ( nośnik elektronów z PSII ) przemieszcza się do kompleksu
cytochromowego b
6
f, który działa jako oksydoreduktaza plastochinol-
plastocyjamina.
W skład tego b
6
f wchodzą między innymi centrum żelazo-siarkowe,
dwie cząst. cytochromu b
6
i cząsteczka cytochromu f.
Energia świetlna jest także przenoszona na fotoukład pierwszy (chlorofil
P700, ma max absorpcji przy 700nm), wtedy plastocyjamina może
przekazać elektron do centrum reakcji PSI. Wzbudzona cząsteczka
chlorofilu staję się reduktorem, który ma silnie elektroujemny potencjał
redox i jest zdolny do przekazania elektronu. Pierwotnym akceptorem
Strona 85
elektronu jest cząsteczka chlorofilu A oznaczana jako A
0
. Drugim
akceptorem jest A
1
(cząst. wit. K
1
) Następnie elektrony przenoszone są
poprzez białka żelazo-siarkowe typu Fe
4
S
4
(F
0,
F
1,
F) na ferredoksynę
(zewnętrzna powierzchnia błon tylakoidów) Ostatnim etapem transferu
elektronów jest ich przeniesienie z ferredoksyny na NADP
+
. W wyniku
redukcji z udziałem reduktazy feeredoksyny-NADP
+
powstaje NADPH
(wymaga 2e pochodzących ze wzbudzenia chlorofilu i 2 protonów z
rozkładu wody). Jest to fosforylacja niecykliczna, ma tam miejsce także
fosforylacja cykliczna- PSI działa niezależnie od PSII (elektrony
transportowane z chlorofilu a, przez ferrodoksyne, plastochinon, kompleks
cytochromowy, plastocyjaninę powracają na pierwotnie wzbudzony chlorofil
P700).
Wzbudzenie PSII i PSI oraz przekazanie elektronów na pierwotne
akceptory zależą od światła, pozostałe reakcje przekazywania e zachodzą
zgodnie z gradientem potencjału redox i mogą przebiegać w ciemności.
Mechanizm rozkładu wody: uczestniczy w nim kompleks enzymat.
zawierający 4 atomy Mn. Kompleks manganowy zmieniając stan utlenienia
przekazuje elektrony do P680. Po odłączenia od atomu Mn 4e następuje
rozszczepienie 2 czast. wody na elektrony-redukują utl. Mn, protony-
uwalniane do wnętrza tylakoidy i tlen-uwalniany do atmosfery.
Metaloporfiryny roślinne
– budowa, znaczenie w metaboliźmie.
Metaloporfiryny to pochodne porfiryn, zawierają atom metalu
(żelazo, miedź, magnez), centralnie wbudowany w układ porfirynowy za
pośrednictwem atomów azotu. Przykładami metaloporfiryn są hem,
heminy, chlorofil.
Chlorofile są związkami charakterystycznymi wyłącznie dla błon
transformujących energię świetlną, pełnią one niezwykle istotną rolę w
organizmach roślinnych. Funkcją chlorofili w organizmach
przeprowadzających fotosyntezę jest wychwytywanie kwantów światła i
przekazywanie energii wzbudzenia do centrum reakcji fotoukładu skąd
wybijane są elektrony, spożytkowane następnie w dalszych etapach
fotosyntezy. Znaczna zawartość chlorofili w organizmach
fotosyntetyzujących jest odpowiedzialna za ich zieloną barwę. Wyróżnia się
wiele rodzajów chlorofili. Najbardziej rozpowszechnione w przyrodzie to
chlorofil a i chlorofil b występujące u wszystkich roślin przeprowadzających
fotosyntezę. Chlorofile c i d występują jedynie u części glonów. U
prokariontów zdolnych do przeprowadzania fotosyntezy mogą występować
chlorofil a u sinic oraz wiele rodzajów bakteriochlorofili oznaczanych
literami od a do g.
Cząsteczka każdego chlorofilu zbudowana jest z pochodnej
porfiryny określanej feoporofiryną. Feoporofiryna to pięciopierścieniowa
porfiryna z różnymi podstawnikami. Cztery z pierścieni to pierścienie
pirolowe, a piąty pierścień tworzą same atomy węgla. Wiązania pomiędzy
atomami tworzącymi pierścienie to następujące po sobie wiązania
pojedyncze i podwójne składające się na układ wiązań sprzężonych.
Centralne miejsce w układzie porfiryny zajmuje atom magnezu łączący się
z atomami azotu każdego z pierścieni. U większości chlorofili (poza
chlorofilami c) feoporfiryna łączy się poprzez wiązanie estrowe z alkoholem
o 20 atomach węgla – fitolem. Porfiryna tworząca kompleks z magnezem
posiada zdolność do absorpcji promieniowania elektromagnetycznego w
zakresie widzialnym. Przyłączony alkohol izoprenowy nie wpływa znacząco
na zdolność absorpcji światła. Jego rolą jest tworzenie hydrofobowego
fragmentu cząsteczki łączącego chlorofil z błonach białkowo-lipidowych.
Obecność magnezu wpływa na zdolność agregacji cząsteczek chlorofilu,
co ułatwia przekazywanie energii wzbudzenia pomiędzy cząsteczkami. Do
układu porfiryny w różnych miejscach przyłączone są dodatkowe grupy.
Wpływają one na niewielkie zmiany zdolności absorpcji kwantów światła
przez poszczególne rodzaje chlorofili.
Fotosyntetyczny transport elektronów.
Fotosyntetyczny transport elektronów wiąże się ze świetlną fazą
fotosyntezy, która polega na wykorzystaniu energii świetlnej do wytworzenia
związków bogatych w energię: ATP i NADPH. Jej istotą w roślinach prowadzących
oksygeniczny typ fotosyntezy, jest oderwanie elektronów od cząsteczki wody i
przeniesienie ich na utlenioną formę NADP czemu towarzyszy znaczne
powiększenie ich zasobu energii swobodnej. Wtransporcie elektronu od wody do
NADP+ uczestniczą oba fotoukładyoraz przenośniki elektronów nie związnae z
fotoukładami.
Energia kwantów światła przekazana do centrum reakcji fotoukładu II
powoduje wybicie elektronu. Elektron jest przekazywany przez cząsteczkę
feofityny, a następnie poprzez cząsteczki plastochinonu połączone z białkami na
wolny plastochinon. Powstały wskutek redukcji plastochinonu, plastochinol
przemieszcza się w błonie tylakoidu, na drodze dyfuzji, do kompleksu
Strona 86
cytochromowego b
6
f. W obrębie kompleksu cytochromowego b
6
f zachodzi cykl Q,
w wyniku którego dodatkowe protony H
+
przemieszczane są ze stromy
chloroplastów do wnętrza tylakoidów. Kompleks cytochromowy b
6
f przekazuje
elektron na niewielkie białko zwierające miedź – plastocyjaninę. Odbiorcą
elektronów od plastocyjaniny jest fotoukład I, po uprzednim wybiciu elektronów z
centrum reakcji. Wybicie elektronu z centrum reakcji fotoukładu I odbywa się
poprzez wzbudzenie cząsteczki chlorofilu. Elektron wybity z centrum reakcji
fotoukładu I przekazywany jest na cząsteczkę NADP
+
, która staje się formą
zredukowaną NADPH. W przekazaniu elektronu na cząsteczkę NADP
+
bierze
udział kilka przekaźników, między innymi cząsteczka witaminy K (filochinon) oraz
ferredoksyna. Miejsce po elektronie oderwanym z centrum reakcji fotoukładu II
zapełniane jest przez elektron oderwany z wody. Reakcja ta jest przeprowadzana
przez kompleks rozkładający wodę. Po oderwaniu 4 elektronów następuje
rozszczepienie 2 cząsteczek wody na 4 protony i cząsteczkę tlenu. W wyniku
uwalniania protonów, z rozkładu wody, wewnątrz tylakoidu – lumen, pobierania
protonów podczas redukcji NADP
+
w stromie chloroplastu oraz transportu
protonów w cyklu Q, ze stromy do wnętrza tylakoidu, powstaje gradient protonowy
– różnica stężeń protonów na zewnątrz i wewnątrz tylakoidu. Gradient protonowy
jest wykorzystywany przez kompleks syntazy ATP do wytwarzania drugiego
produktu fazy jasnej – ATP. Opisany szlak wędrówki elektronów z cząsteczki wody
na cząsteczkę NADP
+
określa się jako fosforylację niecykliczną.
W okresie zwiększonego zapotrzebowania na ATP elektron z ferredoksyny może
zostać przeniesiony nie na NADP
+
, lecz na kompleks cytochromowy b
6
f i następnie
poprzez plastocyjaninę powrócić do centrum reakcji fotoukładu II. Takiemu
cyklicznemu transportowi elektronów towarzyszy przenoszenie protonów przez
błonę tylakoidu, wytwarzanie gradientu stężeń protonów i synteza ATP, nie
powstaje jednak NADPH. Opisany szlak wędrówki elektronu nosi nazwę
fosforylacji cyklicznej.
Fotooddychanie
– współpraca różnych przedziałów
komórkowych
Fotooddychanie to proces biochemiczny zachodzący na świetle w
komórkach roślinnych, objawiający się pobieraniem tlenu i wydzielaniem
dwutlenku węgla na drodze innej niż oddychanie komórkowe.
Biochemicznie proces fotooddychania związany jest z dwufunkcyjnością
enzymu karboksylazy/oksygenazy rybulozo-1-5-bisfosforanu (RuBisCO),
odpowiedzialnego zarówno za przyłączenie do rybulozo-1,5-bisfoforanu (RuBP)
cząsteczki CO
2
, jak i cząsteczki O
2
w chloroplastach podczas oświetlania. CO
2
i O
2
konkurują o miejsce katalityczne Rubisco. W wyniku przyłączenia tlenu do
rybulozo-1-5-bisfosforanu powstaje jedna cząsteczka kwasu fosfoglicerynowego
(jak w fazie ciemnej fotosyntezy) oraz jedna cząsteczka fosfoglikolanu, pierwszego
(dwuwęglowego; C2) produktu fotooddychania. Dalsze reakcje zachodzą w
peroksysomach i mitochondriach, a następnie ponownie w chloroplastach. Stąd
pochodzi inna nazwa fotooddychania - cykl C2. Powstający w chloroplastach
fosfoglikolan ulega defosforylacji i przenoszony jest do peroksysomów. Tam przy
udziale oksydazy glikolanowej przekształcany jest do glioksalanu. Glioksalan ulega
transaminacji w dwóch reakcjach przeprowadzanych przez aminotransferazę
glutaminianową i aminotransferazę serynową, w wyniku których powstaje glicyna.
Glicyna transportowana jest do mitochondriów i przy udziale kompleksu
enzymatycznego dekarboksylazy glicyny (GDC) oraz hydroksymetylotransferazy
seryny (SHMT) przekształcana do seryny z wydzieleniem cząsteczki CO
2
, NH
3
,
oraz NADH. Powstała w mitochondriach seryna transportowana jest do
peroksysomów i przekształcana przy udziale aminotransferazy serynowej do
kwasu hydroksypirogronowego. Kwas ten ulega redukcji do kwasu glicerynowego
przy udziale reduktazy hydroksypirogronianowej. Produkt reakcji przenoszony jest
do chloroplastów i może służyć do odtworzenia cząsteczki rybulozo-1-5-
bisfosforanu. NADH produkowany przy dekarboksylacji glicyny może być
transportowany do cytozolu lub utleniany w mitochondriach.
Fotooddychanie prowadzi zatem do uwolnienia wcześniej związanego
CO
2
, jest więc procesem przynoszącym roślinie straty, marnotrawiącym energię.
Oksygenacja 1 cząsteczki 1,5-bisfosforybulozy i kolejne reakcje procesu
fotooddychania wymagają zużycia 2 cząsteczek ATP i 2,5 NADH.
Fotooddychanie zachodzi głównie u roślin typu C3 zaś w niewielkim tylko stopniu u
roślin C4. Wiąże się to z obecnością mechanizmu zagęszczającego dwutlenek
węgla w komórkach pochwy okołowiązkowej, gdzie przebiegają reakcje cyklu
Calvina-Bensona. Zwiększony stosunek CO
2
do O
2
powoduje, że dominują reakcje
karboksylacvji 1,5-bisfosforybulozy. Ponadto uwalniany dwutlenek węgla ponownie
wiąże karboksylaza fosfoenolopirogronianowa obecna w komórkach miękiszu
liścia. Tak więc rośliny typu C4 – pomimo większego niż u roślin C3 wkładu energii
na związanie 1 cząsteczki CO
2
–rosną szybciej i wykazują większe przyrosty
biomasy.
Wpływ barwy światła na fotosyntezę,
adaptacja chromatyczna.
Wpływ barwy światła na fotosyntezę :
U roślin lądowych w największym stopniu wykorzystywana jest
energia światła pochłanianego przez chlorofil (głównie niebieskie, w
mniejszym, stopniu fioletowe, czerwone, pomarańczowe i żółte), a w
mniejszym przez karotenoidy. U fotoautotrofów wodnych bywa odmiennie.
U zielenic jest podobnie jak u roślin lądowych. U sinic najefektywniej
wykorzystywane jest światło żółte pochłaniane przez niebieską
Strona 87

fikocyjaninę, u wielu krasnorostów – światło żółte i zielone (pochłaniane
przez czerwoną fikoerytrynę), okrzemek i brunatnic (glonów z grupy
stramenopili) – światło niebieskie i zielone pochłaniane przez karotenoidy.
Optymalna barwa światła (długość fali świetlnej) dla organizmów
zajmujących różne siedliska wodne związana jest z różnicami w
rozpraszaniu poszczególnych długości fal przez wodę. Barwa organizmu
fotosyntetyzującego odpowiada pasmu widma, które jest w najmniejszym
stopniu pochłaniane przez barwniki fotosyntetyczne. Glony występujące
głęboko (np. w metalimnionie) muszą zarówno mieć odpowiednią barwę
(czerwoną), jak i wykazywać właściwości skiofityczne. Przykładem są
czerwone sinice z gatunków Planktothrix rubescens i Planktothrix aghardii
var. isothrix lub kryptomonady Rhodomonas minuta osiagająca optimum na
głębokości, do której dociera 50% światła padającego na powierzchnię i
Rhodomonas lens, dla której jest to głębokość otrzymująca 10%. Niektóre
glony zmieniają barwę w zależności od zasiedlanej głębokości, np. sinice
Chamaesiphon subglobosus i Lingbya purpurescens przechodzą od barwy
zielonej do krwistoczerwonej. Zmienność wykazują też inne sinice,
krasnorosty i liczne glony morskie.
Adaptacja chromatyczna :
Adaptacja - cecha dziedziczna i podlegająca rozwojowi, będąca wynikiem
doboru naturalnego, ponieważ pomagała w przetrwaniu organizmu lub też
w jego reprodukcji. Musi ona być zapisana w genach przekazywanych
dzieciom przez rodziców, dlatego zmiany adaptacyjne mogą być
dziedziczne. Organizmy przystosowują się do środowiska, w którym żyją.
Organizmy zamieszkujące podobne siedliska często zyskują zbliżone
przystosowania zwane adaptacjami.
Adaptacja jest istotną cechą wszystkich żywych organizmów i od niej
najczęściej zależy przetrwanie w zmienionym środowisku.
Adaptacje chromatyczną można wyjaśnić przedstawiając zachowanie
glonów na poszczególne rodzaje promieni świetlnych:
glony oprócz chlorofilu posiadają także inne barwniki, które pozwalają
glonom na przystosowanie do wychwytywania światła widzialnego o
różnych długościach - dzięki temu zjawisku rośliny mogą syntetyzować na
dużych głębokościach, ponieważ docierają do nich krótkie fale, bogate w
energię
Wydajność fotosyntezy a czynniki zewnętrzne :
1.Swiatło
Jest niezbędne w pierwszej fazie fotosyntezy natężenie światła zmienia się
w ciągu roku, dnia, jest zależne od zanieczyszczenia powietrza, w lesie się
zmienia
wraz ze wzrostem natężenia światła wzrasta intensywność
przeprowadzania fotosyntezy ale tylko do pewnego czasu, gdy natężenia
jest za duże następuje blokada chlorofilu i zwiększenie transpiracji. Pod
wpływem tolerancji na światło rośliny dzielimy na: Światłożądne- mają duże
zapotrzebowanie na światło, rośliny gór, zboża. Cienioznośne- nie rosną w
pełnym świetle potrzebują jedynie 10%
np. rośliny runa leśnego.
2.CO2
Przy dostatecznym oświetleniu tempo przebiegu fotosyntezy zależy od
stężenia CO2. Wzrost stężenia CO2 o 0.15% powoduje wzrost
intensywności fotosyntezy o 3 razy.
3.Temperatura.
Najwyższa intensywność fotosyntezy jest w temp. Od 20C-30C, za niska i
za wysoka temp. Obniża i zahamowuje fotosyntezę
Przystosowanie roślin do obrony przed zimą:
- zrzucanie liści (żeby nie doprowadzić do nadmiernej utraty wody)
- rośliny iglaste - warstwa komórek tk. okrywającej o zgrubiałej kutykuli
zabezpiecza tkanka liścia, przed niską temp. I parowaniem wody
- aparaty szparkowe w zagłębieniach
4.Woda
niezbędna do I fazy fotosyntezy, decyduje o rozwartości aparatów
szparkowych.
Nadmierny ubytek wody powoduje:
- zamykanie szparek
- hamuje dopływ Co2
- nie zachodzi fotosynteza
5.Sole min.
- potrzebne do budowy zw. organicznych
- regulują procesy życiowe
- magnez- składnik chlorofilu
- azot- jago brak hamuje powstawanie chlorofilu
Strona 88
- żelazo- bierze udział w wytwarzaniu chlorofilu jak rośliny uzupełniają brak
azotu?
- żyjąc w symbiozie z bakteriami azotowymi (rośliny motylkowe)
- łapiąc owady i trawiąc je (rośliny owadożerne)
Zależność fotosyntezy od czynników
zewnętrznych
Fotosynteza zależy od takich czynników zewnętrznych jak :
DWUTLENEK WĘGLA
Średnie roczne stężenie CO2 w dolnych warstwach atmosfery jest na ogół stałe i
wynosi około 0,03% (300 ppm). Według dokładnych pomia¬rów
przeprowadzonych w 1974 r. zawartość CO2 nieco wzrosła w ciągu ostatnich
kilkudziesięciu lat i wynosi obecnie 0,035%, wykazując wy¬raźną tendencję
zwyżkową, wynoszącą około 0,00007% (0,7 ppm) na rok. Stężenie tego gazu w
wodach morskich i śródlądowych jest wyższe niż w atmosferze i wynosi około
0,6%. Głównym źródłem CO2 są procesy rozkładu materii organicznej
prze¬prowadzane w glebie przez mikroorganizmy, procesy oddychania
wszyst¬kich żywych organizmów, procesy spalania paliw w wyniku działalności
człowieka, źródła mineralne i wyziewy wulkaniczne. Dwutlenek węgla wnika do
wnętrza liścia głównie przecz szparki, a tylko nieznaczna jego część poprzez
skórkę, w której największy opór dyfuzyjny stawia kutykula. Transport CO2 z
przestworów między¬komórkowych do wnętrza chloroplastów odbywa się
natomiast znacznie wolniej . Drogę tę pokonuje CO2 pod postacią cząsteczkową,
w formie H2CO3 lub jonu HC O3Penetracja C02 przez błony cytoplazmatyczne
odbywa się najszybciej, gdy znajduje się on w formie cząsteczkowej. Szybkość
dyfuzji tego gazu w wodzie jest około 10 000 razy mniejsza niż w powietrzu. Ten
powolny transport CO2 w obrębie komórek, w połączeniu ze wglądnie jego niskim
stężeniem w powietrzu jest głów¬nym czynnikiem ograniczającym intensywność
fotosyntezy w pogodne dni sezonu wegetacy-jnego, przu optymalnym dostępie
wody i umiarko¬wanej temperaturze powietrza. O szybkości- dyfuzji CO2 z
atmosfery do chloroplastów decyduje jego stężenie w atmosferze i w centrum
reakcji fotosyntetycznej. Im ta różnica jest większa, tym przemieszczanie
CO2następuje szybciej. U roślin typu C4, bardzo sprawnie wiążących CO2
stężenie tego gazu w chloroplastach utrzymuje się na bardzo niskim poziomie, np.
3 ppm u kukurydzy. W takich warunkach szybkość transportu C02 do
chloro¬plastów zależy od jego stężenia zewnętrznego (atmosferycznego). U roślin
typu C, poziom CO2w chloroplastach jest znacznie wyższy i wynosi 30-80 ppm.
Jest to uwarunkowane funkcjonowaniem procesu foto-oddychania Stężenie CO2
przy którym istnieje stan dynamicznej równowagi pomiędzy fotosyntezą i
fotooddychaniem nazywamy punktem kompensacyjnym CO2. Im wyż¬sza jest
jego wartość, tym niższy jest gradient stężenia tego gazu pomiędzy atmosferą i
chloroplastami i tym wolniejsze jest pobieranie CC>2. Dla pomidorów punkt
kompensacyjny wynosi, w zależności od warunków uprawy i odmiany, 44-75 ppm.
Zjawisko to powoduje dalsze zmniejsze¬nie się gradientu stężenia C0„ między
atmosferą i chloroplastami, co zwalnia przebieg fotosyntezy. Stężenie CO_ w
powietrzu atmosferycznym nie jest optymalne dla .przebiegu fotosyntezy.
Zwiększenie jego stężenia, coraz częściej stosowane w uprawie roślin pod
osłonami (szklarnie, tunele foliowe), powoduje znaczny wzrost intensywności
fotosyntezy, pod warunkiem zachowania optymalnych wartości pozostałych
czynników zewnętrznych. Przy stꬿeniu CO2 powyżej 0,4-0,5% u wielu roślin
następuje przymykanie się szparek, co prowadzi do zmniejszenia intensywności
fotosyntezy. Jak już wiemy, źródłem energii dla reakcji fazy fotoche¬micznej
fotosyntezy jest promieniowanie fotosyntetycznie czynne (PAR). Do tego procesu
wykorzystywana jest jedynie nieznaczna cześć PAR padającego na liść.
Promieniowanie nie zaabsorbowane przez bar¬wniki fotosyntetyczne zostaje
wykorzystane głównie w procesie trans-piracji jako ciepło parowania. Część
promieni świetlnych zostaje przepuszczona przez blaszkę liściową (transmisja) lub
odbita od jej powierzchni (refleksja). Ilość światła zaabsorbowanego,
przepuszczonego i odbitego zależy od optycznych właściwości blaszki liściowej, a
więc od jej grubości, gładkości kutykuli i jej zdolności do odbijania promieni
świetlnych, od rodzaju i ilości bar¬wników zawartych w komórkach mezofilu
fotosyntetycznego, jak również od kąta ustawienia blaszki liściowej w stosunku do
kierunku padania promieni świetlnych. Największe zmiany właściwości optycznych
liścia zachodzą w początkowych fazach jego rozwoju. Ilość energii świetlnej
bezpośrednio wykorzystywanej do procesu fotosyntezy jest niewielka i wynosi 0,5-
3,5% u roślin typu C, oraz do 7% u roślin C4 Wartość tę wyrażoną w procentach
światła zaabsor¬bowanego przez liść nazywamy współczynnikiem wy¬korzystania
światła w fotosyntezie. Natężenie światła fotosyntetycznie czynnego, czyli
intensywność napromienienia określamy za pomocą fotointegratorów
elektronicznych. W ciemności odbywa się w liściach proces oddychania mający
prze¬ciwstawny do fotosyntezy kierunek wymiany gazowej . W miarę wzrostu PAR
zmniejsza się udział wymiany gazowej związanej z oddychaniem, w związku z
uruchomieniem procesu fotosyntezy. Przy określonym dla danego gatunku rośliny i
wieku liścia natężeniu PAR, następuje skompensowanie wymiany gazowej
Strona 89

oddychania i fotosyntezy. Objętość C0_ wydzielonego w procesie oddychania
równa jest objętości tego gazu zużytego do procesu fotosyntezy. Natężenie
światła, przy którym na¬stępuje kompensacja obu tych procesów nazywamy
punktem kompensacyjnym świetlnym. Wartość ta zależy od gatunku rośliny, wieku
liścia oraz od niektórych czynników zew¬nętrznych, zwłaszcza temperatury i
stężenia CC>2. Analizator CO2uży¬ty do pomiarów nie wykaże w tych warunkach
żadnej wymiany gazowej między liściem i atmosferą. Wzrost natężenia PAR
powyżej punktu kom¬pensacyjnego ujawni zużywanie CO2, co będzie dowodem
przewagi foto¬syntezy nad oddychaniem. W miarę zwiększania się intensywności
na¬promienienia wzrastać będzie intensywność fotosyntezy. U roślin typu C.
przyrosty zużywania CO2 będą miały miejsce na¬wet przy maksymalnych
natężeniach światła, co obrazuje stale wzno¬sząca się krzywa wykresu
odnoszącego się do kukurydzy (rys. 78). Rośliny typu C^ nie mają zdolności do tak
efektywnego wykorzystywa¬nia wysokich intensywności PAR i ujawniają
stabilizację intensywności fotosyntezy powyżej określonej wartości
napromienienia, zwanej punktem wysycenia. Punkt wysycenia układu fotosyn-
tetycznego światłem zależy od rodzaju i wieku rośliny oraz od nietórych czynników
zewnętrznych, np. stężenia CO2. Znaczne różnice w wartościach punktu
kompensacyjnego świetlnego oraz punktu wysyce-nia istnieją pomiędzy roślinami
światłolubnymi i cieniolubnymi (lub ściślej cienioznośnymi). U tych ostatnich
obydwa punkty przypadają przy znacznie niższych natężeniach PAR, zwłaszcza
punkt wysycenia, a intensywność fotosyntezy jest znacznie niższa niż u roślin
świa-tłolubnych.Nadmiernie wysoka intensywność światła niekorzystnie wpływa na
aparat fotosyntetyczny u roślin typu C4, powodując fotoutle-nianie chlorofilu iw
konsekwencji obniżenie się natężenia fotosyntezy . Szcze¬gólnie wrażliwe na
nadmiernie wysokie wartości PAR są rośliny cienio-lubne. Wysoka zawartość
barwników karotenoidowych zwiększa odporność liści na destrukcyjny wpływ
bardzo intensywnego światła. Obserwowany często spadek natężenia fotosyntezy
przy bardzo wyso¬kich intensywnościach światła nie zawsze jest wynikiem
fotoutlenia-nia chlorofilu. W takich bowiem warunkach blaszka liściowa ulega
nadmiernemu nagrzaniu, któremu towarzyszy początkowo silny wzrost transpiracjl,
czego następstwem są zaburzenia w bilansie wodnym, przymkniecie szparek i w
konsekwencji ograniczenie natężenia foto¬syntezy oraz ograniczenie dalszej
utraty wody.
TEMPERATURA
Fotosynteza może przebiegać w zakresie temperatur, w których zwią¬zki białkowe
wykazują aktywność biologiczną, a więc od około 0C do około 50C. Znane są
jednak przykłady roślin zdolnych do przeprowa¬dzania fotosyntezy w niższych lub
wyższych temperaturach. Tempera¬turę, przy której proces fotosyntezy zostaje
zapoczątkowany nazywamy minimalną. Jest ona różna dla rozmaitych gatunków
roślin i może wynosić poniżej 0C, np. u drzew szpilkowych, zbóż ozimych oraz u
roślin alpejskich i arktycznych, może jednak dochodzić do 5 lub 10C w przypadku
roślin pochodzących z cieplejszych stref klima¬tycznych, np. ogórków, melonów i
wielu roślin ozdobnych. Większość roślin zapoczątkowuje jednak fotosyntezę w
temperaturze zbliżonej do 0C. Nadmierną ciepłotę, przy której fotosynteza ulega
zatrzyma¬niu nazywamy temperaturą maksymalną. Wykażuje ona również pewne
wahania u różnych roślin. Znane są pewne glo-nY żyjące w gorących źródłach,
które przeprowadzają fotosyntezę w temperaturze 70C. Większość roślin
uprawnych zatrzymuje jednak pro¬ces asymilacji C02 już w temperaturze 40-50C,
a rośliny typu C. w 55C. Ciekawą grupę stanowią rośliny arktyczne i alpejskie, u
któ¬rych temperatura maksymalna na ogół nie przekracza 25C. Pomiędzy tymi
skrajnymi wartościami termicznymi dla fotosyntezy mieści się temperatura
optymalna, przy której proces ten przebiega przez długi czas najszybciej i na
stałym poziomie. Tempe¬ratura optymalna dla różnych roślin ma różne wartości. U
roślin CU wynosi ona około 25C, natomiast u C, osiąga 35C. U roślin
ciepło¬lubnych, należących do grupy C.,, np. u ogórka, temperatura optymalna
mieści się w granicach 30-35C. Przy niskich natężeniach światła optimum
temperaturowe dla fotosyntezy zaznacza się bardzo słabo. Nadmienić należy, że
wartość optimum temperaturowego zależy nie tyl¬ko od gatunku rośliny, ale
również od niektórych czynników zewnętrz¬nych, np. stężenia CC>2• Przy
wyższych stężeniach tego gazu tempera¬tura optymalna dla fotosyntezy ulega
podwyższeniu, przy równoczesnym wzroście natężenia procesu. Wzrost
temperatury o 10C w zakresie od temperatury minimalnej do optymalnej zwiększa
intensywność fotosyntezy o 1,2 do 2,7 razy, a wartość tę nazywamy
współczynnikiem Q-in' z9O|3nie z prawem Van't Hoffa, wzrost temperatury o 10C
zwiększa szybkość reakcji chemicznej 2-3 razy. Ponieważ fotosynteza jest
procesem bar¬dzo ułożonym, fotochemiczno-biochemicznym ze znacznym
udziałem zja¬wisk fizycznych (np. dyfuzja gazów), dlatego występują u niej pewne
odchylenia od tego prawa. Przy pomiarze temperatury optymalnej dla fotosyntezy
należy uwz¬ględnić fakt, że liście oświetlone odznaczają się wyższą temperaturą o
około 5C od temperatury otaczającego je powietrza. Dłuższy prze¬bieg
fotosyntezy w temperaturach ponadoptymalnych nie jest wskazany ze wzglądu na
silnie zahamowany powrót do pierwotnej szybkości prze¬biegu procesu, po
Strona 90

obniżeniu temperatury do wartości optymalnej. Tem¬peratura zbliżona do
maksymalnej inaktywuje enzymy katalizujące re¬akcje fazy ciemna j, powodując
zmiany w strukturze białek apoenzymów. Należy podkreślić, że wrażliwość
enzymów aparatu fotosyntetycznego na wyższe temperatury jest większa niż
enzymów zaangażowanych w pro¬Cesie oddychania. Temperatura optymalna dla
oddychania jest z reguływyższa o około 10C od optimum temperaturowego dla
fotosyntezy. Zna¬jomość tego faktu ma duże znaczenie przy uprawie roślin pod
osłonami. Przy uprawie roślin w zbyt wysokich temperaturach przewaga procesu
fotosyntezy nad procesami katabolicznymi drastycz¬nie maleje lub zanika,
natomiast wyraźnie zaznacza się udział, a cza¬sem przewaga procesu
oddychania (i fotooddychania u roślin C4)., . Przy określonej, ponadoptymalnej
temperaturze dla fotosyntezy obserwujemy zanik wymiany gazowej między liściem
i atmosferą. Zjawisko to sygna¬lizuje osiągnięcie punktu kompensacyjnego
termicznego, przy którym intensywność fotosyntezy równo¬ważona jest przez
oddychanie lub fotooddychanie. Na tempo fotosyntezy wywiera również wpływ
temperatura gleby w strefie systemu korzeniowego. Ważne jest, aby nie odbiegała
ona zna¬cznie od temperatury optymalnej dla fotosyntezy. 'Większe różnice w
temperaturze liści i korzeni, np. rzędu 10C, wyraźnie zmniejszają szybkość
przebiegu fotosyntezy. Większość roślin C, w temperaturze poniżej 16-18C
odznacza się wyższą niż u roślin C4. intensywnością fotosyntezy. Przewaga roślin
C^ nad G.J zaznacza, się natomiast w temperaturze powyżej 20C. Zjawisko to
wynika z przesunięcia kardynalnych temperatur dla fotosynte¬zy (minimalnej,
optymalnej i maksymalnej) u roślin C,, ku wyższym wartościom.
TLEN
Tlen w stężeniu atmosferycznym ogranicza tempo fotosyntezy u ro¬ślin C.,. Można
się o tym przekonać mierząc natężenie tego procesu przy stężeniu tlenu 1-3%. W
tych warunkach fotosynteza przebiega o 35-90% szybciej, w zależności od
gatunku rośliny i warunków termicz¬nych. Efekt ten zaobserwowany po raz
pierwszy przez Warburga w 1920 r., został nazwany jego nazwiskiem.
Obniżenie stężenia tlenu poniżej 21% nie wywiera natomiast wpły¬wu na szybkość
fotosyntezy u roślin typu C.. Hamujący wpływ tlenu wiąże się z procesem
fotooddychania, występującym u roślin C,. Stwierdzono, że karboksylaza RuDP
ma równie wysokie powinowactwo do O, jak i do CO2, i przy normalnym składzie
atmosfery funkcjonuje jednocześnie jak karboksylaza i oksygenaza. Tlen i
dwutlenek węgla konkurują ze sobą o aktywne miejsce enzymu. Przy obniżonej
zawarto¬ści tlenu w powietrzu ma przewagę CO2, natomiast przy spadku
stęże¬nia tego gazu karboksylaza RuDP ujawnia przewagę funkcji oksygena-
tywnej. W wyniku tego zmniejsza się produkcja fosfoglicerynianu włą¬czanego w
cykl Calvina-Bensona, natomiast wzrasta produkcja g l i-kolanu będącego
substratem w procesie fotooddychania. Ponadto tlen hamuje również transport
elektronów i fosforylację fotosynte-tyczną oraz sprzyja reakcji fotoutleniania
chlorofilu przy nadmier¬nie wysokich natężeniach światła. W tabeli 22
przedstawiono różnice w intensywności fotosyntezy netto u kilku roślin uprawnych
typu C3 i C4 przy atmosferycznym i obniżonym stężeniu tlenu oraz przy
opty¬malnym natężeniu światła i atmosferycznym stężeniu CO2. Jeżeli stężenie
tlenu przekracza 21%,hamowanie fotosyntezy wystę¬puje nawet u roślin C4:
do 40% tlenu - brak hamowania
przy 80% tlenu - hamowanie w 50%
przy 100% tlenu - hamowanie w 70%.
Po obniżeniu stężenia tlenu ze 100% do 21%, fotosynteza u roślin C. utrzymuje się
przez dłuższy czas na poziomie 30-50% szybkości nor¬malnej . Dane te wskazują,
że działanie tlenu nie ogranicza się tyl¬ko do stymulowania fotooddychania. Wpływ
stężenia tlenu na fotosyntezą u kilku gatunków roślin rolniczych typu C3, i C4
Obniżając stężenie tlenu do poziomu sprzed 2 miliardów lat, a więc 0,02%,
uzyskujemy wzrost intensywności fotosyntezy netto. W ta¬kich warunkach
sprawniej funkcjonuje karboksylaza RuDP, gdyż jej oksygenazowa działalność
zostaje zupełnie przytłumiona. Fakt ten jest mocnym argumentem wskazującym na
starszy ewolucyjnie charakter metabolizmu fotosyntetycznego typu C.
WODA
Woda stanowi jeden z surowców w procesie fotosyntezy, jest bowiem źródłem
elektronów i protonów wodoru, niezbędnych do redukcji zaab¬sorbowanego CO2.
Ze względu na niewielką ilość wody biorącej udział w syntezie cukrów (na syntezę
1 g cukru roślina zużywa 0,6 g wody), wydaje się mało prawdopodobne, aby jej
deficyt w tkankach wywierał bezpośredni wpływ na fotosyntezę.
Niedobór wody w organizmie rośliny wpływa natomiast pośrednio na proces
asymilacji CO,, powodując zamknięcie się szparek liściowych i i odcięcie tym
samym dostępu CO- do liści. Obserwowany niekiedy spa¬dek intensywności
fotosyntezy w upalne dni w godzinach południowych jest najczęściej
spowodowany zamykaniem się szparek. Powoduje to bardzo silny wzrost oporów
dyfuzyjnych dla C02 w liściu, co w przy¬padku mało drożnej dla gazów kutykuli
ogranicza proces fotosyntezy do minimum. Deficyt wody w liściach hamuje nie
tylko szybkość dyfuzji CO2 do chloroplastów, ale również zmniejsza ogólną
aktywność biochemiczną tych organelli. Przekonano się o tym porównując
przebieg fotosyntezy u chloroplastów wyizolowanych z liści zwiędłych oraz z liści
Strona 91

znaj¬dujących się w pełnym turgorze. Ważne jest przeto, aby w warunkach
intensywnej fotosyntezy zabezpieczyć optymalny dostęp wody roślinom
uprawnym. Zawartość wody w liściach waha się w granicach 80-95%.
Przymykanie się szparek następuje przy spadku ilości wody o kilka do około 20%.
Zależy to od tego, czy roślina ma budowę ksero-, czy higromorficzną.
INNE ZEWNĘTRZNE CZYNNIKI FOTOSYNTEZY
Spośród pozostałych czynników zewnętrznych fotosyntezy na uwagę zasługują
ruchy powietrza (wiatr) i składniki mineralne. Wpływ wiatru na fotosyntezę
sprowadza się do usuwania z sąsiedztwa liści warstewek powietrza zubożonych w
CO2 i zastępowania go powietrzem o normalnym stężeniu tego gazu. Silny wiatr,
powodujący przymykanie się szparek, obniża intensywność fotosyntezy. Na
fotosyntezę wywierają silny wpływ składniki mineralne, zwłaszcza te, które
bezpośrednio lub pośrednio uczestniczą w tym procesie. Należą do nich: azot,
potas, fosfor, żelazo, magnez i mangan. Ostatnio stwierdzono również
niezbędność chloru w tym procesie. Istnie¬je wyraźna zależność między
zaopatrzeniem roślin w te składniki, a szybkością fotosyntezy Niedobór azotu
powoduje spadek fotosyntezy, a ponadto objawia się blednięciem liści (chlorozą).
O roli azotu w fotosyntezie świadczy fakt, że 3/4 ogólnej ilości tego pierwiastka w
liściach znajduje się w chloroplastach. Potas spełnia w fotosyntezie rolę
aktywatora enzymów uczestniczących w reakcjach fazy świetlnej, np. w fosforylacji
fotosyntetycznej. Wpływa on również pośrednio na fotosyntezę uczestnicząc we
floemowym transporcie asymilatów oraz w regulacji stopnia otwarcia szparek.
Wpływ fosforu na fotosyntezę zaznacza się słabiej niż azotu. Jego niedobór
zaburza proces fosforylacji i wywołuje deformacją grań, przy czym szczególnie
wyraźnie reagują na jego niedobór buraki i szpinak. Żelazo wpływa na syntezę
chlorofilu nie wchodząc w jego skład, a deficyt tego pierwiastka, poza obniżeniem
intensywności fotosyntezy, powoduje chlorozę liści. Magnez wchodzi w skład
chlorofili i jego niedobór powoduje spadek zawartości tych barwników, zwłaszcza u
liści starszych. Mangan z kolei w niewyjaśniony jeszcze sposób uczestniczy wraz z
chlorem w fotolitycznym rozkładzie wody i pośrednio kontroluje poziom czynnika
redukującego, produkowanego w fazie świetlnej fotosyntezy. Znaczny deficyt
manganu powoduje dezorganizację układu membranowego w chloroplastach, co.
może spowodować obniżenie tempa fotosyntezy o blisko 50%.
PRAWO CZYNNIKA OGRANICZAJĄCEGO W FOTOSYNTEZIE
Prawo to ogłoszone przez Blackmana na początku XX w. jest modyfikacją
znanego prawa minimum Liebiga, według którego wysokośó plonu rośliny zależy
od tego składnika mineralnego, który znajduje się w glebie w minimum
fizjologicznym. Według Blackinana natężenie fotosyntezy kontrolowane przez
wrele czynników zewnętrznych jest determinowane przez ten czynnik, którego
wartość najbardziej odbiega od optimum. Nazywamy go czynnikiem ograniczaj
ącym lub czynnikiem minimum. Prawo to stosuje się również do każdego procesu
fizjologicznego, który jest regulowany przez czynniki zewnętrzne, a w pewnych
przypadkach i wewnętrzne. W tym przypadku wzrost intensywności fotosyntezy
postępuje do stężenia 0,12% CO2 Oznacza to, że przy wymienionym natężeniu
PAR będzie ono czynnikiem ograniczającym dopiero wówczas, gdy stężenie CO2
przekroczy O,12%,natomiast poniżej tej wartości proces będzie limitowany przez
CO2 Z prawem czynnika ograniczającego w fotosyntezie spotykamy się w
praktyce ogrodniczej nieustannie. Jego znajomość jest szczególnie ważna przy
uprawie roślin pod osłonami, gdyż technologia ta pozwala na częściowe
regulowanie najważniejszych czynników fotosyntezy, przede wszystkim
temperatury, CO2, światła i dostępu wody, przez ogrzewanie lub wietrzenie,
dokarmianie CO2 , doświetlanie i podlewanie uprawianych roślin .. Należy przy
tym pamiętać, że poszczególne czynniki nie działają na rośliny niezależnie od
siebie, lecz w sposób kompleksowy, wywierając również wzajemny wpływ na
siebie . Na przykład zwiększeniu intensywności napromieniania towarzyszy
zawsze wzrost temperatury blaszki liściowej. Przewidywanie zmian w
intensywności fotosyntezy pod wpływem zmiany w natężeniu kontrolowanych
przez nas czynników
Natężenie fotosyntezy a czynniki zewnętrzne
•
Światło
-rośliny wykorzystują
∼
4,5-4% całkowitej energii słonecznej docierające do
Ziemi.
-
zakres wykorzystywanego światła, czyli promieniowanie fotosyntetycznie czynne: 400-
700nm
-Wykres zależności natężenia fotosyntezy od natężenia światła:
Linia prosta w zakresie małego
natężenia światła- ukazuje ścisłą
proporcjonalność między natężeniem
fotosyntezy a intensywnością światła,
aż do momentu wysycenia światłem.
Strona 92

Efekt wysycenia- dalsze zwiększanie intensywności nie zwiększy natężenia
fotosyntezy; inne czynniki działają ograniczająco na intensywność
fotosyntezy.
Świetlny punkt kompensacyjny- dla natężeń światła mniejszych niż w tym
pkt. wydzielanie CO2 (proces oddychania) przewyższa proces fotosyntezy
Dla stężenia CO2=0,036% (st. atmosferyczne) i temp.=20st C świetlny pkt.
kompensacyjny≈8-15μmol/m
2
s
-Światło jest bardzo zmiennym czynnikiem. Podlega ciągłym wahaniom
(strefa klimatyczna, pora roku, pora doby, zachmurzenie, pogoda, miejsce
występowania rośliny).
W celu optymalnego wykorzystania światła rośliny wykształciły różne
przystosowania:
Światłolubne różnią się budową liści i strukturą aparatu fotosyntetycznego
od cieniolubnych - Liście cieniolubnych są cieńsze
- mają krótsze komórki miękiszu palisadowego
-posiadają większą proporcję chl.a do chl.b
-Większa proporcja PSII do PSI
-większe anteny energetyczne
- większa il. chlorofilu
- obniżenie świetlnego pkt. kompensacyjnego.
- mniejsze oddychanie mitochondrialne.
Zarówno nadmiar jak i niedobór światła mogą działać ograniczająco na
fotosyntezę. Małe natężenie poniżej pkt. kompensacyjnego powoduje
utratę CO
2
, czyli zachodzi proces oddychania. Duże natężenie powoduje
zmniejszenie fotosyntezy, destrukcję aparatu fotosyntetycznego oraz
fotoinhibicję- nadmiar stanów wzbudzonych barwników
fotosyntetycznych, które nie mogą być wykorzystane do reakcji fotochem.
może prowadzić do uszkodzenia aparatu fotosyntetycznego. Zmniejsza się
wydajność wydzielania O
2
i wiązania CO
2
. Uszkodzeniu ulega PSII.
•
CO
2
-zawartość w powietrzu = 0,036%
-dla fotosyntezy znaczenie ma zawartość CO2 w stromie chloroplastu,
gdzie zachodzi karboksylacja katalizowana przez 1,5-bisfosforybulozę
-barierą dla wnikania CO2 są:
∗
opór warstwy granicznej –warstwa mało ruchliwego powietrza
przylegającego do powierzchni liści
∗
aparaty szparkowe – stopień rozwarcia szparek ma
decydujący wpływ na intensywność wymiany gazowej.
∗
dyfuzja CO2 w przestworach międzykomórkowych miękiszu
gąbczastego
∗
dyfuzja CO2 w komórkach, przebiegająca w cieczy
Przez aparaty szparkowe wydostaje się do atmosfery tlen
produkowany podczas fotosyntezy, oraz para wodna. Rośliny gorącego i
suchego klimatu muszą zamykać
szparki aby ochronić się przed
nadmierną transpiracją zmniejszając
równocześnie dopływ CO
2
co powoduje
zmniejszenie wydajności fotosyntezy.
Rośliny C4 i CAM wykształciły
mechanizmy obronne zagęszczania
CO2 w liściu by jego stężenie było
optymalne w miejscu działanie 1,5-
bisfosforybulozy.
-Obliczenie stężenie CO2 w
przestworach międzykomórkowych:
C
i
= C
a
-
C
i
- ciśnienie parcjalne CO2 w liściu
C
a
- ciśnienie parcjalne w atmosferze
A- natężenie fotosyntezy mierzone np. intensywnością wydzielonego O
2
P- ciśnienie atmosferyczne
g- przenikalność pary wodnej przez szparkę
1,6 – współczynnik dyfuzji między CO2 a H2O
Strona 93

Punkt kompensacyjny stężenia CO2 – określa stężenie, w którym
asymilacja CO2 równoważy jego utratę w procesie oddychania.
Zależność natężenie fotosyntezy od stężenia CO2 dla roślin typu C3 i C4
– w optymalnych pozostałych warunkach wpływających na ten proces:
Linie zielone- stężenie CO2 w otaczającej atmosferze
Linie czarne – aktualne stężenie CO2 w przestworach
międzykomórkowych liścia
Krzywe charakteryzujące tę zależność mają nieco inny przebieg dla
wyliczonego stężenie CO2 wewnątrz liścia niż dla zawartości tego związku
mierzonej w otaczającej atmosferze. To dlatego, że podczas intensywnie
zachodzącej fotosyntezy stężenie CO2 wewnątrz liścia jest mniejsze niż w
otaczającej atmosferze.
Analogicznie do świetlnego punktu kompensacyjnego można wyznaczyć
punkt kompensacyjny stężenia CO2- stężenie, w którym asymilacja CO2
równoważy się z jego utratą w procesie oddychania.
•
Temperatura
- 0-50˚C –zakres temperatur dla których możliwa jest fotosynteza
- Wpływ temperatury na natężenie fotosyntezy ma charakter kompleksowy
i zależy od gatunku rośliny oraz od innych czynników tj. natężenie światła,
stężenie CO2
-Temperatura wpływa na powinowactwo enzymu 1,5-bisfosforybulozy do
CO2
Wzrost temperatury przyspiesza karboksylację lecz jednocześnie
zmniejsza powinowactwo tego enzymu do CO2, co powoduje
przyspieszenie fotooddychania. U roślin C3 ulega zwiększeniu wartość
pkt. kompensacyjnego CO2 i zmniejszenia wydajności kwantowej
fotosyntezy.
-Powyżej 40 st. C. – aparat fotosyntetyczny ulega uszkodzeniu
- 45-50 st. C – inaktywacja układu rozszczepiającego H2O
- 60-70 st. C – denaturacja kompleksów chlorofilowo-białkowych.
- W niskich temperaturach fotosyntezę może ograniczyć dostępność
fosforanów w chloroplastach.
-Zmniejsza się płynność błon fotosyntetycznych, co spowalnia proces
dyfuzji przenośników.
•
Woda
-Wydajność fotosyntezy wiąże się z gospodarką wodną i procesem
transpiracji.
- Otwieranie szparek powoduje wnikanie CO2 i utratę H2O. na ilość straty
wody wpływa temperatura i wilgotność.
U roślin C3 może być to utrata kilkuset cząsteczek wody na 1 pobraną
cząsteczkę CO2
-Niedobór H2O powoduje utratę turgoru – więdnięcie.
- Z początku następuje spowolnienie, po czym całkowite zahamowanie
procesu fotosyntezy.
-Tolerancja na utratę H2O zależy od gatunku. Niektóre więdną przy stracie
30-50%, inne znoszą całkowite odwodnienie.
Substancje zapasowe roślin – krótka
charakterystyka.
UDP-glukoza + fruktozo-6-fosforan -(enzym syntetaza fosforanu glukozy)-
sacharozo-6-fosforan –>( - Pi)
sacharoza
-Komórki odznaczają się zdolnością gromadzenia materiałów zapasowych
takich jak w
ę
glowodany
,tłuszcze wła
ś ciwe i białka
. Niektóre komórki
roślinne, zwłaszcza mi
ę
kiszu spichrzowego
gromadzą bardzo duże ilości
substancji zapasowych.
Cukry
Najczęściej gromadzonym węglowodanem jest skrobia. Jest
podstawowym wielocukrem występującym w roślinach. Od innych
wielocukrów różni się tym, że tworzy ziarna o charakterystycznym dla
Strona 94

danej rośliny kształtach. Skrobia nie jest substancją jednolitą, lecz składa
się z 2 różnych komponentów – amylozy
i amylopektyny
.
amyloza jest zbudowana z 100 – 300 reszt glukozowych,
połączonych (wiązaniami β-1,4-glikozydowymi) w długi nierozgałęziony i
skręcony spiralnie łańcuch.
amylopektyna jest również zbudowana z reszt glukozowych, lecz
na jej łańcuchu głównym osadzone są łańcuchy boczne (wiązanie β-1,6-
glikozydowe) od których odchodzą dalsze rozgałęzienia. W sumie daje to
rozgałęzioną cząsteczkę zbudowaną z około 1000 reszt glukozowych.
Łańcuchy główne i boczne są śrubowo skręcone.
- Skrobia asymilacyjna powstaje w chloroplastach podczas dnia,
kiedy wytwarzanie fosfotrioz w fotosyntezie przewyższa ich eksport do
cytoplazmy. Skrobię wykorzystują rośliny w czasie nocy na potrzeby
energetyczne. Wówczas ulega ona przekształceniu w cukry rozpuszczalne
głównie w sacharoz
ę
i w tej postaci zostaje przetransportowana do innych
organów rośliny.
-Dla zapoczątkowanie syntezy skrobi niezbędna jest obecność
krótkiego łańcucha reszt glukozy, do którego pod działaniem syntetazy
skrobi kolejno przyłączane są cząsteczki UDP lub ADP-glukozy. Tak
powstają nierozgałęzione łańcuchy amylozy. Enzym rozgałęziający
rozrywa ten łańcuch i przenosi jego jedną cześć na drugi łańcuch
amylopektyna.
-w wakuolach buraka cukrowego i trzciny cukrowej magazynowana
jest sacharoza
-
to dwucukier zbudowany z glukozy połączonej z
cząsteczką fruktozy. Jej synteza następuje przez połączenie się UDP-
glukozy z fruktozo-6-fosforanem.
-Sacharoza powstaje albo bezpośrednio z cukrów tworzących się
podczas fotosyntezy, albo pośrednio ze skrobi zmagazynowanej w różnych
częściach rośliny. Jest ona głównym cukrem transportowym.
Tłuszcze
-gromadzone przeważnie w postaci kropli zawieszonych w cytoplazmie.
-gromadzone są w komórkach miękiszu spichrzowego.
-szczególnie dużo tłuszczów magazynują nasiona rzepaku, lnu,
słonecznika (rośliny oleiste).
-
Tłuszcze wła
ś ciwe
(triacyloglicerole) stanowią materiał zapasowy.
Występują, w cytozolu w postaci kropel zwanych oleosomami. Tłuszcze w
roślinach występują w formie olejów (tłuszcze płynne w temperaturze
pokojowej) zawierające znaczny procent kwasów
nienasyconych. Tłuszcze właściwe są estrami wyższych kwasów
tłuszczowych i alkoholi trójwodorotlenowego – glicerolu. Jak wszystkie
tłuszczowce są nierozpuszczalne w wodzie, natomiast łatwo rozpuszczają
się w rozpuszczalnikach (eter, benzen, chloroform).
Białka
-występują w wakuolach i w postaci ziaren aleuronowych w nasionach,
głównie roślin motylkowych i ziarniaków zbóż.
-Zapasowe białka nasion, zmagazynowane w liścieniach lub w bielmie
ulegają podczas kiełkowania hydrolizie pod wpływem proteaz , w rezultacie
powstają wolne aminokwasy, które przemieszczają się do rosnących
tkanek, gdzie służą jako materiał wyjściowy do syntez nowych
aminokwasów i nowych białek. W toku tych przemian zachodzą procesy
transaminacji
(przekazanie grupy aminowej ketokwasów) oraz oksydacyjnej dezaminacji
(odłączenie amoniaku). Wytworzone w ten sposób amidy – glutamina i
asparagina stanowią zapas azotu do dalszych przemian.
-gdy w młodej roślinie zaczyn działać aparat fotosyntetyczny, rozpoczyna
się też synteza nowych aminokwasów. Materiały wyjściowe do produkcji
białek tworzą się w chloroplastach bądź dopływają z korzeni.
-Procesy syntezy białkach dominuj
ą
w młodszych li
ś ciach.
Zapasowe węglowodany roślin:
Najczęściej gromadzonym węglowodanem jest skrobia. Jest
podstawowym wielocukrem występującym w roślinach. Od innych
wielocukrów różni się tym, że tworzy ziarna o charakterystycznym dla
danej rośliny kształtach.
Strona 95
Skrobia nie jest substancją jednolitą, lecz składa się z 2 różnych
komponentów – amylozy
i amylopektyny
.
amyloza jest zbudowana ze 100 – 300 reszt glukozowych,
połączonych (wiązaniami β-1,4-glikozydowymi) w długi nierozgałęziony i
skręcony spiralnie łańcuch.
amylopektyna jest również zbudowana z reszt glukozowych, lecz
na jej łańcuchu głównym osadzone są łańcuchy boczne (wiązanie β-1,6-
glikozydowe) od których odchodzą dalsze rozgałęzienia. W sumie daje to
rozgałęzioną cząsteczkę zbudowaną z około 1000 reszt glukozowych.
Łańcuchy główne i boczne są śrubowo skręcone.
Enzymatyczna faza fotosyntezy – zróżnicowanie przebiegu u różnych
organizmów roślinnych.
Enzymatyczna faza fotosyntezy to tzw. ciemna faza
fotosyntezy.
*Asymilacja CO
2
przez rośliny C
3.
Produkty świetlnej fazy fotosyntezy - ATP i NADPH są zużywane do wbudowania
dwutlenku węgla w związki organiczne w procesie określanym jako ciemna faza
fotosyntezy. Rośliny u których pierwszym produktem asymilacji dwutlenku węgla jest
kwas 3-fosfoglicerynowy oznacza się mianem roślin C
3.
Rośliny C
3
wiążą dwutlenek
węgla w procesie fotosyntezy za pomocą cyklu Calvina-Bensona.
Faza ciemna zachodzi w 3 fazach:
FAZA I KARBKSYLACJA. Akceptorem dwutlenku węgla jest 1,5-
bisfosforybuloza, a reakcje katalizuje karboksylaza 1,5-bisfosforybulozy. Po
połączeniu 1,5-bisfosforybulozy i dwutlenku węgla powstaje nietrwały
związane 6-węglowy, który natychmiast się rozpada na dwie cząsteczki
kwasu 3-fosfoglicerynowego.
Karboksylaza 1,5-bisfosforybulozy (Rubisco) determinuje szybkość
przyswajania dwutlenku węgla. Aktywowana jest przez Mg
+
. Jest to jeden z
najbardziej rozpowszechnionych enzymów w świecie roślin). Jego
aktywność i pozostałych enzymów regulują też:
-alkalizacja stromy
-światło (utrzymuje w stanie zredukowanym grupy sulfhydrylowe)
Szybkość wiązania CO
2
zależy od:
-stężenia metabolitów pośrednich cyklu
-dostępności nieorganicznego fosforanu w stromie (wytwarzanie ATP)
FAZA II
REDUKCJA
Powstały kwas 3-fosfoglicerynowy fosforylowany jest
kosztem ATP do kwasu 1,3-bisfosfoglicerynowego (enzym: kinaza
fosfoglicerynianowa), który z udziałem NADPH ulega redukcji do aldehydu
3-fosfoglicerynowego (enzym: dehydrogenaza aldehydu 3-
fosfoglicerynowego). Powstały aldehyd jest fosfotriozą, monosacharydem.
Jego część służy do syntezy dalszych sacharydów (np. glukoza,
sacharozy), a część jest skierowana na szlak prowadzący do regeneracji
akceptora dwutlenku węgla.
FAZA III
REGENERACJA
Polega na odtworzeniu 1,5-bisfosforybulozy.
Następuję to w serii zachodzących po sobie reakcji, poprzez metabolity
trój-, cztero-, pięcio- i siedmiowęglowe. (enzymy: aldolaza, fosfataza,
izomeraza, transketolaza, epimeraza pentozofosforanowa, kinaza
pentozofosforanowa).
Wiązanie dwutlenku węgla w roślinach typu C
4
i CAM
Obie grupy tych roślin róznią się od roślin C
3
tym że wykształciły dodatkowy
mechanizm wiązania dwutlenku węgla poprzedzający cykl Calvina-Bensona.
Do grupy roślin określanych jako C4 zaliczamy rośliny strefy zwrotnikowej np.
kukurydza, trzcina cukrowa.. Liście tych roślin mają charakterystyczną Budowę
anatomiczną, w której można wyróżnić komórki miękiszu (mezofilu) liścia oraz
specjalną grupę komórek otaczających wiązki przewodzące, zwaną pochwą
okołowiązkową. W cytozolu komórek miękiszu występuje enzym karboksylaza
fosfoenolopirogronianowa , który katalizuje przyłączenie CO
2
do wysokoener-
getycznego związku - fosfoenolopirogronianu. Pierwszym produktem przyłączenia
dwutlenku węgla do fosfoenoopirogronianu jest szczawiooctan. Utworzony
szczawiooctan ulega przekształceniu w jabłczan. który specjalnymi kanałami
plasmodesma jest transportowany do komórek pochwy okołowiązkowej. W ko-
mórkach tych następuje dekarboksylacja jabczanu z udziałem tzw. enzymu
jabłczanowego (dehydrogenaza jabłczanowa dekarboksylująca), a uwolniony CO
2
jest
ponownie wiązany przez obecną w chloroplastach komórek pochwy okołowiązkowej
karboksylazę l,5 bisfoforybulozy i następnie przekształcany zgodnie z reakcjami cyklu
Calvina-Bensona. Tworzący się w procesie dekarboksylacji pirogronian przemieszcza się
z powrotem do komórek mezofilu, gdzie ulega fosforylacji do
Strona 96

fosfoenolopirogronianu . Reakcja jest katalizowana jest przez dikinazę pirogronian-
fosforan, która fosforyluje nie tylko pirogronian, lecz także cząsteczkę fosforanu
nieorganicznego, zużywane są zatem dwa wysokoenergetyczne wiązania ATP.
Do roślin określanych mianem CAM zaliczamy rośliny strefy pustynnej i półpustynnej
Rośliny te ze względu na warunki środowiska muszą prowadzić oszczędną gospodarkę
wodną i aby zapobiec nadmiernej utracie wody, otwierają szparki tylko w nocy kiedy
temperatura znacznie się obniża. Otwarcie szparek umożliwia dopływ dwutlenku
węgla do wnętrza rośliny, ale z powodu braku światła nie przebiegają procesy
świetlnej fazy fotosyntezy, dostarczające ATP i NADPH. Dwutlenek węgla jest więc
wstępnie przyłączany przez znajdującą się w cytozolu komórek karboksylazę do
fosfoenolopirogronianu i powstaje szczawioctan. Fosfoenolpirogronian jest
dostarczany przez glikolizę i pochodzi z rozkład skrobi lub innych cukrów. Szczawio-
octan ulega redukcji do jabłczanu, który jest transportowany do wakuoli i tam gromadzo-
ny w dużych ilościach, powodując jej zakwaszenie. W czasie dnia, kiedy szparki są
zamknięte, jabłczan jest przenoszony na powrót do cytozolu i tam ulega dekarbok-
sylacji przez enzym jabłczanowy, dostarczając dwutlenku węgla. Ponieważ w tym
czasie zachodzą reakcje świetlnej fazy fotosyntezy i stają się dostępne jej produkty -
ATP i NADPH, uruchamia się cykl Calvina-Bensona i zachodzi asymilacja uwolnionego
dwutlenku węgla. W tym czasie następuje też regeneracja zapasów skrobi asymilacyjnej.
Zamknięte w ciągu dnia szparki nie tylko chronią przed transpiracją, ale i nie dopuszcza-
ją do utraty uwolnionego CO
2
do atmosfery.
Rośliny typu CAM podobne są pod pewnymi względami do roślin C4. W obu tych
grupach występuje wstępne wiązanie CO
2
poprzedzające cykl Calvina-Bensona. W
obu przypadkach pierwotnym akceptorem dwutlenku węgla jest fosfoenolopirogronian i
tworzone są przejściowe związki, które ulegając następnie dekarboksylacji
dostarczają odpowiednio dużego stężenia CO
2
, tak aby cykl Calvina-Bensona mógł
przebiegać z odpowiednią wydajnością. Różnicy między tymi dwoma grupami roślin
dotyczą natomiast umiejscowienia zależności czasowych procesów wstępnej karboksylacji i
dekarboksylacji. W roślinach C
4
procesy karboksylacji fosfoenolopirogronianu do
szczawiooctanu (komórka mezofilu) i dekarboksylacji jabłczanu (komórka pochwy
okołowiązkowej) zachodzą równocześnie, ale w różnych typach komórek, są więc
oddzielone przestrzennie. W roślinach CAM oba procesy przebiegają w tych samych
komórkach, są jednak rozdzielone w czasie karboksylacja odbywa się w nocy, zaś
dekarboksylacja - cykl Calvina w ciągu dnia.
W obu przypadkach jest to mechanizm adaptacji roślin do warunków środowiska,
ale prowadzący jednocześnie do wzrostu wydajności fotosyntetycznej. Wiązanie
CO
2
u tych roślin jest procesem o większej złożoności i ma wyższy koszt
energetyczny niż u roślin typu C
3
(wymaga więcej cząst. ATP). Jednak przy silnym
nasłonecznieniu, na skutek uruchomienia cyklicznego transportu elektronów,
zwiększona jest synteza ATP, dlatego dostępność ATP nie jest czynnikiem
ograniczającym fotosynt. wiązanie CO
2
.
Strona 97
Document Outline
- Endogenne inhibitory wzrostu
- - morfaktyny,retardanty, herbicydy.
- Inhibitory wzrostu są to związki org. które w stężeniach fizjologicznych hamują takie procesy jak wydłużanie łodygi oraz jej wycinków, wzrost korzeni, kiełkowanie nasion, otwieranie pąków, i kwitnienie. Hamowanie tych procesów ma charakter odwracalny, ma wiec obniżenie poziomu inhibitora w roślinie wznawia zahamowany poprzednio proces. Spośród związków o charakterze inhibitorów wzrostu najszersze zastosowanie w praktyce rolniczej i ogrodniczej znalazły retardanty i morfaktyny.
- Retardanty: są to syntetyczne inhibitory wzrostu hamujące wzrost elongacyjny łodyg bez powodowania innych deformacji, a działające przeciwnie niż gibereliny. Grupa retardantow obejmuje kilkadziesiąt substancji o rożnej strukturze chemicznej:
- A) chlorek chlorocholiny (chlorek 2-chloroetylotrimetyloaminy ,ccc).
- Jest pochodna choliny, która wchodzi w skład lecytyny ,naturalnego składnika tłuszczowego wszystkich org. żywych.
- B) inne retardanty
- Odmienna budowę chem, lecz zbliżone działanie fizjologiczne posiadają rożne substancje produkowane na skalę przemysłową do potrzeb rolnictwa.
- Rośliny poddane działaniu retardantów maja charakterystyczny pokrój:
- -sa karłowate wskutek silnego skrócenia miedzywiężli,
- -łodygi ich są zgrubiale
- -liście maja zabarwienie ciemnozielone
- Objawy przypominają łączny wpływ działania światła o dużej intensywności oraz niskiej temp. I są przeciwne objawom wywoływanym przez gibereliny.
- Konkurencyjny wpływ giberelin i retaredantow na wzrost roślin wypływa z przeciwnego działania obu typów regulator na podziały komórkowe w merystemie podwierzcholkowym ( gibereliny przyspiesza je, a retardanty hamują powodując w ten sposób skracanie międzywiężli i karlenie roślin). Prawdopodobnie retardanty blokują niektóre ogniwa biosyntezy giberelin, wskutek czego po zastosowaniu retardantow poziom giberelin się obniża. Reatardanty stosuje się w uprawie roślin ozdobnych (azalie, gożdziki iinne) głownie w celu zapobiegania nadmiernemu wydłużaniu łodyg. Reatardanty wzrostu maja również uboczne działanie , niekiedy pożądane z punktu widzenia praktyki, wzmagają odporność roślin na niekorzystne warunki otoczenia ( niska temp. , susza, nidopowedni odczyn podłoża, smog, i inne ) a ponadto zwiększają odporność roślin na choroby wywołane mirkoorganizammi.
- Morfaktyny: są syntetycznymi inhibitorami wzrostu , kotre hamują wzrost elongacyjny łodyg i wywierają głęboki wpływ na organogenze roślin .Pod względem chemicznym morfaktyny są pochodnymi fluorenu.
- Morfaktyny ,wchłonięte przez korzenie albo liście , hamują wzrost i organogeneze młodych organów , nie wpływając na stan organów starych w przeciwieństwie do innych regulatorów wzrostu morfaktyny działają powoli, lecz w sposób długotrwały.
- Morfkatyny wywierają silny wpływ morfologiczny na rośliny hamują one podziały komórkowe w merytsatemach wierzvholkowych , co powoduje skracanie międzywiężli i ogólnie karlenie rośliny. Powierzchnia blaszek liściowych się zmniejsza. Morfaktyny zmieniają dominacje wierzchlowkowa- hamują rozwój paka szczytowego oraz pobudzają rozwój pąków bocznych. Rośliny staja się wiec silnie rozgałęzione , przy czym pędy boczne często ulęgają deformacji np. fascjacji (staśmienieu) . Korzenie pod wpływem morkatyn ulęgają podobnym zmianom morfologicznym ,a ponadto często zaczynają rosnąc w gore ,zamisat jak normalnie w dol (zaburzenia geotropizmu). Morfaktyny działają w pewnych procesach antagonistycznych do gibereln, natomiast w innych antagonistycznie do auksyn lub cytokinin. Nie można jednak uważać morfaktyn ani za antygibereliny ,ani za auksyny,ani tez za antycytokininy >Morfaktyny sa raczej wielofunkcyjnymi substancjami zakłócającymi normalne procesy wzrostu i rozwoju roślin. Hamujące działanie wzrostu roślin wykorzystuje się w przypadkach w których zależy nam na zachowaniu gęstej pokrywy roślinnej terenu łatwo ulęgającego erozji wskutek wiatru lub deszczu., Morkatyny hamują bowiem zbyt bujny wzrost , co pozwala również zaoszczędzać na koszeniu, lecz nie niszczą całkowicie roślin. Morfaktyny mogą być również używane do niszczenia chwastów, szczegfl9onie w połączeniu z niektórymi herbicydami.
- Herbicydy:
- Nie stanowią grupy inhibitorów wzrostu w sensie fizjologicznym, należą do nich związki o rożnej budowie chemicznej. O działaniu , a łączy je ze osobna jedynie podobny sposób stosowania w praktyce .
- Herbicydy są to zawiązki fitotoksyczne (trujące dla roślin) używane do niszczenia nieporządnej roślinności ,a wiec chwastów, roślin rosnących na torowiskach kolejowych, placach budowanych itp.
- Ze względu na sposób stosowania herbicydy można podzielić na:
- a) Totalne - niszczace wszystkie rośliny
- b) Selektywne - niszczące tylko pewne rośliny np. chwasty , lecz nie działające toksycznie na inne gatunki roślin, np. na rośliny uprawne.
- Totalność bądź selektywność zależy od stężenia herbicydów- przy odpowiednio dużych dawkach każdy prawie herbicyd wykazuje selektywność w stosunku do kresloych roślin.
- Herbicydy można zastosować:
- - przedwschodowo – przed wschodami roślin, tak ze wchłaniane są one prze korzenie lub podziemne części pędu
- - powschodowo- wtedy herbicydy działają głownie na liście i pędy.
- W zależności od sposobu działania rozróżniamy herbicydy:
- kontaktowe , czuli działające miejscowo, jedynie na tkankę roślinną, z która się zetknęły,
- -układowe – wchłaniane prze rośliny przemieszczające się w jej systemie przewodzącym w naczyniach lub sitach i działające toksycznie na cały organizm rośliny. Przy opryskiwaniu nadziemnych części rośliny herbicydy systematycznie przedostają się szybko do systemu korzeniowego natomiast przy zastosowaniu doglebowym sa przebrane prze korzenie i dostają się do części nadziemnych.
- Ze względu na budowę chemiczną. Herbicydy dzieli się na :
- - nieorganiczne
- - organiczne
- Fototoksycznosc herbicydów:
- Herbicydy działają niszcząco na rośliny w bardzo niskich stężeniach, co wynika z faktu, ze herbicyd pozostaje w roślinie prze długi okres w postaci niezmienionej i przez cały czas oddziałuje na nią szkodliwie. Dlatego z fizjologicznego punktu widzenia herbicydy można określić jako substancje które dezorganizują równowagę fizjologiczna rośliny na długo przed jej śmiercią.
- Selektywność herbicydów:
- Nie jest jedynie cecha herbicydu , lecz wynika z wzajemnych zależności roślin, herbicydu oraz sposobu jej stosowania. Selektywność może opierać się na czynnikach fizycznych i biochemicznych:
- -selektywność fizyczna (topograficzna) –s tosuje się rożne zabieg i celem zwiększenia kontaktu herbicydów z chwastami w porównaniu z roślinami uprawnymi (stosowanie herbicydu przed wysiewem roślin uprawnych lub przed wschodami) lub zmniejszenie kontaktu herbicydu z roślinami uprawnymi (stosując spryskiwanie w pasach miedzy roślinami np. w uprawach okopowych).
- Selektywność biochemiczna wykorzystuje różnice w metabolizmie pomiędzy roślinami wrażliwymi a odpornymi na działanie herbicydów. Selektywność ta przejawia się w niejednakowym przekształcaniu się herbicydów w roślinach rożnych gatunków. Istnieją dwie możliwości tych przekształceń: u roślin nie wrażliwych herbicyd rozkłada się do nietoksycznych związków w roślinach wrażliwych herbicyd przekształca się na związki toksyczne.
- Endogenne regulatory wzrostu roślin
- – krotka charakterystyka
- Regulatory wzrostu są to związki org. które w bardzo małych ilościach wykształcających oddziaływanie troficzne(odżywcze) zwiększają, hamują lub w inny sposób wpływają na procesy wzrostu i rozwoju roślin. Regulatory wzrostu można uważać za rodzaj chemicznych sygnałów powstających w niewielkich ilościach w określonych częściach roślin. Z tych miejsc regulatory wzrostu są przekazywane przez system prowadzący do innych części, w których kierują procesami wzrostu i rozwoju roślin. Z tej przyczyny przez analogie z hormonami występującymi w organizmach zwierzęcych, regulatora wzrostu roślin są także nazywane hormonami roślinnymi albo fitohormonami.
- Wyróżniamy zasadniczo 5 grup regulatorów wzrostu: auksyny, gibereliny, cytokininy, inhibitory wzrostu, etylen
- Niezależnie od tego podziału, wśród regulatorów wzrostu można wyróżnić regulatory endogenne(naturalne) wytwarzane przez rośliny oraz egzogenne- sztucznie wprowadzane do roślin w postaci syntetycznych preparatów.
- Auksyny -to związki, które charakteryzuje zdolność wywoływania wzrostu elongacyjnego komórek łodyg w sposób podobny do kw. Idolilo – 3 octowego, który jest najpospolitsza i prawdopodobnie jedyna naturalna auksyna.
- Działanie fizjologiczne podobne do IAA maja również auksyny syntetyczne, stosowane w rożnych kw. 2,4 dichlorofenoksyoctowy(2,4-D)
- Auksyny występują we wszystkich roślinach wyższych, a także w niektórych grzybów. Tworzą się przede wszystkim w pakach wierzchołkowych oraz w najmłodszych liściach i tam jest zwykle ich najwyzsze stężenie. Z tkanek tych auksyny są przewodzone do innych części rośliny przy czym transport ten ma charakter polarny, tzn. zależy od kierunku. W kierunku od wierzchołka do podstawy rośliny(bazypetalnie) transport auksyn jest bardzo szybki, prawdopodobnie jest to transport aktywny wymaga bowiem aktywności cukrów i tlenu, a wiec energii uwalnianej w procesie oddychania; w kierunku przeciwnym od podstawy łodygi do wierzchołka (akropetalnie) zachodzi wolno zgodnie z prawem dyfuzji.
- Partenokarpia: auksyny , produkowane prze rozwijające się nasiona pobudzają rozrost zalążka albo dna kwiatowego (partenokarpia wytwarzanie owoców bez zapłodnienia)
- Gibereliny:
- - charakterystyczna cecha giberelin jest zwiększanie wzrostu łodyg, stymulacja podziału kom. Oraz wpływ ba wiele innych procesów fizjologicznych
- - giberelina są to związki org. które maja taki sam szkielet gibam jak kwas giberelowy i wykazują w testach karłowatych uwfantow (przywracają karłowatym odmianom kukurydzy lub grochu normalny wzrost) oraz indukcji amylazy w kiełkujących ziarenkach jęczmienia .
- Gibereliny można zaliczyć do terpenoidow tzn. związków których jednostka budowy jest izopren. Wszystkie gibereliny są kwasami i maja identyczna konfiguracja oparta na czteropierscioeniwym rdzeniu giberenowym. Poszczegolne gibereliny oznacza się symbolem GA z odpowiednia liczba kolejna (GA1 Ga2 itd.). Najlepiej zbadana giberelina jest kw. Giberelowy (GA3) występujący w wielu roślinach oraz produkowany fabrycznie. Gibereliny występują powszechnie w roślinach wyższych , w paprociach , mchach, glonach ,grzybach , bakteriach. Każda roślina wyższa zawiera zwykle kilka giberelin , które różnią się struktura i aktywnością fizjologiczna. Nie ma tu zatem analogii z auksyna , która występuje w roślinach najczęściej w postaci tylko jednego związku –kw. indolilo- 3- octowego i jego pochodnych .Najwyższe stężenie giberelin wykazują szybko rosnące i rozwijające się organy a wiec kiełkujące nasiona , młode liście, wierzchołki łodyg i korzenia, natomiast wyrośnięte w pełni liście oraz łodygi i korzenie zawierające bardzo niewielki ilości giberelin.
- Cytokininy
- Budowa kompleksów łańcucha oddechowego u roślin
- Porównanie zasadniczych cech szlaków asymilacji CO2 - C3, C4, CAM.
- *Asymilacja CO2 przez rośliny C3.
- Produkty świetlnej fazy fotosyntezy - ATP i NADPH są zużywane do wbudowania dwutlenku węgla w związki organiczne w procesie określanym jako ciemna faza fotosyntezy. Rośliny u których pierwszym produktem asymilacji dwutlenku węgla jest kwas 3-fosfoglicerynowy oznacza się mianem roślin C3. Rośliny C3 wiążą dwutlenek węgla w procesie fotosyntezy za pomocą cyklu Calvina-Bensona. Akceptorem dwutlenku węgla u tych roślin jest 1,5-bifosorybuloza zaś enzymem katalizującym tą reakcję-karboksylaza 1,5bifosforybuzozy(inna nazwa rubisco). Karboksylaza l ,5-bisfosforybulozy jest kluczowym enzymem cyklu Calvina-Bensona, determinującym szybkość przyswajania dwutlenku węgla. Przyłącza ona dwutlenek węgla 1,5 bisfosforybulozy dając nietrwały związek 6-węglowy, który natychmiast rozpada się na dwie cząsteczki kwasu 3-fosfoglicerynowego. Związany dwutlenek węgla stanowi grupę karboksylową jednej z tych cząsteczek. Kwas 3-fosfoglicerynowy jest następnie fosforylowany na koszt ATP do do kwasu 1,3 -bisfosfoglicerynowego, który udziałem NADPH ulega redukcji do poziomu cukrów tj. do aldehydu 3-fosfoglicerynowego.
Wyszukiwarka
Podobne podstrony:
opracowania fizjologia roslin
fizjo.egzam, Leśnictwo UP POZNAŃ 2013, Fizjologia roślin drzewiastych
FIZJOLOGIA ROŚLIN - opracowane pytania na egzamin, Student
opracowanie(z grubsza) fizjologii roślin, Biologia, fizjologia roślin
FIZJOLOGIA ROŚLIN - opracowane pytania na egzamin, biotechnologia 2 sem rok2, pobrane z góry DS 7, z
przegląd roślin, 1 Studia ZOOTECHNIKA, Botanika z elementami fizjologii roślin, Opracowania
Fizjologia roślin wykłady, Biologia, fizjologia roślin
fizjo - wyk+éady, Leśnictwo UP POZNAŃ 2013, Fizjologia roślin drzewiastych
Zes. 7, AR Poznań - Leśnictwo, gleboznawstwo LP, Fizjologia roślin, tylko ściągi
instr X 4, Fizjologia Roślin, Biologia podstawowa
wykład 6 fizj roślin, biologia, fizjologia roślin
wyklad 4 fizj roślin, biologia, fizjologia roślin
Pytania z Fizjologii roślin z poniedziałku 3 września
Spr gosp kom, Biologia UWr, II rok, Fizjologia Roślin
fizjologia roslin - testy1+2, UG, FIZJO ROŚLIN, FIZJO, fizjo
instr V 1, Fizjologia Roślin, Biologia podstawowa
fizjo-kiełkowanie-folie111111, Leśnictwo UP POZNAŃ 2013, Fizjologia roślin drzewiastych
więcej podobnych podstron
