Politechnika Łódzka
Wydział Inżynierii Procesowej
i Ochrony Środowiska
Ul. Wólczańska 213, 90-924 Łódź
ĆWICZENIA 4,5
Fermentacja metanowa roślin energetycznych oraz
odpadów organicznych z gospodarstw domowych
Laboratorium z przedmiotu: Biopaliwa
Opracowała: dr inż. Anna Klepacz-Smółka
Wpływ stopnia nawożenia upraw na produkcję biogazu
1. Cel i zakres ćwiczenia
Celem ćwiczenia jest badanie procesu fermentacji metanowej roślin energetycznych.
2. Wstęp teoretyczny
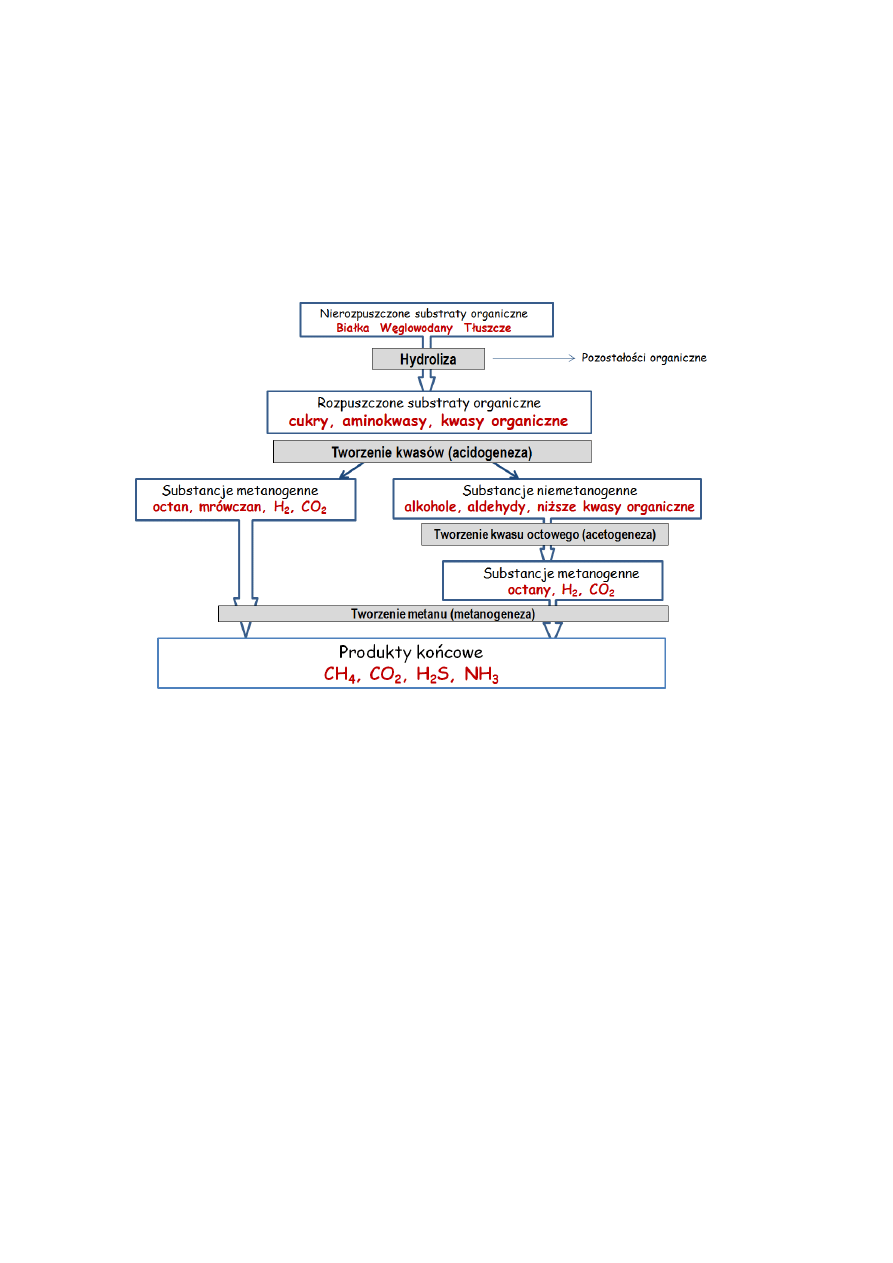
Fermentacja metanowa to zespół beztlenowych procesów biochemicznych, w których
wielocząsteczkowe substancje organiczne ( głównie węglowodany, białka i tłuszcze oraz ich
związki pochodne) są rozkładane do alkoholi lub niższych kwasów organicznych,
a w końcowym etapie do metanu, dwutlenku węgla i wody (biogazu). W przebiegu
fermentacji metanowej można wyróżnić następujące fazy rys1.
Rys. 1 Przebieg fermentacji metanowej.
Biogaz - gaz powstały w czasie fermentacji metanowej, składający się głównie z metanu
(CH4) do 70%, około 30% dwutlenku węgla (CO2) oraz ewentualnie z azotu (N2),
siarkowodoru (H2S) i wodoru (H2).Szacuje się, że obecnie na świecie ilość produkowanego
biogazu wynosi 140Mm
3
/dobę.
Biogaz jako czysta, odnawialna energia może stać się bardzo dobrym substytutem dla
konwencjonalnych źródeł energii (węgla kamiennego, ropy naftowej), które zanieczyszczają
środowisko naturalne, a w dodatku wyczerpują się w bardzo szybkim tempie.
Obecnie coraz większe zastosowanie w produkcji biogazu, w szczególności w Niemczech,
znajdują uprawy celowe roślin energetycznych. Najszersze zastosowanie znajduje kukurydza
pod postacią kiszonki. Ponadto mogą być stosowane: trawa, koniczyna, ziemniaki, kukurydza,
bób, żyto, burak pastewny, buraki cukrowe, cebula, gorczyca, groch, kalarepa, kapusta,
kalafior, pszenica, owies, jęczmień, sorgo, rzepak, dynia, słonecznik. Rośliny te mogą być
stosowane pod postacią całych roślin, osobno owoców, bulw lub liści, jak również nasion
tych roślin lub też roślin po przetworzeniu w formie kiszonki lub słomy. Od strony
technologicznej dobre właściwości i wysoką wydajność zapewnia stosowanie kiszonek
kukurydzy, słonecznika, trawy oraz Sucrosorgo. W ostatnim czasie zaobserwowano zmiany
biogazowni z typowo rolniczych na utylizacyjne, w których jednym z substratów są odpady
organiczne z gospodarstw domowych, zakładów spożywczych, są to na przykład wytłoki
jabłkowe, wywar gorzelniany itp.
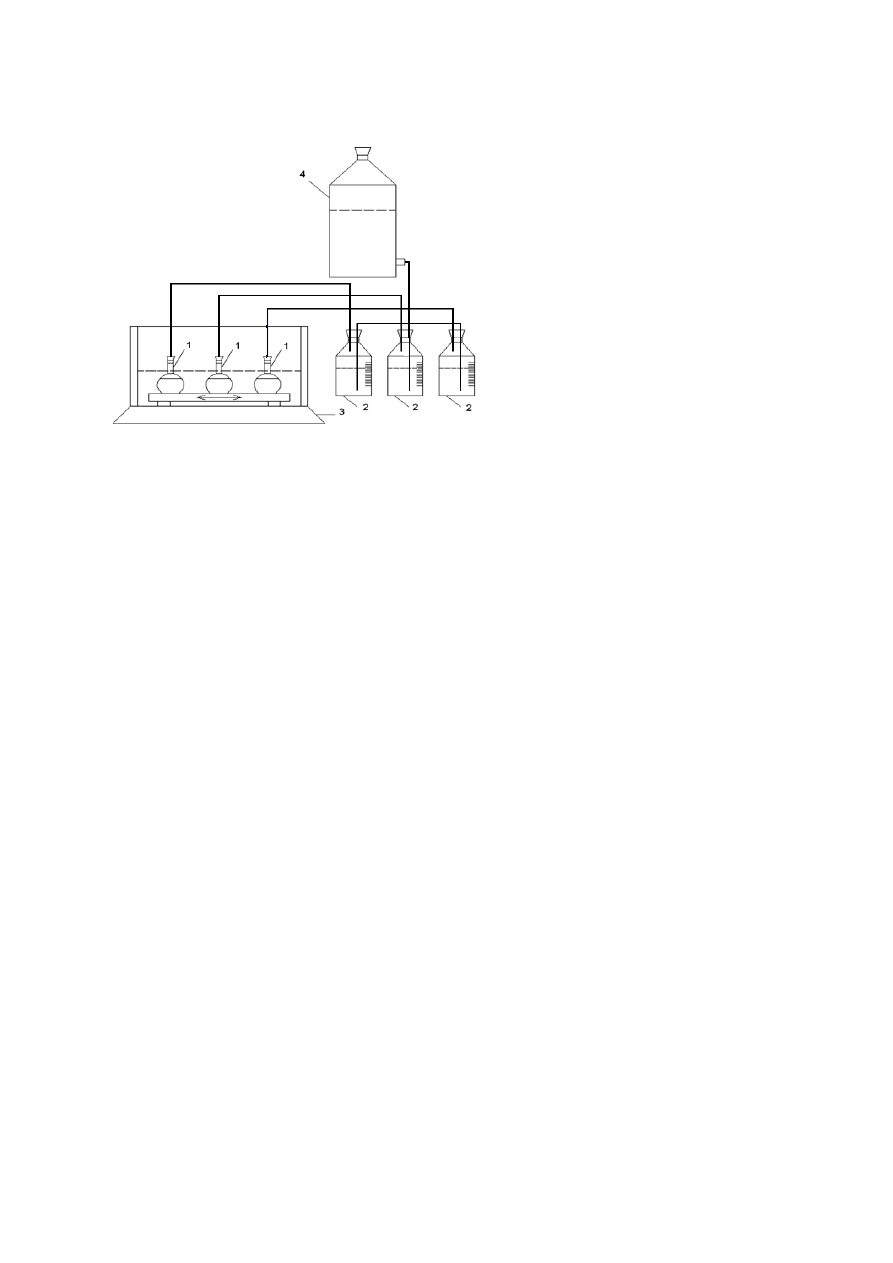
3. Stanowisko badawcze
Rys. 2 Schemat stanowiska badawczego w kolbach wstrząsanych 1 - kolby z mieszaniną
fermentacyjną, 2 – wykalibrowane butle do pomiaru biogazu, 3 - wytrząsarka z łaźnią wodną,
4 – butla utrzymująca ciśnienie wody.
3. Materiały badawcze
Inokulum z GOŚ – zawiesina przefermentowanych osadów pochodzących bezpośrednio
z instalacji do mezofilnej fermentacji metanowej, działającej w GOŚ w Łodzi
Materiał poddawany fermentacji: kiszonki z roślin energetycznych, organiczna frakcja
odpadów z gospodarstw domowych (gotowane ziemniaki, ryż, jabłka, makaron itp.)
4. Metody analityczne
Dla każdej kolby należy wykonać następujące pomiary i analizy.
objętość wydzielonego biogazu
Objętość wyprodukowanego biogazu metodą przelewową w wykalibrowanych butlach
odczytywana wg. zaleceń prowadzącego.
skład biogazu
Udziały procentowe objętościowe metanu i dwutlenku węgla w biogazie przy pomocy
chromatografu gazowego GC SRI 8610C (kolumna Molecular sieve o długości 1 m, natężenie
przepływu 10 ml/min).
W próbkach mieszaniny fermentacyjnej należy określić:
pH
Odczyn mieszaniny fermentacyjnej poddawano niezwłocznie po pobraniu próbki za pomocą
pH-metru firmy WTW pH 540 GLP.
suchą masę, suchą masę organiczną
Suchą masę metoda wagową, jako suchą pozostałość po suszeniu w 105°C do stałej wagi,
w parowniczkach wysuszonych uprzednio do stałej masy. Wyniki oznaczenia suchej masy w
g/dm
3
mieszaniny (wg PN – 75 C – 04616/01).
Suchą masę organiczną, jako różnicę wagi między suchą pozostałością a pozostałością po
prażeniu w 605°C. Wyniki oznaczenia podawano w g/dm
3
mieszaniny (wg PN – 75 C –
04616/01).
W cieczy nadosadowej (uzyskanej po odwirowaniu próbki) należy określić:
chemiczne zapotrzebowanie na tlen ChZT

ChZT z zastosowaniem fiolek LCK 314 i LCK 514 firmy Hach-Lange, zgodnie z procedurą
producenta. Próby po wirowaniu w wirówce laboratoryjnej typu MPW-250 (13000 obr/min
czas 10 min
5. Przebieg ćwiczenia
5.1 Przygotowanie mieszaniny reakcyjnej.
Odmierzyć zadaną ilość inokulum do kolby
Przygotować zadaną ilość materiału badawczego (zmielenie)
Wyregulować pH mieszaniny reakcyjnej
Pobrać próbę do analiz wejściowych
Odczytać startowy poziom cieczy w butlach kalibrowanych
5.2 Odczytywanie wyników (po zadanym okresie)
Odczytać poziom cieczy w butlach kalibrowanych oraz obliczyć objętość
wyprodukowanego biogazu (pobrać próbę biogazu)
Otworzyć kolbę i pobrać próbę do analiz
5.3 Opracowanie wyników
Wykres kumulacyjnej produkcji biogazu.
Przedstawić początkowe i końcowe wartości ChZT, sm i smo oraz całkowitą redukcję
ChZT, sm i smo (tabela).
Wydajność biogazu i metanu w stosunku do usuniętego ChZT, sm, smo (wyniki
przedstawić na wykresie kolumnowym).
Całość podsumować wnioskami.
5.3 Sprawozdanie powinno zawierać:
stronę tytułową z nazwą przedmiotu, tytułem ćwiczenia, rodzajem substratu oraz nazwiskami
wykonawców ćwiczenia
krótki wstęp teoretyczny wraz z opisem surowca
opis przebiegu ćwiczenia (z uwzględnieniem ewentualnych uwag i przygotowania mieszaniny
reakcyjnej)
opracowanie wyników (wraz z przykładowym obliczeniem sm, smo)
zbiorcza tabela wyników
wnioski (można np. znaleźć dane do porównania produkcji biogazu, lub porównać z innymi
grupami)
załącznik w postaci tabeli produkcji biogazu
Literatura
Grzybek A., Możliwości i technologia produkcji biogazu rolniczego, Czysta energia 10, 2004
Buraczewski G, Fermentacja metanowa, PWN Warszawa 1998
Wyszukiwarka
Podobne podstrony:
Laboratorium wiczenie6 id 26186 Nieznany
Laboratoria 1 (pusta) id 261269 Nieznany
Laboratorium 6 protokol id 2616 Nieznany
laboratorium 7 pomoc id 261617 Nieznany
Laboratory 09 id 261962 Nieznany
laboratorium 07 id 261474 Nieznany
Laboratorium wiczenie7 id 26186 Nieznany
Laboratorium wiczenie5 id 26186 Nieznany
Laboratorium wiczenie6 id 26186 Nieznany
5 2 3a CCNA1 Laboratorium pl id Nieznany (2)
LABORATORIUM 1 id 261484 Nieznany
instrukcja laboratoryjna id 216 Nieznany
Laboratorium z TM spr1 id 26189 Nieznany
Laboratorium 8 id 261621 Nieznany
Laboratorium 5 id 261589 Nieznany
laboratorium 01 py id 261468 Nieznany
Badania laboratoryjne id 76309 Nieznany
Laboratoria 3 (wypelniona) id 2 Nieznany
Laboratorium 2i3 zswier id 2615 Nieznany
więcej podobnych podstron