
Wyk
łady z chemii
dla studentów Wydzia
łu Inżynierii Lądowej i Geodezji
Wojskowej Akademii Technicznej
Prowadz
ący:
Dr hab. in
ż. Andrzej Sadkowski, profesor W.A.T.
Wydzia
ł Nowych Technologii i Chemii.
Wyk
ład 8.
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro

2
Korozja metali: Powoduje straty rz
ędu 3% - 6% GNP (w USA 2002 r.)
Mechanizm zawsze elektrochemiczny. Depolaryzacja wodorowa lub tlenowa.
Na niejednorodnej powierzchni metalu (
żelaza, stali itp….) są miejsca
anodowe, na których zachodzi roztwarzanie metalu (utlenianie) do jego
jonów i miejsca katodowe, na których zachodzi reakcja redukcji dope
łniająca
bilans
ładunków do zera. Reakcję tę nazywamy zwana reakcją depolaryzacji.
Depolaryzatorem mo
że być tlen, w roztworze napowietrzonym, lub wodór, przy
braku tlenu w roztworze.
Fe
s
Fe
2
2
e
Utlenianie elektrodowe
żelaza do jonów Fe
2+
(reakcja anodowa)
O
2
2
H
2
O
4
e
4 OH
Redukcja tlenu, depolaryzacja tlenowa.
Alkalizacja!
2
H
2
e
H
2
g
Redukcja jonów wodorowych, depolaryzacja
wodorowa. Roztwór alkalizuje si
ę!
2
H
2
O
2
e
H
2
g
2 OH
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro

3
Na powierzchni metalu tworz
ą się ogniwa lokalne, prąd krąży w nich „w kółko”
bior
ąc udział w roztwarzaniu (utlenianiu) metalu i redukcji depolaryzatora, jak w
normalnym, du
żym ogniwie.
Dalej zachodzi wytracanie osadu produktów korozji i dalsze utlenianie, np.
jonów Fe
2+
do Fe
3+
. Fe
2
O
3
to podstawowy sk
ładnik rdzy.
Fe
2
2 OH
Fe
OH
2
s
Fe
2
O
2
g
4
2
n
H
2
O
2 Fe
2
O
3
.
n H
2
O
s
8
H
rdza
osad produktów korozji
W roztworach oboj
ętnych (pH 7) potencjały depolaryzatorów tlenowego
(O
2
/OH-) i wodorowego (H
2
/2 H
+
) wynosz
ą odpowiednio:
E
depO
= 0,82 V
NHE
i E
depH
= –0.41 V
NHE
(NHE – w skali normalnej elektrody
wodorowej)
Zakwaszenie!
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro
4
Zatem w obecno
ści tlenu będą korodowały wszystkie metale, których
potencja
ły normalne są poniżej 0,82 V
NHE
, w tym tak
że Cu i Ag.
W
środowisku bez tlenu korodować będą tylko metale o potencjałach
normalnych <-0,41 V
NHE
. Nie b
ędzie więc korodować Cu (miedź) ani Ag
(srebro).
Od pH zale
żą też równowagi wielu reakcji elektrodowych zachodzących z
udzia
łem protonów.
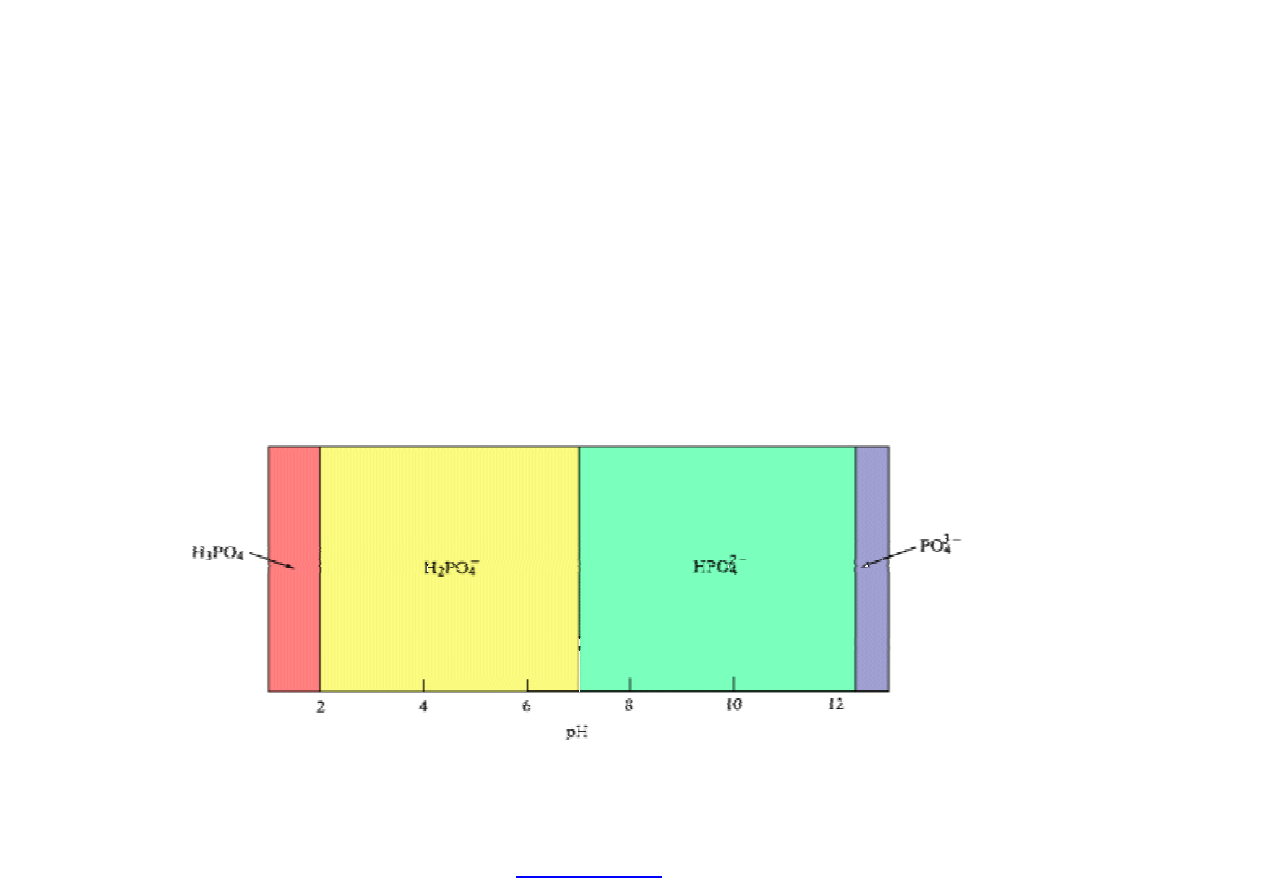
Substancja mo
że mieć różne formy trwałe przy różnych pH, np. dysocjacja H
3
PO
4
.
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro
5
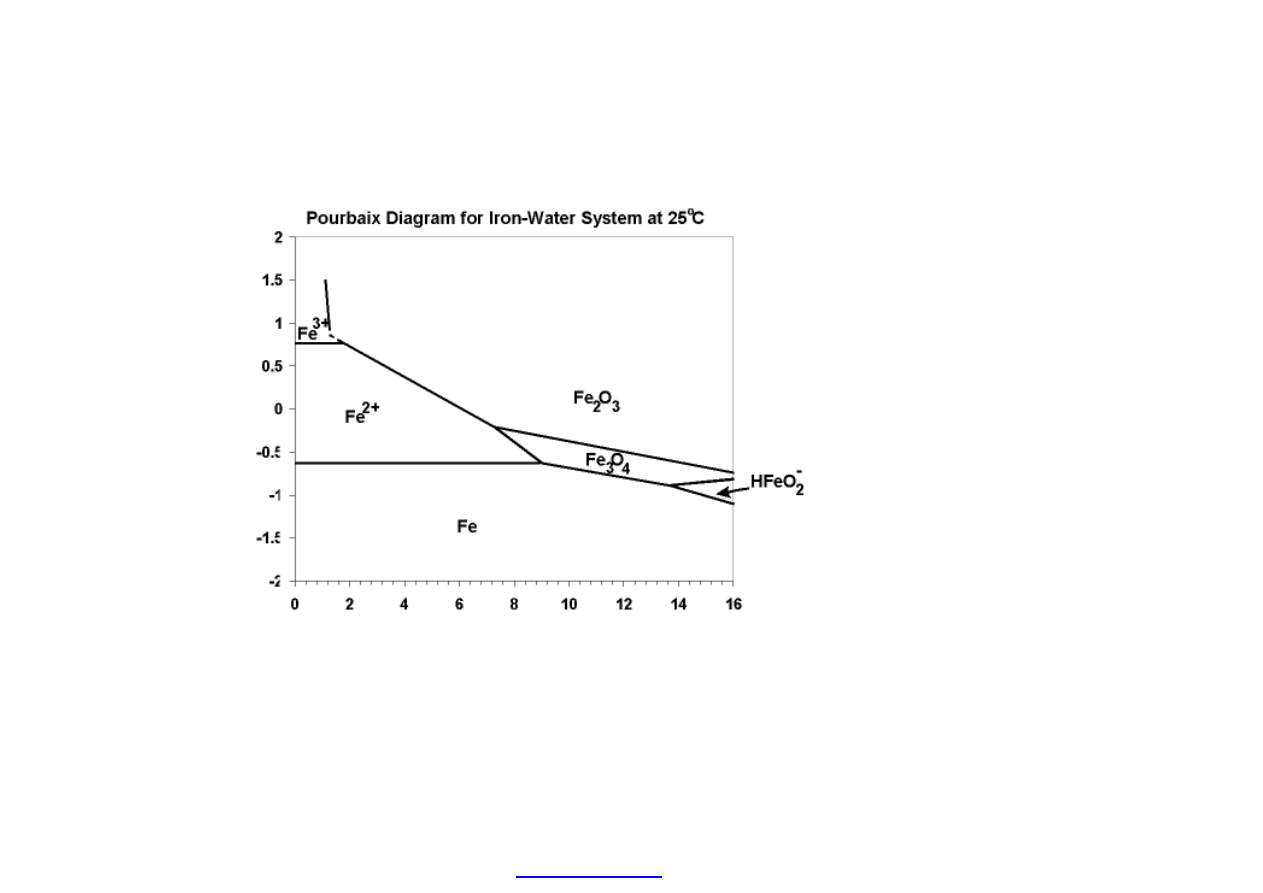
Podobnie korozja i jej produkty (rozpuszczalne i nierozpuszczalne) silnie
zale
żą od pH środowiska. Wpływ potencjału elektrodowego i pH na korozję
obrazuj
ą tzw. wykresy Pourbaix (czytaj: Purbe).
Pasywacja chroni przed korozj
ą metale bardzo aktywne chemicznie, np.
Al, Ti, Mo. Ale tak
że Fe, Ni, Cr.
Dodatek Cr w stali bardzo u
łatwia pasywację. Stale kwasoodporne
zawieraj
ą zawsze chrom i często nikiel i molibden.
E
Fe/Fe2+
= -0,41 V
NHE
jest
to granica depolaryzacji
wodorowej w roztworach
oboj
ętnych.
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro
6
Form O
2
H
2
O stable
Form H
2
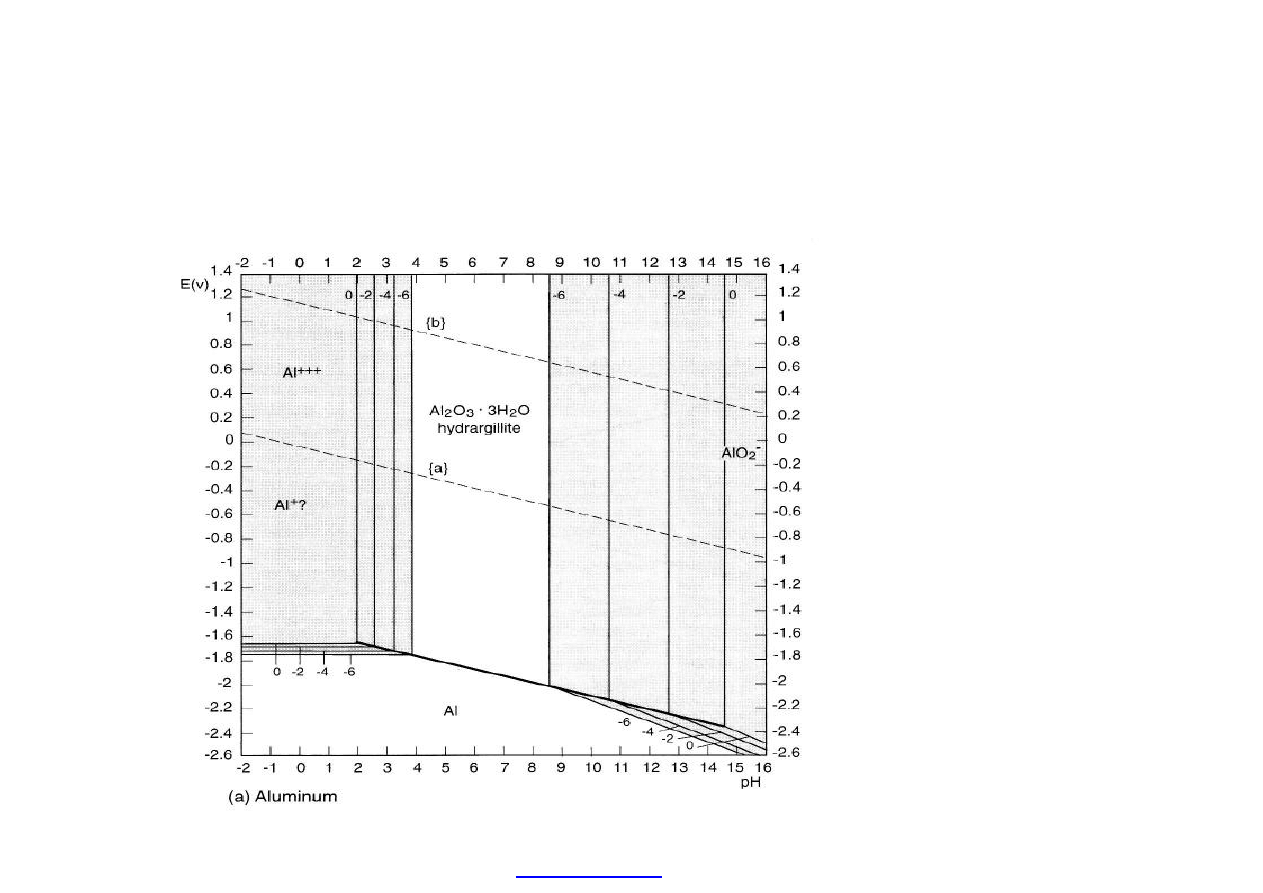
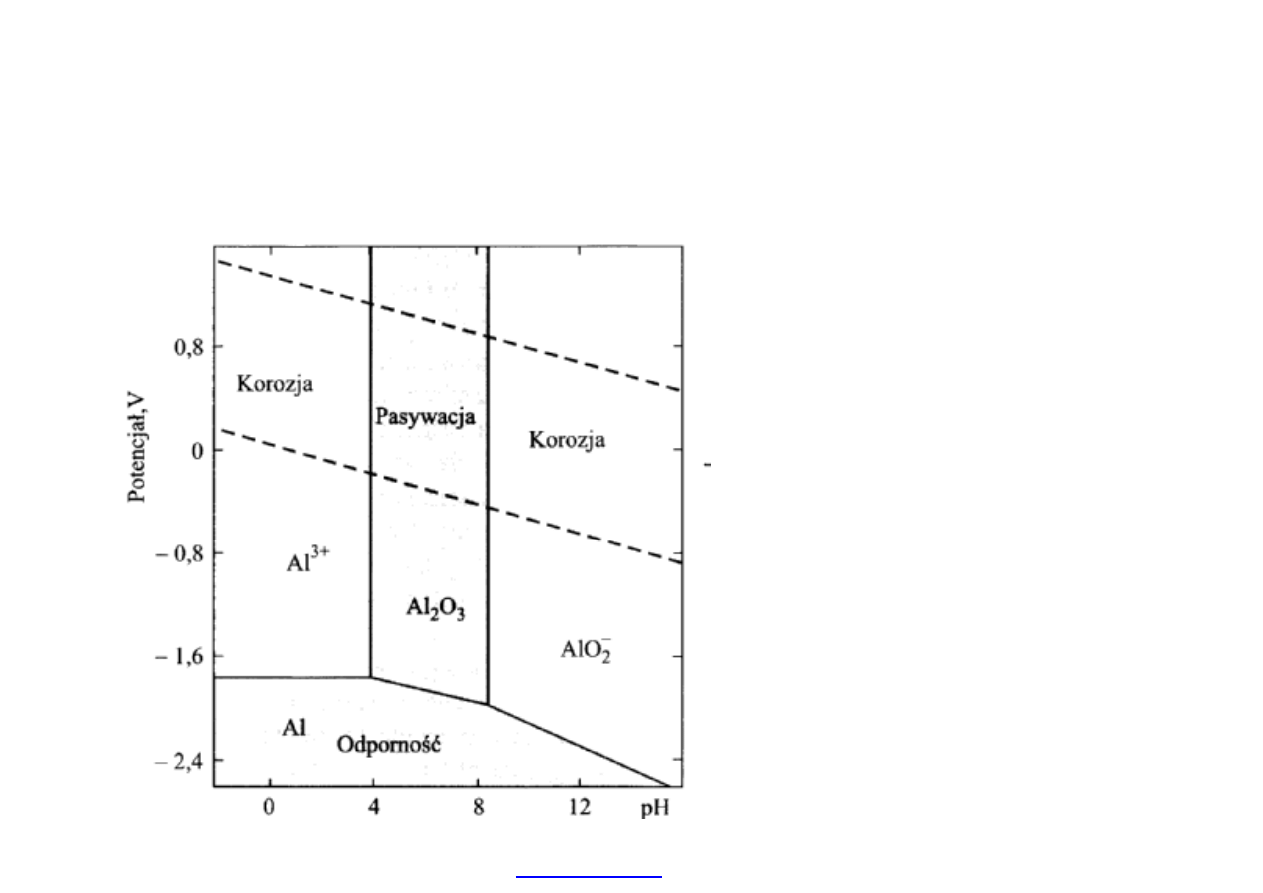
Wykres Pourbaix dla aluminium (Al.) pokazuje obszary trwa
łości i podatności
na korozj
ę.
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro

7
Depolaryzacja wodorowa i ochrona katodowa (patrz ni
żej!) dla żelaza jest
niebezpieczna, bowiem wprowadza wodór atomowy do metalu powoduj
ąc tzw.
krucho
ść wodorową. Wodór gromadzony w sieci metalu rozrywa go, co jest
bardzo cz
ęsta przyczyną awarii np. rurociągów gazowych (sławny na Alasce
kilka lat temu), instalacji gor
ącej wody, szczególnie ciśnieniowych a także
kad
łubów statków i budowli morskich.
Fe + 2 H
+
= Fe
2+
+ 2 H
ab
Pasywacja chroni przed korozja metale bardzo aktywne chemicznie, np.
Al, Ti, Zr, Mo. Ale tak
że Fe, Ni, Cr.
Korozja ogólna i korozja lokalna. K. lokalnej sprzyjaj
ą chlorki, np. sól
rozsypana na jezdni w zimie. Mechanizm adsorpcyjny i kompleksowanie.
Rozpuszczanie tlenków.
Korozja lokalna (w
żerowa) to zdradliwy i szczególnie szkodliwy rodzaj
korozji, cz
ęsto przez długi czas niewidocznej. Wywołują ją chlorki, np. sól
sypana w zimie na jezdni.
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro
8
W istocie, wiekszosc metali sw
ą trwałość w atmosferze ziemskiej
zawdzi
ęcza pasywacji przez warstwy powierzchniowe. Prawdziwie metalem
szlachetnym jest tylko Au (Pt utlenia si
ę już w obecności powietrza).
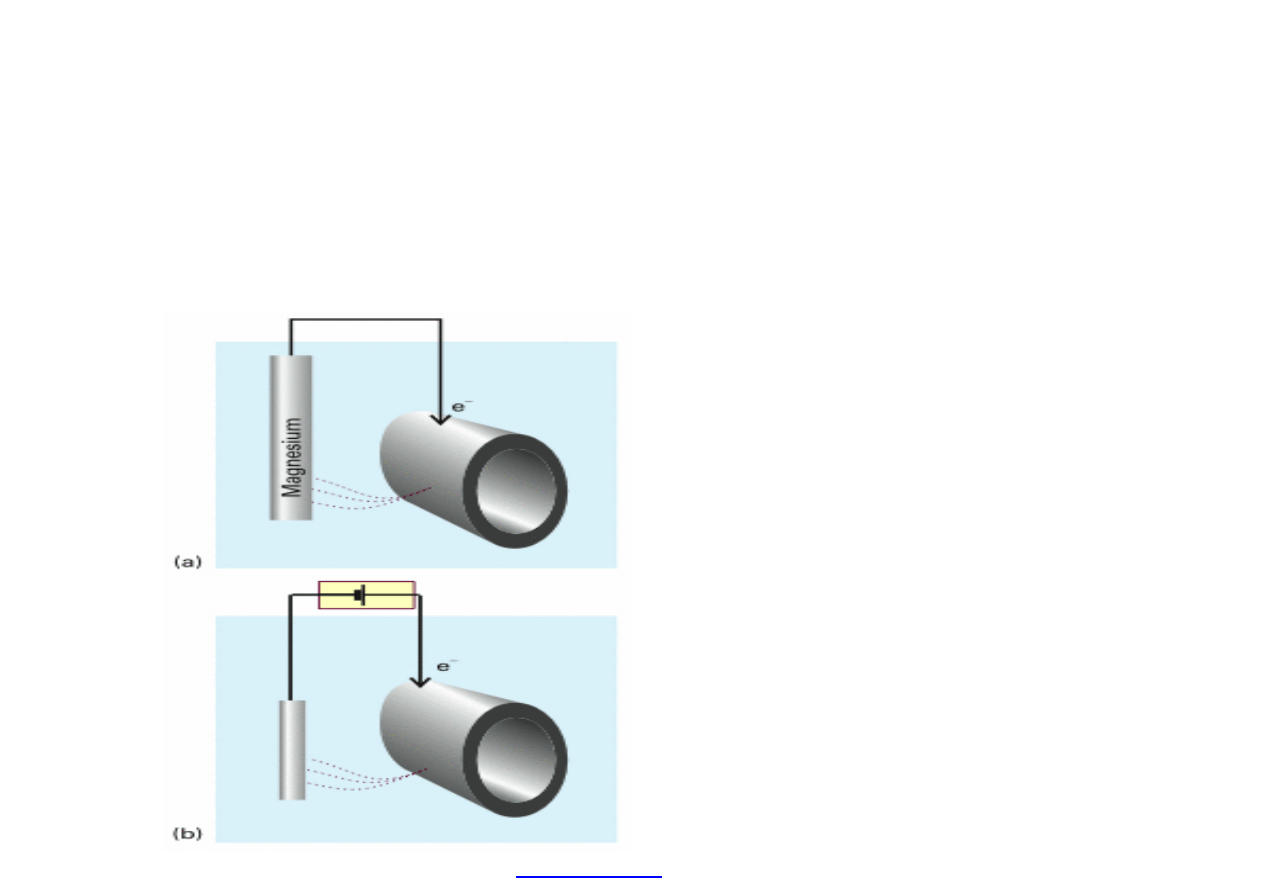
Ochrona przed korozj
ą: galwaniczna – katodowa.
Skutecznym sposobem ochrony jest
cynkowanie (Zn anod
ą, Fe – katodą)
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro
9
Wykres Pourbaix dla Al
Pokazuj
ący obszary
odporno
ści, korozji i
pasywno
ści.
Z ochron
ą anodową trzeba uważać, by nie wejść w obszar transpasywny.
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro
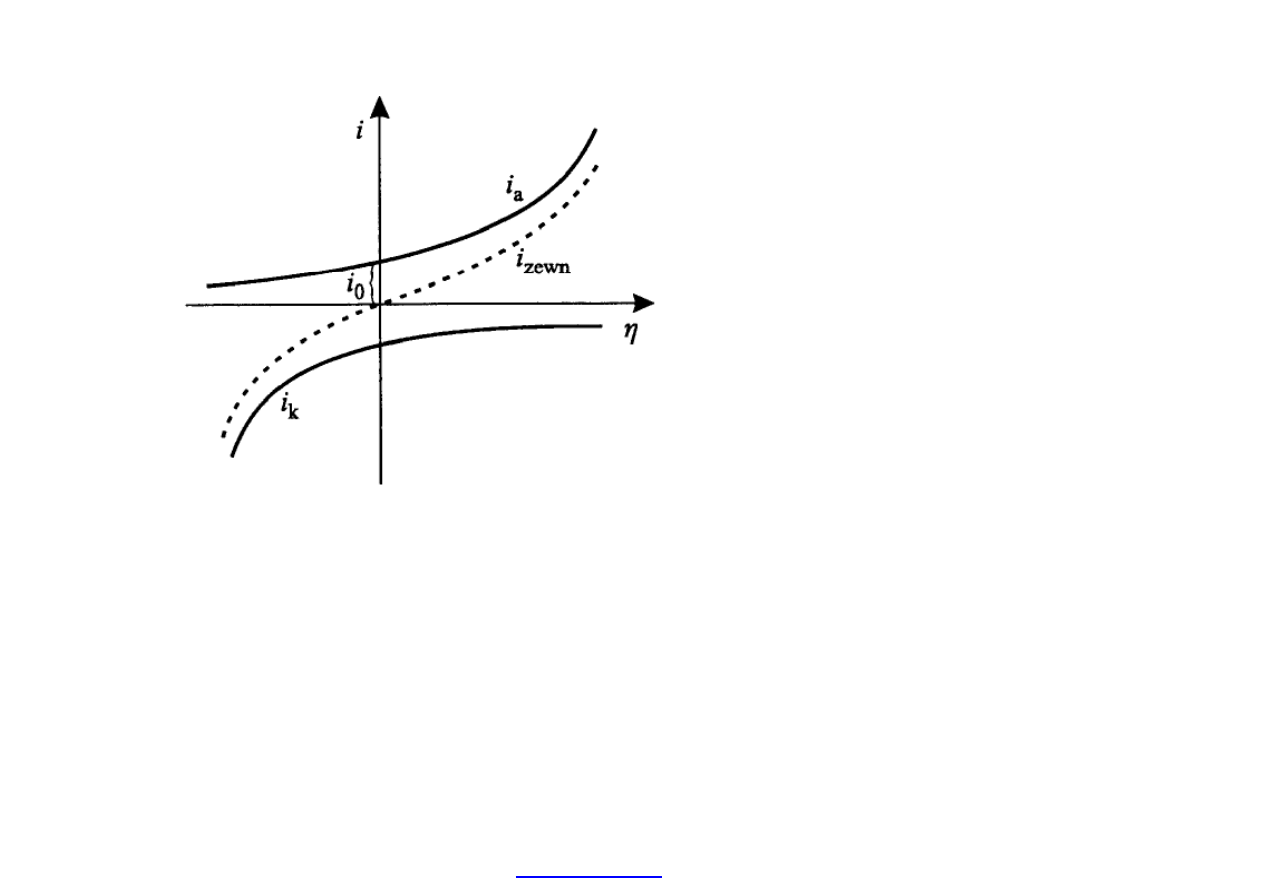
10
Schemat pokazuj
ący prąd anodowy (roztwarzanie), katodowy (depolaryzacja) i
sumaryczny (rejestrowany do
świadczalnie).
η = E – E(0) – nadpotencjał.
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro
11
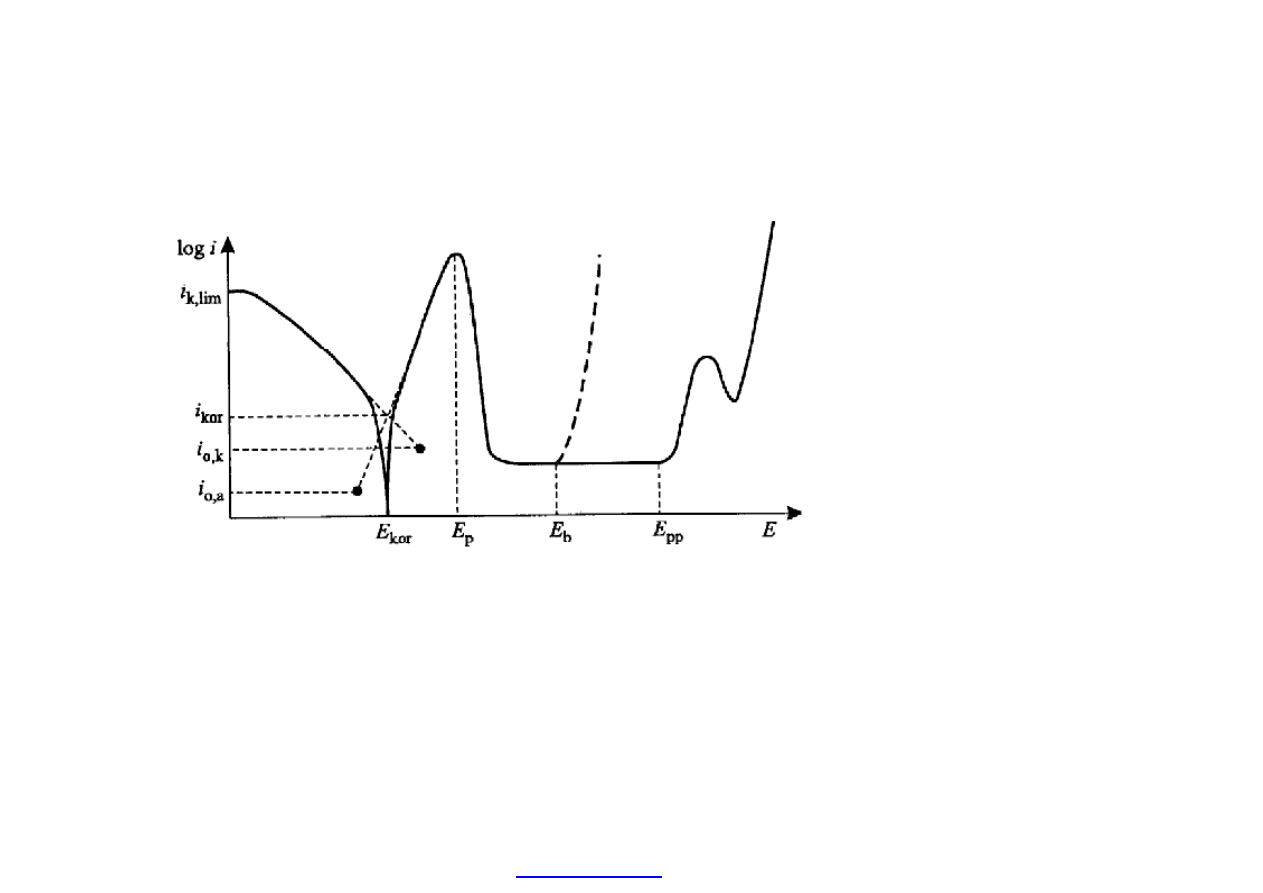
Dla scharakteryzowania uk
ładu korozyjnego (metal + roztwór) wykonujemy tzw.
test krzywej polaryzacji elektrodowej. Liniowa zmiana potencja
łu (potencjostat)
i rejestracja zale
żności gęstość prądu (i) od potencjału (E). Prąd często w skali
log(i).
E
kor
– potencja
ł korozyjny (spoczynkowy, bezprądowy).
i
kor
– pr
ąd korozyjny,
E
p
– potencja
ł (krytyczny) pasywacji,
E
b
– potencja
ł przebicia (początek wżerów),
E
pp
– potencja
ł korozji transpasywnej.
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro

12
Amfoteryczno
ść - > korozja transpasywna: Zn, Cr, Mn, Mo tworzą
sie rozpuszczalne aniony:
Zn - > ZnO
2
2-
Cr -> Cr
2
O
7
2-
Mn -> MnO
4
-
Mo -> MoO
4
2-
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro

13
Inhibitory, pow
łoki lakiernicze.
Inhibitory to np. azotyny dodawane do zamkni
ętych obiegów
gor
ącej wody.
Obecnie stosowane techniki pow
łokowe, w szczególności lakiernicze, są
najskuteczniejsz
ą formą ochrony przed korozja. Karoserie nowoczesnych
samochodów maja 10 lat gwarancji na uszkodzenie korozyjne
(bezwypadkowe!)
Niekiedy szybko
ść korozji zależy też od mieszania, np. przy
granicznych pr
ądach depolaryzacji tlenowej: im intensywniejsze
mieszanie, tym szybsza korozja.
W statkach – korozja na linii wody!
PDF stworzony przez wersj
ę demonstracyjną pdfFactory Pro
Wyszukiwarka
Podobne podstrony:
no8 kopocinscy
no8 ledwina
AarsleffInfo No8 01 id 50011 Nieznany (2)
no8 kopocinscy
no8 malon ziolkowska
KONSPEKT LEKCJI Z PILKI NO8
1931 hudsontriangle vol xx no8 may
concierto no8 en Gminor violinosolo vivaldi
No8
więcej podobnych podstron