
1
Alkohole
Typ wody
H
OH
R
OH

2
H-OH + Na
H-ONa
H-OH + H
+
H-OH
2
+
R-OH + Na
R-ONa
R-OH + H
+
R-OH
2
+
Alkohole
Typ wody
3
Alkohole
R
O
H
R
O
H
R
O
H
R
O
H
R
O
H
R
O
H
R
O
H
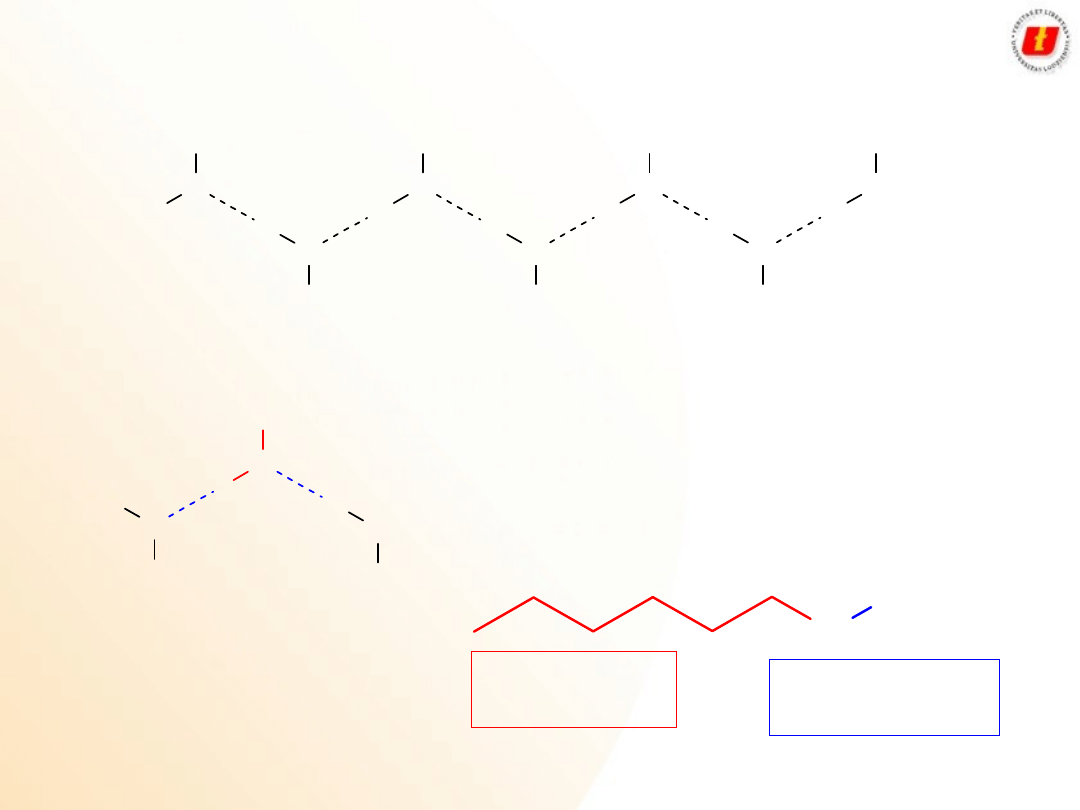
Właściwości fizyczne
Tworzenie wiązań wodorowych pomiędzy cząsteczkami alkoholu
powoduje, że mają one wysoką temperaturę wrzenia
H
O
H
R
O
H
H
O
H
Tworzenie wiązań wodorowych pomiędzy
wodą a alkoholem powoduje, że alkohole
zawierające do 4 atomów węgla doskonale
rozpuszczają się w wodzie
O
H
Część
hydrofobowa
Część
hydrofilowa
4
Alkoh
ol
e
Nazewnictwo
R
OH
R
H
alkan
alkan
ol
CH
3
CH
2
CH
2
CH
3
CH
3
CH
2
CH
2
CH
2
OH
CH
3
CH
2
CH CH
3
OH
butan
Butan-1-
ol
Butan-2-
ol
5
CH
2
C CH CH
3
CH
3
OH
Cl
Cl
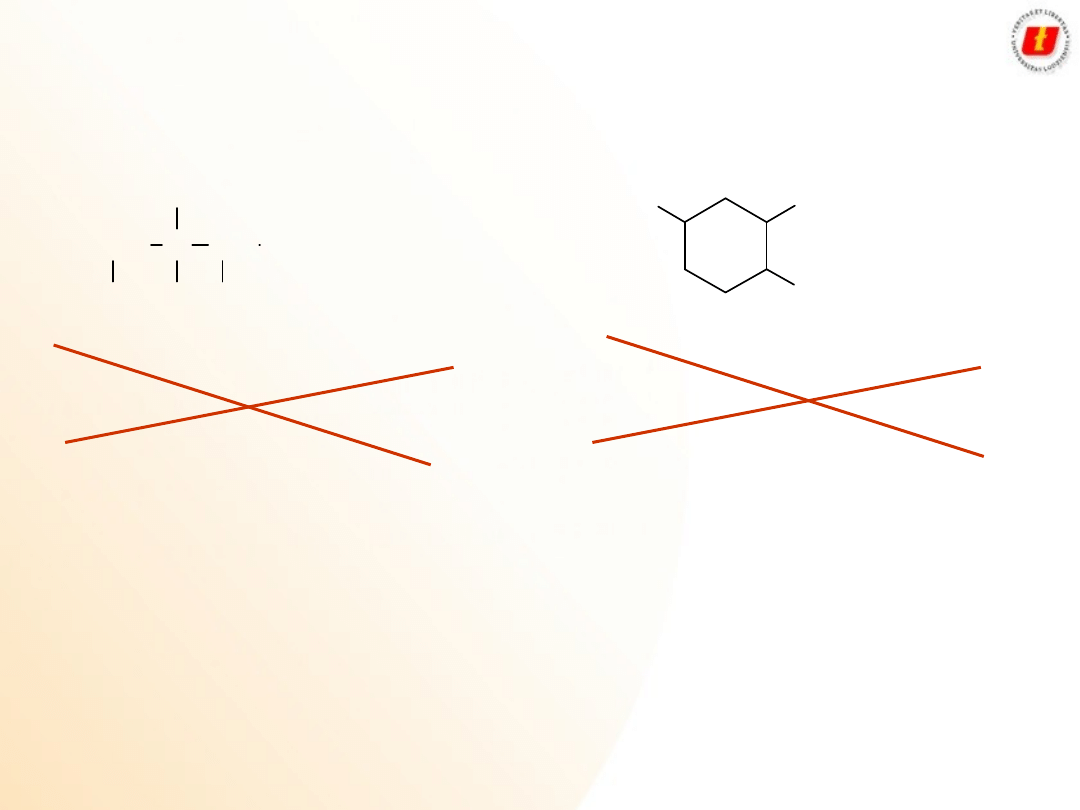
1,2-dichloro-2-metylobutan-3-ol
3,4-dichloro-3-metylobutan-2-ol
O
H
Br
CH
3
2-bromo-1-metylocykloheksan-4-ol
3-bromo-4-metylocykloheksanol
Alkoh
ol
e
Nazewnictwo
6
Alkoh
ol
e
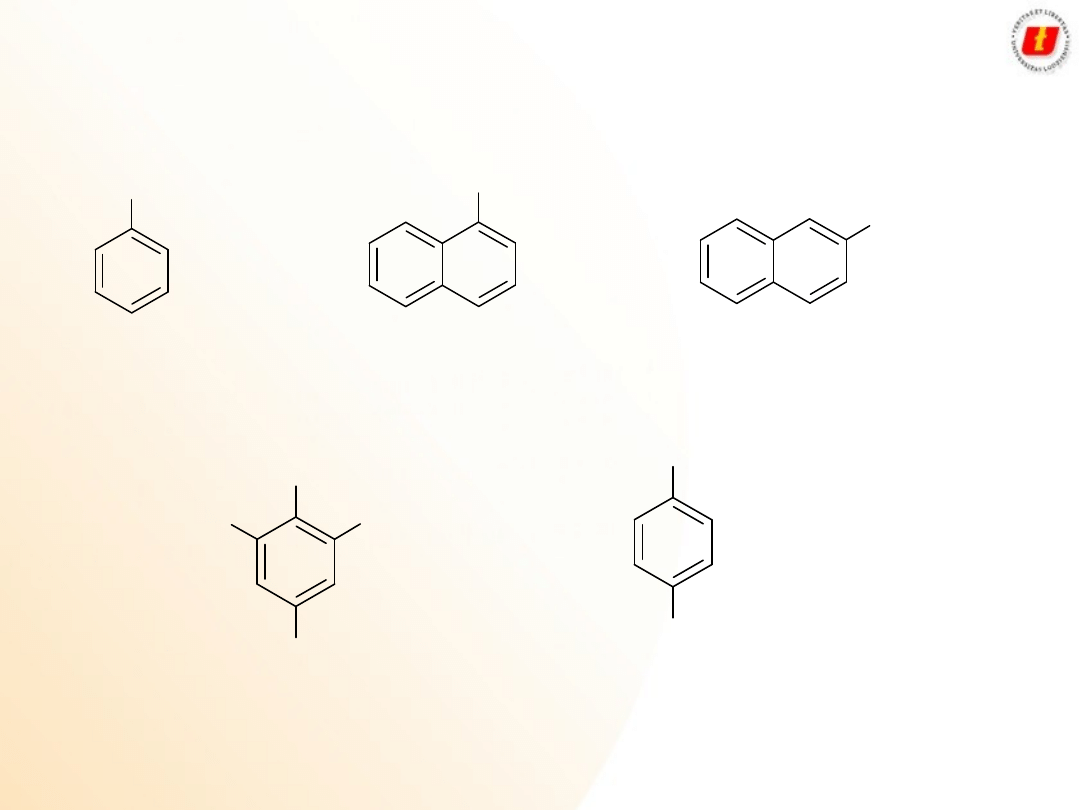
Nazewnictwo
OH
OH
OH
benzenol
fenol
naftalen-1-ol
-naftol
nafalen-2-ol
-nafol
OH
NO
2
NO
2
O
2
N
OH
OH
kwas pikrynowy
hydrochinon

7
Niektóre grupy w nomenklaturze podstawnikowej nigdy nie są
traktowane jako grupy funkcyjne, nazywamy je grupami podrzędnymi.
W nazwie związku ich obecność wskazywana jest wyłącznie w formie
przedrostka:
Niektóre grupy charakterystyczne (podrzędne) wskazywane w
nomenklaturze podstawnikowej wyłączne przedrostkami
Grupa
Przedrostek
-Br
bromo-
-N
3
azydo-
-Cl
chloro-
-NO
nitrozo-
-F
fluoro-
-NO
2
nitro-
-I
jodo-
-O-R
alkoksy- (alkiloksy-)
-S-R
alkilosulfanylo-
Alkoh
ol
e
Nazewnictwo

8
Alkoh
ol
e
Nazewnictwo
Chociaż znanych jest wiele związków wielofunkcynych, to w nazwie
nigdy nie mogą pojawić się dwie grupy funkcyjne w formie przyrostka.
Wsród grup głównych ustalono pewną kolejność pierwszeństwa
(ważność). Tylko grupa o największym pierwszeństwie może być
pokazana w nazwie w formie przyrostka. Pozostałe grupy w
nazwie związku występują w formie przedrostka.
Grupy
główne
wg
pierwszeństwa
kwasy karboksylowe -COOH
bezwodniki kwasowe
estry
halogenki kwasowe
amidy
nitryle
aldehydy i ketony
alkohole i fenole
-ol (hydroksy-)
tiole
aminy
iminy
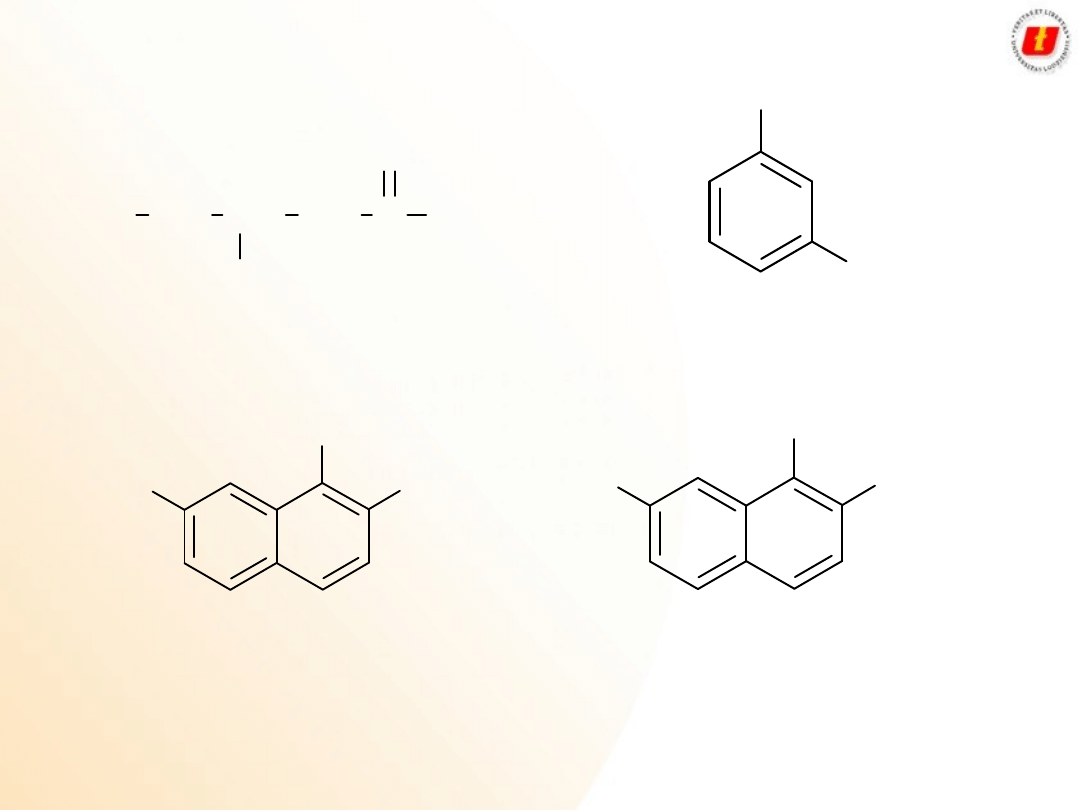
9
Nazewnictwo
Alkoh
ol
e
CH
3
CH
2
CH CH
2
C
O
CH
3
OH
OH
COOH
OH
Br
HO
3
S
OH
Br
C
H
3
4-hydroksyhekan-2-on
Kwas 3-hydroksybenzoesowy
2-bromo-7-metylonaftalen-1-ol
2-bromo-7-metylo-1-naftol
Kwas
7-bromo-8-hydroksynaftaleno-2-
sulfonowy
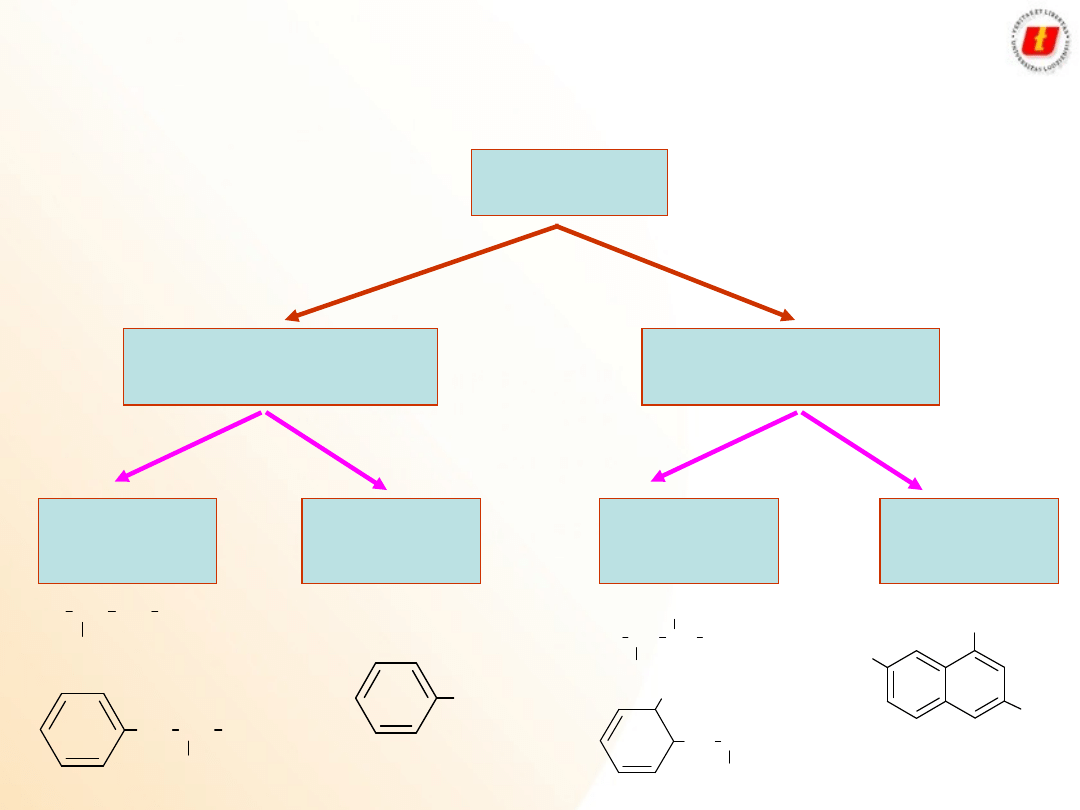
10
Alkohole
podział
Alkohole
monowodorotlenowe
wielowodorotlenowe
alifatyczne
(nasycone)
alifatyczne
(nasycone)
aromatyczne
(fenole)
aromatyczne
(fenole)
CH
3
CH
CH
2
CH
3
OH
CH
2
CH
CH
3
OH
OH
CH
3
CH CH
CH
3
OH
OH
CH
2
CH
2
OH
OH
.
OH
OH
O
H
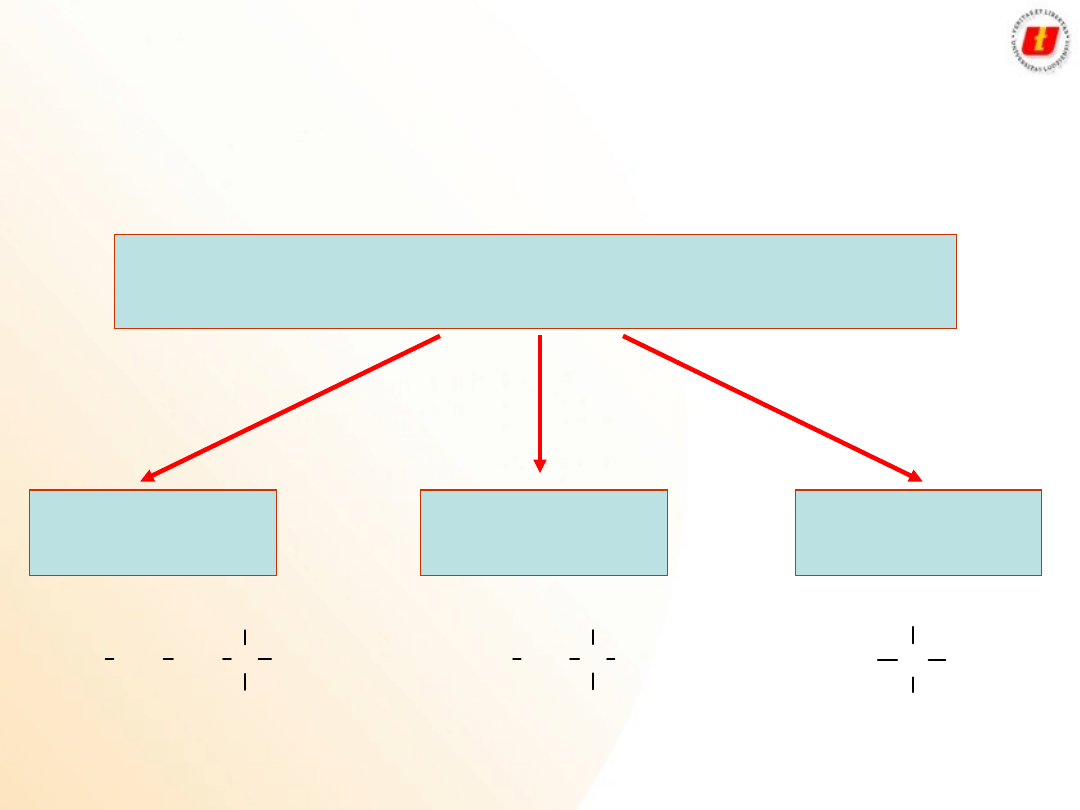
11
Alkohole
podział
Alkohole alifatyczne
Pierwszorzędowe
1
o
Drugorzędowe
2
o
Trzeciorzędowe
3
o
CH
3
CH
2
CH
2
C
OH
H
H
CH
3
CH
2
C
CH
3
OH
H
CH
3
C
CH
3
OH
CH
3

12
Alkohol
alkilowy
Alkohol
bytylowy
Nazewnictwo
Alkoh
ol
e
CH
3
CH
2
CH
2
CH
2
OH
CH
3
CH
2
CH CH
3
OH
CH
3
C CH
3
OH
CH
3
CH
3
CH CH
2
CH
2
OH
CH
3
Alkohol tert-
bytylowy
Alkohol sec-
bytylowy
Alkohol izopentylowy
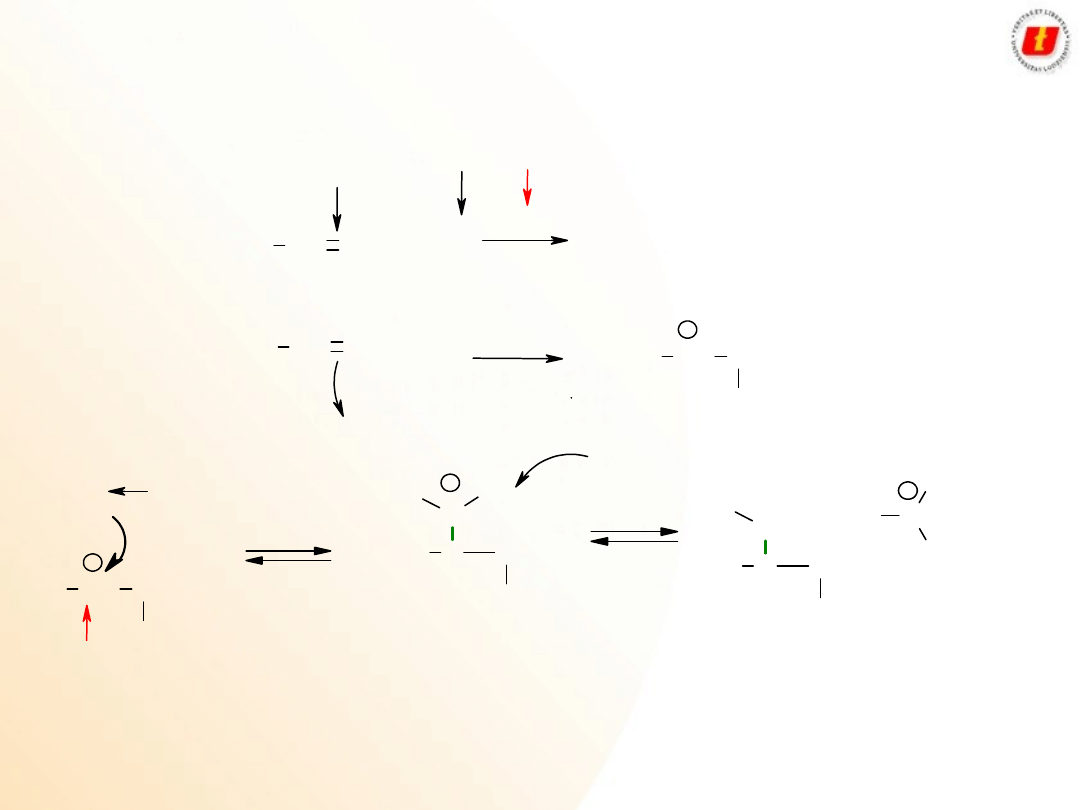
13
Alkohole
Metody
otrzymywania
CH
3
CH CH
2
CH
3
CH CH
2
CH
3
CH CH
2
H
+
CH
3
CH CH
2
H
+
CH
3
C
H
CH
2
H
O
H
H +
+ H
2
O
..
..
c.n.
c.n.
H
+
c.E
H
+
H
2
O
H
2
O
H
2
O
..
..
c.n.
c.E
..
CH
3
C
H
CH
2
H
O
H
+
H O
H
H
H
2
O
..
..
..
..
:
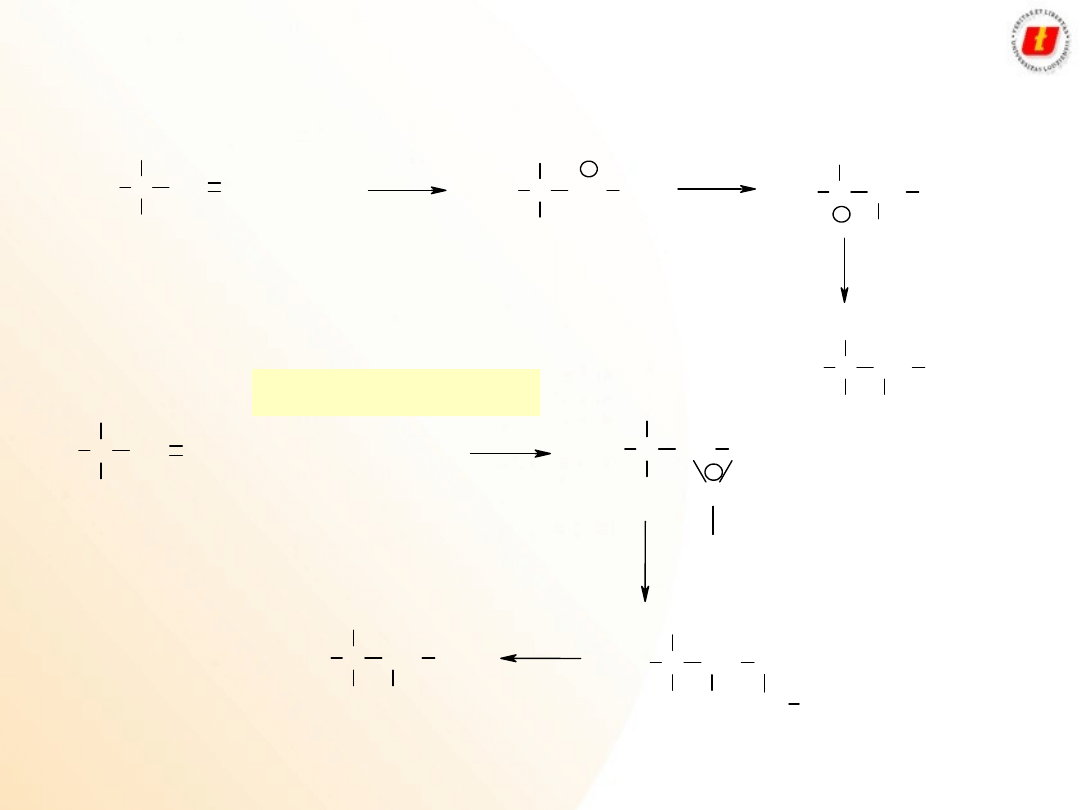
14
CH CH
2
C
CH
3
CH
3
CH
3
CH CH
3
C
CH
3
CH
3
CH
3
+
CH CH
3
C
CH
3
CH
3
CH
3
+
CH CH
3
C
CH
3
CH
3
CH
3
OH
+ H
2
O
H
+
H
2
O
CH CH
2
C
CH
3
CH
3
CH
3
Hg
OOCH
3
+
CH CH
2
C
CH
3
CH
3
CH
3
CH CH
2
C
CH
3
CH
3
C
H
3
Hg OOCH
3
OH
CH CH
3
C
CH
3
CH
3
C
H
3
OH
+ (CH
3
COO)
2
Hg
H
2
O
H
2
O
NaBH
4
Alkohole
Metody
otrzymywania
Dla chętnych – nie obowiązuje w
szkole średniej
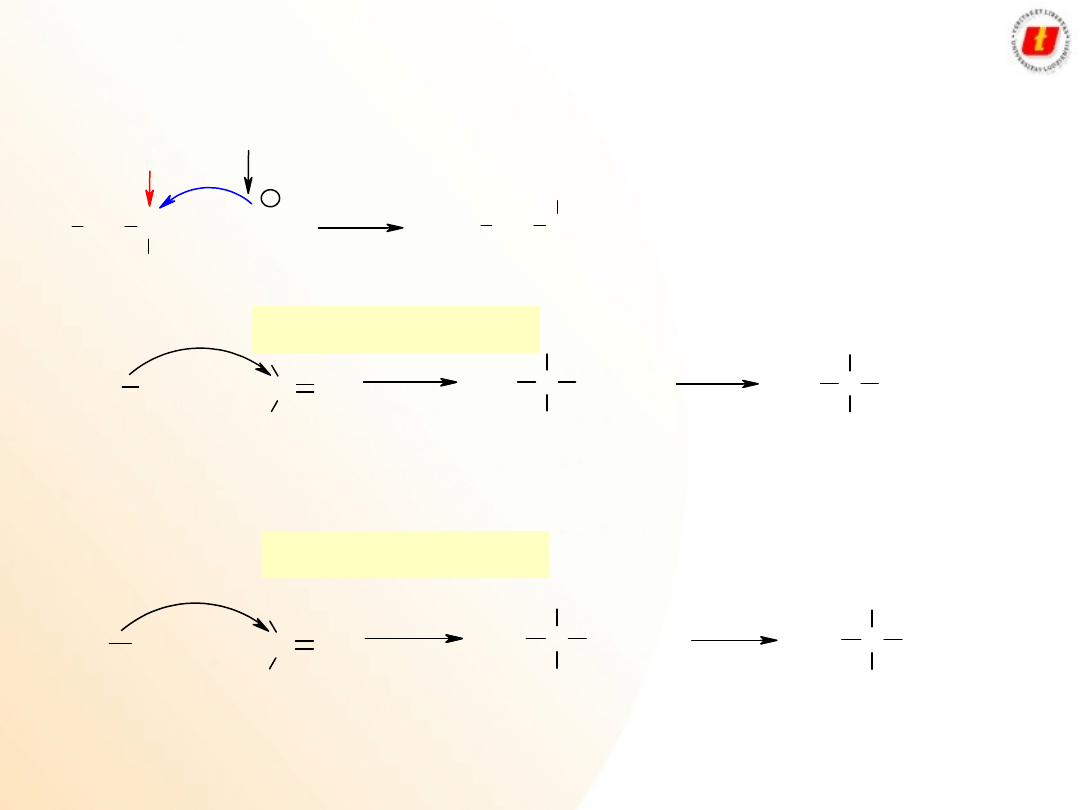
15
CH
3
CH
2
CH
2
Br
-
CH
3
CH
2
CH
2
OH
+ HO
..
..
c.n.
c.E
:
H
2
O
+ Br
-
Alkohole
Metody
otrzymywania
Hydroliza
halogenków
alkilowych
C
H
3
MgCl
C O
H
H
C
H
3
C
H
O-MgCl
H
C
H
3
C
H
OH
H
+
HCl
-MgCl
2
C
2
H
5
MgBr
C O
H
C
H
3
C
2
H
5
C
H
O-MgBr
CH
3
C
2
H
5
C
H
OH
CH
3
+
HCl
-MgBrCl
Otrzymywanie alkoholi 1
o
w reakcji z formaldehydem
Otrzymywanie alkoholi 2
o
w reakcji z dowolnym aldehydem
Dla chętnych – nie obowiązuje w
szkole średniej
Dla chętnych – nie obowiązuje w
szkole średniej
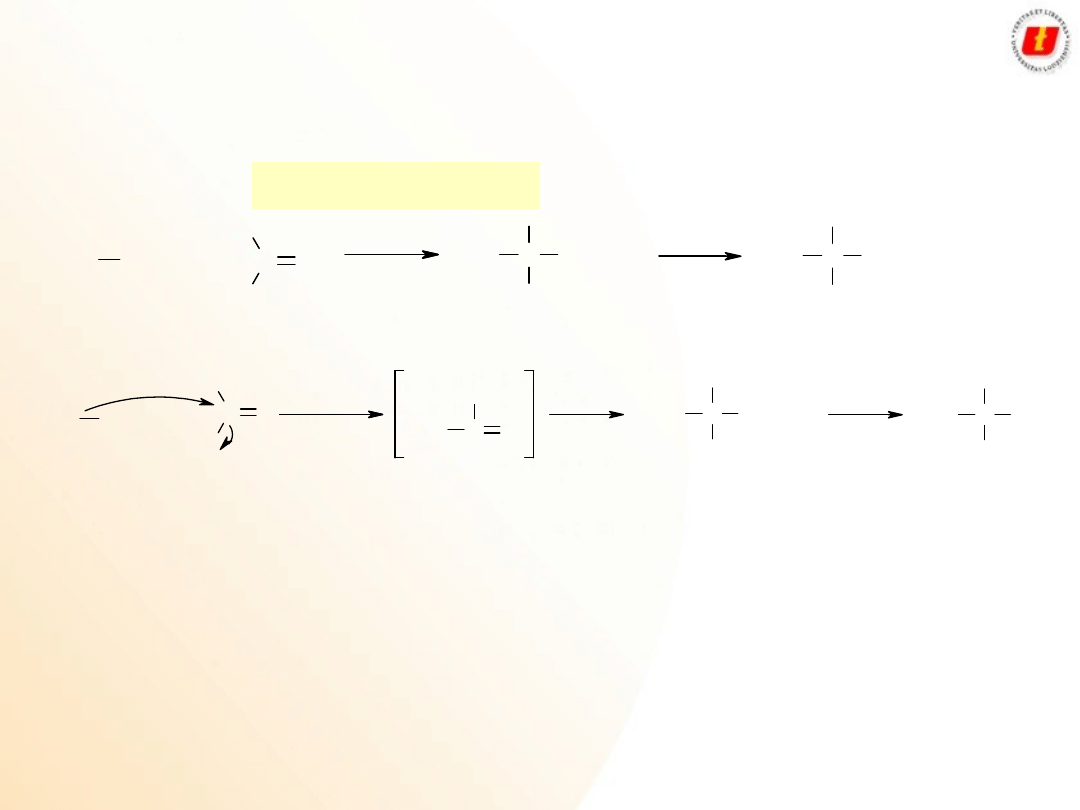
16
C
2
H
5
MgCl
C O
C
H
3
C
H
3
C
2
H
5
C
CH
3
O-MgCl
CH
3
C
2
H
5
C
CH
3
OH
CH
3
+
HCl
-MgCl
2
C
2
H
5
MgCl
C O
C
H
3
MeO
C
2
H
5
C
CH
3
O-MgCl
C
2
H
5
C
2
H
5
C
CH
3
OH
C
2
H
5
C
2
H
5
C
CH
3
O
+
HCl
-MgCl
2
2
-Mg(OCH
3
)Br
Synteza alkoholi 3
o
z ketonów lub estrów kwasów karboksylowych
Alkohole
Metody
otrzymywania
Dla chętnych – nie obowiązuje w
szkole średniej
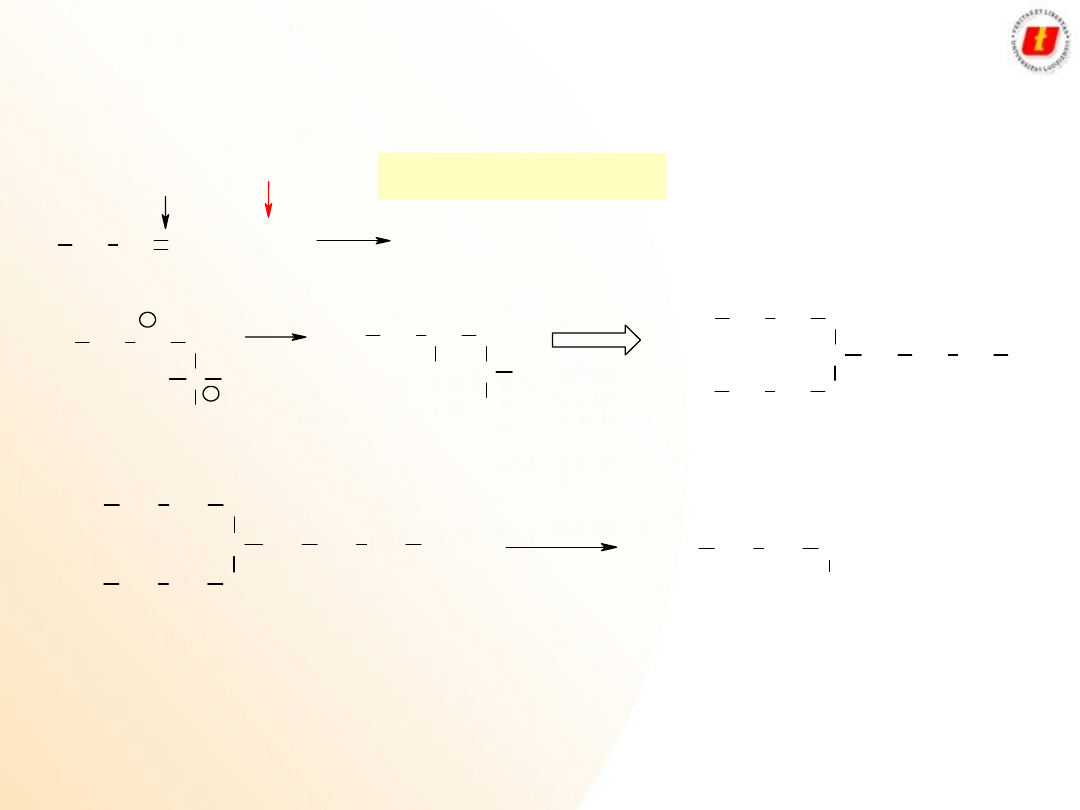
17
CH
3
CH
2
CH CH
2
CH
3
CH
2
CH CH
2
B
H
H
H
+
-
CH
3
CH
2
CH CH
2
B H
H
H
CH
2
CH
2
CH
2
CH
3
CH
3
CH
2
CH
2
CH
2
CH
3
CH
2
CH
2
CH
2
B
c.n
+ BH
3
c.e
Alkohole
Metody
otrzymywania
CH
2
CH
2
CH
2
CH
3
CH
3
CH
2
CH
2
CH
2
CH
3
CH
2
CH
2
CH
2
B
CH
3
CH
2
CH
2
CH
2
OH
H
2
O
2
/OH
-
+Na
3
BO
3
3
Dla chętnych – nie obowiązuje w
szkole średniej
18
O
O
H
NaBH
4
Alkohole i fenole
Metody
otrzymywania
X
OH
1. NaOH/H
2
O
NH
2
OH
SO
3
H
OH
1. NaNO
2
/H
+
2.
1. NaOH/H
2
O
Dopuszczona przez CKE!
Dla chętnych – nie obowiązuje w
szkole średniej
Dla chętnych – nie obowiązuje w
szkole średniej
Dla chętnych – nie obowiązuje w
szkole średniej
19
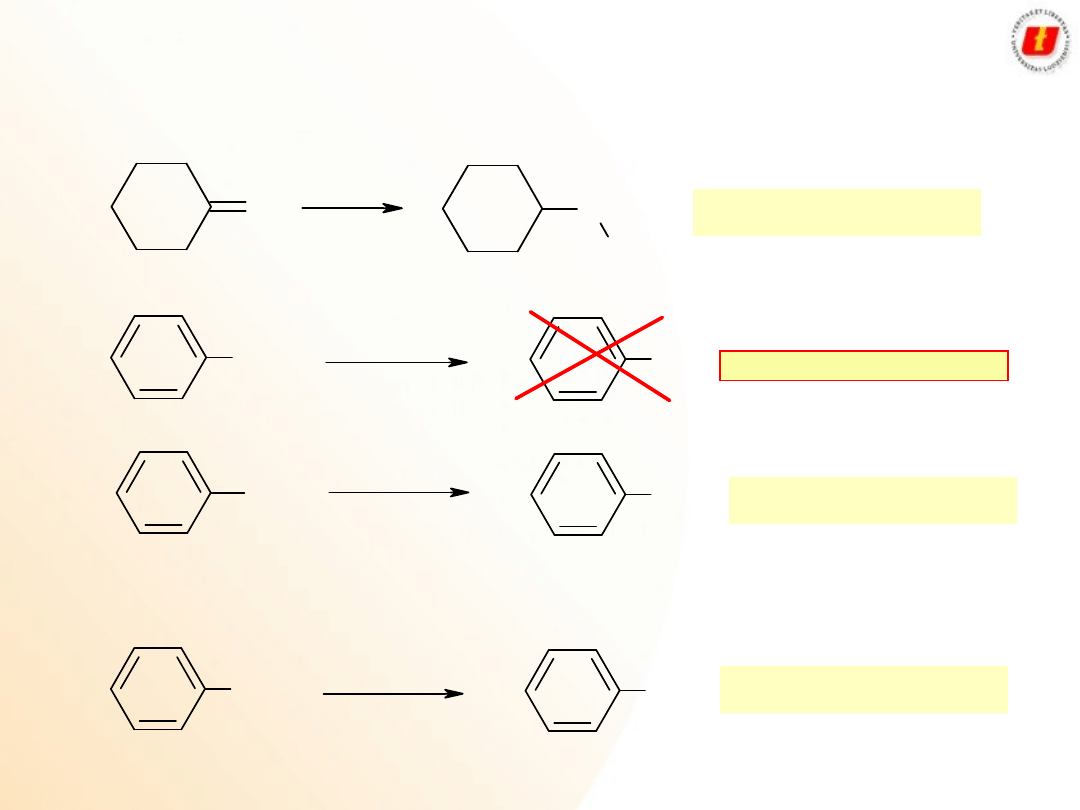
Alkohole i fenole
Właściwości
chemiczne
R
CH
2
O
H
..
..
>
c.E
c.N
c.E
atom wodoru
o charakterze kwasowym
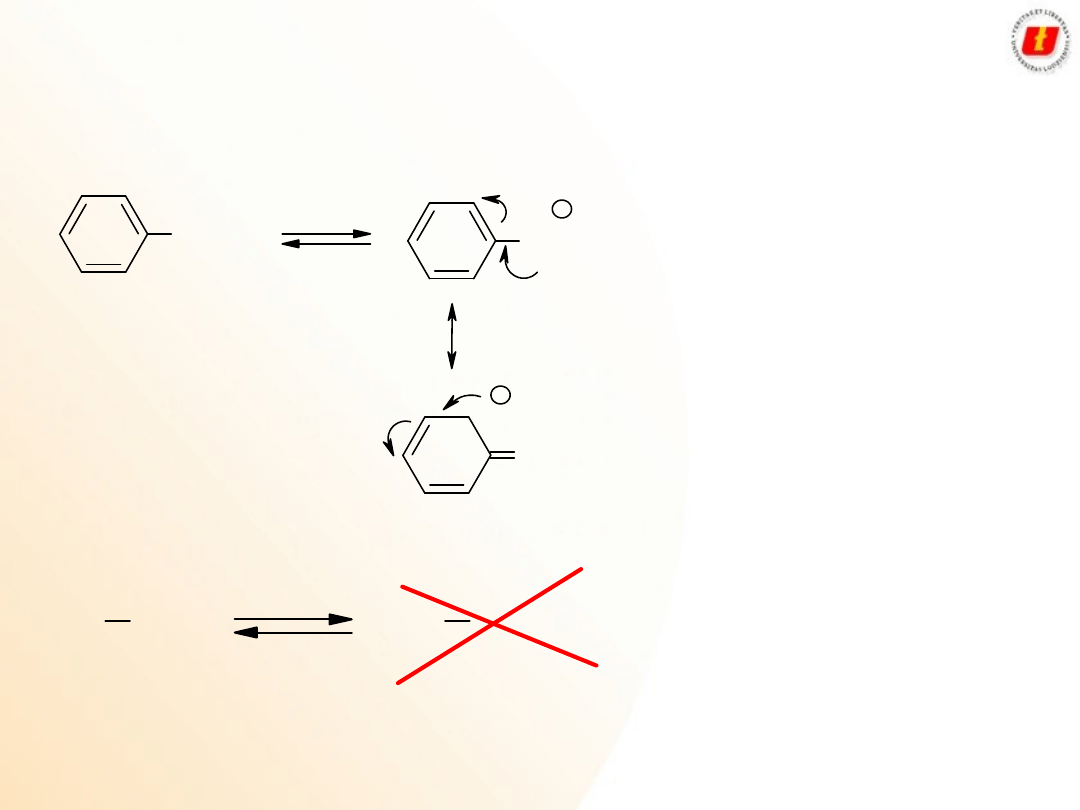
20
Alkohole i fenole
Właściwości
chemiczne
OH
O
H
+
-
O
-
+
..
..:
..
..
:
H
2
O
pK
a
=10
-10
R OH
R O
:
..
..
+ H
+
H
2
O
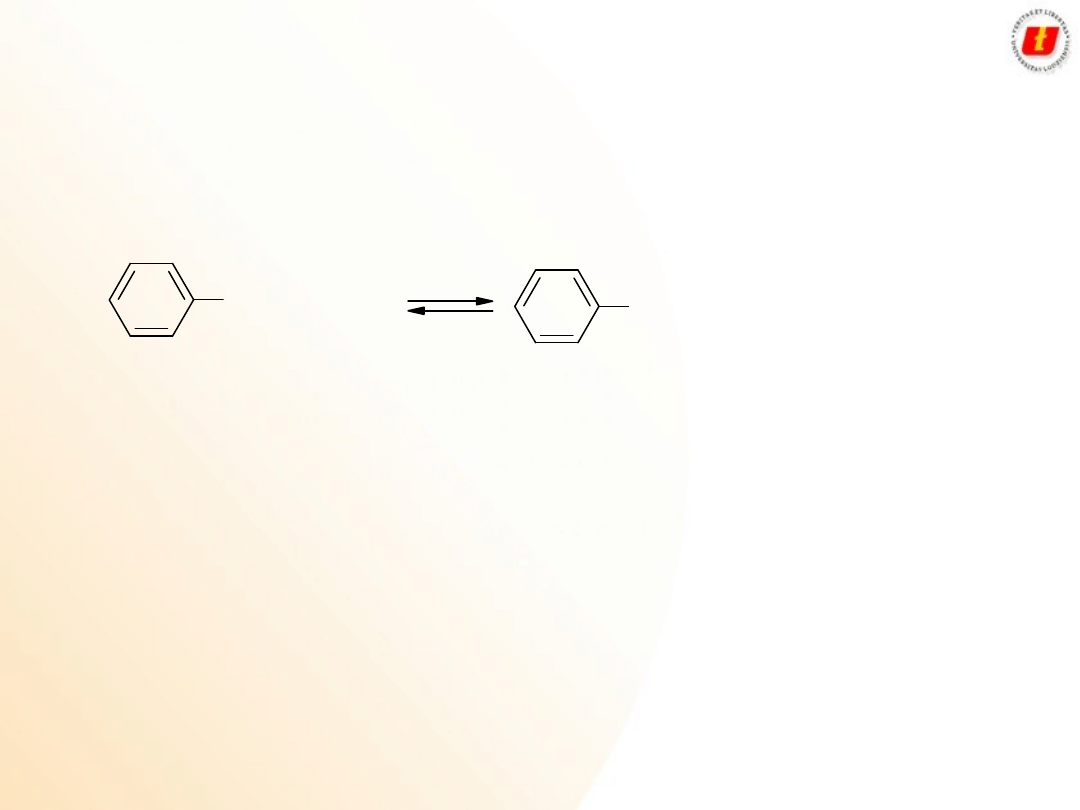
Równowaga bardzo silnie
przesunięta w lewo
21
OH
ONa
CH
3
OH + NaOH reakcja nie zachodzi
+ NaOH
+ H
2
O
Alkohole i fenole
Właściwości
chemiczne
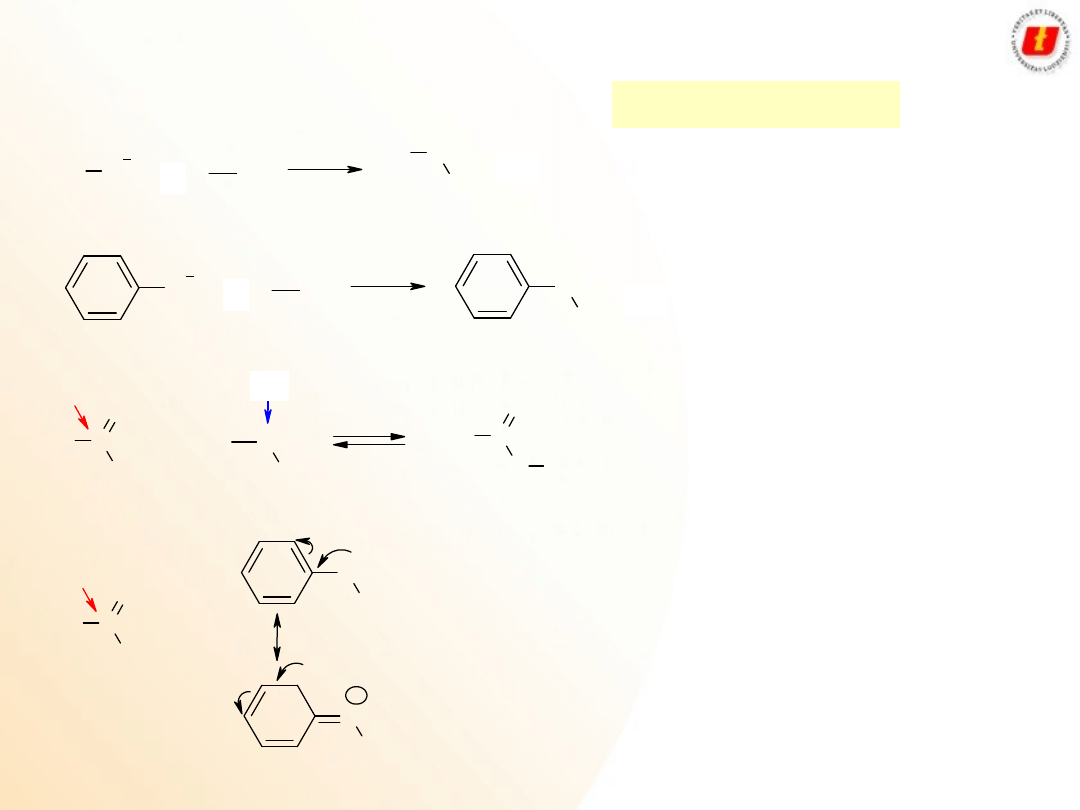
22
R O
R
1
X
R O
R
1
O
R
1
X
O
R
1
+
+ X
-
+
+ X
-
Alkohole i fenole
Właściwości
chemiczne
R
C
OH
O
R
1
O
H
R C
O
O R
1
R
C
OH
O
O
H
O
H
+
+
c.E
c.N
..
..
+ H
2
O
H
+
+
c.E
..
..
..
..
Synteza eterów Williamsona
halogenek powinien być 1
o
Synteza estrów kwasów
karboksylowych
alkan
ian
alkilu:
etani
an
etylu
propan
ian
metylu
alkanokarboksyl
an
alkilu:
cykloheksanokarboksyl
an
propylu
Dla chętnych – nie obowiązuje w
szkole średniej

23
Alkohole
Właściwości
chemiczne
Synteza halogenków alkilowych
R OH
R X
+ PX
3
+ H
3
PO
3
3
3
R OH
R Cl
+ SOCl
2
+ HCl + SO
2
CH
3
CH
2
CH
2
O
H
CH
3
CH
2
CH
2
O
H
H
+
CH
3
CH
2
CH
2
X
-
+ H
+
+ X
-
X
+ H
2
O
chlorek tionylu
Według mechanizmu S
N
2 ulegają reakcji alkohole 1
o
i 2
o
X=Cl
,
Br, I
R OH
R X
+ X
2
P
-H
3
PO
3
2P + 3X
2
2PX
3
X=Br, I
Dla chętnych – nie obowiązuje w
szkole średniej
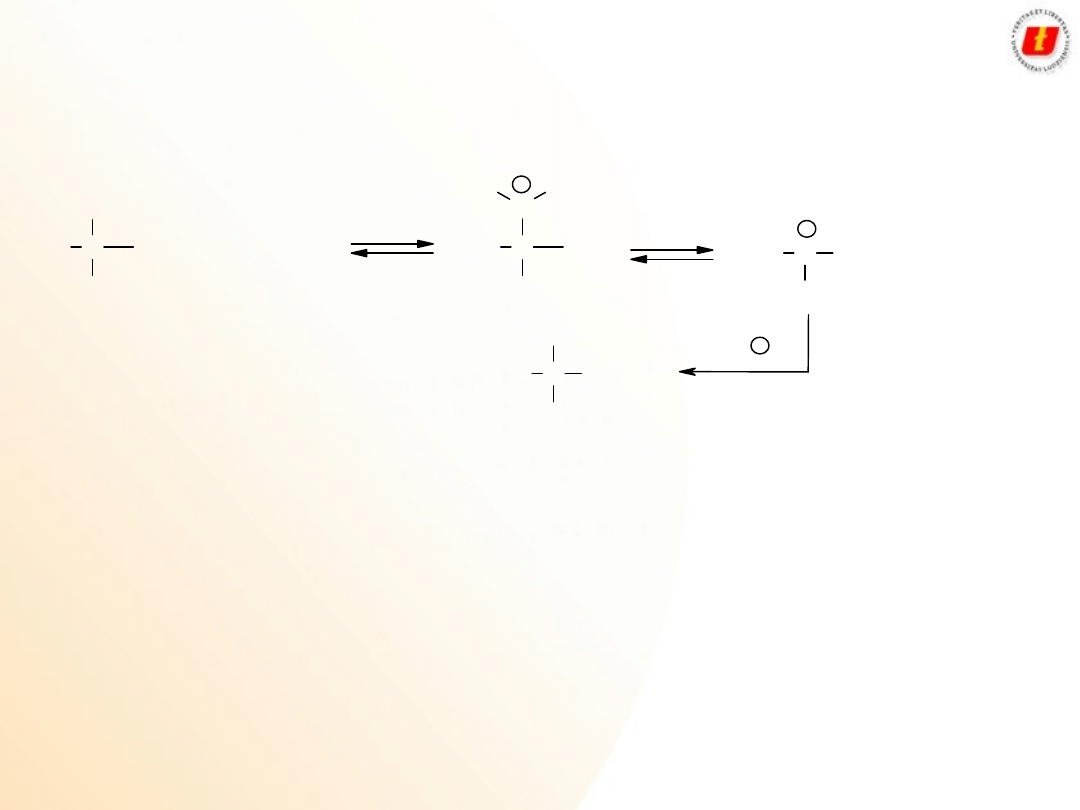
24
CH
3
C
CH
3
OH
CH
3
CH
3
C
CH
3
O
H
H
CH
3
+
CH
3
C CH
3
CH
3
+
CH
3
C CH
3
X
CH
3
-
X
+ H
+
+ X
-
+ H
2
O
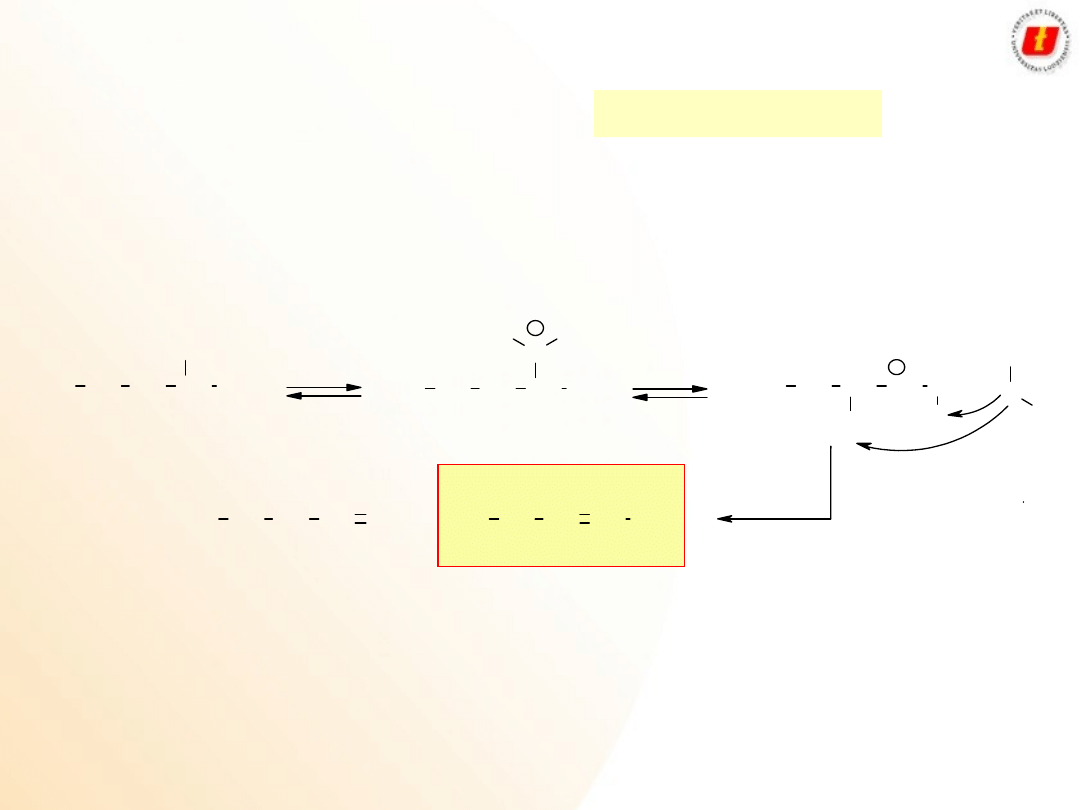
Alkohole
Właściwości
chemiczne
Alkohole 3
o
reagują według mechanizmu S
N
1
25
Alkohole
Właściwości
chemiczne
W przypadku gdy reszta kwasowa charakteryzuje się znikomą
nukleofilowością, alkohole 2
o
i 3
o
ulegają reakcji eliminacji H
2
O
(H
2
SO
4
, H
3
PO
4
CH
3
CH
2
CH
2
CH CH
3
OH
CH
3
CH
2
CH
2
CH CH
3
O
H
H
CH
3
CH
2
CH CH CH
2
H
H
+
+
O
H
H
CH
3
CH
2
CH CH CH
3
CH
3
CH
2
CH
2
CH CH
2
H
2
SO
4
Według identycznego mechanizmu reagują
alkohole 3
o
Dla chętnych – nie obowiązuje w
szkole średniej
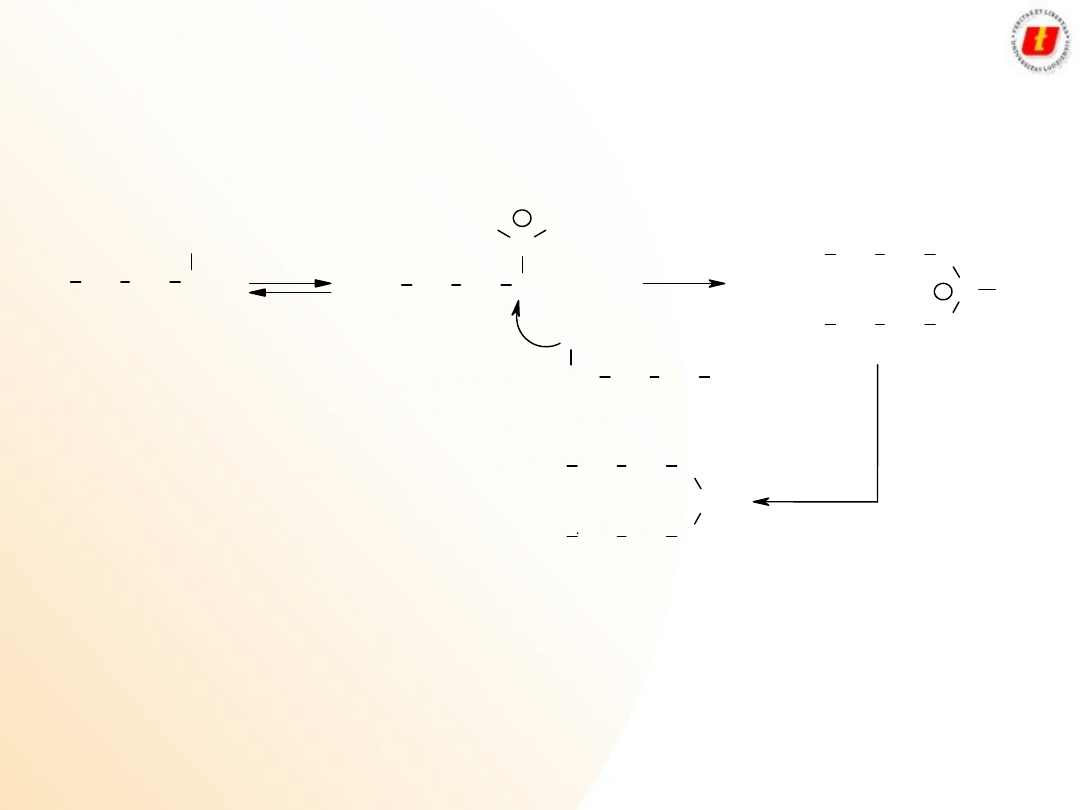
26
Alkohole
Właściwości
chemiczne
CH
3
CH
2
CH
2
CH
2
OH
CH
3
CH
2
CH
2
CH
2
O
H
H +
CH
2
CH
2
CH
2
CH
3
OH
CH
3
CH
2
CH
2
CH
2
CH
3
CH
2
CH
2
CH
2
O H
+
CH
3
CH
2
CH
2
CH
2
CH
3
CH
2
CH
2
CH
2
O
H
2
SO
4
-H
+
27
Alkohole
Właściwości
chemiczne
-
utlenianie
1
o
rzędowe alkohole utleniane są do kwasów karboksylowych
CH
3
CH
2
CH
2
CH
2
OH
CH
3
CH
2
CH
2
C
O
OH
KMnO
4
/H
+
Na
2
Cr
2
O
7
/H
+
2
o
rzędowe alkohole utleniane są do kwasów karboksylowych
CH
3
CH
2
CH CH
3
OH
CH
3
CH
2
C CH
3
O
KMnO
4
/H
+
Na
2
Cr
2
O
7
/H
+
CH
3
CH
2
C CH
3
OH
CH
3
KMnO
4
/H
+
Na
2
Cr
2
O
7
/H
+

28

29

30

31

32
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
Wyszukiwarka
Podobne podstrony:
Alkoholizm (11 stron) 4KRGM6N2DRS7GDIS4B77CD6RXIW2X5YTVMZYDOI
Moczydłowska, J (1996) Doświadczanie poczucia winy u nieletnich prostytutek, Problemy alkoholizmu, 1
Moczydłowska, J (1996) Doświadczanie poczucia winy u nieletnich prostytutek, Problemy alkoholizmu, 1
Z 11 Alkohole itd
psychozy alkoholowe 13.11.2005, Studia, Psychoprofilaktyka
W- 11- monograficzny, ALKOHOL A ZDROWIE
Zatrucia alkoholami niekonsumpcyjnymi - Nowa Klinika 2000 Vol 7 Nr 11-12, uczelnia awf, pierwsza pom
Æwiczenie 11 Alkohole
11 (Liche c5 84) Wsp c3 b3 c5 82uzale c5 bcnienie alkoholowe
Z 11 Alkohole etery
11.Alkohole, Notatki AWF, Biochemia
5 alkohole 07 11 2015 2014
11.Alkohole i etery, MATERIAŁY NA STUDIA, Chemia
Æwiczenie 11 Alkohole
Z 11 Alkohole itd
psychozy alkoholowe 13.11.2005, Studia, Psychoprofilaktyka
C6wiczenie 11 =2D Alkohole=2Epdf =
Wobiz Współuzależnienie w rodzinie alkoholowej, str 11 64 (rozdz 1 2)
więcej podobnych podstron