
Struktura
pasmowa ciał
stałych
opis struktury elektronowej
pasma energetyczne
masa efektywna elektronu i
dziury
Wykład – 10 -
2
Prof. J. Zieliński
Terminy zaliczeń poprawkowych w semestrze letnim
2010/11
o 28 marzec
o 18 kwiecień
o 16 maj
o 13 czerwiec
Przypominam, że
Przypominam, że
na wszystkie kolejne terminy poprawkowe
obowiązują karty zie-lone.
Do zaliczenia można podejść po zaliczeniu ćwiczeń
rachunko-wych
zaliczona w terminie zerowym teoria a nie wpisana
zaliczona w terminie zerowym teoria a nie wpisana
do indeksu została skreślona
do indeksu została skreślona
Zaliczenia zaczynają się o
godz. 15
sala 2 bud 5

W tym semestrze
Zaliczenie przedmiotu jest w formie egzaminu
> Aby móc przystąpić do egzaminu trzeba mieć
zaliczone ćwicze-nia i laboratoria. Pozytywne oceny
muszą być wpisane do karty o-cen i do indeksu.
Egzamin składa się z dwóch części:
- Pisemnej student pisze odpowiedź na 3 pytania z
zestawu 4-ech
- Ustnej odpowiedzi uzupełniające na pytania z
zestawu pisemne-go + inne pytania.

Właściwości elektronów w ciałach stałych
wynikają z ich oddziaływania między sobą i
oddziaływania z atomami (jonami) sieci. Jednakże
każde z tych oddziaływań jest skomplikowane.
Wystarczy sobie bowiem uświadomić, że w 1 cm
3
ciała stałego znajduje się około 10
23
elektronów i
jonów będących w ciągłym ruchu i oddziaływujących
na siebie.
W
celu
prześledzenia
wpływu
pola
elektrycznego na pozio-my energetyczne elektronów
w atomie, rozpatrzymy następujący wyidealizowany
przykład, który pozwala w sposób jakościowy zro-
zumieć zachodzące zjawiska. Rozmieścimy N atomów
sodu w wę-złach sieci przestrzennej odpowiadającej
kryształowi sodu, ale w tak dużych odległościach aby
można było pominąć ich wzajemne oddziaływanie. W
takim przypadku stany energetyczne elektronów będą
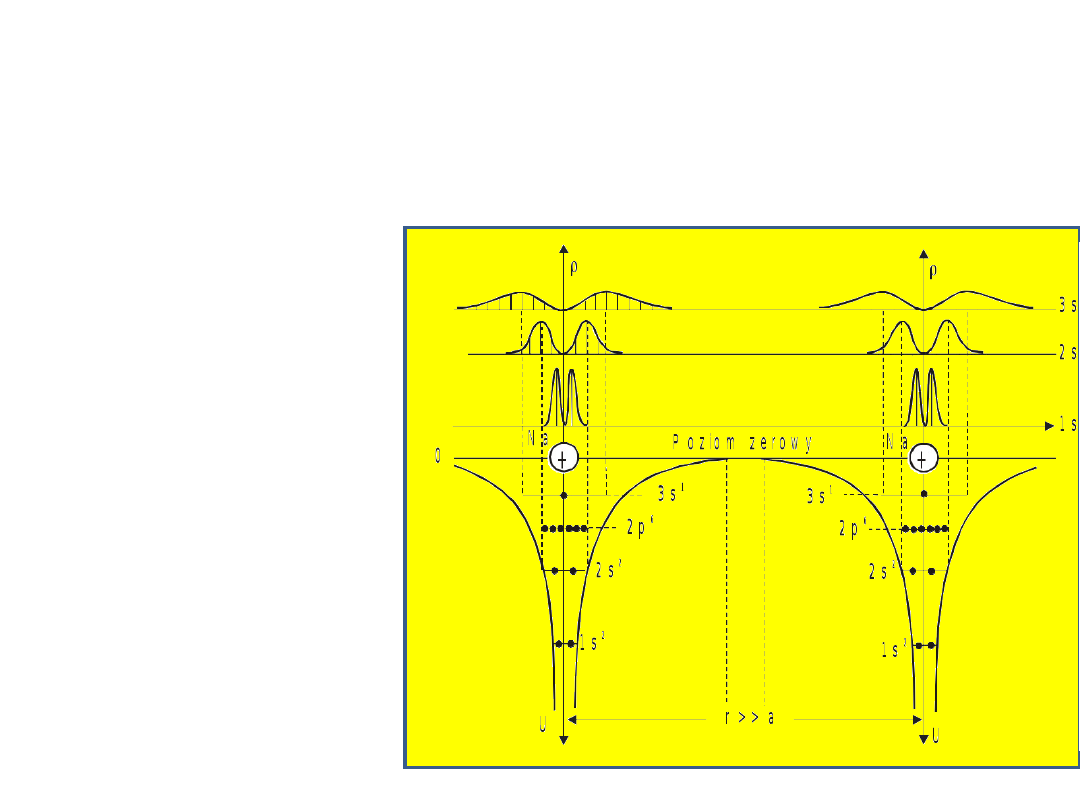
odpowiadały stanom atomu izolowanego. Na rys.
16.1a pokazano schemat poziomów energetycznych
dwóch izolowanych atomów sodu.
Izolowane (swobodne)
atomy sodu (Na)
• w atomie swobodnym
każdy poziom jest
2(2l+1)
krotnie
zdegenerowany
• dla N atomów liczba
pod-poziomów wynosi
2N(2l+1)
• bariera potencjału nie
ze-zwala elektronom
swo-bodnie poruszać
się mię-zy atomami
• elektrony
są
zlokalizowa-ne,
funkcje falowe nie za-
chodzą na siebie
W atomie tym jak wiadomo, poziomy
energetyczne 1s, 2s i 2p są zapełnione całkowicie, a
poziomy rozmieszczone powyżej 3s są wolne.
Zauważmy, że bariera potencjału nie pozwala
elektronom poruszać się swobodnie między
poszczególnymi atomami.
Poddajemy
teraz
sieć
jednorodnemu
ściskaniu
. W miarę zbliżania się atomów do siebie,
wzrasta ich oddziaływanie i w odległościach równych
parametrowi sieci (a = 0,43 nm) energia
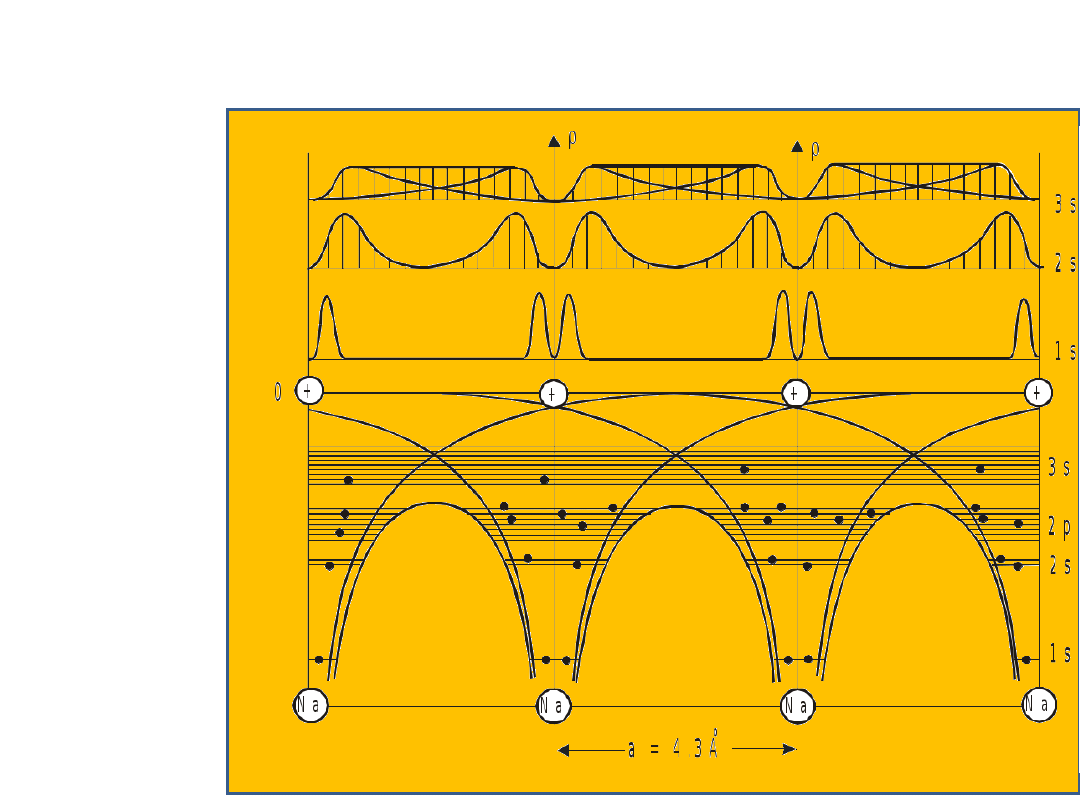
oddziaływania osiąga wartość minimalną. Na rys.
16.1b pokazano schemat poziomów energetycznych
elektronów
odpowiadający
zbliżeniu
atomów.
Widzimy,
że
krzywe
potencjalne
oddzielające
sąsiednie atomy częściowo zachodzą na siebie dając
wypadkową krzywą potencjalną, która przebiega
poniżej poziomu zerowego. Godnym uwagi jest fakt,
że wysokość ta jest nawet nieco mniejsza od
początkowego
położenia
poziomu
elektronów
walencyjnych 3s. Dlatego też elektrony walencyjne
uzyskują możliwość przechodzenia z jednego atomu
do
drugiego.
Elektrony
takie
nazywamy
swobodnymi
Zmiana stanu elektronów
przy zbliżaniu się atomów
•
obniżenie poziomu potencjału
poniżej stanu 3s
•
elektrony 3s stają się
swobodne
•
funkcje falowe tych
elektronów zachodzą na
siebie
•
funkcje falowe elektronów
wewnętrznych nie ulegają
zmianie
•
pojedyncze poziomy ulegają
rozszczepieniu tworząc pasmo
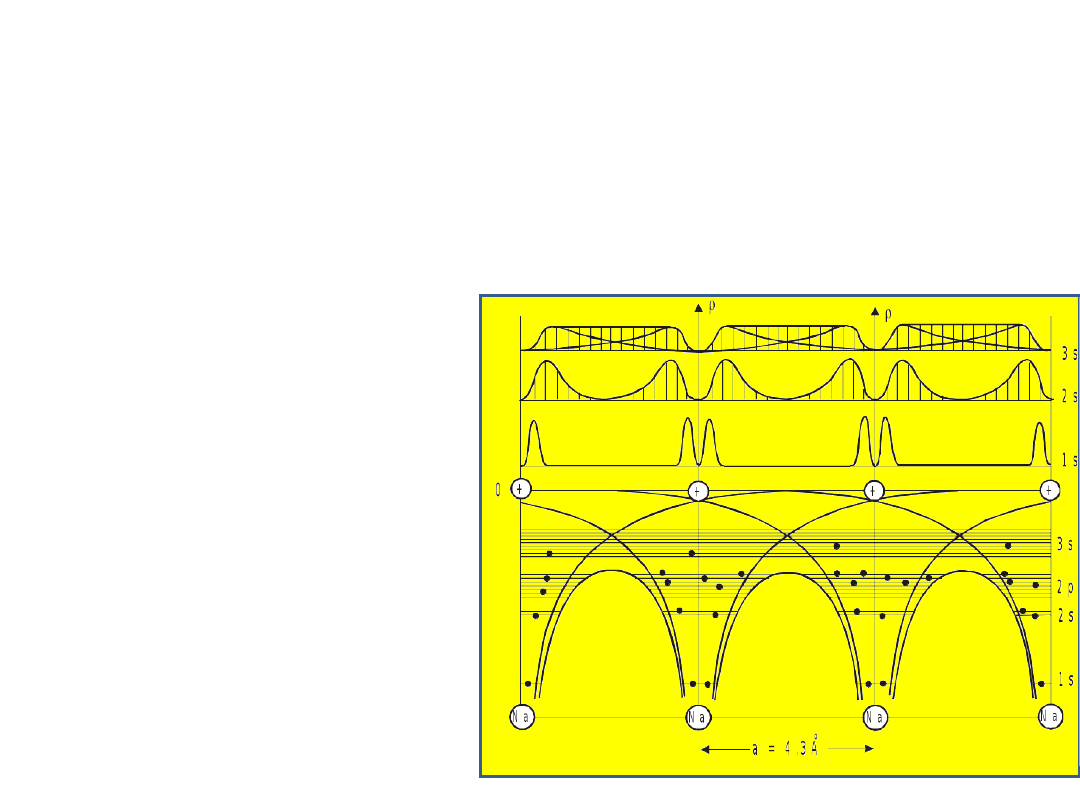
Przy odległościach równych stałej sieci 0,43 nm
otrzymujemy:
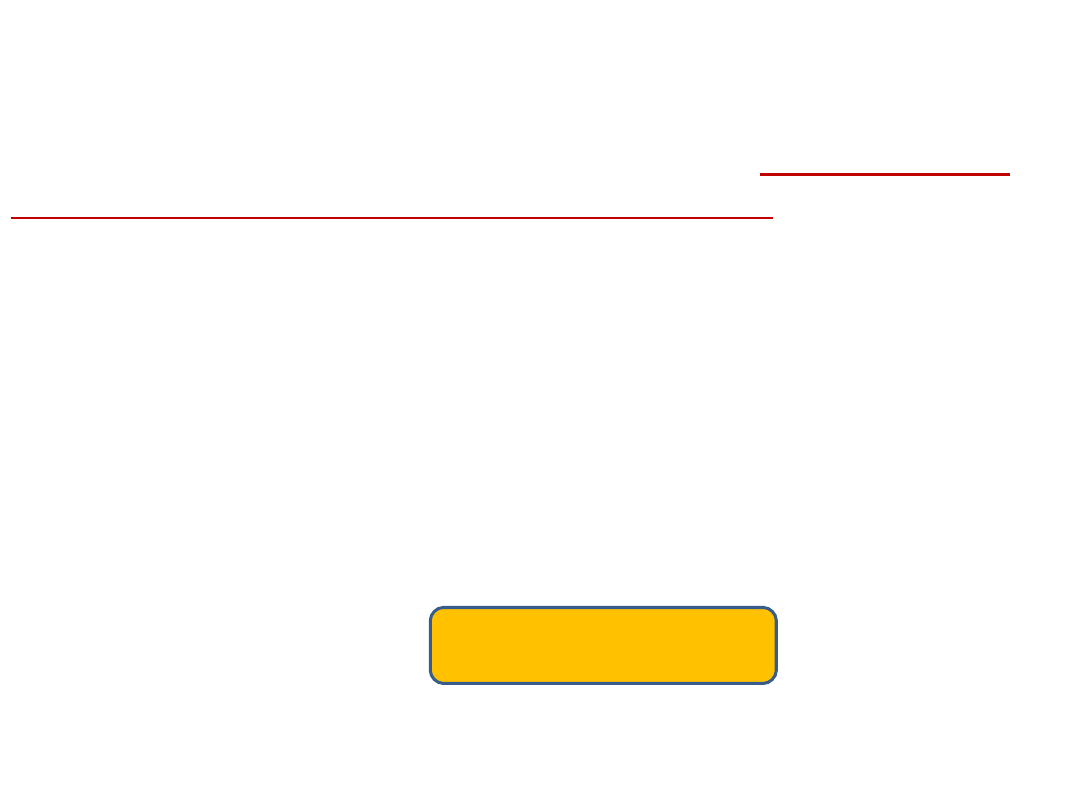
Zauważmy, że charakter funkcji falowych tych
elektronów jest taki, że zachodzą one na siebie w
takim stopniu, że tworzą chmurę o prawie
równomiernej gęstości, a to oznacza
stan pełnego
uwspólnienia elektronów walencyjnych
. Natomiast
chmury
elektro-nowe
wewnętrznych
powłok
elektronowych atomów nie pokrywają się i stany
elektronów wewnętrznych atomów kryształu pozostają
w zasadzie takie same jak w atomach izolowanych.
Należy ponadto zauważyć, że pojedyncze poziomy
atomowe uległy rozszczepieniu na zespoły poziomów
zwanych dozwolonymi pasmami energetycznymi.
Ponieważ prędkość ruchu elektronu jest rzędu 10
5
m/s, a
rozmiary ato-mu wynoszą 10
–10
m, to elektron
walencyjny znajduje się w danym wę-źle w czasie Δt =
10
–15
s co powoduje, że szerokość poziomu energe-
tycznego elektronu walencyjnego ΔE jest w przybliżeniu
równa .
eV
t
/
h
E
1

Jeżeli
poziomy
energetyczne
w
atomie
swobodnym były (2l+1) -krotnie zdegenerowane (bez
uwzględnienia spinu), to odpowiada-jące im pasma
energetyczne będą miały N(2l+1) podpoziomów (N –
ilość atomów); np. z poziomu p wytworzy się pasmo
składające się z 3N podpoziomów mogących zmieścić
6N elektronów. Jeżeli dalej uwzględnimy, że 1 g ciała
stałego zawiera N = 10
22
atomów i że każdy pojedynczy
poziom energetyczny rozpada się na N poziomów, to
przy szerokości pasma rzędu 1 eV odległości między
poziomami wynoszą około 10
–22
eV, co wskazuje, że nie
ma możliwości doświadczalnego ich rozróżnienia. O
takiej właśnie grupie poziomów mówimy jako o paśmie
dozwolonym uważając, że elektrony w tym paśmie
mają ciągły rozkład energii. Pasma te są rozdzielone
pasmami wzbronio-nymi.

Wyniki poglądowo przedstawione powyżej
uzyskuje
się
również
rozwiązując
kwantowo-
mechaniczne zagadnienia ruchu wielu elektronów w
polu ruchu jonów. Złożoność tego zagadnienia zmusza
nas do wprowadzenia szeregu uproszczeń. Dlatego
analizu-jąc zachowanie elektronów w sieci stosujemy
wiele
przybliżeń.
Dwoma
skrajnymi
przeciwstawnymi przybliżeniami są: przybliże-
nie
elektronów
prawie
swobodnych
i
przybliżenie elektronów silnie związanych
. W obu
tych przypadkach otrzymujemy zakresy energii
dozwolonych i zabronionych dla elektronów. Kształt
pasm energetycznych i ich zapełnienie przez elektrony
jest jednym z najpoważniejszych zagadnień w fizyce
ciała stałego.
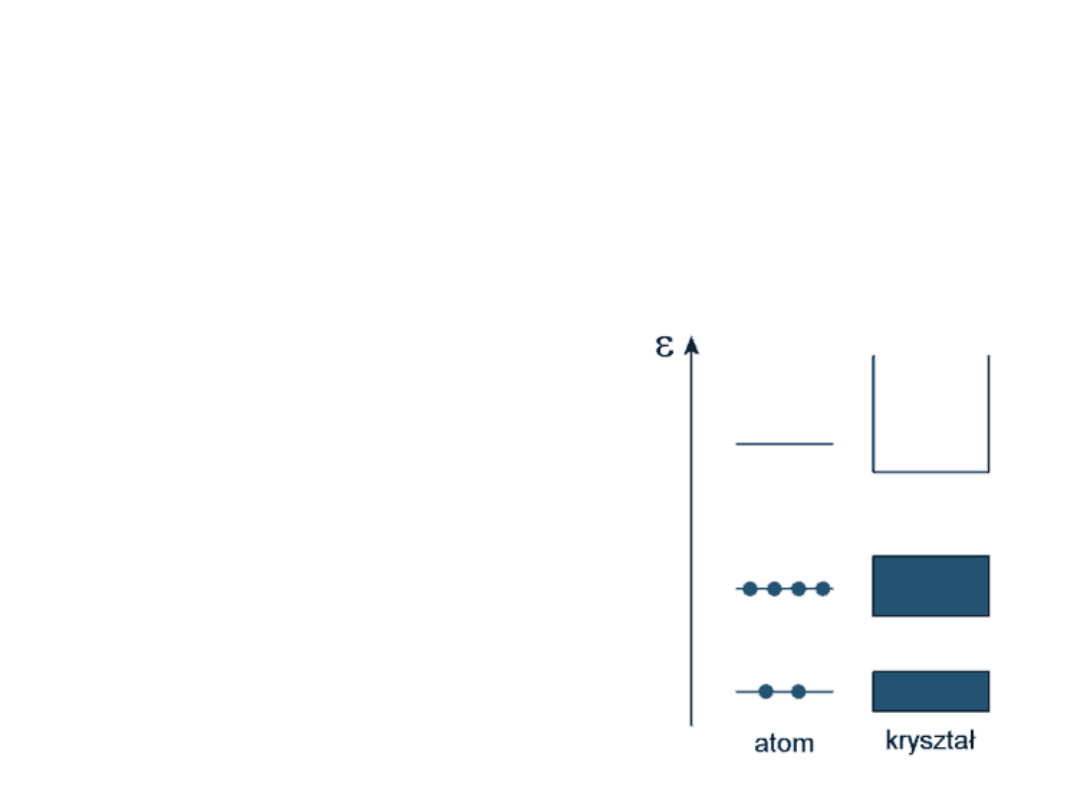
Co to jest teoria pasmowa
Teoria pasmowa jest kwantowo-
mechanicznym opisem zachowania
elektronów w krystalicznym ciele stałym
.
Nazwa
teoria
pasmowa
pochodzi od najważniejszej
cechy widma energety-cznego
w krysztale:
w
przeciwieństwie
do
dyskretnych
poziomów
dla
izolowanych atomów, widmo
energetyczne kryształu chara-
kteryzują
pasma
energii
dozwolonych
o
skończonej
szerokości

Równanie Schrodingera
Przyjęcie wspólnego potencjału U(r) umożliwia opis
stanów
ele-ktronowych
przy
pomocy
jedno-
elektronowych funkcji falo-wych. Postać funkcji
falowych
i wartości własne energii E uzyskuje się
z rozwiązania równanie Schrödingera, które w przy-
padku jednowymiarowym ma znaną nam postać
Podstawą teorii pasmowej jest założenie, że
oddziaływania elektro-nów w ciele stałym można
opisać przy pomocy periodycznego po-tencjału U(r),
który nie zmienia się w wyniku przesunięcia o wektor
sieciowy R = n
1
a + n
2
b + n
3
c
U(r + R) = U(
r
)
0
2
2
2
2
x
U
E
m
dx
d
U(x + a) = U
(x)
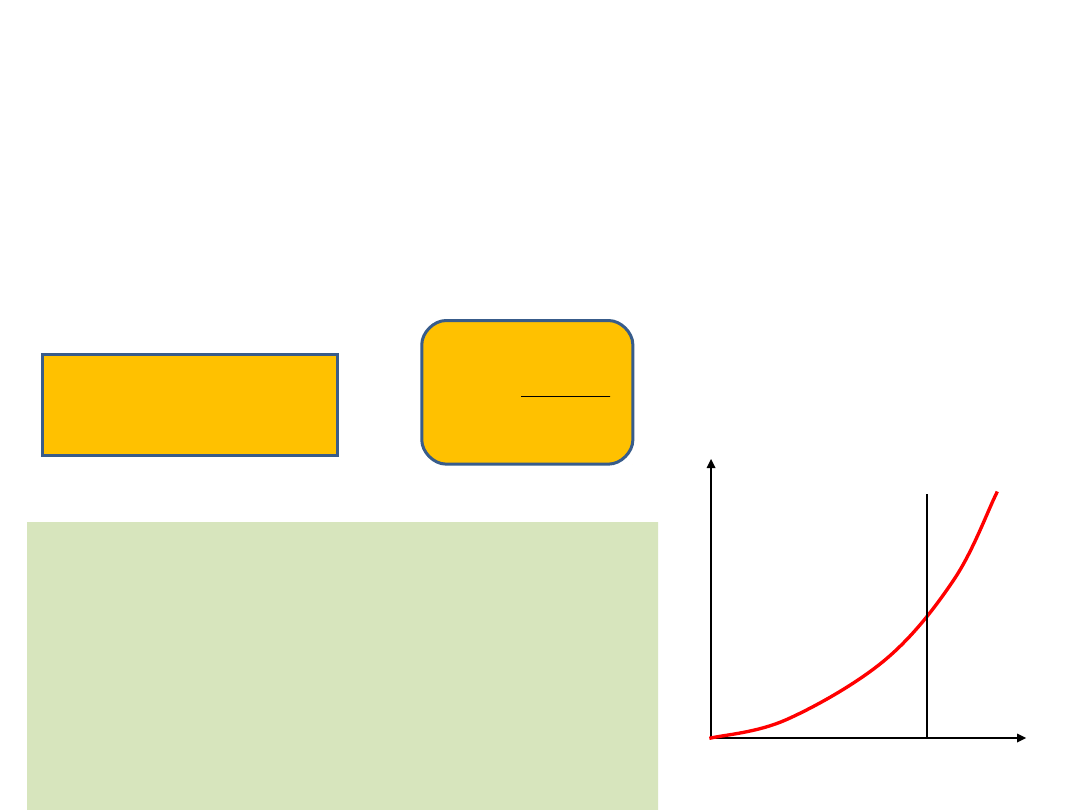
Model elektronów
swobodnych
m
k
E
2
2
2
E(k)
/a
k
Jedyne ograniczenie ruchu elektronów swobodnych jest
spowodowane
przez
powierzchnię
kryształu.
Z
równania Schrödingera wynika, że za-leżność energii od
wektora falowego jest quasi-ciągłą funkcją parabo-
liczną
Elektron praktycznie
może przyj-mować
dowolne wartości energii,
jedynie obsadzanie
stanów ener-getycznych
odbywa się zgodnie z
zakazem Pauliego
ikx
Ae
x
Wady modelu elektronów
swobodnych
• przyjęcie stałego potencjału w
modelu elektronów swobodnych
nie
uwzglę-dnia
dyskretnej
struktury krystalicznej ciał stałych
• istotny wpływ na zachowanie
elektro-nów
odgrywa
ich
oddziaływanie z jonami sieci
• brak również uwzględnienia oddzia-
ływania elektronów pomiędzy sobą
• oba typy oddziaływań można
rozdzielić stosując różne rodzaje
przybliżeń:
jednoelektronowe,
elektronów prawie swobodnych lub
silnie związanych
E
x
0
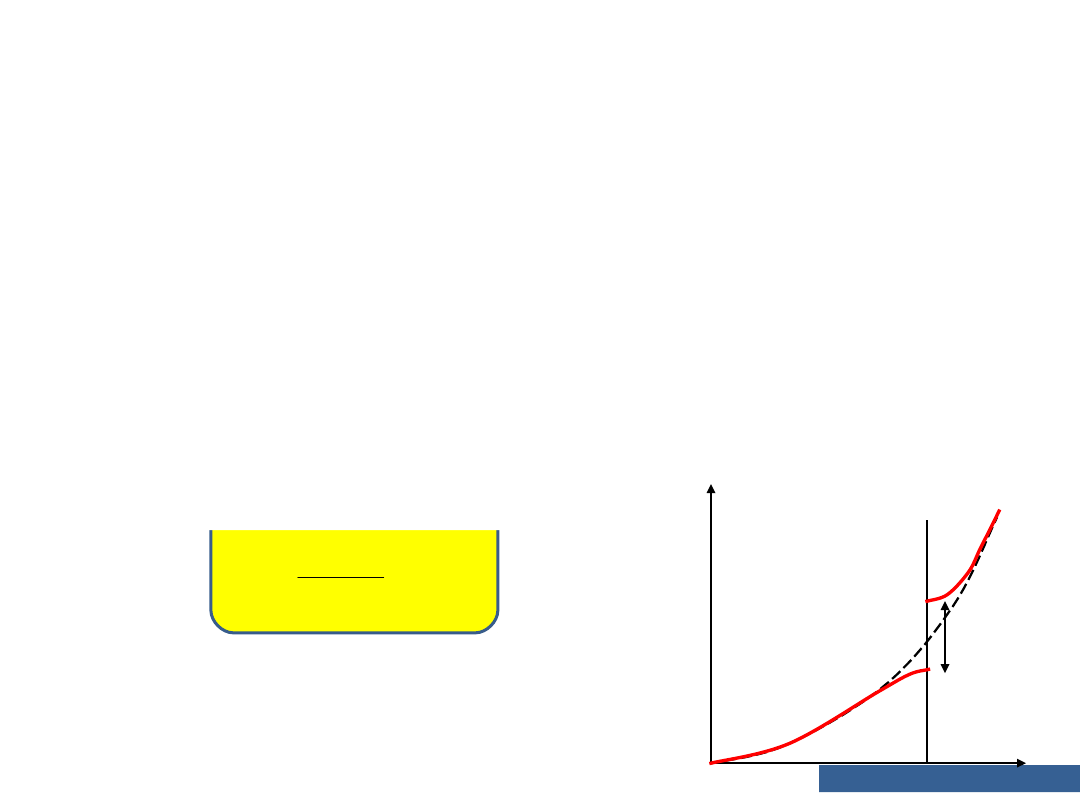
Przybliżenie elektronów
prawie swobodnych
Z rozwiązania równania Schrodingera wynika, że
energia elektro-nów o wektorach falowych leżących
na granicy tzw. strefy Bril-louina może przybierać
dwie wartości różniące się o 2V
g
– prowa-dzi to do
powstania nieciągłości energii
g
V
m
k
E
2
2
2
E(k)
/a
k
2V
g
Fale o tych wektorach falowych
ulegają całkowitemu odbiciu i nie
mogą rozcho-dzić się w krysztale -
powstaje fala stojąca.
Zakładamy, że potencjał U(r) działający na elektrony
poruszające się w krysztale jest tak mały, że można
potraktować go jako małe zaburzenie
W przybliżeniu elektronów słabo związanych
zakładamy, że energia oddziaływania elektronu z
siecią jest znacznie mniejsza od energii ki-netycznej.
Sytuacja taka ma miejsce w przypadku elektronów
najsła-biej związanych z atomami, czyli elektronów
przewodnictwa
w
meta-lach.
Pole
elektryczne
wytworzone przez jony jest kompensowane przez pole
wszystkich
pozostałych
elektronów
oprócz
rozpatrywane-go. Niewielkie, nieskompensowane pole
ma charakter okresowy o okresie równym stałej sieci. Z
okresowości tej wynika, że funkcja falo-wa opisująca
stan elektronu będzie funkcją Blocha.
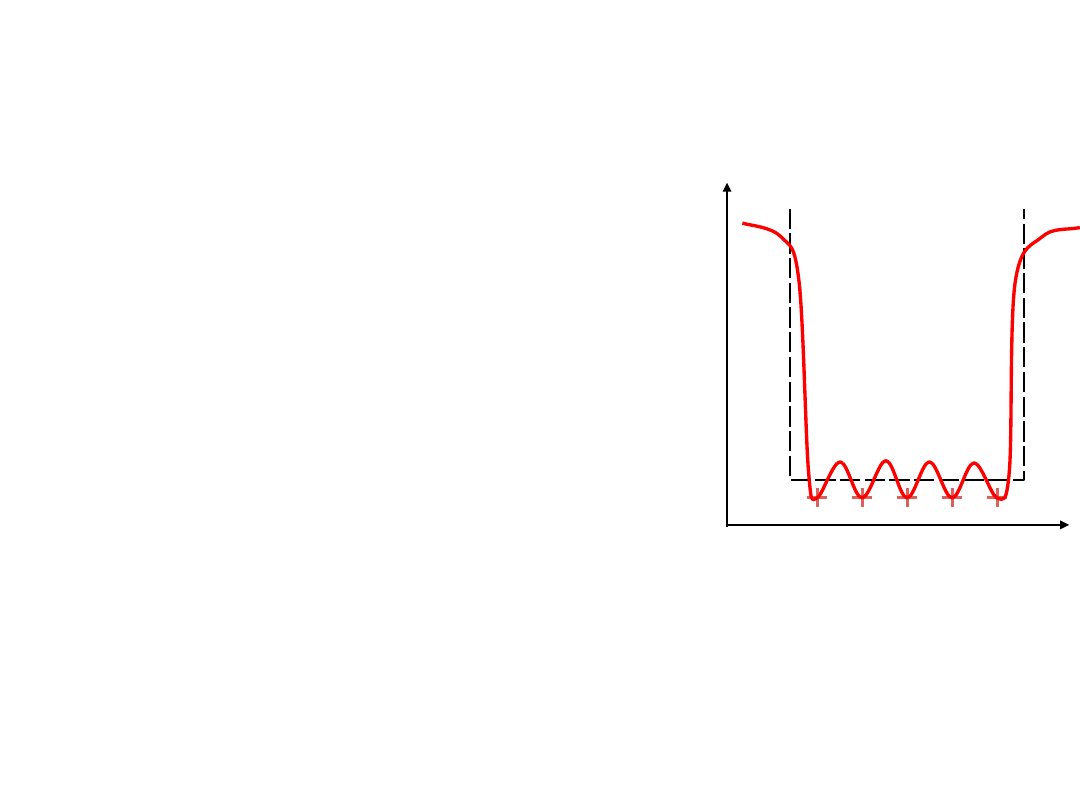
Aby
opisać
ruch
elektronu
w
polu
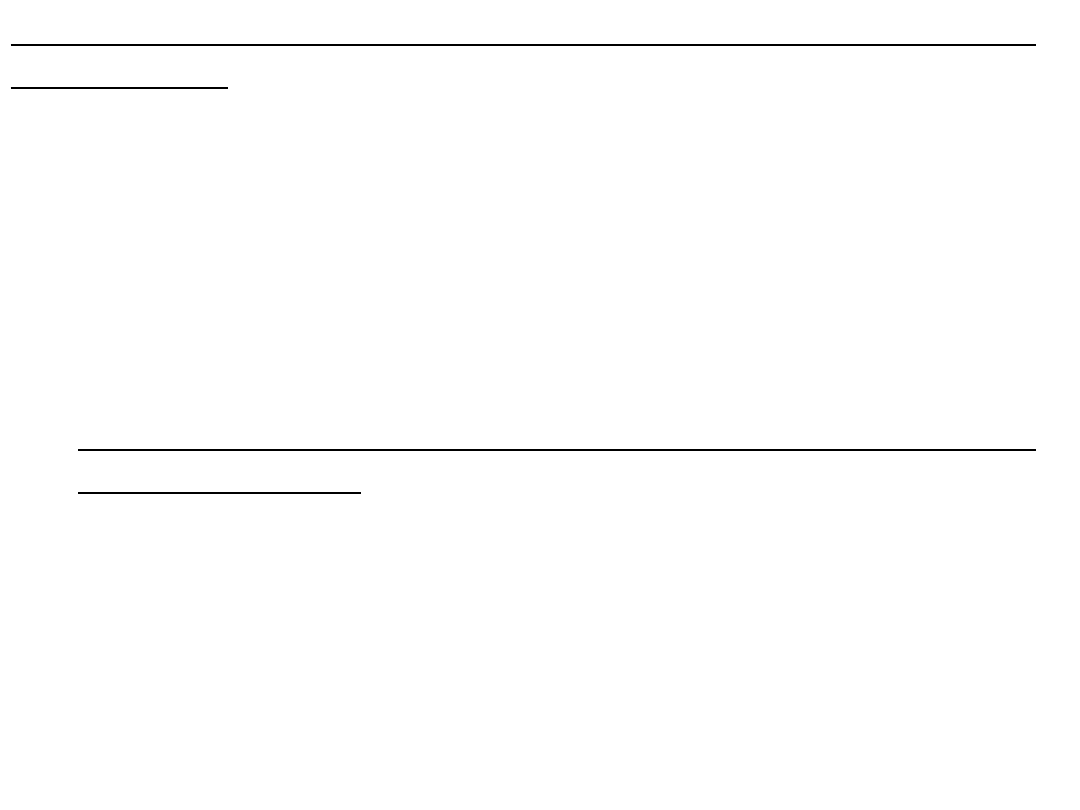
periodycznym, posłużymy się modelem Kröniga-
Penneya. W modelu tym potencjał rzeczywisty w
krysztale zastępujemy przez nieskończoną liczbę
prostokątnych barier potencjalnych o szerokości b i
wysokości U
o
. Studnia poten-cjału oddzielająca
bariery ma szerokość a i energię U
o
rys
Potencjał ten odtwarza wprawdzie w niewielkim
stopniu warunki występujące w krysztale, jednak
uzyskane
rozwiązanie
umożliwia
sformułowanie
pewnych ogólnych wniosków dotyczących zależności
dyspersyjnej dla elektronu w ośrodku periodycznym.
Potencjał jest więc okresowy o okresie d = a + b.
Zakładamy, że energia całkowita elektronu E < U
o
.
Równanie Schrödingera ma postać
0
2
2
2
2
E
m
dx
d
0
2
2
2
2
E
U
m
dx
d
o
dla 0 < x < a
dla –b < x < 0
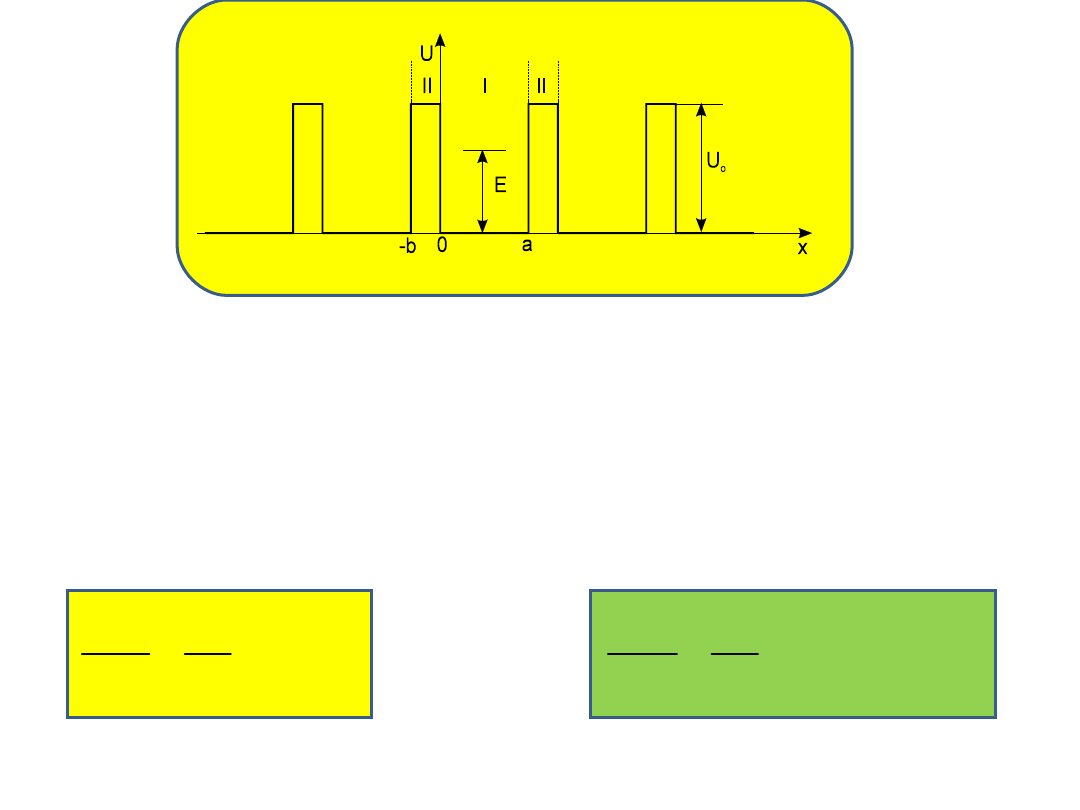
Rozwiązaniem powyższych równań są funkcje
x
i
x
i
e
B
e
A
1
1
1
x
x
e
B
e
A
2
2
2
dla 0 < x < a
dla –b < x < 0,
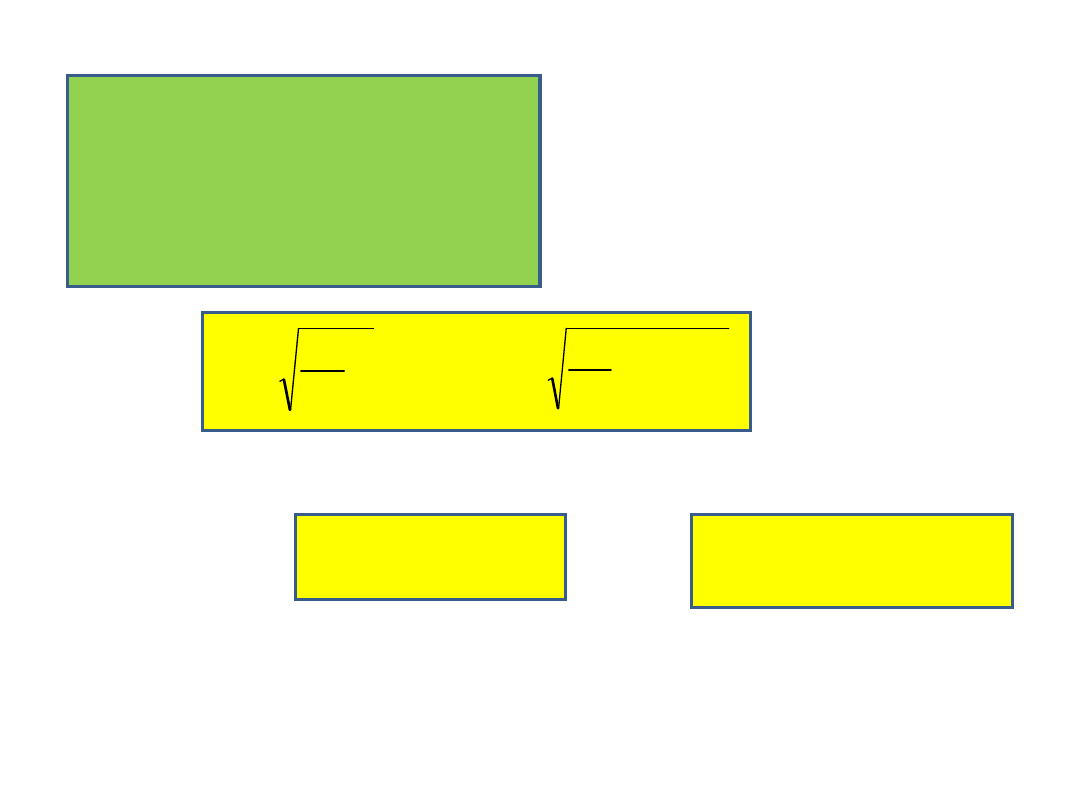
gdzie
E
m
2
2
E
U
m
o
2
2
Wiemy już, że jeśli potencjał jest periodyczny, to
funkcja Ψ(x) speł-nia warunek
ikx
e
x
u
x
skąd
ikx
e
x
x
u
………
Po kolejnych podstawieniach otrzymujemy układ 4-
ech równań w których niewiadome stanowią A
1
, A
2
,
B
1
, B
2
:

2
2
1
1
B
A
B
A
2
2
1
1
B
ik
A
ik
B
k
i
A
k
i
b
ik
b
ik
a
k
i
a
k
i
e
B
e
A
e
B
e
A
2
2
1
1
b
ik
b
ik
a
k
i
a
k
i
e
B
ik
e
A
ik
e
B
k
i
e
A
k
i
2
2
1
1
Układ ten posiada niezerowe rozwiązanie tylko wtedy,
gdy wyznacznik macierzy współczynników przy A
1
, A
2
, B
1
,
B
2
równa się zeru
b
a
k
cos
a
cos
b
cosh
a
sin
b
sinh
2
2
2
Równanie to nakłada warunki na α i β, a co z tym się
wiąże i na dopu-szczalne wartości energii. Analiza tego
równania jest jednak dość uciążliwa. Dlatego
zastosujemy uproszczenie Kröniga i Penneya pole-
gające na założeniu, że U
o
dąży do nieskończoności,
natomiast b dąży do zera w taki sposób, że iloczyn U
o
b
pozostaje skończony.
Po uproszczeniu równanie ma postać
ka
cos
a
cos
a
a
sin
P
gdzie ; przyjęto też, że sinhβb = βb i cosh βb = 1.
Wielkość P można traktować jako miarę trudności
pokonywania bariery przez elektron.
- 3
- 2
2
3
a
-
- 1
+ 1
a
s in
a
a
s in
P
Równanie
wyraża
za-
leżność
energii
ele-ktronu
(poprzez a) od
liczby falowej k.
Na
rys.
przedstawiono
rozwiązanie
powyż-szego
równania meto-
dą graficzną
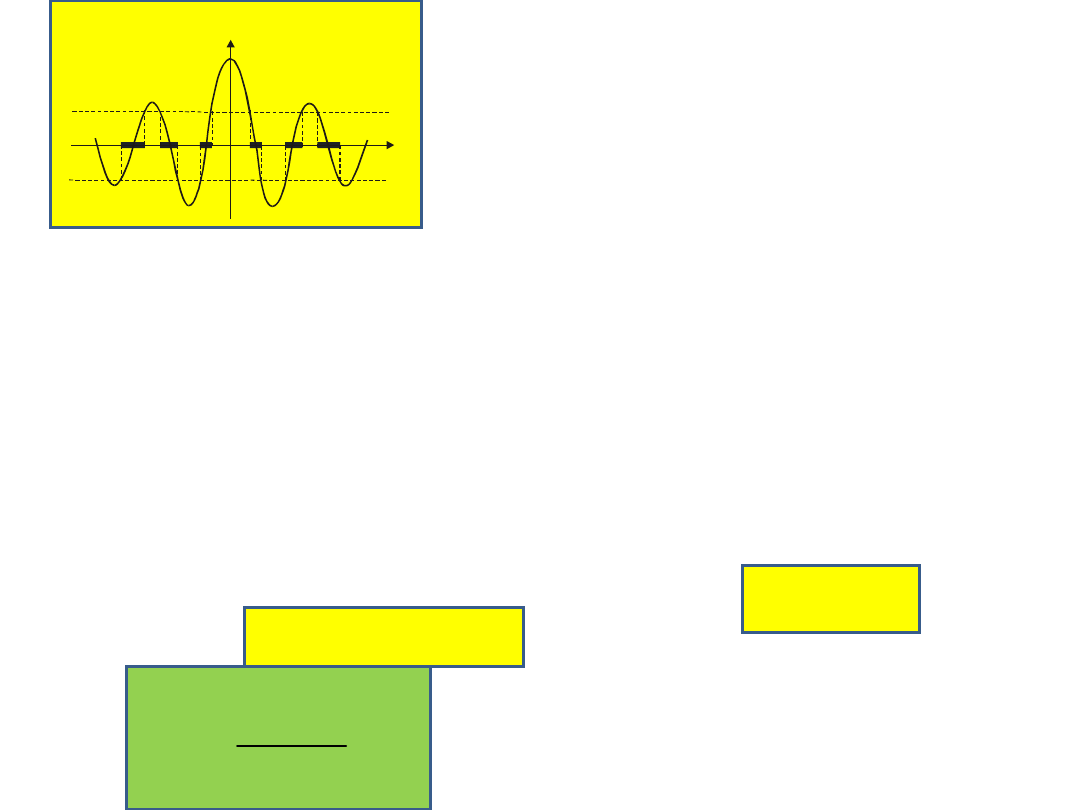
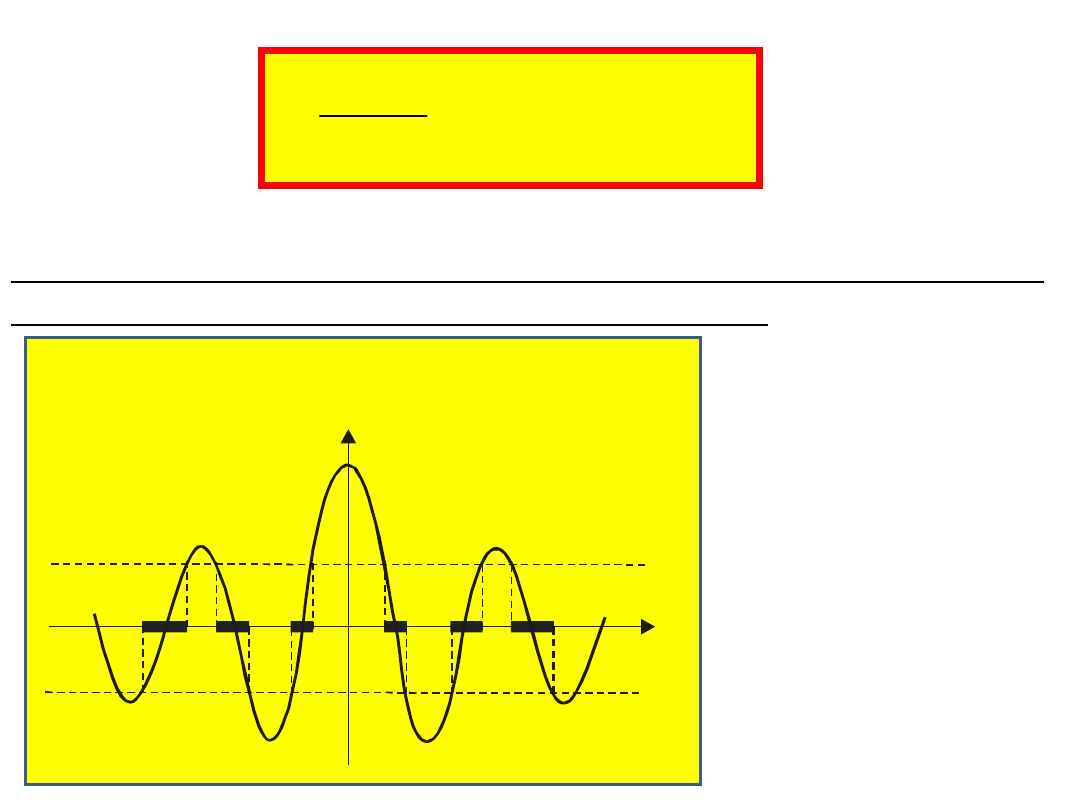
mieszczą się w przedziale [–1,1]. Wartości αa
spełniające ten warunek zaznaczono grubą linią.
Widać, że dopuszczalne wartości energii tworzą
pewne przedziały, tzw. pasma energetyczne.
Poszczególne pasma energetyczne oddzielone są przez
obszary o wzbronionych wartościach energii. W miarę
wzrostu αa (a więc wartości energii, gdyż a jest
ustalone) dozwolone pasma energetyczne stają się
coraz szersze. Szerokość pasm zależy także od
parametru P.
Ponieważ coska znajdujący się
po pra-wej stronie równania
jest zawarty w przedziale [–
1,1], a więc dopuszczalne
mogą być tylko te wartości αa,
dla któ-rych wartości lewej
strony równania
- 3
- 2
2
3
a
-
- 1
+ 1
a
s in
a
a
s i n
P
Ze wzrostem P pasma dozwolone zwężają się; w
szczególności gdy P>∞, równanie ma rozwiązanie tylko
wtedy gdy
czyli αa = nπ, a
Stąd
0
a
sin
3,....
2,
,
n
1
2
2
2
2
2
n
ma
E
Otrzymujemy więc poziomy
dyskret-ne jak w
odosobnionej studni poten-
cjału.
a
a
2
a
3
a
3
a
2
a
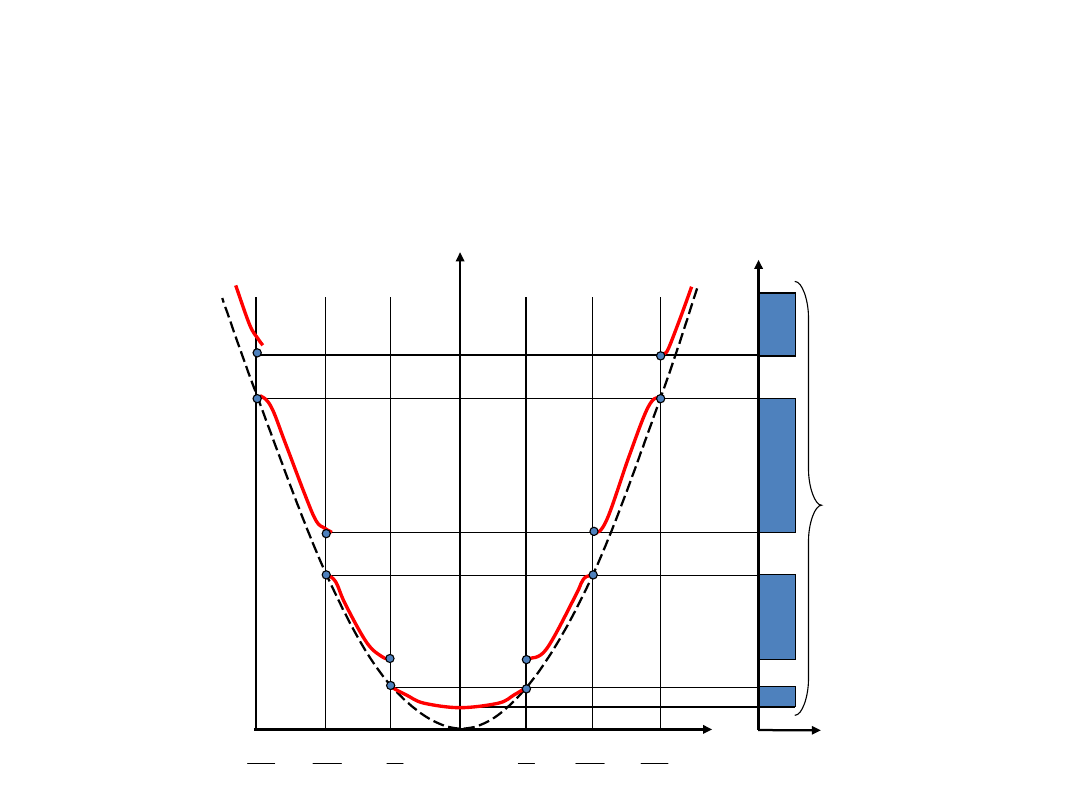
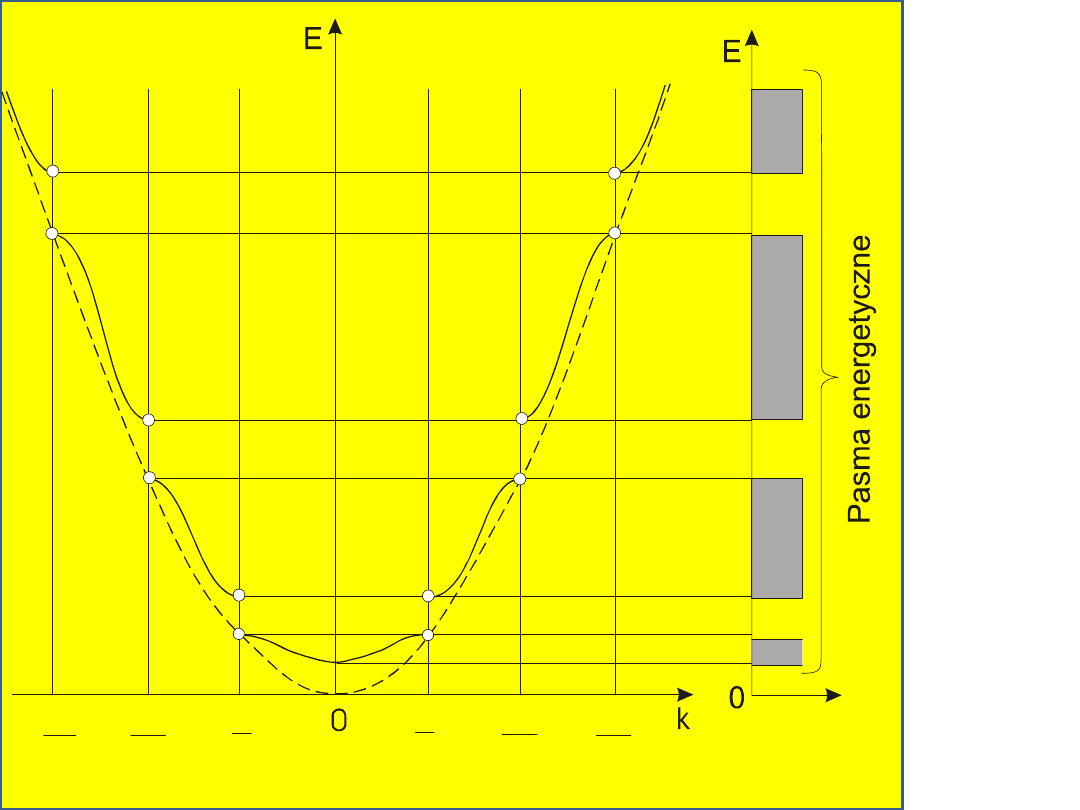
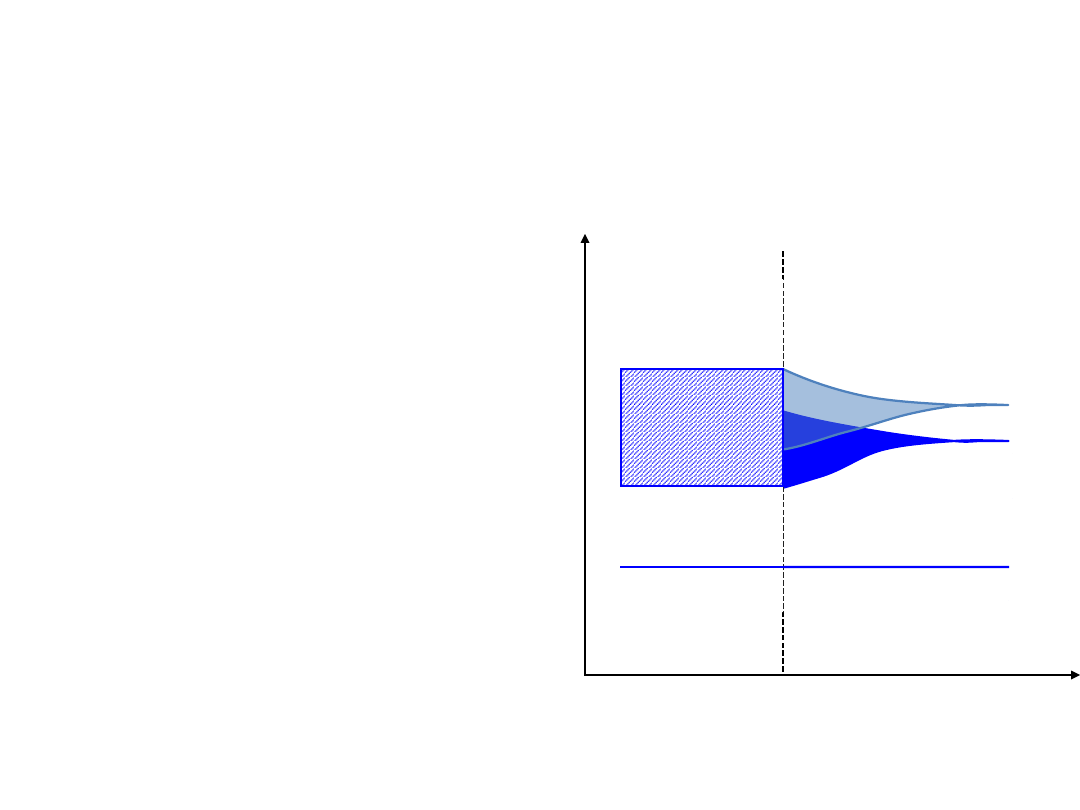
Zależność dyspersyjna
E(k)
E
E
k
0
0
a
a
2
a
3
a
a
2
a
3
p
a
sm
a
e
n
e
rg
e
ty
cz
n
e
Przybliżenie elektronów
silnie związanych
• jako punkt wyjścia przyjmujemy
funkcje falowe i zdegenerowane
poziomy energetyczne pojedyn-
czych atomów
• w wyniku zbliżania atomów
nastę-puje rozszczepienie
poziomów w pasma i
ewentualne przekrywanie
(zlewanie)
• szerokość pasma zależy od
prze-krywania odpowiednich
funkcji falowych
• głęboko leżące poziomy są
niezna-cznie poszerzone i
zachowują swój atomowy
charakter
odległość r
r
0
e
n
e
rg
ia
e
le
k
tr
o
n
u
E
1s
2s
2p
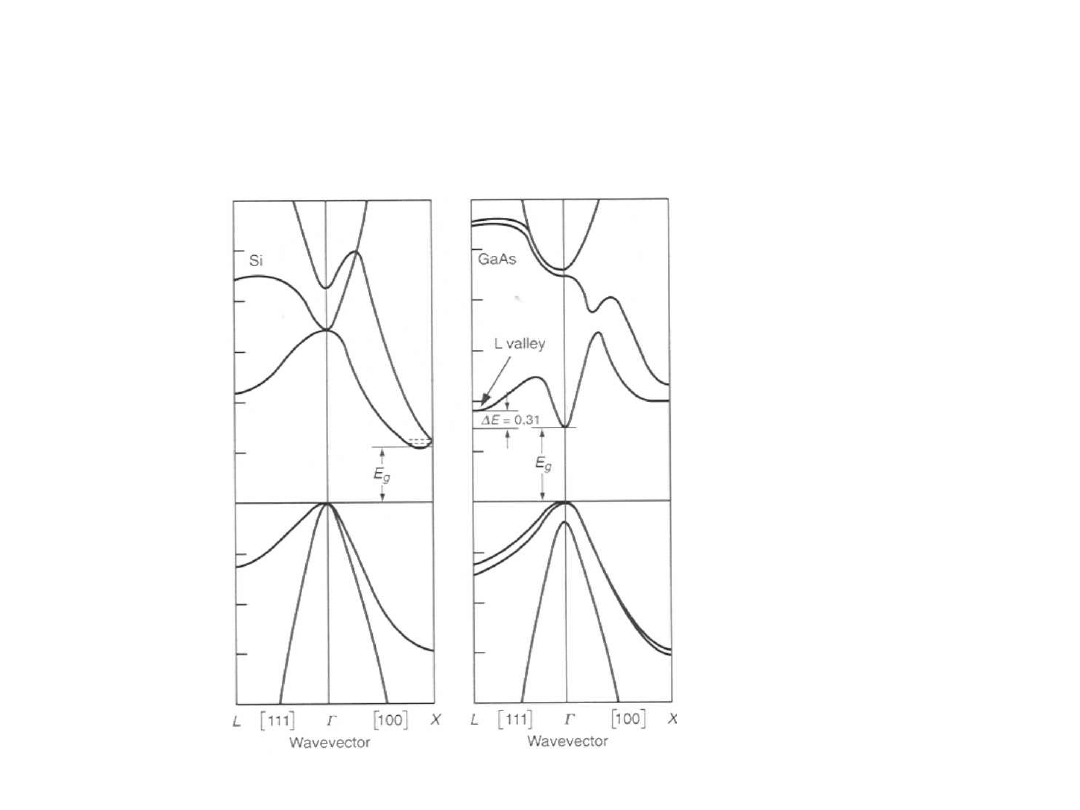
Kształt pasm Si i GaAs
Krzywe dyspersyjne

Zapełnianie pasm przez
elektrony
• izolatory i półprzewodniki - niższe pasma
całko-wicie zapełnione, wyższe poczynając
od pewne-go, całkowicie puste
• metale proste - nad całkowicie
zapełnionymi pasmami istnieje pasmo
zapełnione częściowo
• metale z pasmami nakładającymi się -
najwyższe całkowicie zapełnione pasmo,
zachodzi na poło-żone nad nim najniższe
pasmo puste, wtedy oba zapełniają się
częściowo
Pod względem charakteru zapełnienia pasm
przez elektrony możemy podzielić wszystkie
ciała na trzy grupy:
E
k
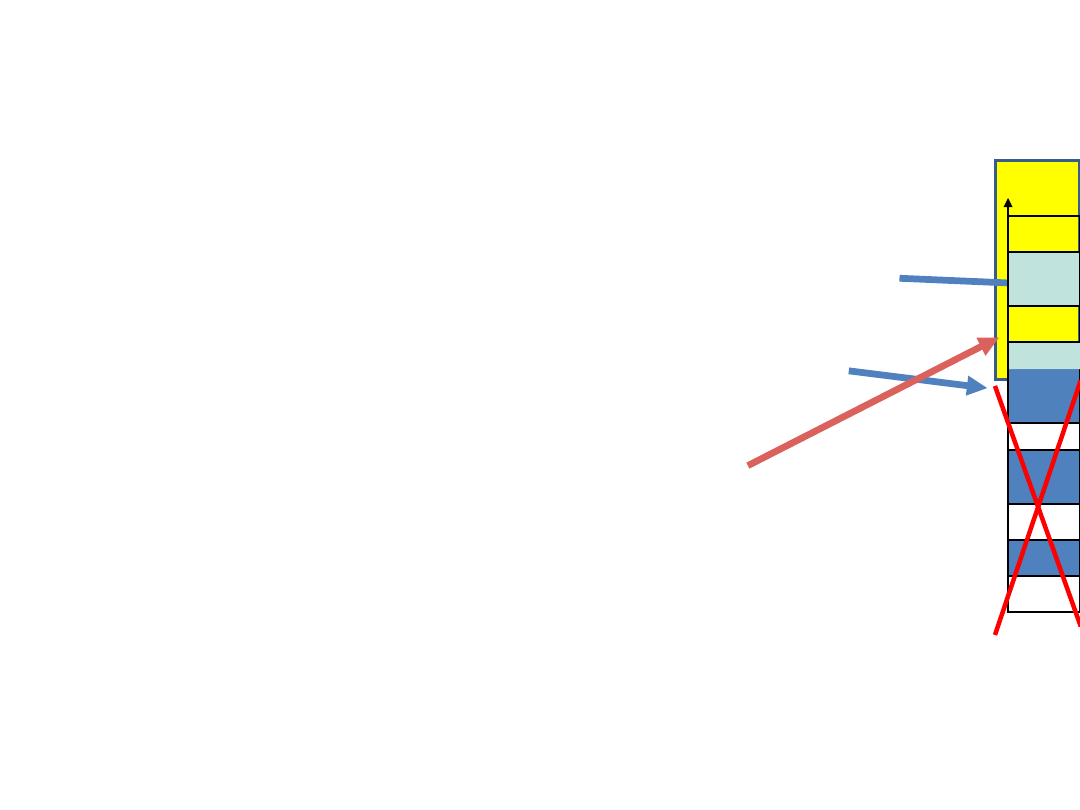
Podział ciał stałych
O własnościach fizycznych ciał stałych decydują:
• kształt i sposób obsadzenia elektronami dwóch
najważniej-szych pasm energetycznych
– pasma przewodnictwa - najniższego pasma nie
zapełnio-nego
– pasma podstawowego (walencyjnego) -
najwyższego pasma obsadzonego przez
elektrony
• odległość między tymi pasmami E
g
- zwana przerwą
energetyczną (pasmem zabronionym)
– izolatory E
g
> 3 eV - nie przewodzą prądu
– półprzewodniki E
g
< 3 eV, choć GaN ( 3,4eV)
diament (5,4eV)
– metale E
g
= 0 - pasma zachodzą na siebie
– ta sama substancja może mieć w pewnych warunkach
bądź właściwości półprzewodnikowe, bądź metaliczne
E
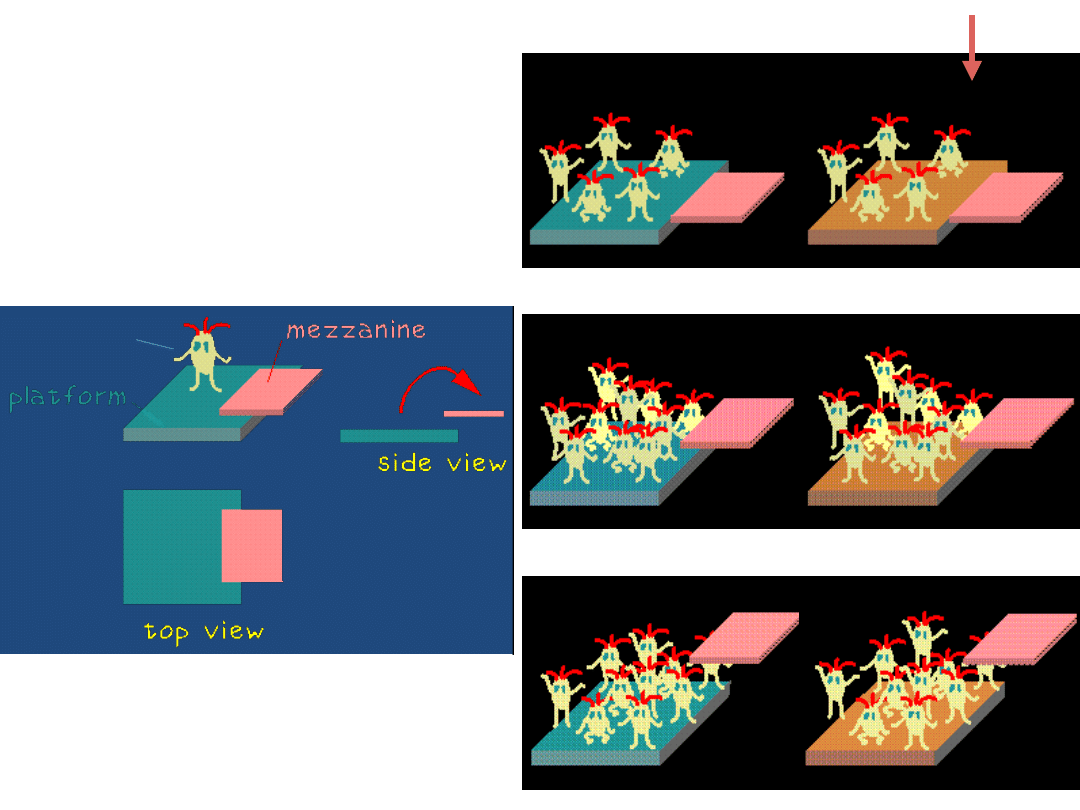
creature
przewodnik
półprzewodnik
izolator
Stworzenia próbują się
dostać
z platformy na antresolę.
W zależności od położenia
antresoli i temperatury
platformy wyróżniamy
trzy przypadki
grzanie
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
Wyszukiwarka
Podobne podstrony:
Fizyka 1d struktura energetyczna ciał stałych S1E
7 Dyfrakcyjne metody badania struktury ciał stałych
Ćw 7 'Dyfrakcyjne Metody?dania Struktury Ciał Stałych' Strona Tytułowa
Ćw 7 'Dyfrakcyjne Metody?dania Struktury Ciał Stałych' Obliczenia
Ćw 7 'Dyfrakcyjne Metody?dania Struktury Ciał Stałych' Wykresy
3 budowa cial stalych
12 Wyznaczanie współczynnika przewodnictwa cieplnego ciał stałych metodą Christiansena
Fizyka laboratorium 4?danie ciepła właściwego cieczy i ciał stałych
Mechanika Ciał Stałych opracowanie egzamin
4 Reakcje w układach ciało stałe gaz, korozja gazowa ciał stałych
1 Charakterystyka cial stalych
kk6 Właściwości elektryczne ciał stałych
więcej podobnych podstron