
SMOG
=
SMO
KE + F
OG
Smog – utrzymujące się nad terenami wielkich miast i centrów
przemysłowych zanieczyszczenia atmosferyczne zawierające:
- składniki pierwotne (pyły, gazy),
- produkty fotochemicznych i chemicznych przemian
składników pierwotnych
Smog tworzy się w warunkach inwersji temperatury przy słabej
wymianie powietrza (brak wiatru lub niska prędkość wiatru).
Pierwsze obserwacje smogu – 1930 (dolina Mozy, Belgia)
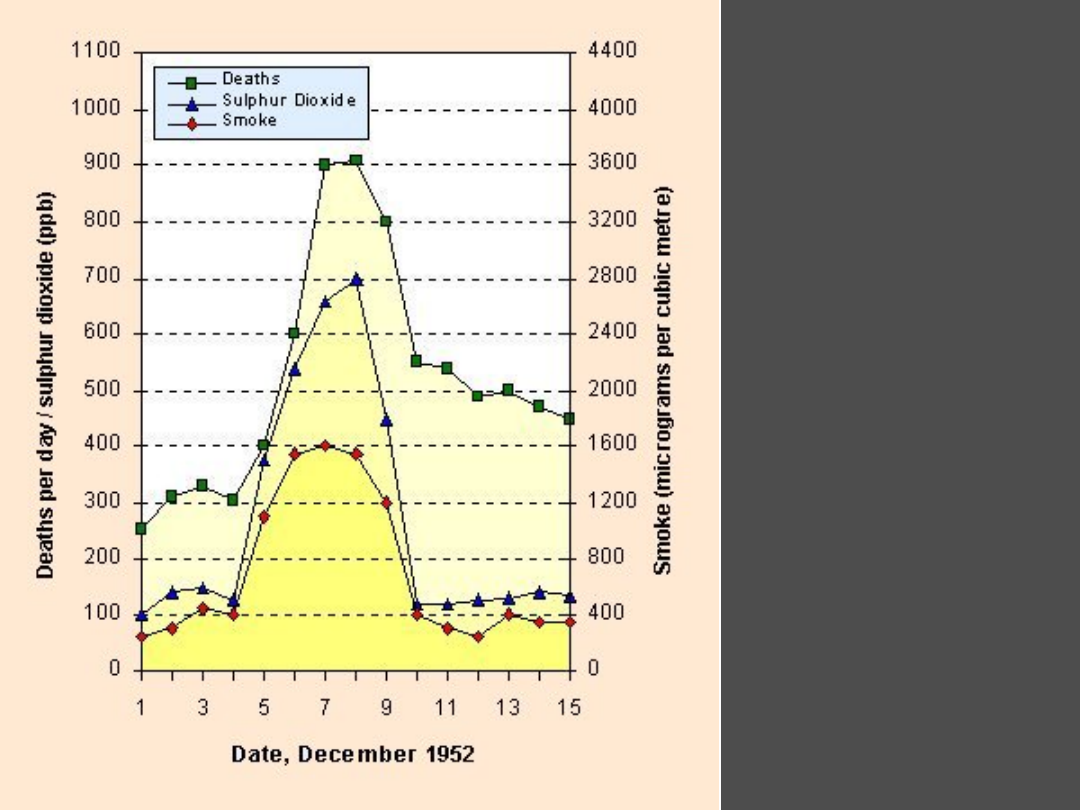
Ponad 4000 zgonów
wiąże się ze smogiem
w Londynie w grudniu
1952. Według niektó-
rych ocen liczba
przedwczesnych zgonów
w okresie od grudnia
1952 do lutego 1953
wyniosła 12000 osób.
Wykres z:
gov.uk/education/
historic/smog.html

SMOG LONDYŃSKI (SIARCZANOWY)
POWSTAJE GŁÓWNIE PRZY SPALANIU WĘGLA
(PRODUKCJA ENERGII I CIEPŁA W DUŻYCH MIASTACH)
SMOG SIARCZANOWY NAJCZĘŚCIEJ POWSTAJE W OKRESACH
ZIMOWYCH I NOCĄ
W WIELU KRAJACH ZNACZENIE SMOGU TEGO TYPU
JEST OBECNIE ZNACZNIE ZREDUKOWANE

Mechanizm powstawania smogu londyńskiego (siarczanowego)
Przy spalaniu węgla powstaje CO
2
– C(s) + O
2
(g) CO
2
(g)
Gdy ograniczony jest dopływ tlenu powstaje CO
– 2C(s) + O
2
(g) 2CO(g)
– (CO jest silnie toksyczny; blokuje transport O
2
we krwi)
Gdy dopływ tlenu jest jeszcze bardziej ograniczony można otrzymać
węgiel, tzn. sadzę
Przy spalaniu węgla powstaje też SO
2
(udział pirytu, innych siarczków, siarczanów)
– S(s) + O
2
(g) SO
2
(g)
SO
2
reaguje z tlenem ==> SO
3
– 2SO
2
(g) + O
2
(g) 2SO
3
(g)
– SO
3
reaguje z wodą ==> kwas siarkowy
Smog londyński zawiera też niespalone cząstki węgla (sadze)
pH aerozolu w Londynie podczas wielkiego smogu (1952)
wynosiło 1.6

Zawartość siarki w paliwach (z: Andrews i in., 2000)
Paliwo
Zawartość siarki (% wag.)
Węgiel
0.2 – 7.0
Paliwa płynne
0.5 – 4.0
Koks
1.5 – 2.5
Paliwo Diesla
0.3 – 0.9
Ropa naftowa
0.1
Nafta
0.2
Drewna
znikoma
Gaz ziemny
znikoma

Alarm smogowy w Duisburgu, 1985
(z: http://www.deutsches-museum.de/ausstell/dauer/umwelt/)

Nowy Jork przed i w trakcie smogu fotochemicznego
(fotografie z: http://hk.geocities.com)

Smog fotochemiczny
nad Los Angeles,
maj 1972
(fot. Gene Daniels;
z:
/history/photos/p06.htm
Stężenia ozonu
powyżej 600 g/m
3
z: http://www.gios.gov.pl/
raport/1web/index.html

Smog fotochemiczny w Los Angeles, maj 1972
Z: Pickering & Owen, 1995

Smog nad Atenami
(z: http://www.fdl.uea.ac.uk/airpol/modules/typology.asp)

SMOG LOS ANGELES (SMOG FOTOCHEMICZNY)
NAJCZĘSTSZY WE WSPÓŁCZESNYCH DUŻYCH MIASTACH
PIERWOTNYM ŹRÓDŁEM SĄ SPALINY SAMOCHODOWE I/LUB
PRODUKTY SPALANIA PALIW PŁYNNYCH (NO, WĘGLOWODORY)
Istotna jest wysoka koncentracja fotoutleniaczy
(np. ozon, tlenki azotu) w atmosferze.
Smog fotochemiczny określany jest również
terminem
smogu letniego.
W Europie najwyższe stężenia średnie godzinne
ozonu - do 520 g/m
3
notowane były na Wyspach
Brytyjskich, a w Ameryce Północnej - w Kalifornii,
gdzie przekraczały poziom 660 g/m
3
.

Mechanizm powstawania smogu typu Los Angeles
(fotochemicznego)
Azot i tlen w silniku samochodowym reagują tworząc NO
W wysokiej temperaturze płomienia molekuły składników powietrza
mogą ulec rozbiciu i stosunkowo bierna cząsteczka N
2
wchodzi
w reakcję
- O(g) + N
2
(g) NO(g) + N(g)
- N(g) + O2(g) NO(g) + O(g); czyli w sumie:
– N
2
(g) + O
2
(g) 2NO(g)
NO powoli reaguje tworząc NO
2
(brązowy gaz)
– 2NO(g) + O
2
(g) 2NO
2
(g)
Brązowy gaz jest substancją absorbującą światło, aktywną pod
względem fotochemicznym i ulegającą dysocjacji

Mechanizm powstawania smogu typu Los Angeles
(fotochemicznego)
Podczas słonecznego dnia w wyniku reakcji fotochemicznej
powstaje O
– NO
2
(g) + h NO(g) + O
Rodnik ten jest silnie reaktywny
– O + O
2
(g) O
3
(g) (ozon)
Ozon nie jest emitowany – jest zanieczyszczeniem wtórnym

Mechanizm powstawania smogu typu Los Angeles
(fotochemicznego)
Rodniki tlenowe mogą reagować z niespalonymi węglowodorami
emitowanymi z silników samochodowych
– O + C
n
H
m
aldehydy
Np.:
CH
4
(g) + 2O
2
(g) + 2NO(g) H
2
O(g) + HCHO(g) + 2NO
2
(g)
aldehyd mrówkowy
Ozon może reagować z NO
2
i węglowodorami
O
3
+ C
n
H
m
+ NO
2
PAN (peroxyacetylnitrate - azotan nadtlenku
acetylu [azotan nadtlenooctowy]– substancja silnie drażniąca)
h

ZWALCZANIE SMOGU FOTOCHEMICZNEGO
Stosowanie katalizatorów w silnikach samochodowych
- eliminacja CO i węglowodorów (~1971)
- eliminacja CO, węglowodorów, NO, NO
2
(~1981)

Stężenia ozonu zmieniają się cyklicznie
w okresie doby, tygodnia i roku.
Na ich poziom największy wpływ mają
warunki meteorologiczne (zwłaszcza
natężenie promieniowania słonecznego i
temperatura powietrza) oraz zmiany
natężenia emisji i stężeń tlenków azotu i
węglowodorów, zależne przede wszystkim od
intensywności ruchu pojazdów.
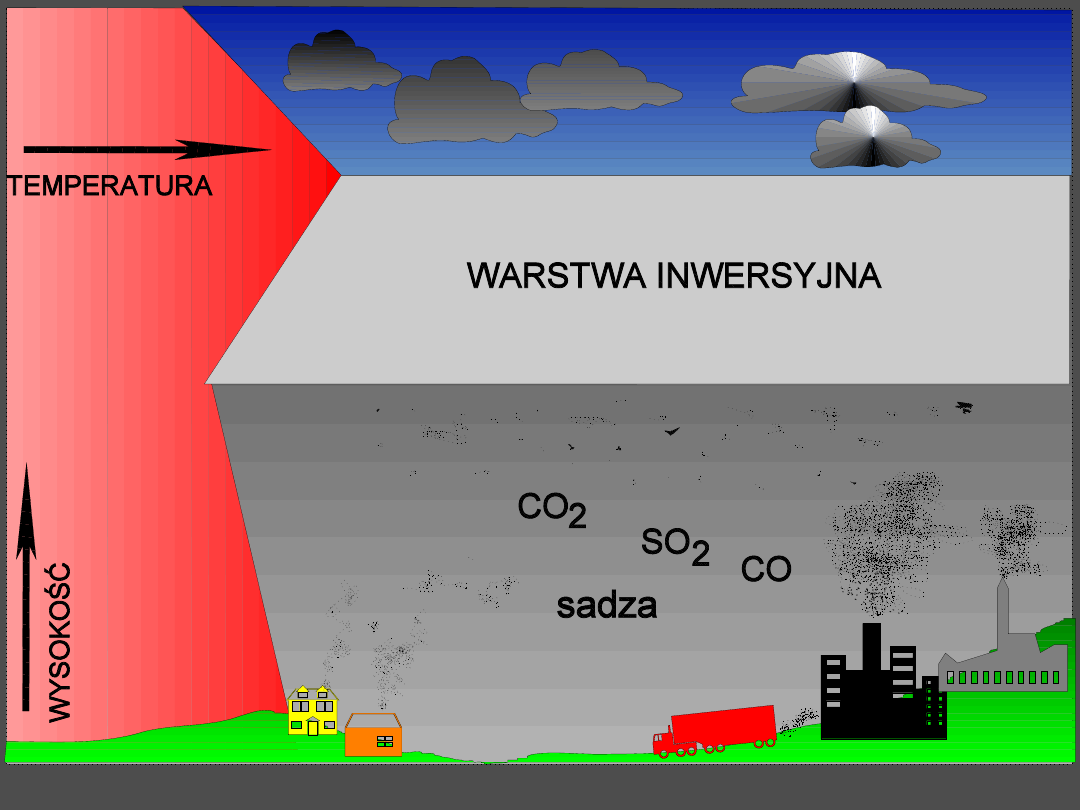
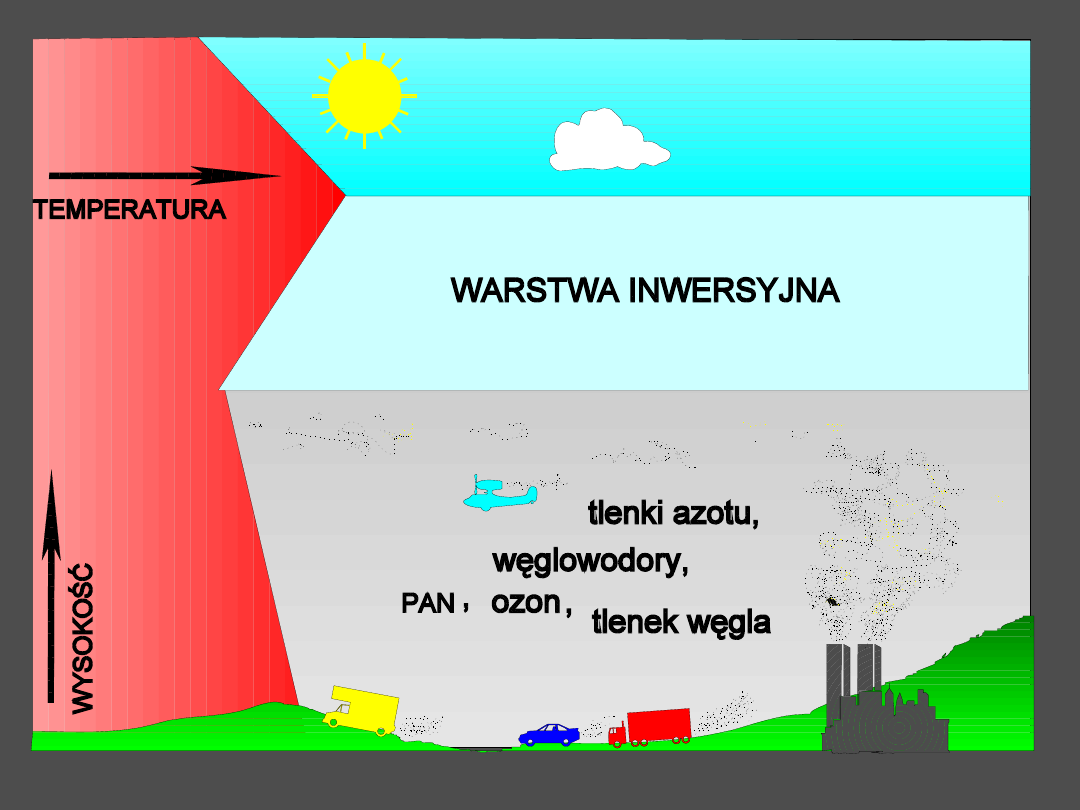

Porównanie smogu w Los Angeles i w Londynie
(z: Andrews i in., 2000)
Cecha
Los Angeles
Londyn
Temperatura powietrza
24-32
o
C
-1 - +4
o
C
Wilgotność względna
<70%
85% (+mgła)
Prędkość wiatru
<3 ms
-1
cisza
Widzialność
<0.8-1.6 km
<30m
Miesiąc najczęstszego
sierpień-
grudzień-
występowania
wrzesień
styczeń
Główne paliwa
ropa naftowa
węgiel i produkty
przerobu ropy
Główne składniki
O
3
, NO, NO
2
, CO
cząstki stałe, CO,
związki S
Rodzaj reakcji chemicznej
utlenianie
redukcja
Pora największego nasilenia południe
wczesny ranek
Wpływ na zdrowie
podrażnienie oczu
podrażnienie
oskrzeli, kaszel
Najważniejsze obserwowane
objawy
PAN
SO
2
/dym
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
Wyszukiwarka
Podobne podstrony:
Oswojony smog przyjazny telefon komórkowy
Smog i, Biologia UŚ !, Ochrona środowiska
smog fotochemiczny
smog, Milena Duk, Maria Matulewicz, Anna Mazurek gr 1 OŚ
Smog typu 1
SMOG gazetka
WYKLAD Skutki zan powietrza i smog 11
smog
Smog in ChinaStudent
Smog moja prezentacja
Smog informacyjny prezentacja
Smog elektromagnetyczny w naszych mieszkaniach, PROMIENIOWANIE ELEKTROMAGNETYCZNE PEM
Smog, Dokumenty(1)
RT smog[1], MARKETING INTERNETOWY
Kwaśne deszcze i smog
więcej podobnych podstron



