
Leczenie przewlekłego
Leczenie przewlekłego
zakażenia HCV
zakażenia HCV
w świetle nowych standardów
w świetle nowych standardów
Waldemar Halota
Waldemar Halota
Katedra i Klinika Chorób Zakaźnych i
Katedra i Klinika Chorób Zakaźnych i
Hepatologii
Hepatologii
Collegium Medicum im. L.Rydygiera w
Collegium Medicum im. L.Rydygiera w
Bydgoszczy
Bydgoszczy
Uniwersytet Mikołaja Kopernika w Toruniu
Uniwersytet Mikołaja Kopernika w Toruniu
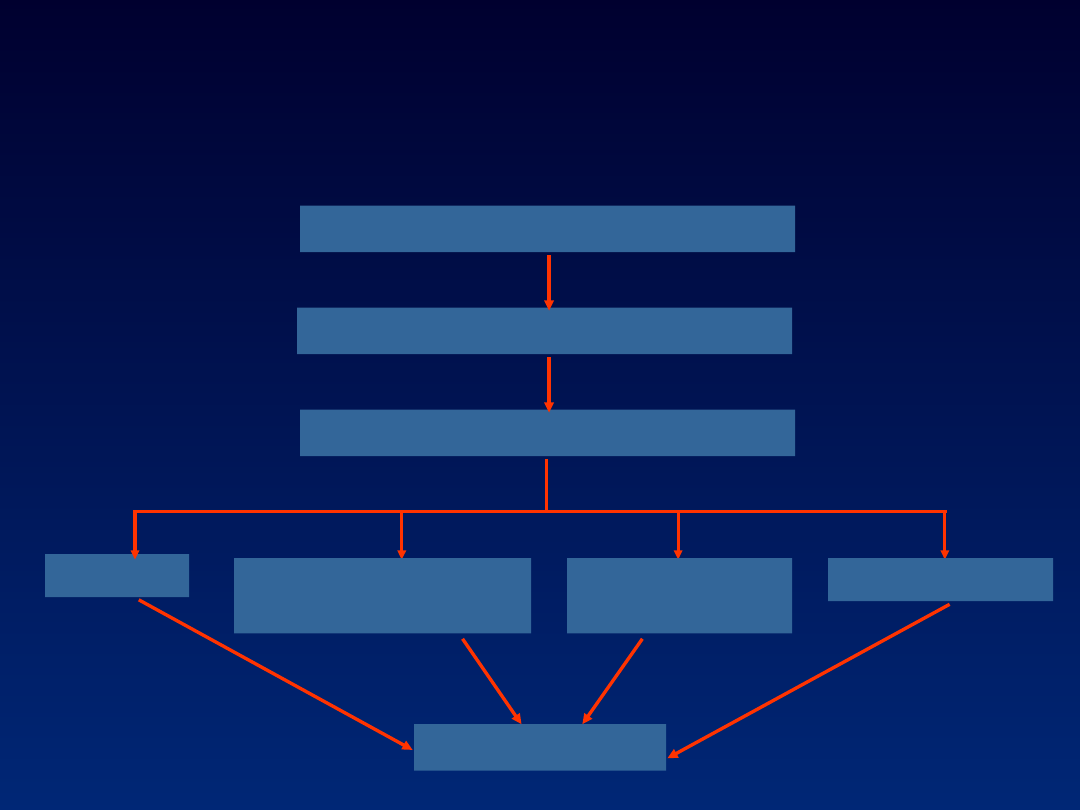
HCV - „cicha epidemia”
Buti i wsp. J.Hepatol. 2000
HCC
HCC
ostre zakażenie C
ostre zakażenie C
zgon
zgon
pzw C
pzw C
marskość wątroby
marskość wątroby
krwotok z
krwotok z
żylaków przełyku
żylaków przełyku
encefalopati
encefalopati
a wątrobowa
a wątrobowa
wodobrzusze
wodobrzusze
~ 80%
20% 20 lat
1,1% /r
0,4% /r
86% /r
40% /r
68% /r
11% /r
1,5% /r
2,5% /r
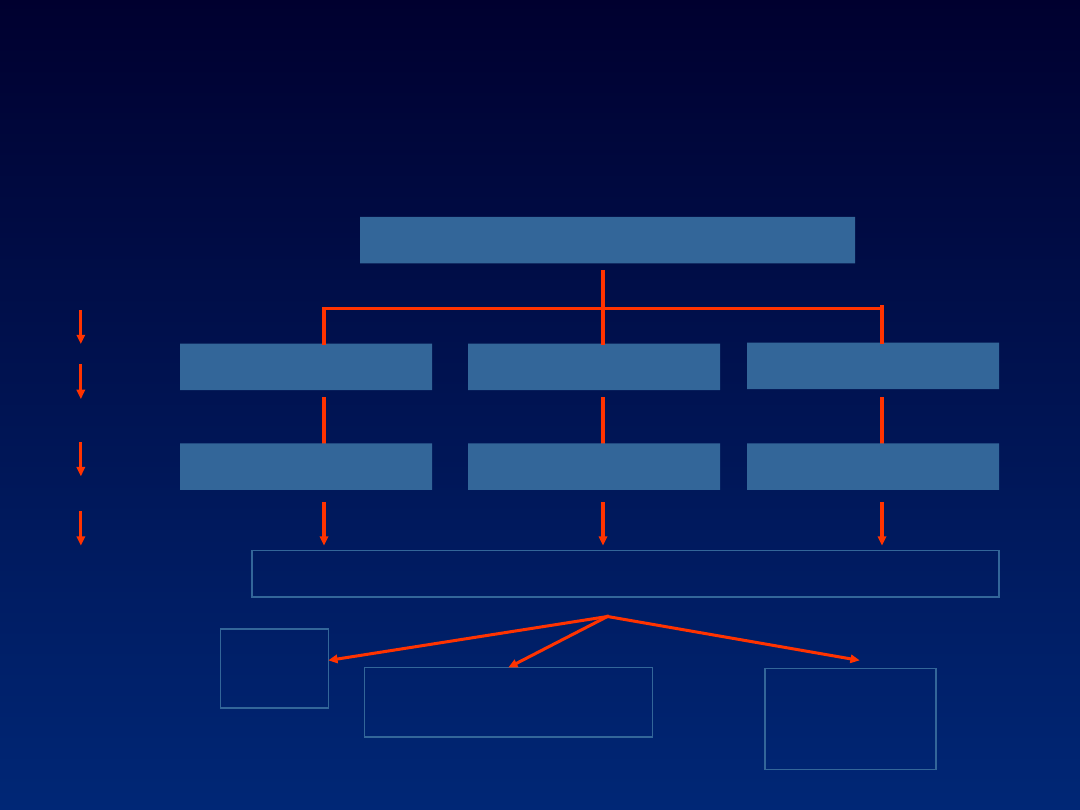
Modele progresji
choroby
Alberti, London 1998
szybka
szybka
Progresja
Progresja
marskość
marskość
5-10 lat
5-10 lat
15-30 lat
15-30 lat
> 30 lat
> 30 lat
wolna
wolna
pośrednia
pośrednia
HCC
HCC
3% /r
3% /r
niewyrównanie
niewyrównanie
5% - 10% /r
5% - 10% /r
zgon
zgon
2% -
2% -
5% /r
5% /r
włóknienie
włóknienie
0
0
1
1
2
2
3
3
4
4

Cele terapii przeciwwirusowej
•
eradykacja wirusa
eradykacja wirusa
•
zmniejszenie aktywności zakażenia
zmniejszenie aktywności zakażenia
•
zahamowanie lub spowolnienie włóknienia
zahamowanie lub spowolnienie włóknienia
•
zapobieganie nieprawidłowej proliferacji
zapobieganie nieprawidłowej proliferacji
hepatocytów
hepatocytów

•
„
„
ostre” wzw C
ostre” wzw C
•
HCV-RNA(+) / morfologia wątroby /
HCV-RNA(+) / morfologia wątroby /
genotyp
genotyp
•
pozawątrobowe manifestacje zakażenia
pozawątrobowe manifestacje zakażenia
HCV
HCV
•
wyrównana marskość wątroby
wyrównana marskość wątroby
•
koinfekcja HCV/HBV
koinfekcja HCV/HBV
•
koinfekcja HCV/HIV
koinfekcja HCV/HIV
•
hemodializowani
hemodializowani
•
oczekujący na przeszczepienie
oczekujący na przeszczepienie
Motywowane oczekiwanie pacjenta
Motywowane oczekiwanie pacjenta
Kryteria kwalifikacji do leczenia
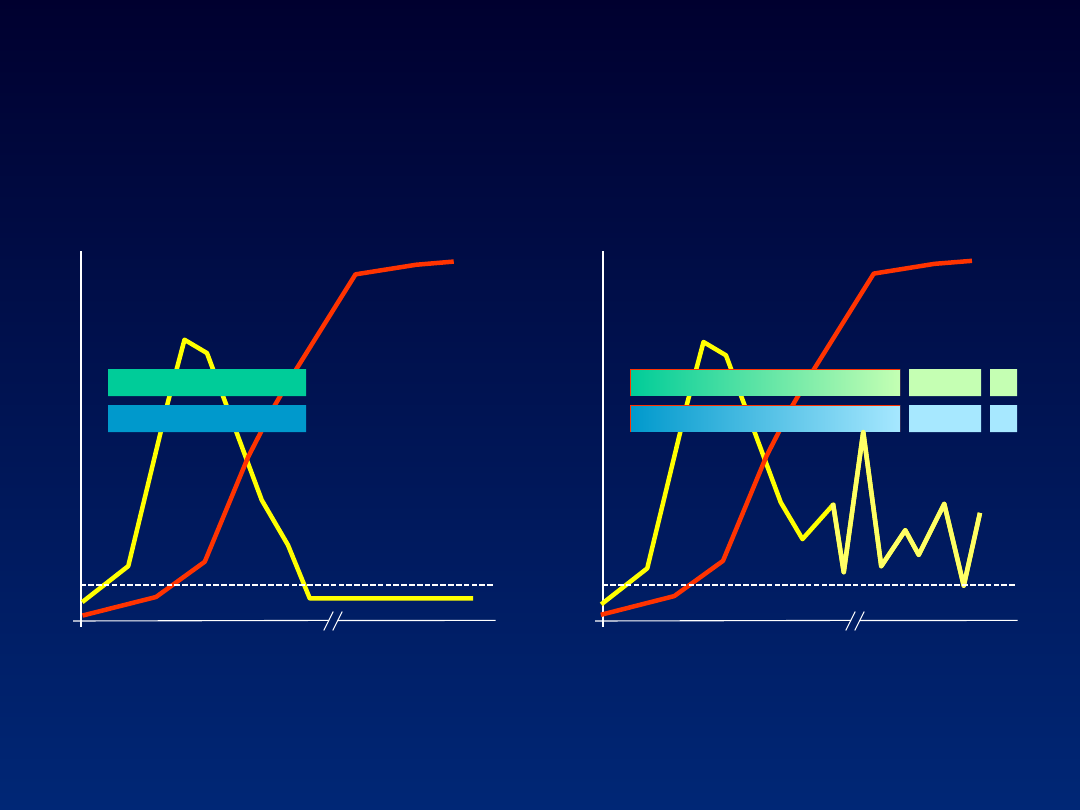
Zakażenie HCV
Mondelli M.U.: J.Hepatol.
2005
SAMOOGRANICZAJĄCE SIĘ
PRZEWLEKŁE
0 1 2 3 4 5 6
1 2 3
4
Czas po
ekspozycji
Lat
a
Miesią
ce
C
za
s
anty-
HCV
AlA
T
objawy
+/-
HCV RNA
Core Ag
1 2 3
4
Czas po
ekspozycji
Lat
a
Miesią
ce
C
za
s
anty-
HCV
AlA
T
objawy
+/-
HCV RNA
Core Ag
0 1 2 3 4 5 6

Ostre wzw typu C
•
okres wylęgania
okres wylęgania
5-12 tygodni;średnio 8 tygodni
5-12 tygodni;średnio 8 tygodni
•
czas trwania
czas trwania
2-12 tygodni
2-12 tygodni
•
HCV RNA
HCV RNA
2-14 dni po ekspozycji
2-14 dni po ekspozycji
•
AlAT
AlAT
wkrótce potem
wkrótce potem
•
anty-HCV
anty-HCV
20-150 dni; średnio 60 dni
20-150 dni; średnio 60 dni
•
ustępowanie HCV RNA
ustępowanie HCV RNA
3-6 miesięcy po wzw (lub
3-6 miesięcy po wzw (lub
później)
później)
•
przewlekłość zakażenia
przewlekłość zakażenia
po 6 miesiącach
po 6 miesiącach
(?)
(?)
HCV RNA w teście TMA (5-10 IU) nie HCV core Ag !
HCV RNA w teście TMA (5-10 IU) nie HCV core Ag !

Ostre wzw typu C - leczenie
Ostre wzw typu C - leczenie
rozpoczęcie
rozpoczęcie
leczenia
leczenia
•
w
w
9.
9.
tyg. - gdy wiremia w 8 tyg. obserwacji >800.000
tyg. - gdy wiremia w 8 tyg. obserwacji >800.000
IU/ml
IU/ml
•
w
w
13.
13.
tyg. - gdy jest niższa i utrzymuje się do 12
tyg. - gdy jest niższa i utrzymuje się do 12
tygodnia choroby
tygodnia choroby
•
stosujemy monoterapię
stosujemy monoterapię
interferonami naturalnymi
interferonami naturalnymi
,
,
rekombinowanymi
rekombinowanymi
lub
lub
pegylowanymi
pegylowanymi
Interferony naturalne lub rekombinowane
Interferony naturalne lub rekombinowane
stosujemy
stosujemy
przez pierwsze cztery tygodnie codziennie, a
przez pierwsze cztery tygodnie codziennie, a
następnie przez 20 tygodni 3 razy w tyg.
następnie przez 20 tygodni 3 razy w tyg.
Interferony pegylowane
Interferony pegylowane
stosujemy przez 24 tygodnie,
stosujemy przez 24 tygodnie,
zgodnie z zaleceniami producenta.
zgodnie z zaleceniami producenta.

Przewlekle z
Przewlekle z
akażeni HCV -
kogo leczyć?
Seeff L.B.: Hepatology 2002
PREPARATIONS FOR LIVER
PREPARATIONS FOR LIVER
BIOPSY
BIOPSY
inva
sive
inva
sive
pro
ced
ur
pro
ced
ur
e
e
sam
plin
g
sam
plin
g
err
or
err
or
does
not
does
not
refe
ct
refe
ct
dyna
mic
dyna
mic
matr
ix
matr
ix
turno
ver
turno
ver
Pacjentów, którzy:
Pacjentów, którzy:
•
demonstrują objawy choroby
demonstrują objawy choroby
•
z podwyższonym ryzykiem
z podwyższonym ryzykiem
włóknienia
włóknienia
•
z zaawansowanym włóknieniem
z zaawansowanym włóknieniem
•
„
„
łatwych” do leczenia
łatwych” do leczenia
•
reterapia
reterapia
2002 NIH Consensus Conference:
2002 NIH Consensus Conference:
„
„
Każdy chory na przewlekłe zapalenie
Każdy chory na przewlekłe zapalenie
wątroby typu C jest potencjalnym
wątroby typu C jest potencjalnym
kandydatem do leczenia”
kandydatem do leczenia”
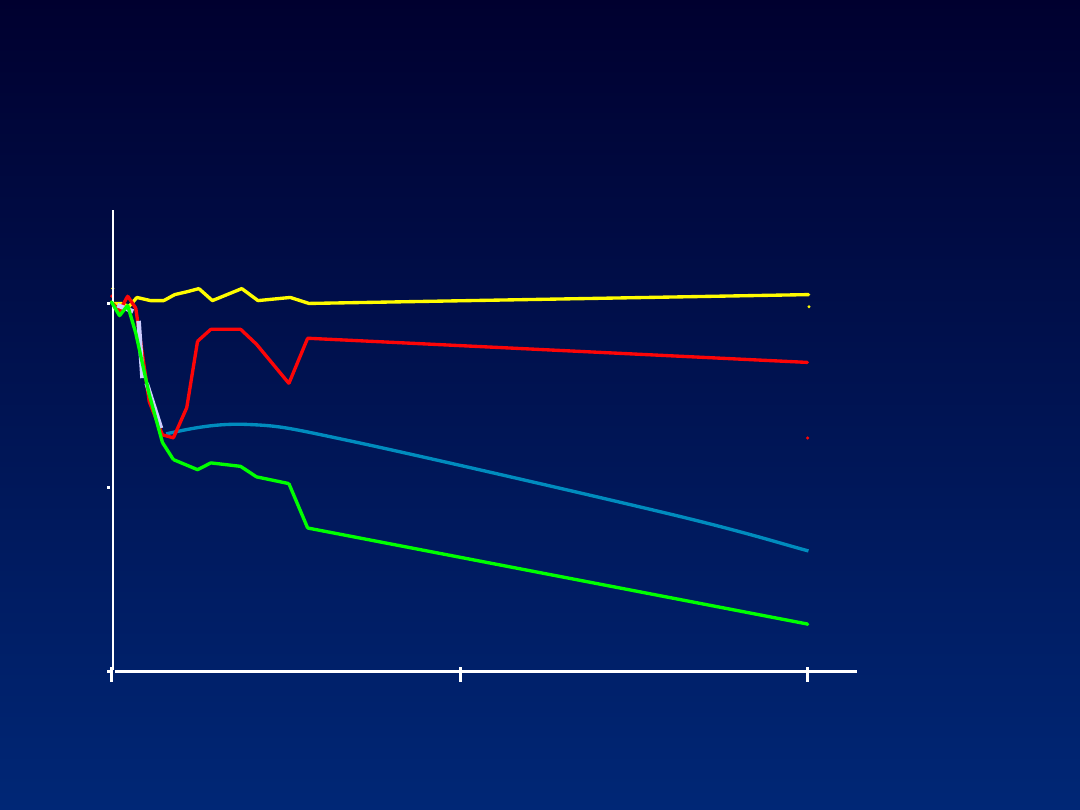
-2
0
d0
d7
d14
kontrola
kontrola
Dynamika HCV RNA
Pawlotsky JM, Neumann AU, et al., 2000 ; Zeuzem et al., 2000
IFN
IFN
PEG-IFN
PEG-IFN
+
+
rybawiryna
rybawiryna
IFN +
IFN +
r
r
y
y
ba
ba
w
w
ir
ir
y
y
n
n
a
a
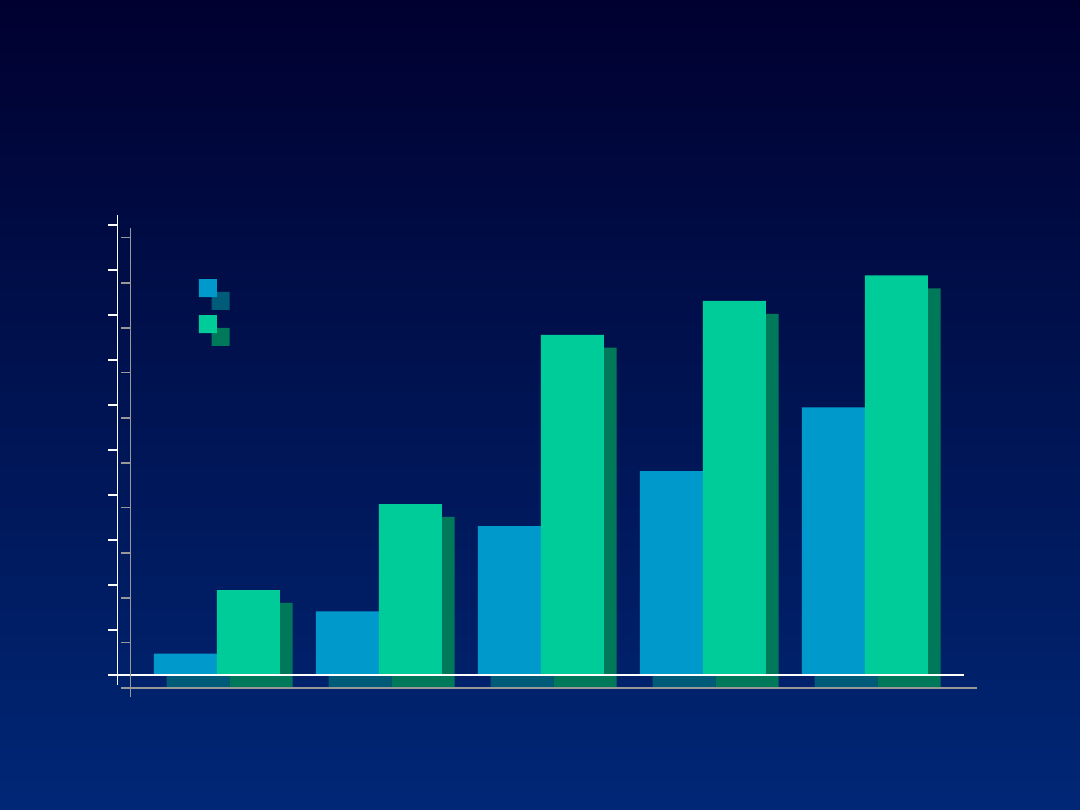
Poynard. Lancet 2003
5%
5%
5%
5%
20%
20%
20%
20%
15%
15%
15%
15%
40%
40%
40%
40%
35
35
%
%
35
35
%
%
80%
80%
80%
80%
48
48
%
%
48
48
%
%
88%
88%
88%
88%
63
63
%
%
63
63
%
%
94%
94%
94%
94%
0
0
0
0
10
10
10
10
20
20
20
20
30
30
30
30
40
40
40
40
50
50
50
50
60
60
60
60
70
70
70
70
80
80
80
80
90
90
90
90
10
10
0
0
10
10
0
0
IFN 24 tyg.
IFN 24 tyg.
IFN 24 tyg.
IFN 24 tyg.
IFN 48 tyg.
IFN 48 tyg.
IFN 48 tyg.
IFN 48 tyg.
IFN + R
IFN + R
IFN + R
IFN + R
PEG + R
PEG + R
PEG + R
PEG + R
PEG + R > 10,6
PEG + R > 10,6
adherencja
adherencja
PEG + R > 10,6
PEG + R > 10,6
adherencja
adherencja
genotyp 1, 4, 5, 6
genotyp 1, 4, 5, 6
genotyp 1, 4, 5, 6
genotyp 1, 4, 5, 6
genotyp 2, 3
genotyp 2, 3
genotyp 2, 3
genotyp 2, 3
Skuteczność leczenia (SVR) a
genotyp HCV

Wiremia HCV a odpowiedź na
leczenie
Pre-treatment HCV RNA
Pre-treatment HCV RNA
(IU/mL)
(IU/mL)
Estimated probability of
Estimated probability of
SVR
SVR
100,000
100,000
71%
71%
400,000
400,000
51%
51%
600,000
600,000
46%
46%
800,000
800,000
44%
44%
2,000,000
2,000,000
43%
43%
4,000,000
4,000,000
44%
44%
8,000,000
8,000,000
42%
42%

•
podstawą różnicowania LVL i HVL jest
podstawą różnicowania LVL i HVL jest
400.000 IU/mL (?)
400.000 IU/mL (?)
•
podział ten pozostaje w związku z SVR
podział ten pozostaje w związku z SVR
•
szansa osiągnięcia SVR koreluje z obniżaniem
szansa osiągnięcia SVR koreluje z obniżaniem
się HCV RNA
się HCV RNA
•
HVL jest niekorzystnym prognostykiem terapii
HVL jest niekorzystnym prognostykiem terapii
Wiremia HCV a skuteczność
leczenia
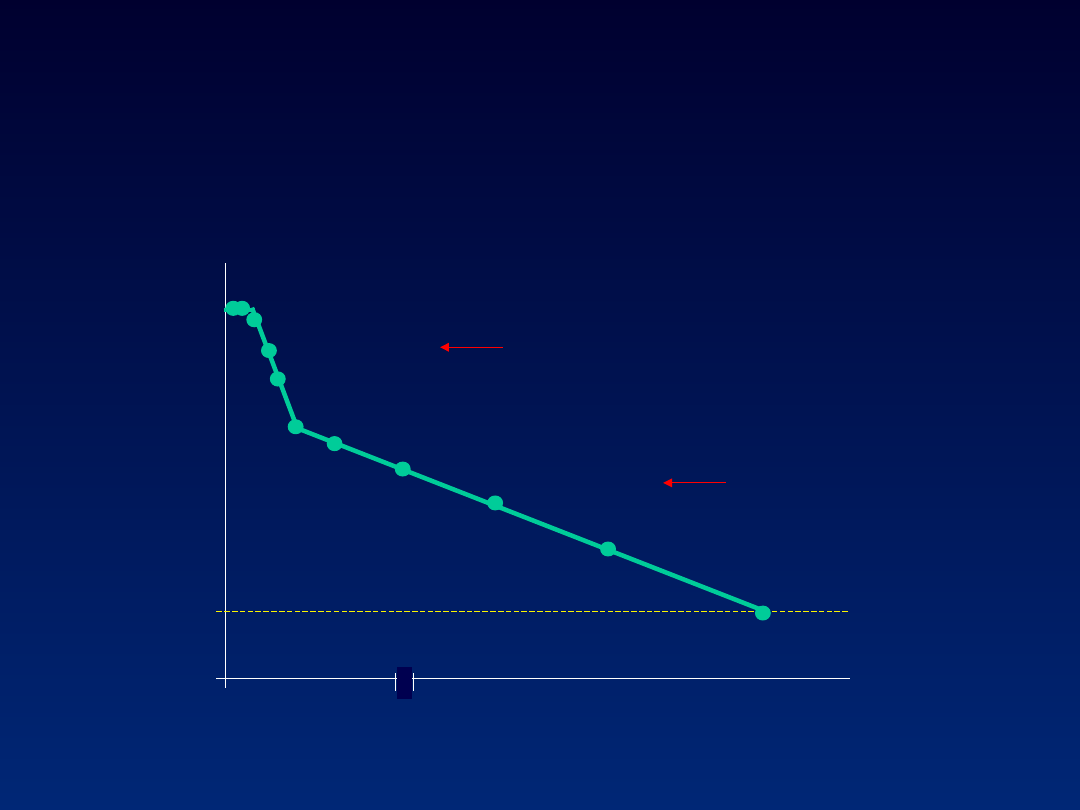
0 1 2 3 7 14
T(n)
dni
7
6
5
4
3
2
1
Neumann i wsp., Science 1998
Neumann i wsp., Science 1998
Ładune
k
wirusa
log
IU/ml)
Cutof
faza I
faza
II
•
zależna od dawki interferonu
•
zależna od genotypu (szybsza
2,3 HCV)
•
wolniejsza
•
mało zależna od
dawki
Kinetyka wiremii HCV
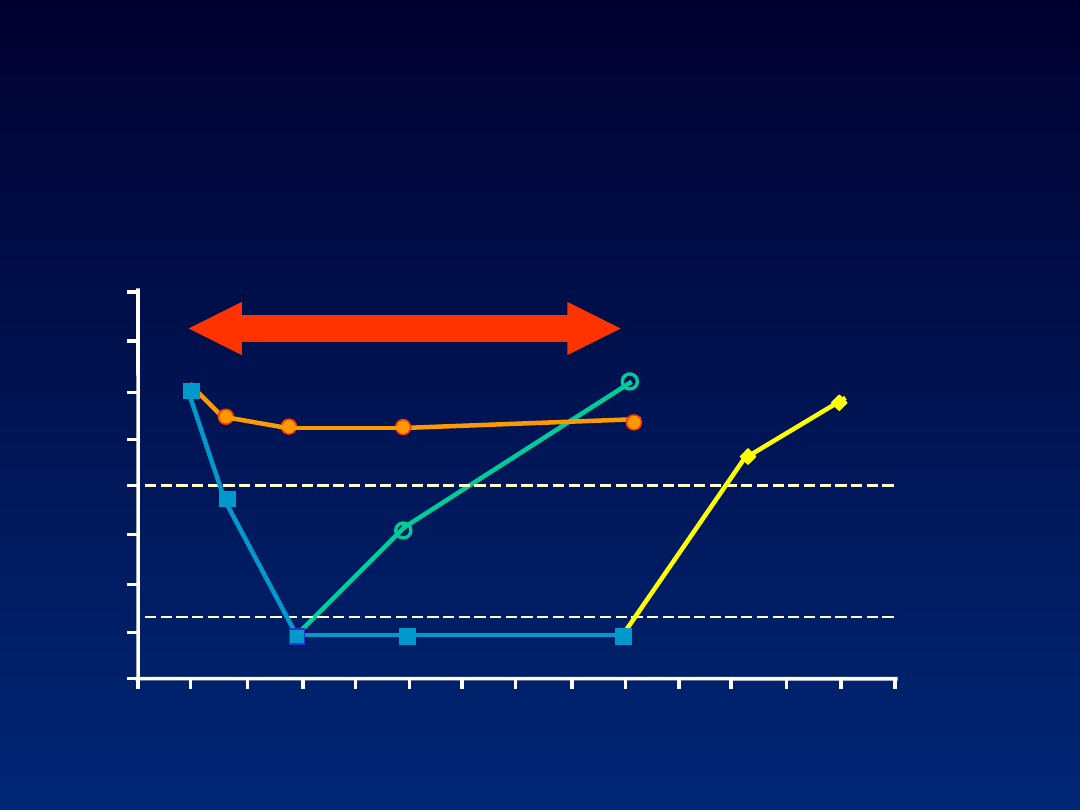
0
1
2
3
4
5
6
7
8
-6 0
6 12 18 24 30 36 42 48 54 60 66 72 78
Weeks
H
C
V
R
N
A
(
lo
g
I
U
/m
L
)
2 log decline
Limit of
detection
PegIFN/RBV
Relapse
Breakthrough
Nonresponse
Brak odpowiedzi, przełom i
nawrót
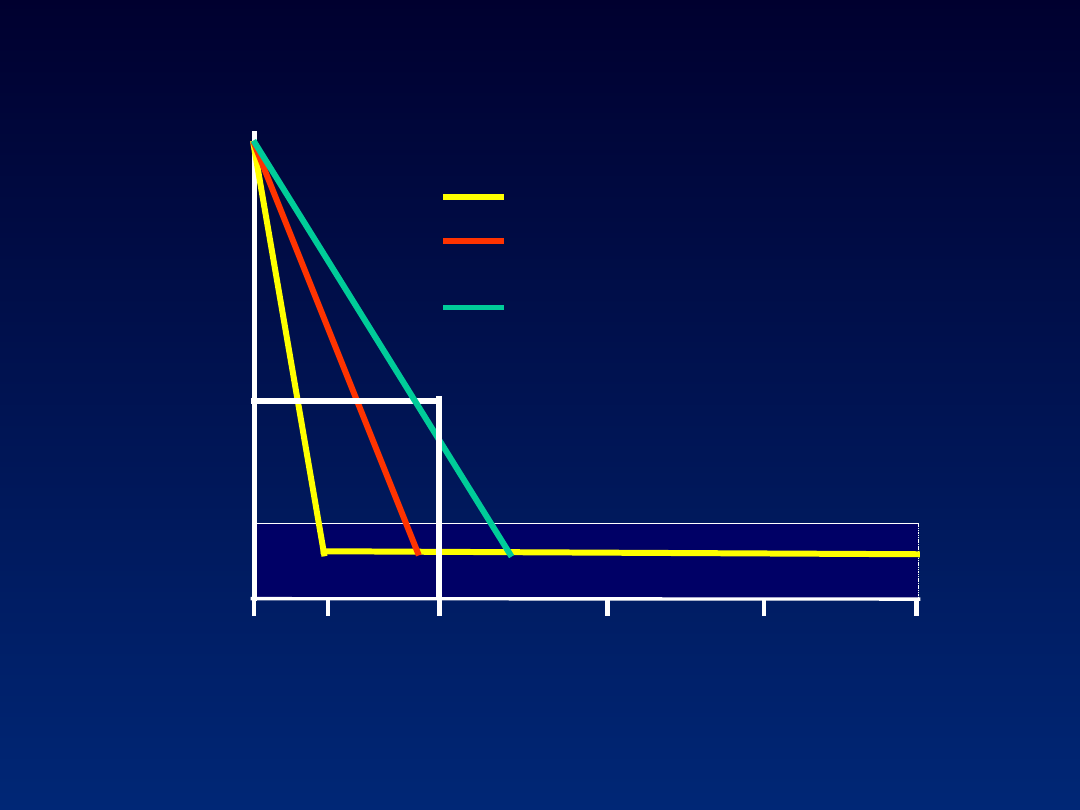
Definicje
H
C
V
R
N
A
d
e
c
re
a
se
(
IU
/m
L
)
ETR
SVR
72
4
48
Weeks of
therapy
0
12
Undetectab
le HCV RNA
(<50
IU/mL)
0
RVR = undetectable HCV RNA at
week 4
cEVR = no RVR but undetectable
HCV RNA at week 12
>2 log
10
pEVR = no RVR and detectable HCV
RNA, but >2 log
10
drop at week 12
24
RVR = rapid virological response; cEVR = complete early virological
response;
pEVR = partial early virological response; ETR = end of treatment
response
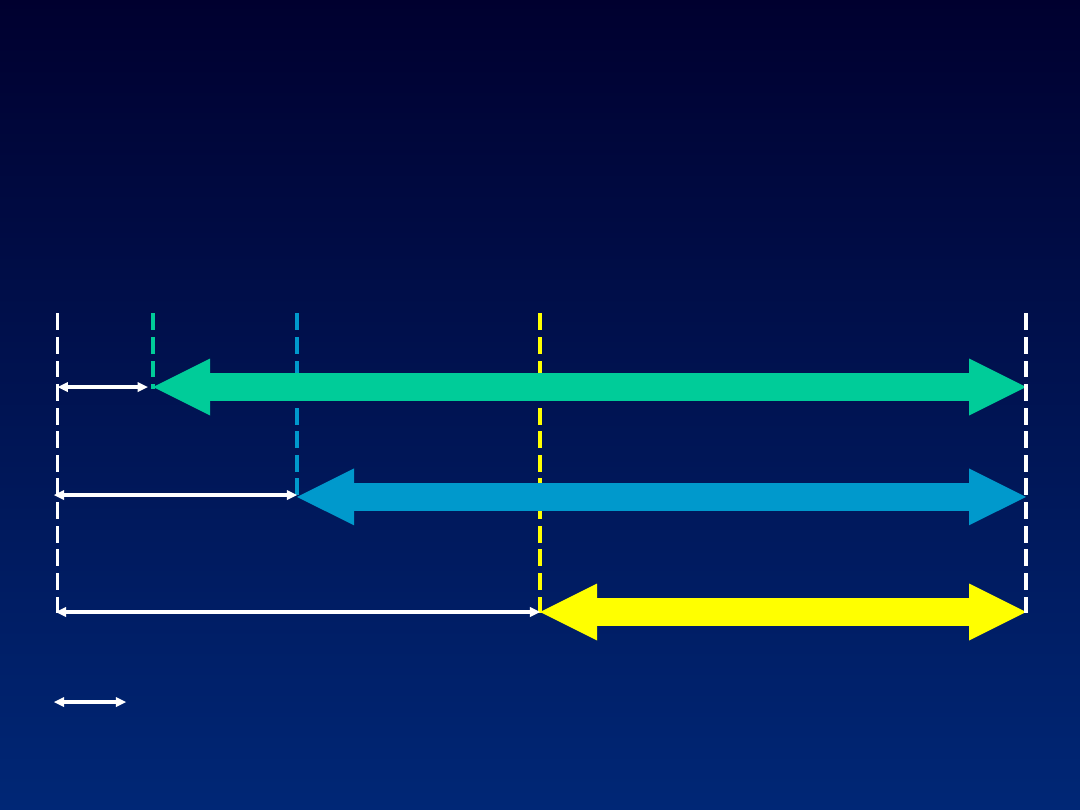
Wk 4
Wk 0
Wk 12
Wk 24
Wk 48 (EOT)
HCV RNA undetectable for 44 weeks
HCV RNA undetectable for 36 weeks
HCV RNA undetectable for 24 weeks
Time to HCV RNA negativity
Negatywizacja wiremii a SVR
Modified from figure by Michael Fried, MD.
Prognozowanie odpowiedzi
terapeutycznej
•
wśród różnych czynników najważniejszy jest
wśród różnych czynników najważniejszy jest
genotyp i wyjściowy ładunek HCV
genotyp i wyjściowy ładunek HCV
•
zachowanie się wiremii HCV w 4 i 12 tygodniu
zachowanie się wiremii HCV w 4 i 12 tygodniu
podstawowym elementem indywidualizacji
podstawowym elementem indywidualizacji
terapii
terapii
(RVR, cEVR, pEVR)
(RVR, cEVR, pEVR)
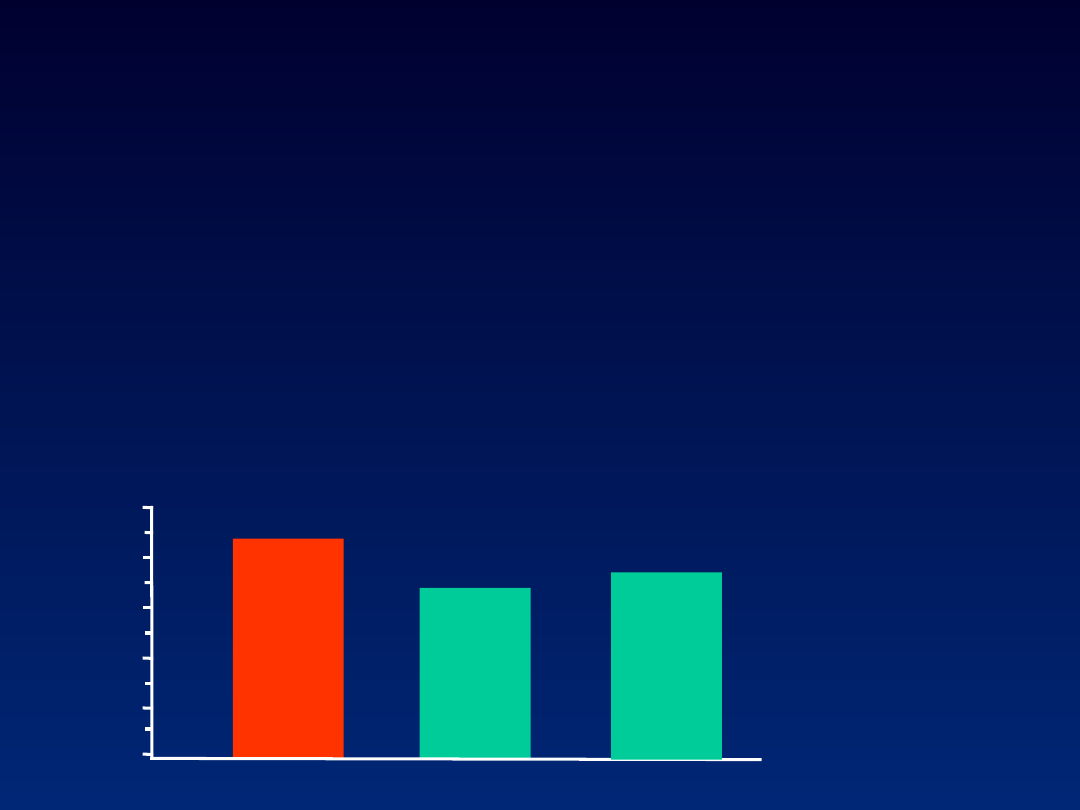
n=
79/90
156/236
66%
88%
RVR
S
V
R
(
%
)
0
20
40
60
80
100
cEVR
10
30
50
70
90
72%
RVR or cEVR
235/326
48 weeks’ PEGASYS 180 g/wk + COPEGUS
1000–1200
mg/day, G1
Data from 2 studies, n=569
Marcellin P
Marcellin P
, et al.
, et al.
APASL
APASL
200
200
7
7
;
;
Abstract
Abstract
453
453

Czas leczenia
Czas leczenia
•
zakażenie genotypem 1, 4, 5, 6
zakażenie genotypem 1, 4, 5, 6
48 tyg.
48 tyg.
niska wiremia + RVR
niska wiremia + RVR
24 tyg.
24 tyg.
pEVR i negatywizacja w 24 tyg.
pEVR i negatywizacja w 24 tyg.
72 tyg
72 tyg
•
zakażenie genotypem 2, 3
zakażenie genotypem 2, 3
24 tyg.
24 tyg.
pegylowany interferon alfa + rybawiryna
pegylowany interferon alfa + rybawiryna
Standard
POLSKA
POLSKA
1b
1b
~
~
75%
75%
1a
1a
~
~
5%
5%
3a
3a
~
~
17%
17%
4c+d
4c+d
< 1%
< 1%

Dawkowanie leków
•
Peg IFN alfa-2a
Peg IFN alfa-2a
podskórnie 180
podskórnie 180
g 1x/tydz.
g 1x/tydz.
•
Peg IFN alfa-2b
Peg IFN alfa-2b
podskórnie 1,5
podskórnie 1,5
g/kg mc
g/kg mc
•
Rybawiryna
Rybawiryna
w zależności od mc 800-1200 mg
w zależności od mc 800-1200 mg
codziennie
codziennie

Przeciwwskazania do leczenia
Przeciwwskazania do leczenia
IFN alfa
IFN alfa
Bezwzględne
Bezwzględne
•
ciąża
ciąża
•
okres
okres
karmienia
karmienia
•
alergia na lek
alergia na lek
Względne
Względne
•
choroby psychiczne
choroby psychiczne
•
choroba wieńcowa
choroba wieńcowa
•
zaburzenia krążenia
zaburzenia krążenia
mózgowego
mózgowego
•
znaczna leukopenia (<2.500)
znaczna leukopenia (<2.500)
•
znaczna trombocytopenia
znaczna trombocytopenia
(<50.000)
(<50.000)

Przeciwwskazania do leczenia
Przeciwwskazania do leczenia
rybawiryną
rybawiryną
•
końcowy okres niewydolności nerek
końcowy okres niewydolności nerek
•
znaczna niedokrwistość
znaczna niedokrwistość
•
hemoglobinopatie
hemoglobinopatie
•
ciąża
ciąża
•
podeszły wiek
podeszły wiek
•
niewyrównane nadciśnienie tętnicze
niewyrównane nadciśnienie tętnicze
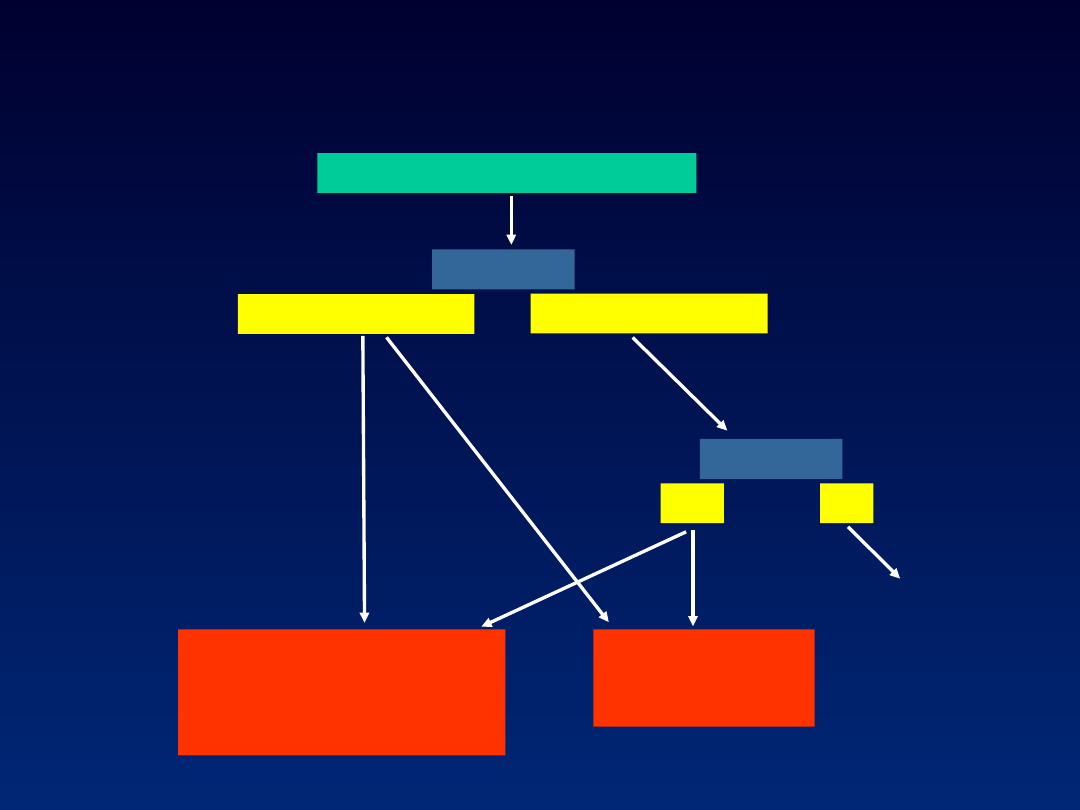
HCV RNA, AlAT, anty-
HCV
IFN-alfa2a, IFN-alfa2b,
IFN naturalny
4 tyg.: 1xdz.
20 tyg.: 3xtyg.
HCV RNA
8 tyg.
1 tyg.
>800.000 IU/mL
800.000 IU/mL
PegIFN-alfa2a,
PegIFN-alfa2b,
24 tyg.: 1xtyg
1 tyg.
4 tyg.
HCV RNA
(+)
(-)
nie leczyć
Zasady leczenia ostrego wzw typu C
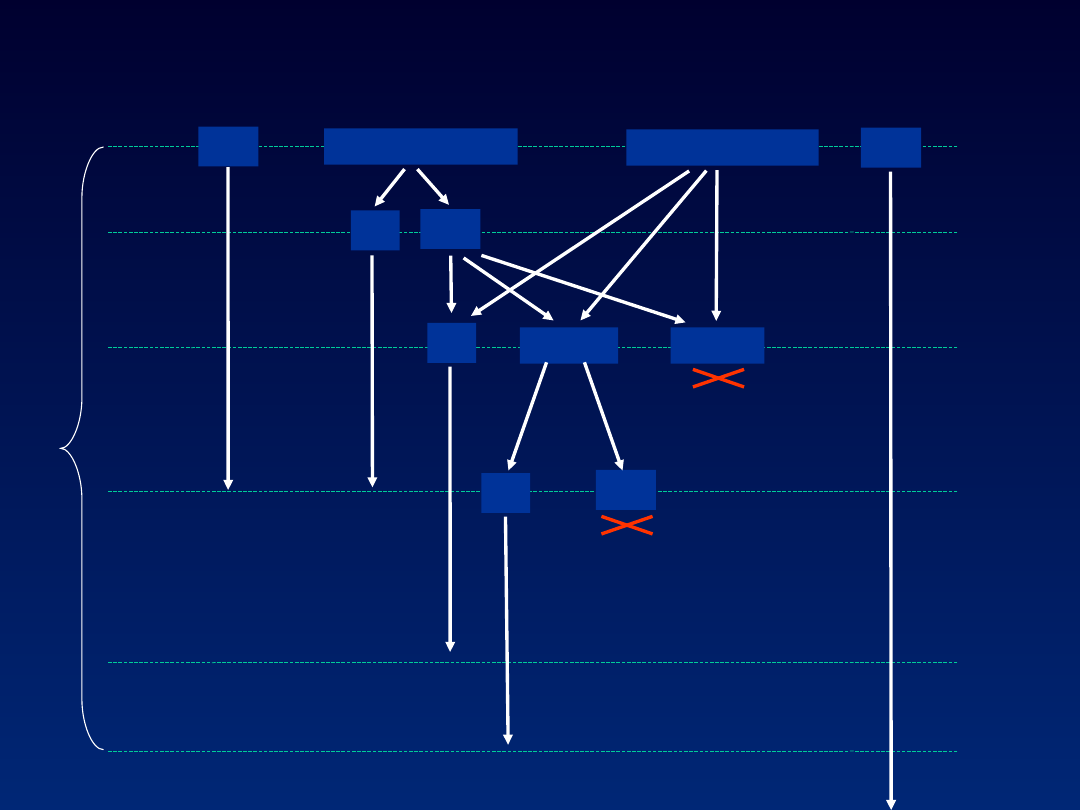
genotyp 2 i 3
0 tyg.
4 tyg.
12 tyg.
24 tyg.
48 tyg.
72 tyg.
genotyp 1
<600.000 IU/mL
600.000 IU/mL
MW
(-)
(+)
2log
2log
(-)
(+)
(-)
(+)
(+)
?
H
C
V
R
N
A
genotyp 1
Postępowanie w PWZW typu C
konsensusu „Zakopane 2007”


Typy interferonów
Typy interferonów
•
interferon alfa
interferon alfa
– monocyty, makrofagi, limfocyty
– monocyty, makrofagi, limfocyty
–
leukocytarny (Le-IFN
leukocytarny (Le-IFN
)
)
–
limfoblastoidalny (Ly-IFN
limfoblastoidalny (Ly-IFN
)
)
–
rekombinowany (rIFN
rekombinowany (rIFN
)
)
–
pegylowany interferon alfa (Peg-IFN
pegylowany interferon alfa (Peg-IFN
)
)
•
interferon beta
interferon beta
– fibroblasty
– fibroblasty
•
interferon gamma
interferon gamma
– limfocyty T
– limfocyty T
•
interferon omega
interferon omega
przeciwwirusowe, immunomodulacyjne i
przeciwwirusowe, immunomodulacyjne i
antyproliferacyjne
antyproliferacyjne

Mechanizmy działania
Mechanizmy działania
przeciwwirusowego
przeciwwirusowego
i
i
immunomodulacyjnego
immunomodulacyjnego
IFN
IFN
•
replikacja RNA
replikacja RNA
•
translacja i degradacja mRNA
translacja i degradacja mRNA
•
synteza i elongacja białek
synteza i elongacja białek
•
dojrzewanie wirionów
dojrzewanie wirionów
•
dojrzewanie i proliferacja komórek efektorowych
dojrzewanie i proliferacja komórek efektorowych
typu NK i makrofagów oraz cytotoksycznych T
typu NK i makrofagów oraz cytotoksycznych T
•
synteza dopełniacza
synteza dopełniacza
•
proliferacja i dojrzewanie komórek linii B
proliferacja i dojrzewanie komórek linii B
•
ekspresja antygenów zgodności tkankowej klasy
ekspresja antygenów zgodności tkankowej klasy
I i II
I i II
Pegylowane cząsteczki
Pegylowane cząsteczki
•
wydłużony okres półtrwania w
wydłużony okres półtrwania w
surowicy
surowicy
•
obojętne chemicznie
obojętne chemicznie
•
rozpuszczalne w wodzie
rozpuszczalne w wodzie
•
nietoksyczne
nietoksyczne
•
wielkość zależy od ilości
wielkość zależy od ilości
przyłączonych grup oksyetylenowych
przyłączonych grup oksyetylenowych
O
CH
3
-
(OCH
2
CH
2
)
n
-
O
-
C
-
N protein
H
m

Rybawiryna
Rybawiryna
(syntetyczny analog guanozyny)
(syntetyczny analog guanozyny)
•
hamuje aktywność monofosforanu
hamuje aktywność monofosforanu
dehydrogenazy inozyny (IMPDH)
dehydrogenazy inozyny (IMPDH)
•
modyfikuje RdRp
modyfikuje RdRp
•
inhibitor polimerazy NS5B
inhibitor polimerazy NS5B
•
jest mutagenem RNA-HCV (katastrofa z
jest mutagenem RNA-HCV (katastrofa z
nadmiaru błędów)
nadmiaru błędów)
•
przyspiesza klirens komórek zakażonych
przyspiesza klirens komórek zakażonych
•
utrudnia zakażenie de novo
utrudnia zakażenie de novo
•
mediuje równowagę Th1, Th2
mediuje równowagę Th1, Th2
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
Wyszukiwarka
Podobne podstrony:
06 pamięć proceduralna schematy, skrypty, ramyid 6150 ppt
7 aglebra schematow bloczkowych
wZ 2 Budowa wiedzy społecznej teoria schematów
3 ogolny schemat replikacji i onkogeza DNA wirusowa
Schematy animacji
wykład 5 schematy, przywileje, role
schemat mechanika
schemacik prezentacji
5 Algorytmy i schematy blokowe
Propozycja przygotowania schema Nieznany
f Obraz 6 plan 1 schemat
GH 7 082 schemat
poznawczo behawioralne schematy poznawcze
Ethnobotany of psilocybin mushrooms especially psilocybe cubensis J of Ethnopharmacology 10 (1984) 2
ICh S schemat rozw zad konwekcja
więcej podobnych podstron