
Z
11
11
17
17
6
7
8
9
Katowice 01.03.2004
V Wojewódzki Konkurs Dru ynowy
DUETY CHEMICZNE
I etap
ZADANIE I. TEST.
1. Na zaj ciach kółka chemicznego nauczyciel dokładnie omawiał budow atomu. Opisuj c składniki
j dra atomowego wspomniał, e okres półtrwania wolnych neutronów wynosi 12 min. Wyja nił tak e
uczniom, i okres półtrwania to czas, w którym rozpada si połowa pierwotnie istniej cych cz stek.
Ustal ile wolnych neutronów pozostanie po upływie 24 minut je li w chwili pocz tkowej było ich 1 gram.
a) 0,75g
b) 0,5g
c) 0,25g
d) 0g
2. Do opisu pierwiastka cz sto stosuje si poj cia: liczba atomowa i liczba masowa.
Przyjmuj c nast puj ce oznaczenia:
A
E
gdzie: A – liczba masowa, Z – liczba atomowa, E – symbol pierwiastka
Wybierz spo ród ni ej przedstawionych par izotopów tego samego pierwiastka:
a)
23
E,
23
E
b)
25
E,
27
E
c)
14
E,
14
E
d)
18
E,
19
E
3. Które spo ród wymienionych pierwiastków s w temperaturze pokojowej cieczami?
a) brom i rt
b) rt i jod
c) hel i brom
d) jod i hel
4. Zapis Zn
2+
oznacza:
a) dwudodatni kation cynku
c) dwudodatni kation cyny
b) dwudodatni anion cynku
d) dwudodatni anion cyny
5. Kasia spaliła kawałek wst ki magnezowej, a nast pnie zapisała na tablicy równanie reakcji:
Mg + O
→
MgO. Czy jest to prawidłowe równanie ilustruj ce ten proces?
a) tak, równanie jest prawidłowe
b) nie, w równaniu nie podano wszystkich produktów reakcji
c) nie, w równaniu nie uwzgl dniono, e tlen wyst puje w postaci cz steczek dwuatomowych
d) nie, w równaniu le napisano wzór tlenku magnezu
6. Je li na pasku bibuły naniesiemy mazakiem zielon plam i zanurzymy koniec bibuły w wodzie, to po
chwili zaobserwujemy, e woda wznosz c si po bibule do góry powoduje „znikni cie” plamy zielonej
i pojawienie si nieco wy ej plam: ółtej i niebieskiej. Zjawisko to obrazuje proces:
a) ekstrakcji
b) chromatografii
c) sublimacji
d) sedymentacji
7. W szczelnym naczyniu szklanym ustawiono dwie wypełnione do połowy zlewki: jedn ze st . H
2
SO
4
,
a drug z wod . Po kilku dniach wzrosła obj to kwasu i zmniejszyła si obj to wody. Przyczyn
tego zjawiska jest fakt i :
a) st . H
2
SO
4
jest ciecz lotn
c) st . H
2
SO
4
pochłania CO
2
z powietrza
b) st . H
2
SO
4
ma g sto wi ksz ni woda
d) st . H
2
SO
4
pochłania par wodn
8. Niektóre pierwiastki wyst puj w przyrodzie w postaci rodzimej tzn.
a) w postaci tlenków
c) w postaci czystych pierwiastków
b) w postaci soli uwodnionych (hydratów)
d) w postaci minerałów
9. Gdyby Robinson Crusoe dysponował odpowiednim sprz tem i chciał uzyska sól kuchenn ze słonej
wody morskiej to któr z metod rozdziału mieszanin powinien wykorzysta ?
a) destylacj
b) sedymentacj
c) krystalizacj
d) dekantacj
10. Paulina wykonała znany wszystkim eksperyment:
na dnie krystalizatora wypełnionego do połowy wod
postawiła zapalon wieczk i nakryła j odwróconym
do góry dnem cylindrem miarowym w ten sposób, e
poziom wody znajdował si na kresce z liczb 100.
Po chwili wieczka zgasła, a poziom wody podniósł si
do kreski oznaczonej liczb :
a) 80
b) 60
c) 40
d) 20
V Wojewódzki Konkurs Dru ynowy* DUETY CHEMICZNE* I etap * V Wojewódzki Konkurs Dru ynowy* DUETY CHEMICZNE* I etap *

11. Mały chłopiec mieszał dokładnie w słoikach ró ne substancje. Sporz dził w ten sposób pi
mieszanin: I – piasek z wod , II – ocet z cukrem, III – drobna kasza z olejem, IV – majonez z ketchupem,
V – mleko z wod . Które z mieszanin s niejednorodne?
a) I, II i III
b) I, IV I V
c) II i III
d) I i III
12. Umieszczony na opakowaniu z substancj chemiczn znak:
informuje, e jest to substancja:
a) promieniotwórcza
b) łatwopalna
c) toksyczna
d) wybuchowa
13. ”Stosunek masowy pierwiastków w zwi zku chemicznym jest wielko ci stał dla danego zwi zku
chemicznego”. Jest to tre prawa:
a) działania mas
b) stało ci składu
c) zachowania masy
d) okresowo ci
14. W schematycznym zapisie reakcji chemicznej:
x A
2
B
3
+ y C
→
z A + q CB
2
(gdzie A,B i C – to symbole pierwiastków chemicznych)
literom x, y, z i q odpowiadaj współczynniki stechiometryczne:
x
y
z
q
a)
1
3
2
3
b)
3
2
6
2
c)
2
3
4
3
d)
1
2
3
2
15. Je eli we wzorze sumarycznym soli wyst puj dwie reszty kwasu fosforowego (V) i trzy atomy
metalu to warto ciowo tego metalu wynosi:
a) I
b) II
c) III
d) V
16. Dwaj polscy uczeni: Karol Olszewski i Zygmunt Wróblewski w 1883 r po raz pierwszy skroplili
powietrze ozi biaj c je do temp. ok. –200
0
C. Ze skroplonego powietrza mo na przez podgrzanie
wydzieli metod destylacji poszczególne jego składniki. Znaj c temperatury wrzenia trzech składników
powietrza: azot: -196
0
C, argon: -186
0
C, tlen: -183
0
C, ustal w jakiej kolejno ci uzyskiwane b d te
substancje podczas destylacji skroplonego powietrza.
a) tlen, argon, azot
b) tlen, azot, argon
c) azot, tlen, argon d) azot, argon, tlen
17. Dlaczego słuszne jest powiedzenie: ”pami taj chemiku młody, wlewaj zawsze kwas do wody”?
a) poniewa g sto st onych kwasów jest wi ksza od g sto ci wody i kwas opada na dno naczynia,
a wydzielone w tym procesie ciepło stopniowo oddawane jest wodzie
b) poniewa mo na w ten sposób doda dokładnie tak ilo kwasu jaka jest potrzebna do sporz dzenia
roztworu o okre lonym st eniu
c) poniewa mieszaniu si kwasu z wod towarzyszy pochłanianie ciepła (jest to proces
endoenergetyczny) i wi ksza ilo wody pozwala przeprowadzi ten proces w sposób bezpieczny
d) poniewa stary przes d alchemików głosi, e w przeciwnym wypadku do wiadczenia
z wykorzystaniem tego roztworu nie powiod si
18. W jaki sposób utylizuje si rt (np. z rozbitego termometru)?
a) kuleczki rt ci zbiera si do pojemnika z wod , w którym po pewnym czasie rt si rozpuszcza
b) kuleczki rt ci posypuje si siark – rt reaguje z siark tworz c czarny proszek – siarczek rt ci
c) kuleczki rt ci nale y zebra i wprowadzi na metalowej ły ce do płomienia palnika – rt ulegnie
wówczas sublimacji
d) kuleczki rt ci mo na posypa chlorkiem sodu – powstanie wówczas nieszkodliwy dla człowieka
chlorek rt ci
19. Przedstawiony na poni szym rysunku zestaw nie nadaje si do zbierania gazów:
a) l ejszych od powietrza
b) toksycznych
c) dobrze rozpuszczalnych w wodzie
d) nierozpuszczalnych w wodzie
V Wojewódzki Konkurs Dru ynowy* DUETY CHEMICZNE* I etap * V Wojewódzki Konkurs Dru ynowy* DUETY CHEMICZNE* I etap *
20. Je li do probówki z ółtym roztworem chlorku elaza (III) dodamy roztwór wodorotlenku sodu to
str ci si brunatny osad wodorotlenku elaza (III). Równanie tej reakcji przedstawione w formie jonowej
mo na zapisa nast puj co:
a) Fe
3+
+ 3OH
-
→
Fe(OH)
3
↓
b) Fe
3+
+ 3Cl
-
+ 3Na
+
+ 3OH
-
→
Fe
3+
+ 3OH
-
+ 3Na
+
+ 3Cl
-
c) FeCl
3
+ 3NaOH
→
Fe
3+
+ 3OH
-
+ 3NaCl
d) FeCl
3
+ 3OH
-
→
Fe(OH)
3
↓
+ 3Cl
-
21. Polskie normy okre laj , e warzywa dopuszczone do sprzeda y powinny zawiera nie wi cej ni
2000 mg azotanów na kilogram masy. Z tego wynika, e główka sałaty wa ca 150 gramów mo e
zawiera maksymalnie:
a) 3 mg azotanów
b) 30 mg azotanów
c) 300 mg azotanów
d) 3 g azotanów
22. Przyjmuj c, ze jeden papieros typu „light” zawiera 0,5 mg nikotyny, z czego ok. 90% dostaje si do
płuc palacza, oblicz ile nikotyny przenika do płuc osoby, która wypali 10 papierosów.
a) ok. 450 mg
b) ok. 45 mg
c) ok. 4,5 mg
d) ok. 045 mg
23. Ile kilogramów roztworu substancji A o st eniu 8% nale y doda do 2 kg roztworu tej substancji
o st eniu 4%, aby otrzyma roztwór o st eniu 6%?
a) 1 kg
b) 2 kg
c) 3 kg
d) 4 kg
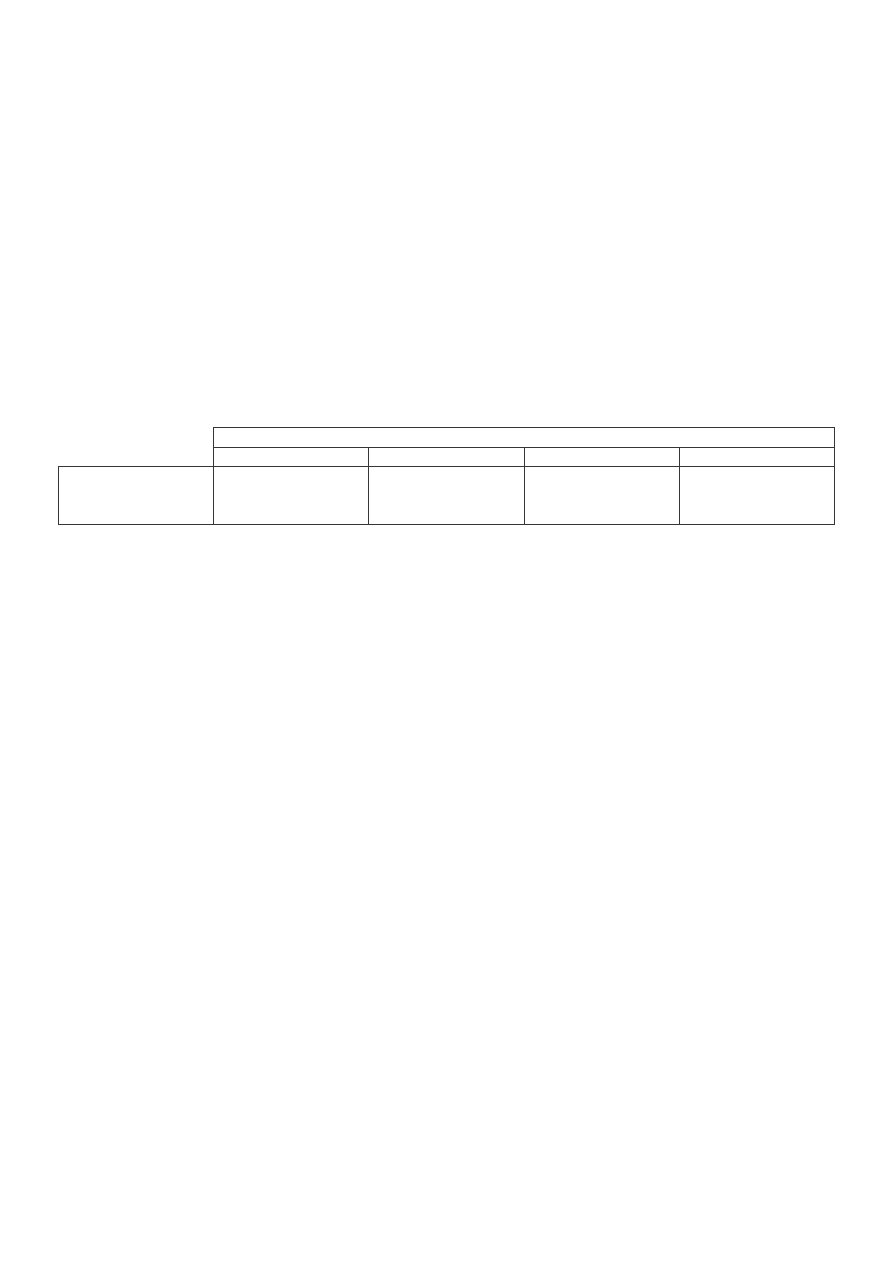
24. Korzystaj c z danych zawartych w tabeli sprawd ile gramów Pb(NO
3
)
2
mo na jeszcze rozpu ci
w 435 gramach roztworu tego zwi zku nasyconego w temperaturze 10
0
C po podniesieniu temperatury
o 20
0
C.
temperatura
10
0
C
20
0
C
30
0
C
40
0
C
rozpuszczalno
Pb(NO
3
)
2
[g/100g H
2
O]
45
52
61
70
a) 21 g
b) 48 g
c) 156 g
d) 183 g
25. Szkło wodne (czyli roztwór krzemianu sodu Na
2
SiO
3
) znalazło zastosowanie m.in. do impregnowania
tkanin w celu zabezpieczenia ich przed zapaleniem. Oblicz ile gramów Na
2
SiO
3
powstanie w reakcji 40 g
NaOH z odpowiedni ilo ci SiO
2
je li wiadomo, e drugim produktem tej reakcji jest woda.
a) 30,5 g
b) 61 g
c) 122 g
d) 244 g
26. Popularny materiał wybuchowy – trotyl, to zwi zek organiczny o nazwie trinitrotoluen (TNT). Jego
wzór sumaryczny mo na zapisa : C
7
H
5
O
6
N
3
. Uwzgl dniaj c masy atomowe pierwiastków wchodz cych
w skład tego zwi zku ustal skład procentowy trotylu i odpowiedz którego pierwiastka (procentowo) jest
najwi cej w tym zwi zku.
a) wodoru
b) w gla
c) tlenu
d) azotu
27. W siarczku pewnego dwuwarto ciowego metalu stosunek masowy siarki do metalu wynosi 4:5.
Metalem tym jest:
a) Ca
b) Fe
c) Zn
d) Pb
28. Ile moli tlenu cz steczkowego otrzymamy z rozkładu 6 moli nadtlenku wodoru (H
2
O
2
)?
a) 1 mol
b) 3 mole
c) 4 mole
d) 6 moli
29. Aby przygotowa 0,5 kg 5%-owego roztworu kwasu borowego aptekarz musi u y :
a) 5 g H
3
BO
3
i 495 g H
2
O
c) 25 g H
3
BO
3
i 475 g H
2
O
b) 10 g H
3
BO
3
i 490 g H
2
O
d) 50 g H
3
BO
3
i 450 g H
2
O
30. Oblicz jakie jest st enie molowe 96%-owego roztworu H
2
SO
4
o g sto ci 1,84 g/cm
3
.
a) ok. 1,8 mol/dm
3
b) ok. 9 mol/dm
3
c) ok. 18 mol/dm
3
d) ok. 22 mol/dm
3
MASY ATOMOWE [u] : H – 1,
B – 11,
C – 12,
N – 14,
O – 16,
Na – 23, Si – 28,
S – 32,
Ca – 40, Fe – 56, Zn – 65, Pb – 207
V Wojewódzki Konkurs Dru ynowy* DUETY CHEMICZNE* I etap * V Wojewódzki Konkurs Dru ynowy* DUETY CHEMICZNE* I etap *
ZADANIE II. PRAWDA I FAŁSZ O UKŁADZIE OKRESOWYM PIERWIASTKÓW.
Ustal, które ze zda s prawdziwe, a które fałszywe. Postaw znak X we wła ciwym miejscu na karcie
odpowiedzi.
1. Pionowe kolumny tablicy Mendelejewa zwane s okresami.
2. Wzdłu okresu maleje reaktywno metali, a wzrasta reaktywno niemetali.
3. W ostatniej (osiemnastej) grupie układu okresowego znajduj si gazy szlachetne.
4. Numer grupy informuje ile powłok elektronowych posiada dany pierwiastek.
5. Przewa aj c ilo pierwiastków układu okresowego stanowi metale.
6. Pierwiastki w układzie okresowym uło one s w kolejno ci wzrastaj cych liczb atomowych.
7. Pierwiastki le ce w jednej grupie maj zbli one wła ciwo ci chemiczne.
8. Symbole wszystkich pierwiastków s dwuliterowymi skrótami pochodz cymi m.in. od nazw
łaci skich lub nazwisk odkrywców.
9. Wszystkie pierwiastki znajduj ce si w układzie okresowym wyst puj w przyrodzie.
10. W układzie okresowym istnieje kilka pierwiastków (tzw. półmetali), które wykazuj wła ciwo ci
zarówno metali jak i niemetali.
ZADANIE III. IDENTYFIKACJA GAZÓW.
Nazwom gazów przypisano rysunkowe symbole:
gaz
wodór
tlen
dwutlenek
w gla
chlor
dwutlenek
siarki
amoniak
symbol
Przyporz dkuj odpowiednim symbolom przedstawione ni ej opisy (zwi zane z identyfikacj gazów).
1. Gaz ten przepuszczany przez wod wapienn powoduje jej zm tnienie.
2.
Je li do wylotu probówki wypełnionej tym gazem przybli ymy płomie to gaz spali si
w powietrzu wydaj c charakterystyczny odgłos.
3.
Ten gaz o charakterystycznym zapachu zmienia barw zwil onego papierka uniwersalnego na
zielon .
4.
arz ce si łuczywo wło one do probówki z tym gazem zapala si .
5. Ten zielono ółty gaz o charakterystycznym zapachu wybiela wilgotny papierek lakmusowy,
a papierek jodoskrobiowy barwi na granatowo.
6. Ten gaz powoduje zmian koloru bibuły filtracyjnej nas czonej kwa nym roztworem
dwuchromianu potasu z pomara czowej na zielon .
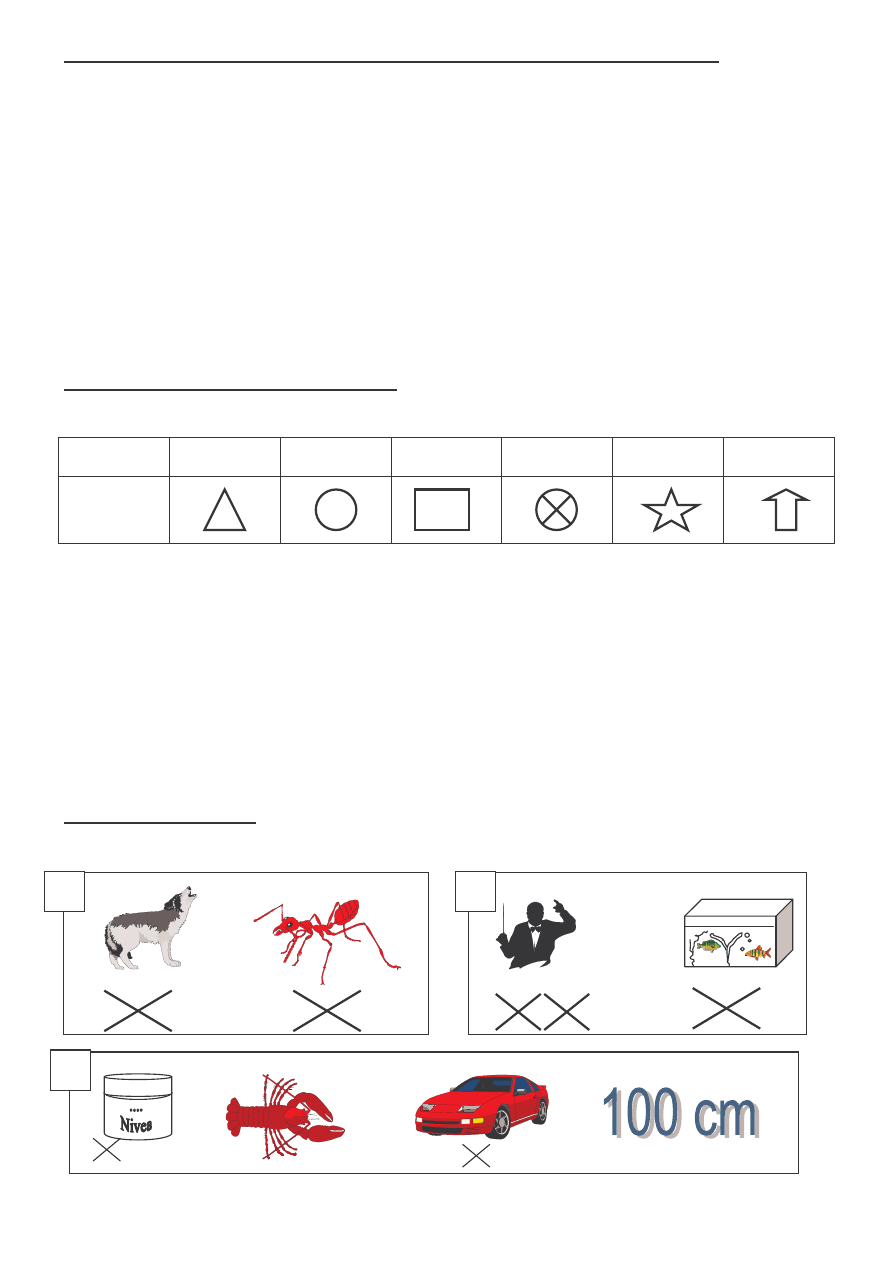
ZADANIE IV. REBUSY.
Rozwi rebusy - odgadnij nazwy sprz tów stanowi cych wyposa enie pracowni chemicznych.
100
LK M ...ry...nt akwa
K m=f au
V Wojewódzki Konkurs Dru ynowy* DUETY CHEMICZNE* I etap * V Wojewódzki Konkurs Dru ynowy* DUETY CHEMICZNE* I etap *
1.
2.
3.
Wyszukiwarka
Podobne podstrony:
3 etap 2004 solutions
3 etap 2004 problems
mzm - etap wojewódzki - poziom rozszerzony 2004, Matematyka
ref 2004 04 26 object pascal
Konkurs historyczny SP etap rejonowy
Etap rejonowy 2007 2008 klucz
antropomotoryka 26 2004 id 6611 Nieznany (2)
2004 07 Szkoła konstruktorów klasa II
brzuch i miednica 2003 2004 23 01
2004 06 21
dz u 2004 202 2072
Mathematics HL May 2004 TZ1 P1
Deklaracja zgodno¶ci CE 07 03 2004
biuletyn 9 2004
Prawo telekomunikacyjne 2004
więcej podobnych podstron