
Działanie promieniowania na poziomie
molekularnym, subkomórkowym i komórkowym.
Wpływ wielkości dawki i czynników
dodatkowych (moc dawki; obecność wody,
temperatura, utlenowanie).
Względna skuteczność biologiczna, mechanizmy
śmierci komórkowej. Zróżnicowanie odnowy
tkanek i ich promieniowrażliwości.

W następstwie promieniowania na systemy biologiczne wywoływane
są procesy trwające od ułamków sekund do wielu miesięcy i lat.
Można wyróżnić trzy najistotniejsze fazy:
Fizyczną
, trwającą 10
-12
- 10
-18
s, powstawanie wolnych rodników,
wzbudzenie, jonizacja (w ilości ponad 10
5
po dawce 1 Gy w każdej
komórce o średnicy 10 μm, ale tylko jedna z nich ma charakter
letalny),
Chemiczną
, 10
-12
- 1 s, reakcje chemiczne, enzymatyczne,
Biologiczną
, 1 - 10
6
dni, reakcje wczesne, poźne, karcynogeneza,
procesy naprawcze, proliferacja komórek

Efekty działania promieniowania
Poziom molekularny:
• uszkodzenia na skutek pośredniego lub
bezpośredniego działania promieniowania
Poziom komórki:
• śmierć mitotyczna (reprodukcyjna)
• śmierć interfazalna (apoptotyczna lub nekrotyczna)
Poziom organizmu:
• efekty stochastyczne i deterministyczne
• wczesne i późne skutki po napromienieniu

Efekty działania promieniowania
na poziomie molekularnym
Najbardziej wrażliwą na promieniowanie częścią
komórki jest jej materiał genetyczny –
DNA.
Jest to związane z faktem, że cząsteczki DNA
występują w komórce na ogół w jednej kopii,
natomiast inne makrocząsteczki (białka, kwasy
rybonukleinowe) – w wielu kopiach, a informacja
zawarta w DNA pozwala na ich odtworzenie.

Efekty działania promieniowania
na poziomie molekularnym
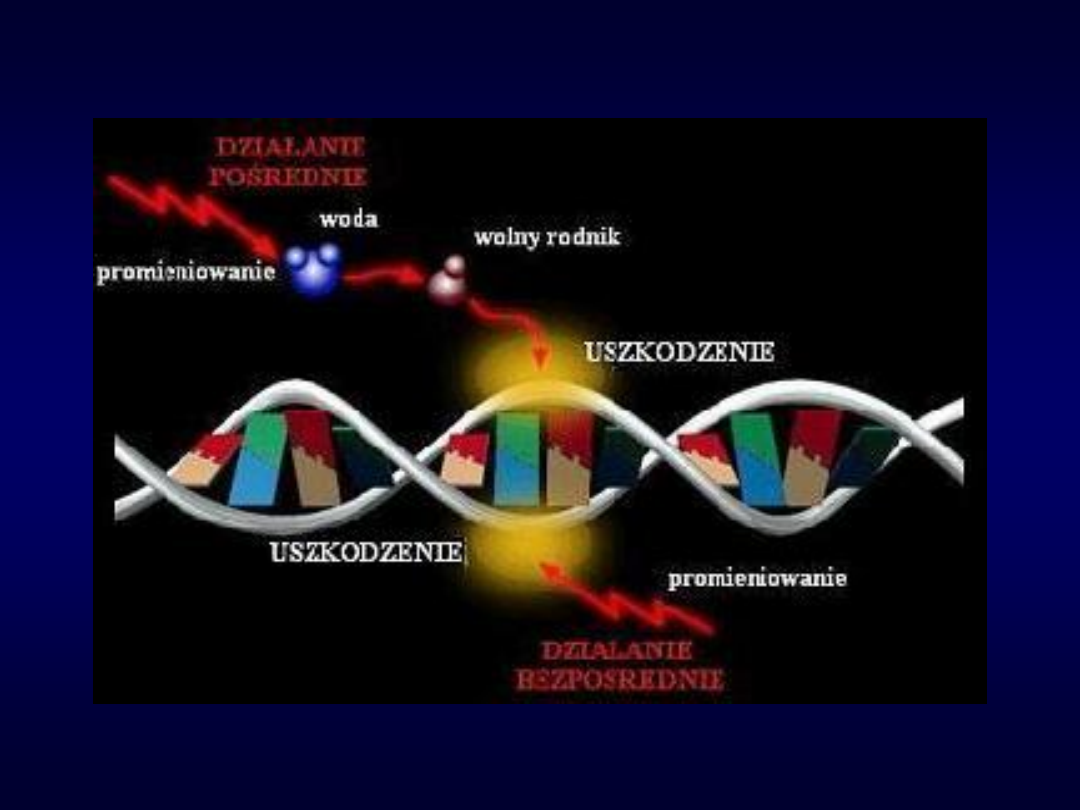
– Uszkodzenie materiału genetycznego DNA
– skutek
bezpośredniego
działania promieniowania przez
zderzenie cząstki promieniowania z nicią DNA (faza
fizyczna)
– skutek
pośredniego
działania promieniowania poprzez
oddziaływanie produktów radiolizy wody (wolnych
rodników) znajdującej się w jądrze komórkowym z DNA

Efekty działania promieniowania
na poziomie molekularnym
– Uszkodzenie materiału genetycznego DNA
Proporcje między bezpośrednim i pośrednim efektem
działania promieniowania na DNA zależą od rodzaju
promieniowania.
W przypadku promieniowania o małej gęstości jonizacji,
np.
X
, uszkodzenia DNA w 70-90% powstają na skutek
działania
pośredniego
.
Ze względu na dużą gęstość jonizacji,
neutrony, protony i
cząstki alfa
uszkadzają DNA w ponad 90% w sposób
bezpośredni
.

Uszkodzenia DNA
Ze względu na to, że woda stanowi zasadniczą część
masy komórki, produkty jej radiolizy odgrywają
wiodącą rolę w mechanizmie pośrednim działania
promieniowania.
Ilość wody w organizmie człowieka jest różna i zależy od wieku,
płci, a także od budowy ciała. Z wiekiem zawartość wody w
organizmie zmniejsza się.
Embrion
ludzki zawiera do
98%
wody,
organizm noworodka ok. 75-80% wody, organizm dorosłego
mężczyzny zawiera ok. 60%, kobiety ok. 54%, natomiast u
starszych
M ok.
54
%
, K ok
.
46%

Uszkodzeniapośrednie
– Cząstki promieniowania jonizują wodę:
H
2
O → H
2
O
+
+ e
–
– Zjonizowana cząsteczka wody (nietrwały jon rodnikowy)
może :
1. Reagować z cząsteczką niezjonizowaną, tworząc
uwodniony wodór (proton) oraz
rodnik wodorotlenkowy:
H
2
O
+
+ H
2
O→ H
+
aq
+
OH
.
2. Połączyć się z uwolnionym elektronem, tworząc
wzbudzoną cząsteczkę wody:
H
2
O
+
+ e
–
→ H
2
O*
Na skutek
jej rozpadu
powstają produkty silnie reagujące ze
związkami chemicznymi wchodzącymi w skład komórek
organizmu:
H
2
O* → H
.
+
OH
.

Efekt tlenowy
Decydujący wpływ na rozmiary efektu pośredniego ma
cząstkowe ciśnienie tlenu w komórce. Tlen reaguje z powstałym
na skutek radiolizy wody rodnikiem wodoru, co prowadzi do
powstania
niestabilnego rodnika wodoronadtlenkowego
H
.
+ O
2
→
HO
2
.
Ten rodnik reaguje z drugim takim samym rodnikiem lub z
rodnikiem wodoru tworząc
nadtlenek wodoru
,
cząsteczkę silnie
utleniającą, która powoduje liczne uszkodzenia DNA
2HO
2
.
→
H
2
O
2
+ O
2
HO
2
.
+ H
.
→
H
2
O
2

Wolne rodniki i tlen
Rodniki
są fragmentami cząsteczek chemicznych
zawierającymi w powłoce niesparowany elektron. Mają
krótki okres trwania (ok. 10
-5
s) i cechują się wysoką
reaktywnością (tworzą wolne rodniki organiczne),
reagując z DNA i białkami niszczą je.
Cząsteczkowy
tlen
wykazuje do rodników duże
powinowactwo. Wysokie stężenie O
2
w komórce nasila
i utrwala niekorzystne efekty promieniowania.

Wolne rodniki i tlen
Hipoksja
zmniejsza biologiczne skutki promieniowania.
Podobnie jak cząsteczki zawierające
grupy wodorosiarczkowe
(cysteina, cysteamina i glutation)
,
enzymy
(katalaza,
peroksydaza, dysmutaza ponadtlenkowa),
vit. C, E
,
polifenole
w
zielonej herbacie,
beta-karoten
,
retinol
,
selen
i inne.
Cząsteczki te unieczynniają wolne rodniki – dostarczenie ich
zwierzętom lub kulturom tkankowym bezpośrednio przed
napromienianiem zmniejsza nawet dwukrotnie liczbę trwałych
uszkodzeń popromiennych. Po napromienianiu uczynniane są
enzymy katalizujące
zobojetniające rodniki (największe
znaczenie odgrywa S-transferaza glutationowa).

Uszkodzenia DNA powstałe na skutek
pośredniego lub bezpośredniego
działania promieniowania nie różnią
się od siebie.

Uszkodzenia DNA
– Uszkodzenie podwójnej nici DNA,
– Uszkodzenie pojedynczej nici DNA,
– Uszkodzenie lub utrata zasad azotowych
(purynowej lub pirymidynowej),
– Uszkodzenia reszt cukrowych i fosforanowych,
– Powstawaniu krzyżowych połączeń białek
jądrowych i DNA (w obrębie jednej lub dwóch nici)

Uszkodzenia DNA
–
Pęknięcia jednoniciowe
zachodzą bardzo często w DNA
bez
udziału promieniowania i są
łatwo
oraz
skutecznie
naprawiane
przez swoiste grupy enzymów (homogenne odtwarzanie wiązań i
struktury).
– Istnieją
określone miejsca
w nici DNA, których
kilkuogniskowe
uszkodzenie jest nieodwołalnie
letalne
.
– Pęknięcia dwuniciowe
- bardziej skomplikowane strukturalnie
są najtrudniejsze do naprawienia (odtwarzanie niehomogenne) i
najczęściej doprowadzają do
śmierci komórki
. Nie w pełni
naprawione pęknięcia mogą prowadzić do
aberracji
chromosomowych i do
mutacji
genowych
.

Mutacje DNA
Mutacja
naprawiona
- komórka zdolna do życia
Mutacja utrwalona - transformacja w
komórkę
nowotworową
Mutacja
letalna
- śmierć komórki

Naprawa DNA
Podczas terapeutycznego napromieniania dawką 1 Gy
powstaje ok.
10
5
jonizacji
na 1 komórkę ale
tylko jedna
ma nieodwracalny
,
letalny
charakter.
W zdecydowanej większości przypadków
wewnątrzkomórkowe mechanizmy naprawcze są w
stanie zneutralizować wywołane uszkodzenia. W części
przypadków może dochodzić do uszkodzeń utajonych,
które stają się nieodwracalne przy zadziałaniu
dodatkowych czynników fizycznych lub chemicznych
(np. tlenu, ciepła).

Naprawa DNA
Naprawa DNA nie jest procesem przebiegającym bezbłędnie.
Uszkodzenia mogą zostać nie naprawione lub naprawione
błędnie, prowadząc do śmierci komórki lub jej transformacji w
komórkę nowotworową.
Prawdopodobieństwo
utrwalenia uszkodzenia
lub
błędnej
naprawy
jest wprost proporcjonalne do
dawki promieniowania
(wzrasta z poziomem uszkodzenia). O ile można ustalić pewną
progową liczbę uszkodzeń, po której przekroczeniu komórka
ginie, to nie istnieje próg dawki promieniowania, poniżej którego
uszkodzenia zostaną w stu procentach bezbłędnie naprawione.

Mechanizmy naprawy DNA
– Wycinanie uszkodzonych zasad:
glikozylazy i endonukleazy
,
–Bezpośrednia naprawa uszkodzenia:
alkilotransferaza, dioksygenaza
,
–Usuwanie wiązań krzyżowych:
TOP1-DNA
,
–Naprawa niesparowanych zasad,
–Naprawa przez wycinanie nukleotydu:
helikaza, ATP-zależna ligaza DNA
,
–Rekombinacja homologiczna:
egzonukleaza, nukleazy
,
–Niehomologiczne scalanie końców DNA:
ligaza, nukleaza
,
–Modulacja puli nukleotydowej:
dUTPaza
,
–Katalityczne podjednostki polimeraz:
podj. polimerazy DNA (zeta)
,
–Nukleazy wycinające:
5'naukleaza, 3'-egzonukleaza
,
–Szlak Rad6:
enzym koniugujący ubikwitynę
,
–Regulacja struktury chromatyny:
białko histonowe
,
–inne

Następstwa
braku
naprawy
lub
niewiernej naprawy
DNA
Przy braku lub niepełnej naprawie DNA powstają aberracje:
– delecje ( dominują w mutacjach spontanicznych),
– aberracja chromosomalna (uszkodzenie obu chromatyd w tych
samych miejscach) powstają w fazie G1
– Aberracja chromatydowa lub subchromatydowa (uszkodzenie
chromatydy lub jej podjednostki) chromatydowe - powstają w
fazach S i G2, subchromatydowe powstaja we wczesnej profazie.

Śmierćinterfazalna
Śmierć interfazalna następuje w dowolnej części cyklu.
Zachodzi w ciągu od kilku do kilkudziesięciu godzin po
napromienieniu. Może nastąpić w dwojaki sposób: jako
śmierć
apoptotyczna lub nekrotyczna.

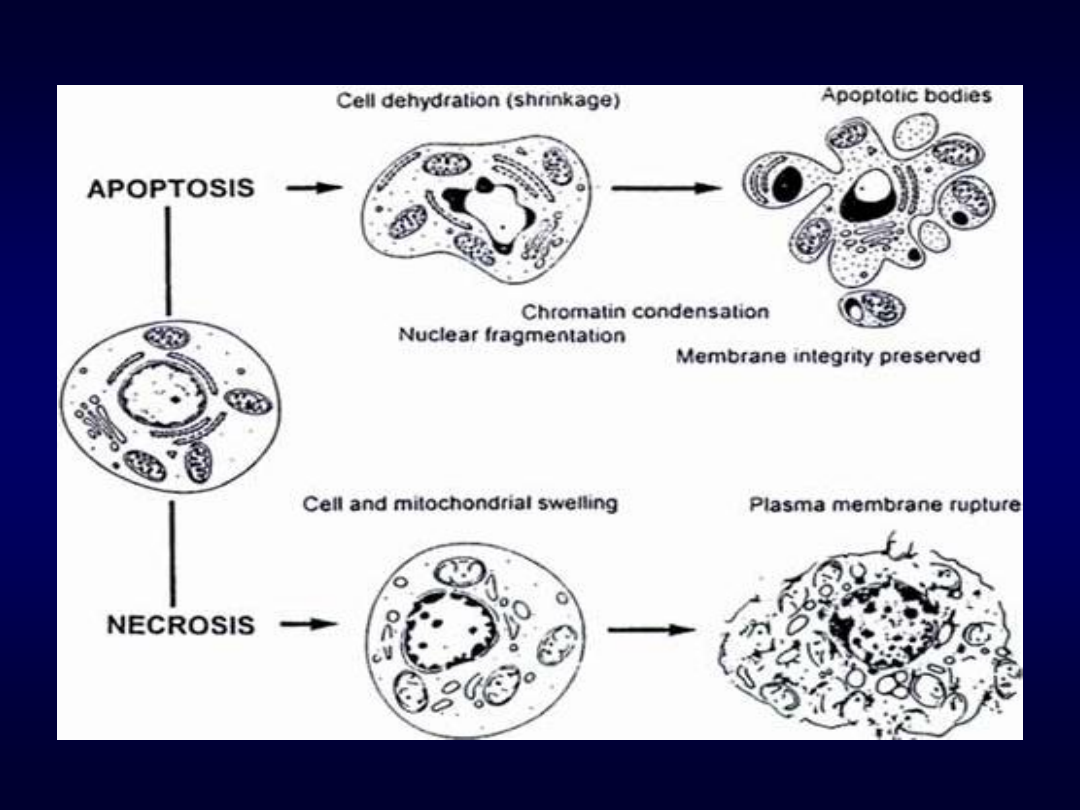
Apoptoza
Komórka skierowana na drogę apoptozy początkowo
kurczy się, następnie na jej powierzchni pojawiają sie
pęcherzyki, chromatyna zaś ulega kondensacji i
fragmentacji. Wkrótce potem cała komórka rozpada się,
a jej fragmenty są szybko trawione przez sąsiadujące
komórki.

Śmierćnekrotyczna
Nastepuje wówczas, gdy komórki zostają bardzo
poważnie uszkodzone wysokimi dawkami
promieniowania i tracą zdolność zachowania
równowagi wodno-elektrolitowej. Woda i jony, których
nadmiar normalnie usuwany jest na zewnątrz, wnikają
do wnętrza komórki, powodując jej spęcznienie i
nieodwracalne uszkodzenie.

Na ogół
niskie dawki
promieniowania powodują śmierć
mitotyczną lub apoptotyczną. Nie wszystkie komórki
mają zdolność apoptozy, a szczególnie podatne na nią
są komórki grasicy – tymocyty.
Wyższe dawki
promieniowania powodują śmierć
nekrotyczną wszystkich typów komórek.

Transformacja nowotworowa
Nie wszystkie aberracje prowadzą do śmierci komórki. Różnego
rodzaje przemieszczenia, zwane
translokacjami
nie zmieniają
morfologii chromosomów i mogą być przekazywane komórkom
potomnym. Zawsze towarzyszą im mutacje na poziomie DNA, a
gdy nastepują one w genach odpowiedzialnych za kontrolę cyklu
komórkowego lub naprawy DNA są najbardziej niebezpieczne.
Mogą zmienić komórkę prawidłową w nowotworową
(transformacja nowotworowa).
Zwykle następuje to po wielu
mutacjach ale nie można wykluczyć, że jedna mutacja wyzwoli
kaskadę dalszych zmian genetycznych prowadzących do
transformacji.

Efekty działania promieniowania
na poziomie molekularnym
Uszkodzenie innych makrocząsteczek
(białek, kwasów rybonukleinowych)
zniszczenie struktury przestrzennej, wytworzenie wiązań
krzyżowych i zerwanie wiązań kowalencyjnych w
łańcuchach peptydowych zachodzi po napromienieniu
dawkami wielokrotnie wyższymi
od tych, które uszkadzają
DNA (w stopniu wykrywalnym metodami
fizykochemicznymi). Może wpływać na funkcje enzymów,
błon komórkowych, mitochondriów (zaburzając reakcje
biologicznego utleniania i syntezy ATP, przepuszczalność
błon komórkowych).

Promieniowrażliwość
Śmierć mitotyczna leży u podstaw popromiennego deficytu
komórek w tych tkankach i narządach, których funkcjonowanie
wymaga częstej odnowy komórkowej. Dlatego najbardziej
promieniowrażliwe
są te tkanki i narządy, które ulegają
częstej
odnowie
:
szpik kostny, grasica, śledziona, ściany przewodu
pokarmowego, moczowego i oddechowego, skóra oraz gonady
męskie.
Jajniki oraz mózg
i inne części CUN są stosunkowo
promieniooporne – ich uszkodzenie jest jednak nieodwracalne ze
względu na brak komórek macierzystych, które mogłyby zastąpić
utracone komórki funkcjonalne (oocyty i kom. nerwowe).

Promieniowrażliwość
Komórki, które osiągnęły już swój stopień specjalizacji
lub te, które dzielą się rzadko lub wcale są względnie
oporne na dawki promieniowania powodujące śmierć
mitotyczną komórek macierzystych lub często
dzielących się. Z podobnych powodów
rosnące narządy
dzieci i młodzieży
wykazują
znacznie większą
promieniowrażliwość
niż narządy osób dorosłych.
Wyszukiwarka
Podobne podstrony:
8 Działanie promieniowania gamma na właściwości mechaniczne i termiczne folii z politereftalanu etyl
Negatywne skutki działania promieniowania UV na organizm
W 11 Leki działające pobudzająco na ośrodkowy układ
Wpływ pyłów i promieniowania na uszkodzenie j ustenj(2)
Nauka o lekach Działanie leków na organizm
Działanie żołnierza na polu walki w dzień i w nocy - konspekt, Konspekty, SZKOLENIE TAKTYCZNE
Jaki jest mechanizm działania zabiegów na rozstępy
04 Rozdział 03 Działania arytmetyczne na liczbach rzeczywistych
Mechanizm wyzwalania reakcji biologicznych pod wpływem działania promieni UV
Zarys działalności ONR na Pomorzu 1934 – 1939, Polityka
prelekcja na POZ, III rok V semestr, POZ III rok
DZIAŁANIE PROMIENIOWANIA LASEROWEGO
Zewnetrzne zrodla finansowania dla otwieranych i dzialajacych firm na rynku nieruchomosci[1]
plan pracy - taktyka - działanie żołnierza na polu walki, Taktyka
Działania promocyjne na rynku budowlanym (15 stron) ITZF3TVWFHPG753XM7BPUDYOAFD6NIZWQGD2OGA
III koło, TOKSYKOLOGIA - ściąga rośliny, Działające pobudzająco na ośrodkowy układ nerwowy:
SEMESTR I, wyklad 3, Planowanie - zabieg umysłowy, który poprzedza właściwą czynność, jest zatem dzi
fiz20-ad, Wynikiem działania siły na elektron będzie zakrzywienie jego toru w płaszczyznie prostopad
więcej podobnych podstron