
Leki pochodzenia
naturalnego
dr inż. Monika Kowalewska

Saponiny
Saponiny są to związki pochodzenia roślinnego zbudowane z dwóch części:
aglikonu – sapogeniny (sapogenol) i glikonu – sacharydu (cukru). Część
cukrową najczęściej stanowi arabinoza, glukoza, ramnoza, ksyloza i
galaktoza. Saponiny zmieniają strukturę błon komórkowych i tym samym
nabłonków, czyniąc je bardziej przepuszczalnymi dla składników organicznych
(cukrów, białek, tłuszczów). Saponiny mają zdolność przyłączania się do
cholesterolu, tworząc stosunkowo stabilne związki, aktywne farmakologicznie.
Saponiny to poliglikozydy zawierające kilka reszt cukrowych - w zależności
od ilości łańcuchów cukrowych wyróżnia się:
• monodesmozydy – zawierające 1 łańcuch cukrowy w pozycji C3
• bidesmozydy – dwa niezależne łańcuchy cukrowe – pozycja C3 oraz C17 lub
C26 aglikonu
• tridesmozydy zawierające 3 łańcuchy cukrowe
Łańcuchy cukrowe mogą być proste lub rozgałęzione

Saponiny
W zależności od budowy aglikonu saponiny dzielimy na:
steroidowe
–
zawierają
układ
steranu
C27
(cyklopentanoperhydrofenantrenu)
triterpenowe – glikozydy trzech pochodnych izomerycznych względem
siebie alkoholi
triterpenowych pentacyklicznych o składzie C
30
H
50
O
Aktywność farmakologiczna saponin:
saponiny są związkami biologicznie czynnymi
mogą powodować hemolizę erytrocytów
działają wykrztuśnie – drażnią błonę śluzową, jamę nosową, gardło, oskrzela
i na drodze odruchowe powodują wydzielanie śluzu
glicyryzyna wykazuje działanie przeciwzapalne, właściwości zbliżone do
kortykosteroidów – leczenie wrzodów żołądka i dwunastnicy
escynon działa p/zapalnie oraz p/wysiękowo
dodatkowo wykazują działanie p/ grzybicze, p/wirusowe
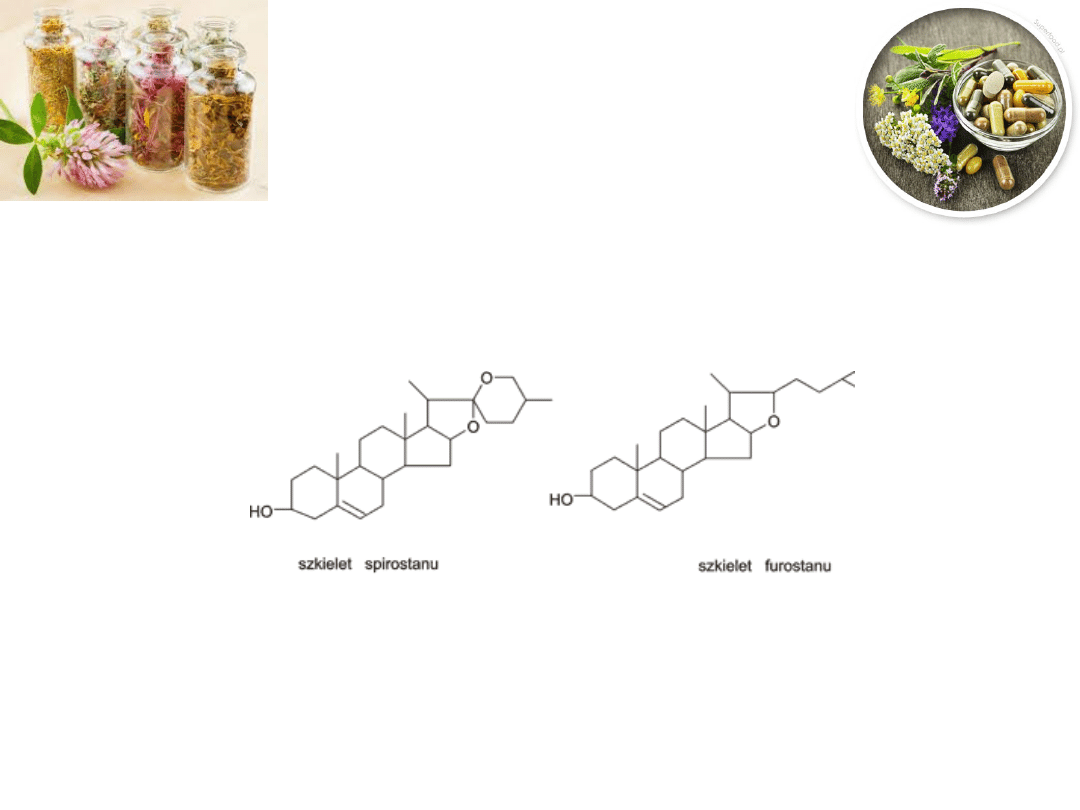
Saponiny steroidowe
W
przypadku
saponin
steroidowych
występuje
układ
steranu
(cyklopentanoperhydro-fenantren), dzielimy je ze względu na budowę na:
pochodne spirostanu – przy C22 występuje ugrupowanie spiroketalowe
pochodne furostanu – przy C22 występuje rozgałęziony fragment
łańcuchowych
W pochodnych spirostanowych występuje ugrupowanie spiroketalowe – dwa
pierścienie tlenowe (5- i 6-członowe) połączone są wspólnym atomem węgla
C22 – układ taki jest aktywny chemiczne – 6-członowy pierścień
tetrahydropiranu ulega otwarciu, powstaje produkt o szkielecie furostanu,
który na drodze chemicznej można zdegradować do steroidów C21 –
półprodukty służą do syntezy kortykosteroidów i hormonów płciowych.
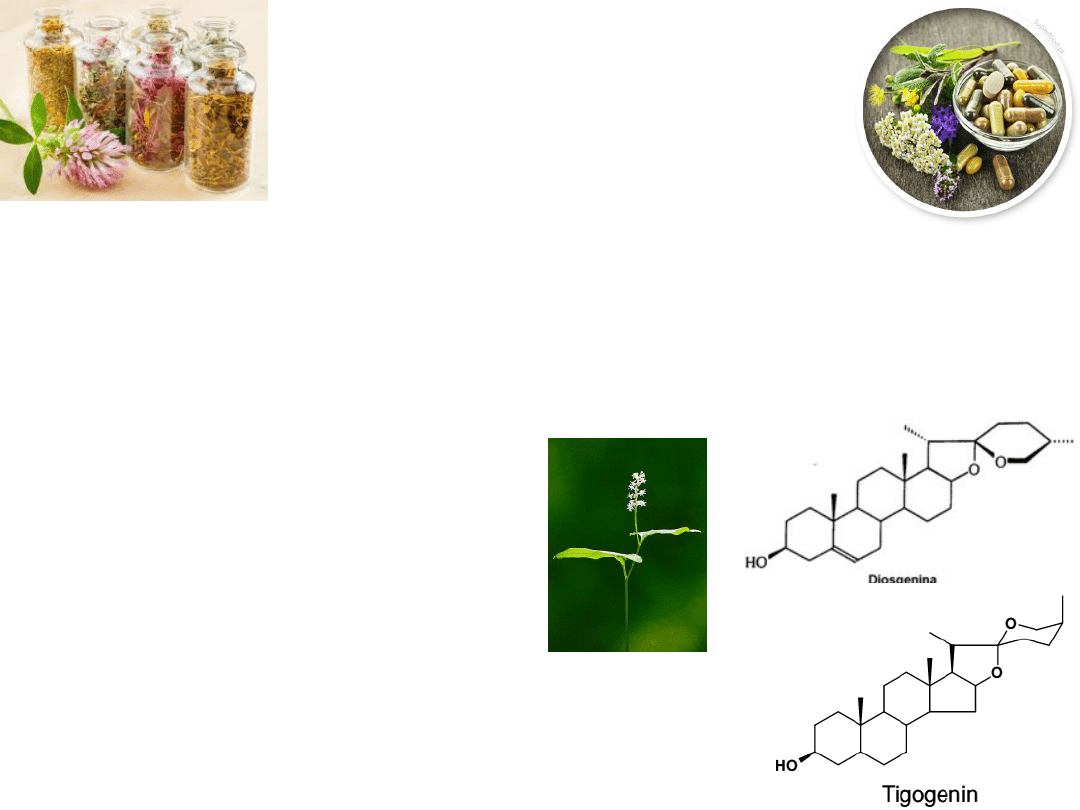
Saponiny steroidowe
W zależności od konfiguracji grupy –CH
3
przy C25 wyróżniamy dwa szeregi
saponin spirostanowych:
saponiny właściwe (-CH
3
w pozycji aksjalnej)
izosaponiny (-CH
3
w pozycji ekwatorialnej)
Większość saponin to pochodne spirostanu, poszczególne aglikony różnią się:
podstawnikami (grupy hydroksylowe)
konfiguracją pierścienia A i B
obecnością wiązania podwójnego
konfiguracją grup funkcyjnych
Przykłady występowania:
diosgenina – konwalijka dwulistna, kozieradka
tigogenina – psianka
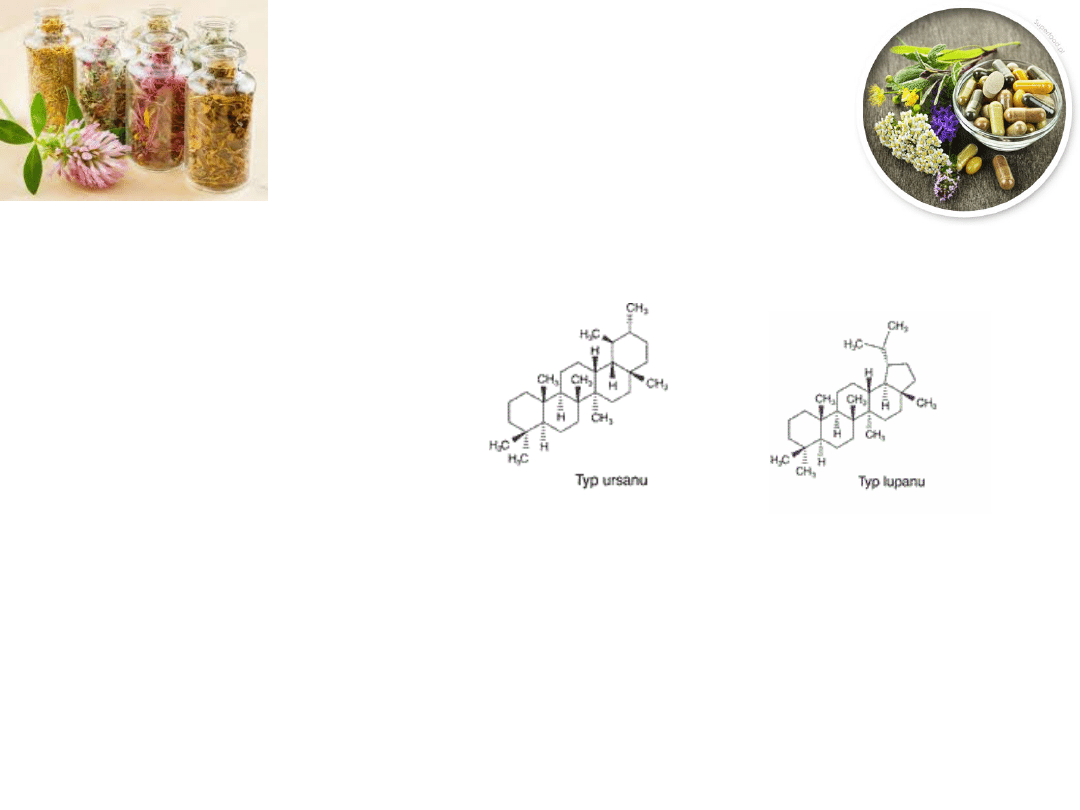
Saponiny triterpenowe
Saponiny triterpenowe są glikozydami trzech pochodnych izomerycznych
względem siebie alkoholi triterpenowych pentacyklicznych o składzie C
30
H
50
O
(składają się z 6 jednostek izoprenu) należących do typu:
ursanu (α-amyryny)
oleananu (β-amyryny)
lupanu (lupeolu)
damaranu
Większość saponin triterpenowych należy do grupy β-amyryny; różnią się one
rodzajem, ilością i położeniem grup funkcyjnych tj. –OH, -CH
2
OH, -COOH,
-CHO, C=O
saponiny triterpenowe mogą mieć charakter obojętny lub słabo kwaśny, który
uwarunkowany jest występowaniem grupy karboksylowej w aglikonie lub
kwasu uronowego w części cukrowej
saponiny obojętne są monodesmozydami
saponiny kwaśne są bidesmozydami (łańcuch cukrowy w pozycji C3 i drugi
połączony estrowo w pozycji C17)

Kumaryny
Kumaryny to pochodne α-pironu i fenylopropanu. Wyróżniamy w tej grupie:
1. Kumaryna - benzo-α-piron - najprostszy związek bez podstawników, stąd
nie tworzy wiązań glikozydowych. Występuje w różnych gatunkach
nostrzyków, marzance wonnej, turówce wonnej (trawka w żubrówce).
2. Hydroksykumaryny i metoksykumaryny - wszystkie są podstawione gr.
– OH przy:
C-7 w hydroksykumarynach,
C-6 i C-7 w dihydroksykumarynach
C-6, C-7 i C-8 w trihydroksykumarynach.
3. Furanokumaryny - benzo-α-piron jest skondensowany z pierścieniem
furanu:
a. w pozycjach C-6, C-7 – typ psolarenu
b. w pozycjach C-7, C-8 – typ angelicyny
4. Piranokumaryny- benzo-α-piron jest skondensowany z pierścieniem
piranu:
a. w pozycjach C-7, C-8 – typ seseliny
b. w pozycjach C-5, C-6 – typ alloksantyletyny
c. w pozycjach C-6, C-7 – typ ksantyletyny

Kumaryny
Związki kumarynowe są rozpowszechnione w świecie roślin, występują
zarówno
w postaci wolnej jak i glikozydowej. Sporadycznie występują w grzybach
(Aspergilus)
i promieniowcach. Poznanych mamy ponad 200 kumaryn, ich zawartość w
roślinie może przekraczać 20% wszystkich związków.
Aktywność farmakologiczna kumaryn:
działają spazmolityczne – piranokumaryny występujące w owocu aminka
egipskiego rozszerzają naczynie wieńcowe i mózgowe poprzez blokowanie
kanałów wapniowych.
przeciwobrzękowo – kumaryny nostrzyka i kasztanowca - usprawniają
krążenie żylne i limfatyczne
właściwości światłochłonne – eskulina i metoksykumaryny – mogą być
wykorzystywane w produkcji preparatów absorbujących promieniowanie UV
fotouczulające – furanokumaryny typu psolarenu – stosowany w
skojarzonym leczeniu łuszczyc, pobudzają pigmentacje skóry w bielactwie,
obniżają krzepliwość krwi – dikumarol – dimer kumaryny wykryty w
gnijącym zielu nostrzyka
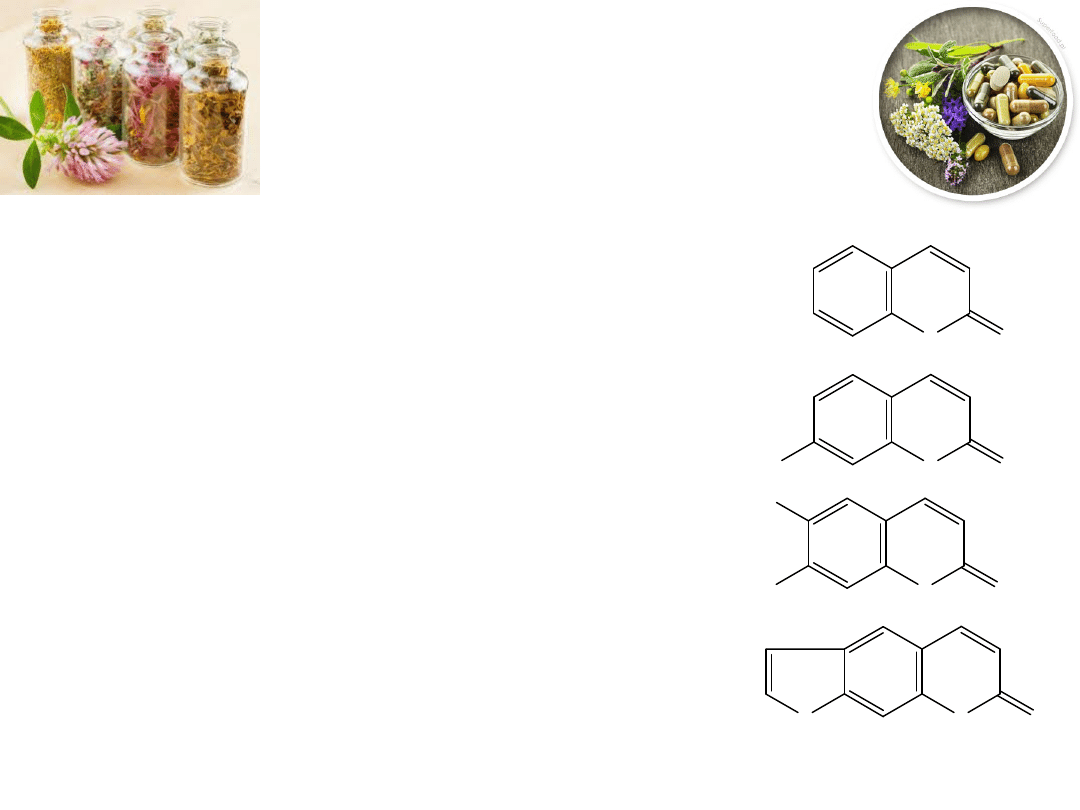
Kumaryny
Kumaryna – benzo-α-piron, działa spazmolitycznie,
przeciwobrzękowo, depresyjnie na OUN, hepato-
toksycznie.
Umbeliferon – 7-hydroksykumaryna – najczęściej
spotykana kumaryna, wykazuje fluorescencje.
Eskulina – zwana także eskulozydem, występuje w
korze
kasztanowca,
wzmacnia
naczynia
krwionośne, działa światłoochronnie.
Psolaren – podstawowa furanokumaryna – jest
związkiem silnie uczulającym na światło, toksyczna.
Stosowany
w leczeniu bielactwa.
O
O
O
O
HO
O
O
HO
HO
O
O
O
Kumaryna
Umbeliferon
Eskulina
Psolaren

Garbniki
GARBNIKI są to bezazotowe substancje o dużej masie cząsteczkowej 500-
3000 jednostek, rozpuszczalne w wodzie, posiadające wiele grup
hydroksylowych. Mają charakter polifenoli. Mogą trwale łączyć się z białkami
ponieważ mają wolne grupy –OH.
Są szeroko rozpowszechnione w prawie wszystkich organach roślin, jednakże
na ogół występują w niskich stężeniach. Większe ilości garbników spotkać
można
w
starych
i zamierających komórkach.
Surowce garbnikowe – tanina, kora dębu, kłącze wężownika, liść orzecha
włoskiego, liść maliny.
Garbniki dzielimy na:
hydrolizujące (galotaniny) – galotaniny i elagotaniny - ulegające całkowitej
hydrolizie na kwas galusowy i cukry proste.
elagenowe (częściowo hydrolizujące) – glikozydy kwasu elagenowego nie
ulegające dalszej hydrolizie.
katechinowe (skondensowane) – flawolany – produkty trwałej kondensacji
kilku cząsteczek katechiny, nie ulegające hydrolizie.

Garbniki
Garbniki hydrolizujące - mają charakter estrów, rzadziej glikozydów,
główny związek to tanina. To związki wielkocząsteczkowe ulegające hydrolizie
kwasowej lub enzymatycznej, zbudowane ze składnika fenolowego i nie-
fenolowego np. cukier, alkohol cukrowy.
Garbniki katechinowe - nie hydrolizują - to polimery katechiny lub
leukantocyjanidyny.
garbniki kory dębu, świerku, sosny, kasztanu , akacji
oligomeryczne garbniki skondensowane to proantocyjanidyny
mają układ flawonu
Właściwości farmakologiczne i działanie:
Większość biologicznych właściwości wiąże się z ich zdolnościami do
tworzenia kompleksów z białkami i polisacharydami:
1. Przeciwzapalne
zewnętrznie – kurczą powierzchniowe naczynia, przyczyniają się do
uszczelnienia włośniczek, działając przeciwysiękowo i przeciwobrzękowo- w
stanach zapalnych skóry i błon śluzowych

Garbniki
słabo znieczulająco- znoszą pieczenie, swędzenie towarzyszące stanom
zapalnym
zabezpieczają skórę i błony śluzowe przed wyschnięciem i chronią warstwy
leżące poniżej przed działaniem niekorzystnych czynników
2. Przeciwbiegunkowo
podane doustnie działają ściągająco na błonę śluzową przewodu
pokarmowego
zmniejszają resorpcję toksyn bakteryjnych
3. Antyseptycznie
działają bezpośrednio na drobnoustroje denaturując białka co ma
znaczenie
w leczeniu biegunek bakteryjnych i schorzeń dermatologicznych
4. Przeciwkrwotocznie
powodują aglutynację erytrocytów i ułatwiają powstawanie skrzepów
włóknikowych, co łącznie z uszczelniającym wpływem na naczynia
włosowate prowadzi do zmniejszenia krwawień
5. Antyoksydacyjne
6. W zatruciach solami metali ciężkich i alkaloidami- ponieważ łączą się
z nimi umożliwiając ich wypłukanie z żołądka.

Antrazwiązki
Antrazwiązki są pochodnymi trójpierścieniowego związku aromatycznego –
antracenu, w zależności od stopniu utlenienia układu podstawowego
wyróżnia się:
antrony
antranole (formy zredukowane)
antrachinony (forma utleniona)
Dodatkowo występują diantrony oraz nafrodiantrony (formy dimeryczne).
Antrachinony i antrony różnią się od siebie stopniem utlenienia
podstawowego szkieletu, natomiast antranole są tautomeryczną formą
antronów.
Antrazwiązki są substancjami stałymi, o czerwonej, pomarańczowej lub żółtej
barwie. Do ich charakterystycznych cech fizykochemicznych należy duża
skłonność do ulegania przemianom oksydoredukcyjnym. Dzieje się tak
podczas suszenia i przechowywania surowców. Sprawia to, że antrazwiązki
występują w surowcach na różnych stopniach utlenienia, a co za tym idzie, w
formach o różnej sile działania.

Antrazwiązki – działanie
farmakologiczne
1) przeczyszczające- wykazują je antrazwiązki posiadające grupy OH przy
pierwszym
i ósmym atomie węgla oraz podstawnik przy trzecim atomie węgla.
Aglikony antrachinonowe ze względu na dobrą rozpuszczalność w lipidach,
są częściowo wchłaniane w jelicie cienkim, natomiast glikozydy dobrze
rozpuszczalne w wodzie, przechodzą z treścią jelitową do jelita grubego,
gdzie pod wpływem flory bakteryjnej podlegają hydrolizie i redukcji.
Powstałe antrony i antranole drażnią bezpośrednio ścianę jelita grubego,
wzmagają jego sekrecję i ruchy perystaltyczne. Efekt przeczyszczający
uzyskuje się po 8-12 godzinach od czasu podania.
2) pobudzają wydzielanie soku żołądkowego.
3) żółciopędne i żółciotwórcze - część wchłoniętych w jelicie cienkim
antrazwiązków dociera do wątroby z krwiobiegiem i prawdopodobnie na
skutek drażnienia miąższu wątroby, wzmaga jej czynności żółciotwórcze.
4) właściwości uczulające na światło UV- wykazują niektóre dimery
pochodne antracenu, np. hyperycyna z ziela dziurawca i fagopiryna z ziela
gryki.
5) działanie dezynfekujące i p/grzybicze - np. chryzarobina stosowana w
dermatologii w schorzeniach skóry (grzybica, łuszczyca).

Antrazwiązki
Efekty uboczne stosowania surowców antrachinonowych:
• nudności
• wymioty
• bolesne skurcze jelit
• przekrwienie jelit
• skurcze mięśniówki gładkiej narządów miednicy
Surowce – aloes uzbrojony, kruszyna pospolita, marzanna barbierska,
rzewień lekarski, dziurawiec zwyczajny.

Gorycze
Gorycze są to bezazotowe związki najczęściej o charakterze glikozydowym,
które wykazują silnie gorzki smak i odruchowo zwiększają wydzielanie śliny,
kwasu solnego, soku jelitowego i trzustkowego. Jest to nazwa o znaczeniu
historycznym, bowiem zbiorcza dla rozmaitych substancji o smaku gorzkim,
często bardzo różnorodnych pod względem chemicznym.
Działają ogólnie wzmacniająco w różnego rodzaju osłabieniach. Polepszają
trawienie, pobudzają apetyt, podwyższają kwasowość soku żołądkowego,
przyspieszają wchłanianie mleczka pokarmowego (strawiony, upłynniony
pokarm) z jelit do krwi i limfy. Większość z nich działa także żółciopędnie i
dlatego stosuje się je w przypadku przewlekłych chorób układu żółciowego.
Glikozydy gorczyczne zawarte są np. w goryczkach (gencjopikrozyd), w
bobrku (loganina), w bylicy (absyntyna), w centurii (amarogentyna).
Do substancji gorzkich należą także olejki gorczyczne, to jest
izotiocyjaninowe
o ogólnym wzorze R-N:C:S. Podstawową strukturą olejków gorczycznych jest
układ izonitryli. Działają silnie odkażająco i żółciotwórczo (np. rzodkiew,
gorczyca).
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
Wyszukiwarka
Podobne podstrony:
4 Monika Kowalewska zut
7 Monika Kowalewska zut
2 Monika Kowalewska zut
więcej podobnych podstron