WS TiP
dysocjacja elektrolityczna,
reakcje w roztworach wodnych,
pH
wykład nr 2b
Elektrolity i nieelektrolity
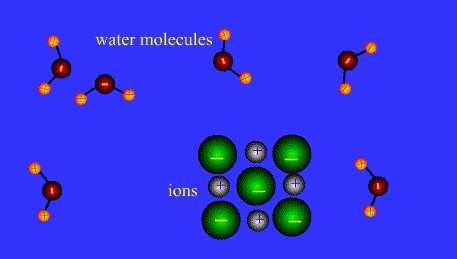
Wpływ polarnej budowy cząsteczki wody na proces
rozpuszczania kryształu jonowego i
cząsteczkowego
Definicja dysocjacji jonowej
Proces dysocjacji kwasów, zasad i soli.
Elektrolity:
kwasy, zasady i sole podczas rozpuszczania w wodzie
rozpadają się na elementy naładowane elektrycznie, czyli ulegają tzw. dysocjacji elektrolitycznej(jonowej). Elementy te nazwano jonami. Jony naładowane dodatnio nazywa się kationami, a ujemne anionami.
suma ładunków elektrycznych kationów i anionów, powstających na skutek dysocjacji elektrolitycznej elektrolitów jest zawsze równa zeru.
Nieelektrolity:
substancje, które w roztworach i w stanie stopionym nie przewodzą prądu elektrycznego, nie ulegają dysocjacji
elektrolitycznej.
właściwości chemiczne jonów różnią się zupełnie od własności obojętnych atomów i cząsteczek
Nie wszystkie substancje dysocjują w roztworach wodnych.
Warunkiem takiego zachowania się jest odpowiednia budowa i rodzaj wiązania w cząsteczkach związku chemicznego.
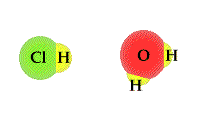
Cząsteczki wody mają budowę polarną, są dipolami:
δ-
O
H
H
δ+
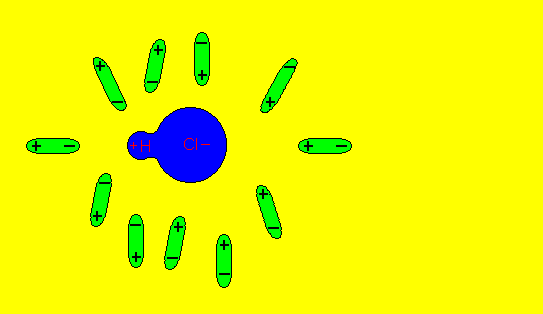
mechanizm dysocjacji
W rezultacie dipole wody powodują osłabienie, a następnie rozerwanie wiązania związku i uwolnienie jonów na : dodatni kation H+ i ujemny anion B- (przykład: dysocjacja HCl)
HCl
<=>
H+ + Cl –
Jeżeli równowaga dysocjacji jest przesunięta w kierunku tworzenia jonów, to w roztworze nie ma (jest bardzo mało) cząsteczek niezdysocjowanych. Takie roztwory bardzo dobrze przewodzą prąd elektryczny.


mechanizm dysocjacji
Definicja dys ocjacji
elektrolitycznej
Cząsteczki substancji rozpuszczonej pod wpływem cząsteczek wody ulegają w roztworze rozpadowi na jony dodatnie(kationy) i jony ujemne(aniony) jest to proces dysocjacji elektrolitycznej.
elektrolitycznej kwas ów,
zas ad i s oli
Kwasami są związki chemiczne, które podczas rozpuszczania w wodzie dysocjują całkowicie lub częściowo na kationy wodorowe i aniony reszt kwasowych. Dysocjację tę można przedstawić następująco:
HNO --> H+ + NO -
3
3
H SO --> 2H+ + HSO 2-
2
4
4
elektrolitycznej kwas ów,
zas ad i s oli
Kwasy takie jak HNO3, które w czasie dysocjacji odczepiają jeden kation wodorowy nazywamy jednoprotonowymi. Kwasy posiadające w cząsteczkach dwa atomy wodoru zdolne do oddysocjowania w postaci kationów - dwuprotonowymi, trzy-, trójprotonowymi
elektrolitycznej kwas ów,
zas ad i s oli
Zasady są to związki chemiczne, które podczas
rozpuszczania w wodzie dysocjują całkowicie lub
częściowo na aniony wodorotlenowe OH- i kationy
metali. A oto równania dysocjacji niektórych
zasad.
NaOH --> Na+ + OH-
KOH --> K+ + OH-
Ca(OH) --> Ca2+ + 2OH-
2
elektrolitycznej kwas ów,
zas ad i s oli
Sole są produktami reakcji kwasów z zasadami.
Związki te w temperaturze pokojowej występują na
ogół w stanie stałym, krystalicznym i mają budowę
jonową, czyli składającą się z kationów metali lub
kationu amonowego i anionów reszt kwasowych.
elektrolitycznej kwas ów,
zas ad i s oli
Proces rozpuszczania soli w wodzie polega zatem na przechodzeniu do roztworu istniejących już w krysztale kationów i anionów. Jonowa budowa soli tłumaczy również zdolności przewodzenia prądu przez stopione sole.
NaCl <=> Na+ + Cl-
dys ocjacji
Definicja stopnia dysocjacji.
Zależność stopnia dysocjacji od rodzaju elektrolitu i stężenia elektrolitu.
Elektrolity słabe i mocne.
Definicja s topnia dys ocjacji
Do porównania mocy elektrolitów Arrhenius wprowadził pojęcie stopnia i stałej dysocjacji elektrolitycznej.
Stopień dysocjacji elektrolitu określa się stosunkiem liczby moli cząsteczek zdysocjowanych na jony do liczby moli cząsteczek substancji rozpuszczonej.
x
α = -----
n
gdzie: (alfa) - stopień dysocjacji, x - liczba moli cząsteczek zdysocjowanych na jony, n - liczba moli cząsteczek substancji rozpuszczonej
Zależnoś ć s topnia dys ocjacji
od rodzaju elektrolitu i
s tężenia roztworu
Stopień dysocjacji wzrasta z rozcieńczeniem elektrolitu i w roztworach bardzo rozcieńczonych wszystkie elektrolity
wykazują stopień dysocjacji zbliżony do jedności, tzn.
niemal wszystkie cząsteczki lub zgrupowania jonów
substancji rozpuszczonej ulegają zdysocjowaniu na jony.
Elektrolitami mocnymi nazywamy takie związki, które w niezbyt stężonym roztworze wodnym są całkowicie zdysocjowane na jony. Ich stopień dysocjacji jest równy jedności. Do elektrolitów mocnych należą prawie wszystkie sole oraz niektóre kwasy i zasady (H SO , HNO , HCl, NaOH, KOH).
2
4
3
Elektrolitami słabymi nazywamy takie związki, które w roztworze wodnym tylko częściowo dysocjują na jony, a więc roztwór oprócz jonów zawiera zawsze cząsteczki
niezdysocjowane. Stopień dysocjacji słabych elektrolitów jest mniejszy od jedności ponieważ rośnie wraz z rozcieńczeniem roztworu więc przy określaniu jego wartości należy zawsze uwzględniać stężenie elektrolitu.
Należą do nich wszystkie kwasy organiczne oraz pozostałe kwasy i zasady nie wymienione w mocnych elektrolitach.
cząs teczkowy i jonowy
1.
Przykład reakcji zobojętniania.
2.
Cząsteczkowy, jonowy i jonowy skrócony zapis równań
reakcji zobojętniania.
3.
Stosunki stechiometryczne w reakcjach zobojętniania.
Przykład reakcji zobojętniania
Jedną z ważniejszych reakcji chemicznych jest reakcja
zobojętniania. Przedstawia ona połączenie jonu hydroniowego z jonem wodorotlenowym
H O+ + OH- --> 2H O
3
2
Jest to reakcja odwrotna do reakcji dysocjacji wody. Wyjaśnia to fakt, że o ile zmieszamy kwas i zasadę, to w wyniku reakcji tworzy się woda jako produkt końcowy, czemu towarzyszy efekt cieplny 13,8 kcal/mol.
Całkowitą reakcję zobojętniania można ująć następująco:
H O+ + A- + B+ + OH- --> 2H O + B+ + A-
3
2
Drugi obok wody produkt tej reakcji (B+ + A-) nazywany jest solą.
zobojętniania
NaOH + HCl --> NaCl + H O
2
Ca(OH) + 2 HNO --> Ca(NO ) + 2H O
2
3
3 2
2
zobojętniania
Na+ +OH - + H + + Cl- → Na+ + H O + Cl-
2
Ca2+ + 2 OH - + 2 H + + 2 Cl- → Ca2+ + 2 H O + 2 Cl-2
Podkreślone jony biorą udział w tworzeniu cząsteczki wody, pozostałe występują w tej samej postaci przed i po reakcji (nie biorą więc udziału w reakcji).
reakcji zobojętniania
2 OH- + 2 H+ → 2 H O
/ :2
2
OH- + H+ → H O
2
S tos unki s techiometryczne ,
a rodzaj pows tałej s oli
Ilość użytych substancji powoduje całkowite zobojętnienie jonów H+
powstanie soli obojętnej, natomiast w przypadku innej proporcji możemy otrzymać wodorosól (metal + wodororeszta)- aby z niej otrzymać sól obojętną należy wodór zastąpić metalem.
Możemy także otrzymać hydroksosól (metal z resztą OH + reszta kwasowa)- aby z niej otrzymać sól obojętną należy grupy OH
zastąpić resztą kwasową (resztami).
Definicja reakcji strąceniowych
Przykłady reakcji
Zapisy reakcji
Tablice rozpuszczalności
s trąceniowej
Jest to reakcja między jonami, które łącząc
się,dają trudnorozpuszczalny związek.
Cu2+ + 2 OH- → Cu(OH) (Skrócony)
2
Cu2+ +SO 2- + 2 K+ + 2 OH- → Cu(OH) + 2 K+
4
2
+SO 2- (Jonowy)
4
CuSO + 2 KOH → Cu(OH) + K SO
4
2
2
4
(Cząsteczkowy)
Ag+ + Cl- → AgCl
Znajomość rozpuszczalności różnych związków
trudnorozpuszczalnych pozwala więc przewidzieć
przebieg reakcji i sposób wydzielania produktów.
Istnieją odpowiednie tablice rozpuszczalności związków, z których można w razie potrzeby skorzystać. W
tablicach przy pomocy symboli i kolorów przedstawia się barwę powstałego roztworu lub osadu
Cechą charakteryzującą kwasowe lub zasadowe
właściwości roztworów jest ich odczyn. Nadmiar jonów
wodoru H+ powoduje odczyn kwasowy roztworu, nadmiar
jonów wodorotlenkowych OH - odczyn zasadowy roztworu,
natomiast gdy jest równowaga między tymi jonami
uzyskujemy odczyn obojętny roztworu.
Miara odczynu roztworu - pH
pH definiujemy jako ujemny logarytm dziesiętny z
wartości liczbowej stężenia jonów hydroniowych
pH = - lg[H O+]
3
analogicznie
pOH = - lg[OH-]
Ponieważ stężenie czystej wody w wodzie jest wielkością stałą to iloczyn K * [H O]2 jest również wielkością stałą i nazywany jest 2
iloczynem jonowym wody K .
w
K = K * [H O]2 = [H O+] * [OH-] = 10-14 (mol/dm3)
w
2
3
W temperaturze 298,15oK stężenie jonów hydroniowych w czystej wodzie jest równe stężeniu jonów wodorotlenowych i wynosi:
[H O+] = [OH-] = 1,00 * 10-7 mol/dm3
3
Podobnie jak w czystej wodzie, również we wszystkich
roztworach obojętnych [H O+] = 10-7 mol/dm3. W roztworach 3
kwaśnych [H O+] > 10-7 mol/dm3 a w roztworach zasadowych 3
[H O+] < 10-7 mol/dm3.
3
Posługiwanie się tak małymi stężeniami jest niewygodne w zapisach i obliczeniach. Dlatego przyjęto wyrażać aktywność jonów wodorowych w roztworze w tzw. skali pH
pH
0
3
7
11
14
[H O+]
3
100
10-3 10-7
10-11 10-14
mol/dm3
Sole pochodzące od mocnych kwasów i słabych zasad ulegają hydrolizie kationowe – roztwór wodny wykazuje odczyn kwasowy.
Sole pochodzące od słabych kwasów i mocnych zasad ulegają hydrolizie anionowej – roztwór wodny wykazuje odczyn
zasadowy.
Sole pochodzące od słabych kwasów i słabych zasad ulegają hydrolizie kationowo-anionowej – roztwór wodny wykazuje odczyn obojętny lub słabo zasadowy, lub słabokwasowy.
Sole mocnych zasad i mocnych kwasów nie ulegają
hydrolizie – roztwór obojętny.
odczynu wodnych
roztworów s oli
Odczyn kwasowy roztworu powoduje nadmiar powstałych
jonów H+ (hydroliza kationowa).
Odczyn zasadowy roztworu powoduje nadmiar powstałych
jonów OH- (hydroliza anionowa)
Odczyn obojętny powstaje gdy moc słabego kwasu i słabej zasady jest zbliżona (hydroliza kationowo-anionowa)
Wyszukiwarka
Podobne podstrony:
Chemia wyklad I i II (konfiguracja wiÄ…zania Pauling hybrydyzacja wiazania pi i sigma)
Chemia Wykład 6
pytania testowe i chemia budowlana -zestaw3, Szkoła, Pollub, SEMESTR II, chemia, wykład, testy
Chemia Wyklad 4 id 111675
chemia wykłady (6)
Chemia Wykład 9
ściąga chemia wykład, Studia, Sem 1,2 +nowe, ALL, szkoła, Chemia
chemia wykład
(CHEMIA WYKŁAD 7)
chemia wyklady wskrzynka(1), BUDOWNICTWO PŁ, Semestr I, chemia wykład
10.dysocjacja wykład, AGH różne, chemia wykłady
Chemia wykłady, koło II sem v.3.0 - do nauki, Izomeria optyczna
chemia wykład 2
3 chemiaogolna wyklad 061009
chemia wykłady (2)
pytania testowe i chemia budowlana -zestaw1, Szkoła, Pollub, SEMESTR II, chemia, wykład, testy
więcej podobnych podstron