1. Korozja definicja, skutki, podział
Korozją jest nazywane oddziaływanie fizykochemiczne i elektrolityczne między materiałem metalowym a otaczającym środowiskiem, w wyniku którego następuje uszkodzenie korozyjne powodujące zmniejszenie własności metalu.
Ze względu na typ reakcji powodujących niszczenie metalu i stopów istnieje korozja :
elektrochemiczna
chemiczna
Skutki:
Korozja powoduje znaczne obniżenie własności mechanicznych i użytkowych maszyn, urządzeń i elementów, np. kotłów parowych, konstrukcji mostów, łopatek turbin, instalacji chemicznych, zbiorników, rurociągów, samochodów, istotnie zmniejszając bezpieczeństwo ich stosowania. Dotyczy to ok. 30% ogólnej liczby produktów z metali i ich stopów.
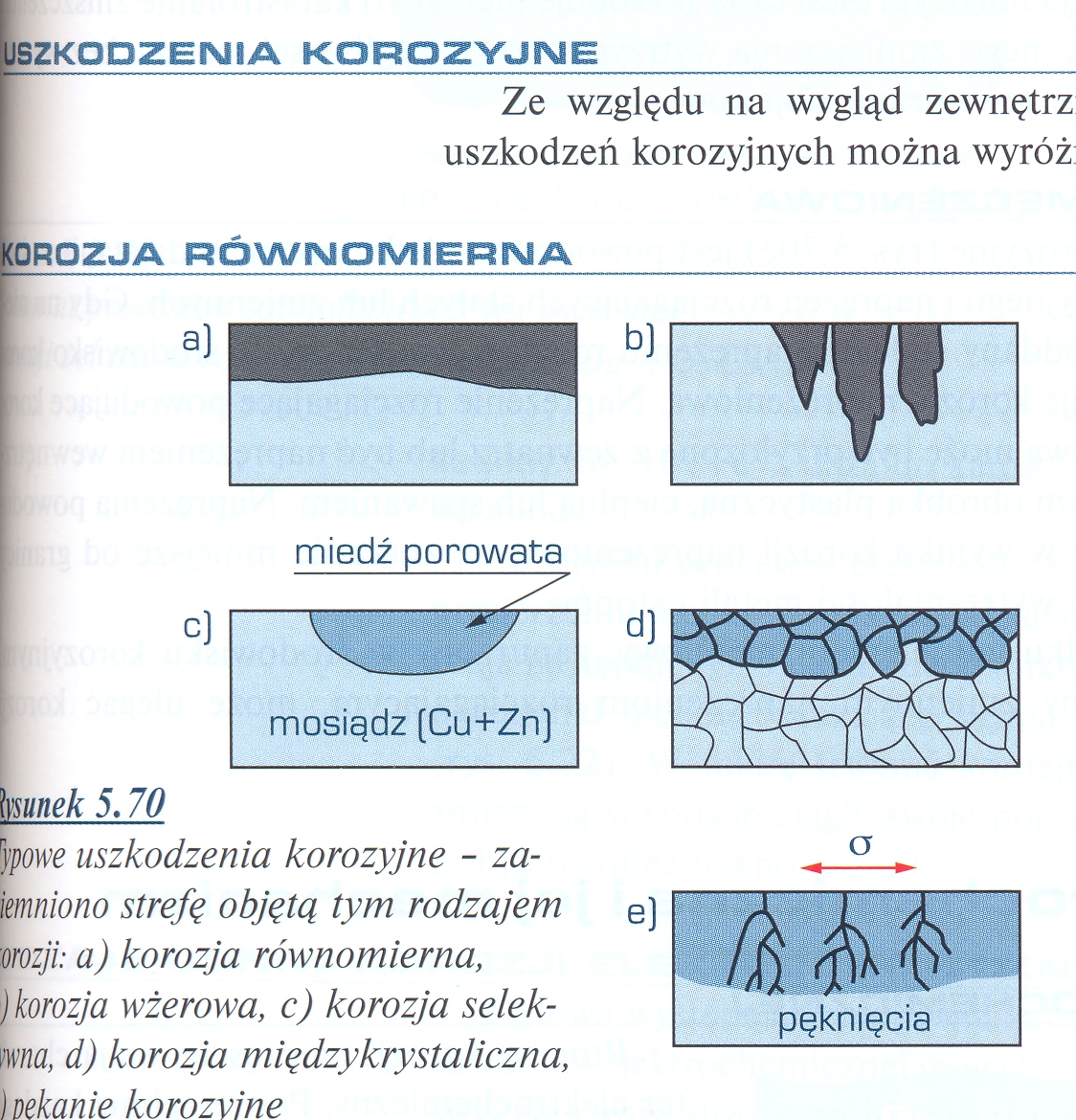
Ze względu na wygląd zewnętrzny i zmiany własności fizycznych wyróżnić można kilka zasadniczych odmian:
korozja równomierna
korozja wżerowa
korozja selektywna
korozja międzykrystaliczna
pękanie korozyjne
2. Przebieg korozji elektrochemicznej
Procesy korozji najczęściej mają charakter elektrochemiczny. Powierzchnię każdego metalu stanowi zbiór elektrod dodatnich i ujemnych, zwartych przez sam metal.
Powierzchnia każdego metalu lub stopu stanowi zbiór elektrod dodatnich i ujemnych, pomiędzy którymi występuje różnica potencjałów
Gdy na metal działa elektrolit (kwas, woda, wodne roztwory soli), tworzą się lokalne mikroogniwa i lokalny przepływ prądu elektrycznego
Towarzyszą temu reakcje redukcji i utleniania
Reakcja redukcji zachodzi na elektrodzie zwanej katodą. Polega na przepływie elektronów, anionów np. Cl-, OH-, do anody.
Reakcja utleniania zachodzi na anodzie. Polega na przepływie kationów, np. H+, Fe2+, z anody do katody.
Korozja następuje tylko na anodach mikroogniw, gdzie zwykle tworzą się sole, lub wodorotlenki.
3. Czynniki decydujące o przebiegu korozji elektrochemicznej
Skłonność metalu lub stopu do korozji elektrochemicznej wzrasta wraz ze zwiększeniem siły elektromotorycznych ogniw korozyjnych.
Metale uporządkowano w tak zwanym szeregu napięciowym według malejących standardowych potencjałów utleniających, tj. potencjałów równowagi danego metalu z jego jonami o jednostkowej aktywności (większa aktywność większa podatność na korozję)
O przebiegu korozji elektrochemicznej decyduje również środowisko korozyjne.
Mechanizm korozji elektrochemicznej występuje w środowisku wodnym, wodnych roztworach kwasów, soli i zasad.
Korozji elektrochemicznej ulegają również metale i stopy zakopane w ziemi i podlegającym działaniu prądów błądzących (źródła prądów błądzących np. elektryczne linie kolejowe, tramwajowe, elektryczne urządzenia spawalnicze, galwanizernie, uziemione linie wysokiego napięcia)
4. Przebieg korozji gazowej
Proces korozji chemicznej polega na niszczeniu metali i stopów w wyniku reakcji chemicznych. W odróżnieniu od korozji elektrochemicznej korozja chemiczna przebiega na sucho, bez udziału elektrolitu. Podstawowym typem reakcji powodujących korozję gazową przede wszystkim podczas obróbki plastycznej i cieplnej jest reakcja chemiczna utleniania, którą dla najprostszego przypadku utleniania czystego metalu dwuwartościowego można przedstawić następująco:
M + 0,5 X2 -> MX
M-metal
X2-utleniacz, np. O2, S2, N2
Etapy elementarnej reakcji utleniania:
Adsorpcja (gromadzenie się na powierzchni metalu cząstek utleniacza) lub chemisorpcja (gromadzenie się na powierzchni metalu cząstek utleniacza i tworzenie połączeń chemicznych z metalem)
Powstawanie jonów utleniacza na powierzchni adsorbującej warstwy i wbudowanie się w sieć krystaliczna metalu
Dyfuzja (przepływ) jonów metali i elektronów od metalu do zgorzeliny
Dyfuzja odrdzeniowa jonów metalu i elektronów od granicy faz rdzeń metalowy-zgorzelina do powierzchni warstwy przez defekty sieciowe
Dyfuzja dordzeniowa jonów utleniacza
Czynniki wpływające na korozję gazową
Skład chemiczny atmosfery korozyjnej
Temperatura
Rodzaj metalu
Skład chemiczny stopu
5. Mechanizmy powstawania zgorzelin na czystych metalach i ich stopach
Szybkość elementarnych procesów cząstkowych reakcji utleniania metali i stopów zależy od temperatury i ciśnienia.
W wysokiej temperaturze reakcje chemiczne przebiegają szybciej niż dyfuzja jonów metalu lub utleniacza przez warstwę zgorzeliny.
Z tego powodu dyfuzja określa szybkość reakcji sumarycznej.
Produkty reakcji utleniania metalu zwykle występują w stanie stałym, rzadko w stanie ciekłym lub gazowym.
Warstwy stałego produktu reakcji utleniania w zależności od grubości są nazywane:
Zgorzelinami jeśli ich grubość jest większa od 10 um.
Warstwami nalotowymi - grubość mniejsza od 10 um.
Mechanizm jonowo-ektronowy powstawania zgorzelin zwartych jednofazowych.
Gdy zgorzelinę tworzy związek o niedomiarze atomów metalu typu M1-xX np. NiO; Cu2O3; FeO o szybkości reakcji decyduje dyfuzja odrdzeniowa jonów metalu przez wakanse kationowe, w których występują braki jonów metalu, oraz dyfuzja elektronów przez dziury dodatnie, w których występują braki elektronów
Gdy zgorzelinę tworzy związek o nadmiarze atomów metalu w sieci typu M1+xX np. ZnO; Al2O3; TiO2 o szybkości reakcji decyduje dyfuzja odrdzeniowa jonów metalu przez przestrzenie międzywęzłowe, wraz z dyfuzją elektronów przez dziury dodatnie, do zewnętrznej powierzchni elektronów.
Zgorzelina wielofazowa powstaje na metalu, gdy w podwyższonej temperaturze metal tworzy z utleniaczem kilka związków trwałych termodynamicznie o różnym stopniu utlenienia.
6. Zasady doboru składu chemicznego stopów odpornych na korozje
Zasady doboru składu chemicznego stopów w celu zwiększenia odporności na korozję elektrochemiczną
Podatność metali i stopów na korozję elektrochemiczną zależy od składu chemicznego i struktury fazowej stopu. Odpowiedni dobór składu chemicznego powoduje przesunięcie standardowego potencjału elektrodowego stopu do wartości dodatnich, zapewniając wysoką odporność na korozję. Działanie takie wywołuje chrom w stali o zaw. 13%.
Wysoką odporność na korozję elektrochemiczną wykazują stopy lub metale jednofazowe, gdyż nie występują na ich powierzchni mikroogniwa między dwiema fazami. Dążenie do uzyskania struktury jednofazowej stanowi jedą z zasad doboru składu chemicznego stali i stopów odpornych na korozję elektrochemiczną.
Zasady doboru składu chemicznego stopów w celu zwiększenia odporności na korozję gazową
Skład chemiczny stali i jego zdolność do tworzenia zgorzeliny stanowiącej jednocześnie rolę warstwy ochronnej, należy do najistotniejszych czynników decydujących o przebiegu korozji gazowej.
Dobre własności ochronne wykazuje zgorzelina w postaci ciągłej warstwy jednofazowej związku - np. BX utworzona na powierzchni przez dodatek stopowy o znacznym powinowactwie chemicznym z utleniaczem. Dodatkami takimi są: Zn, Al., Si, Cr, Be i Mg.
Istotne jest przy tym, by związek ten ściśle przylegał do rdzenia metalicznego i nie tworzył niskotopliwych eutektyk.
7. Ochrona katodowa
Metodą tą można chronić:
Stale, miedź, ołów, mosiądze pracujące w roztworach wodnych lub glebie.
Metale i stopy pasywne takie jak aluminium lub stal odporna na korozję
Stale niskowęglowe, magnez
Metale i stopy ulegające korozji naprężeniowej i zmęczeniowej
Stale kwasoodporne i duraluminium uegające korozji międzykrystalicznej
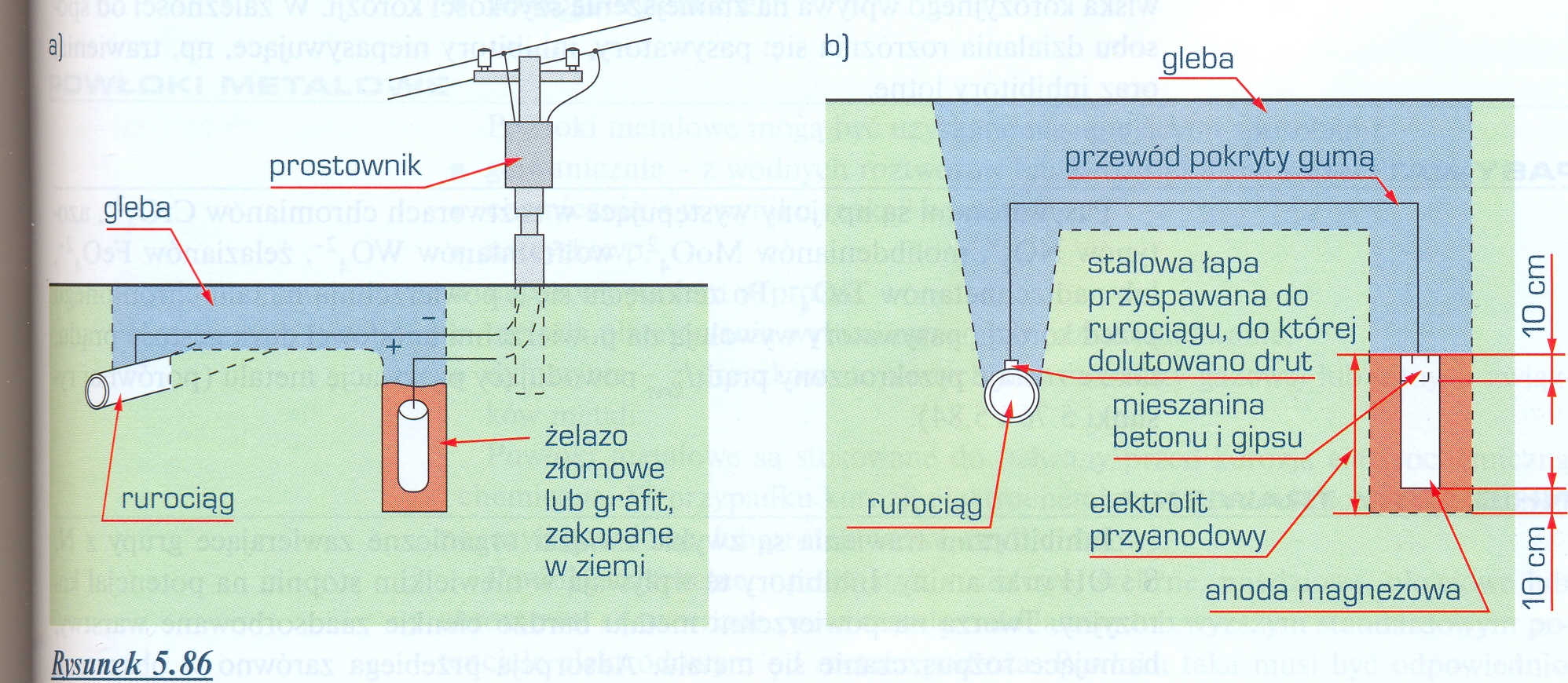
Ochrona katodowa polega na polaryzacji zewnętrznym prądem metalu, na powierzchni którego występują lokalne ogniwa korozji elektrochemicznej.
Prąd ze źródła prądu stałego płynie przez elektrodę odniesienia (anodę) z dowolnego metalu i elektrolit do metalu korodującego, a następnie do źródła prądu.
W wyniku polaryzacji elektrody katodowe występujące na powierzchni metalu korodującego osiągają potencjał anody ogniwa otwartego.
Następuje zatem wyrównanie potencjału na całej powierzchni metalu i nie występuje przepływ prądu korozyjnego, a zatem nie występuje korozja.
8. Ochrona protektorowa
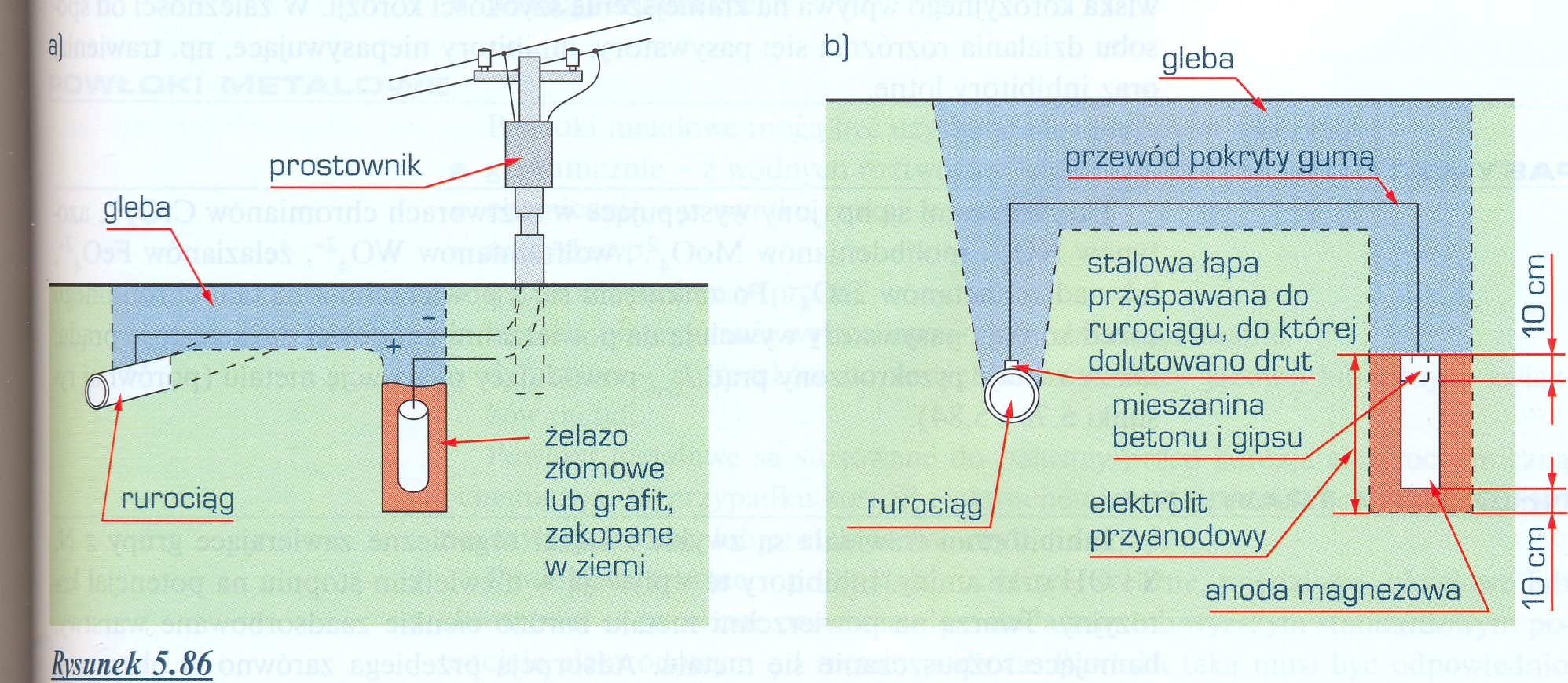
Ochrona protektorowa jest odmianą ochrony katodowej. Jeżeli zewnętrzna elektroda charakteryzuje się niższym potencjałem elektrodowym w szeregu napięciowym niż chroniony metal, nie trzeba stosować zewnętrznego źródła prądu stałego.
Anoda taka zwana protektorową, którą zwykle stanowi magnez, cynk lub aluminium, wykazuje w stosunku do stali niewielką różnicę potencjału, np. w wodzie morskiej od ok. -1,3 V dla Mg do -0,8 V dla Zn.
9. Anodowa ochrona przed korozja
Ochrona anodowa znacznie zmniejsza szybkość korozji, lecz nie powoduje jej całkowitego ustania. Metodą tą mogą być chronione zbiorniki i cysterny do przewozu i magazynowania kwasów siarkowego i fosforowego, wodorotlenków oraz roztworów soli, np. siarczanów. Ochrony anodowej nie można stosować w przypadku działania na stale kwasu solnego i roztworów wodnych chlorków. Ochrona anodowa nie może być stosowana do cynku, mangany, srebra, miedzi i ich stopów.
10. Działanie ochronne inhibitorów dodawanych do środowisk korozyjnych
Inhibitorem jest nazywana substancja chemiczna, która po dodaniu do środowiska korozyjnego wpływa na zmniejszenie szybkości korozji.
W zależności od sposobu działania rozróżnia się: pasywatory, inhibitory niepasywujące, np. trawienia oraz inhibitory lotne.
Pasywatory po zetknięciu się z powierzchnią metalu chronionego przed korozją pasywatory wywołują na powierzchni anodowej prąd większy od prądu Ikryt powodujący pasywację metalu.
Inhibitory trawienia wpływają w niewielkim stopniu na potencjał korozyjny. Tworzą na powierzchni metalu bardzo cienkie zaadsorbowane warstwy, hamujące rozpuszczanie się metalu.
Inhibitory lotne środki te są używane do czasowego zabezpieczenia przed korozja np. łożysk kulkowych i umożliwiają ich stosowanie bez czyszczenia.
11. Jakie są rodzaje powłok ochronnych stosowanych w celu zapobieżenia korozji? Na czym polega ich działanie?
Powłoki nieorganiczne:
Najczęściej są to powłoki ceramiczne, np. z emalii szklanych. Całkowicie nie przepuszczają wody i tlenu.
Chronią metale, stal a także wolfram, molibden i tytan do temperatury 750oC.
Stosuje się m.in. Do ochrony elementów wylotowych silników lotniczych, a także w naczyniach kuchennych.
Warstwy fosforanowane - nakłada się na nie farby malarskie itd.
Powłoki organiczne:
Są to powłoki malarskie, stanowiące mieszaninę nierozpuszczalnych pigmentów w nośniku organicznym lub wodzie
Nośniki olejowe w zetknięciu z olejem polimeryzują, żywice syntetyczne polimeryzują lub wysychają przez odparowanie tworząc na powierzchni cieniutką warstwę zapobiegającą korozji.
W zależności od użytych materiałów rozróżnia się:
-powłoki metalowe
-powłoki nieorganiczne
-powłoki organiczne
Powłoki metalowe mogą być uzyskane następującymi sposobami:
*galwaniczne - z wodnych roztworów lub z roztopionych soli
*chemiczne - w wyniku reakcji wymiany
*natryskowo
*naparowymi w próżni
*metodą platerowania wybuchowego lub przez walcowanie
*dyfuzyjnie - z proszków stopionych metali, z fazy gazowej lub lotnych związków metali.
Powłoki metalowe
Powłoki metalowe są stosowane do ochrony przed korozją elektrochemiczną i chemiczną. W przypadku korozji elektrochemicznej powłoki mogą być szlachetne, czyli katodowe, lub protektorowe, czyli anodowe. Powłoki szlachetne są tworzone przez metale o dodatnim lub wyższym standardowym potencjale elektrodowym od metalu podłoża. Powłoka taki musi być odpowiednio gruba gdyż w przypadku odsłonięcia przebiega bardzo intensywnie korozja elektrochemiczna. Powłoki szlachetne powodują ochronę katodową metalu podłoża. Warunkiem skuteczności ochrony jest trwały styk powłoki z metalem podłoża oraz odpowiednio wysoki prąd płynący w utworzonym ogniwie galwanicznym od powłoki metalu podłoża. Grubość powłoki decyduje o czasie ochrony katodowej podłoża.
Powłoki nieorganiczne
Najczęściej stosowane z tej grupy to powłoki ceramiczne. Bardzo dobre własności powłok ceramicznych polegają na całkowitej nieprzepuszczalności dla wody i tlenu. Stosuje się je w celu zabezpieczenia przed utlenianiem w temperaturze niż wyższej niż ok. 750oC, np. w układach wylotowych silników lotniczych.
Powłoki organiczne
Powszechny sposób zapobiegania przed korozją, polega na pokrywaniu metalu powłokami malarskim, stanowiącymi mieszaninę nierozpuszczalnych cząstek pigmentów w nośniku organicznym lub wodzie. Warstwy malarskie powinny stanowić barierę dla dyfuzji par gazów, wykazywać własności inhibitora korozji oraz duża trwałość. Elementy metalowe można zabezpieczyć przed działaniem ciekłych i gazowych środowisk korozyjnych również przez pokrycie warstwą gumy lub tworzyw sztucznych.
12. Narysuj schematy ochrony katodowej i protektorowej rurociągów zakopanych w ziemi.
Ochrona katodowa: Ochrona anodowa:
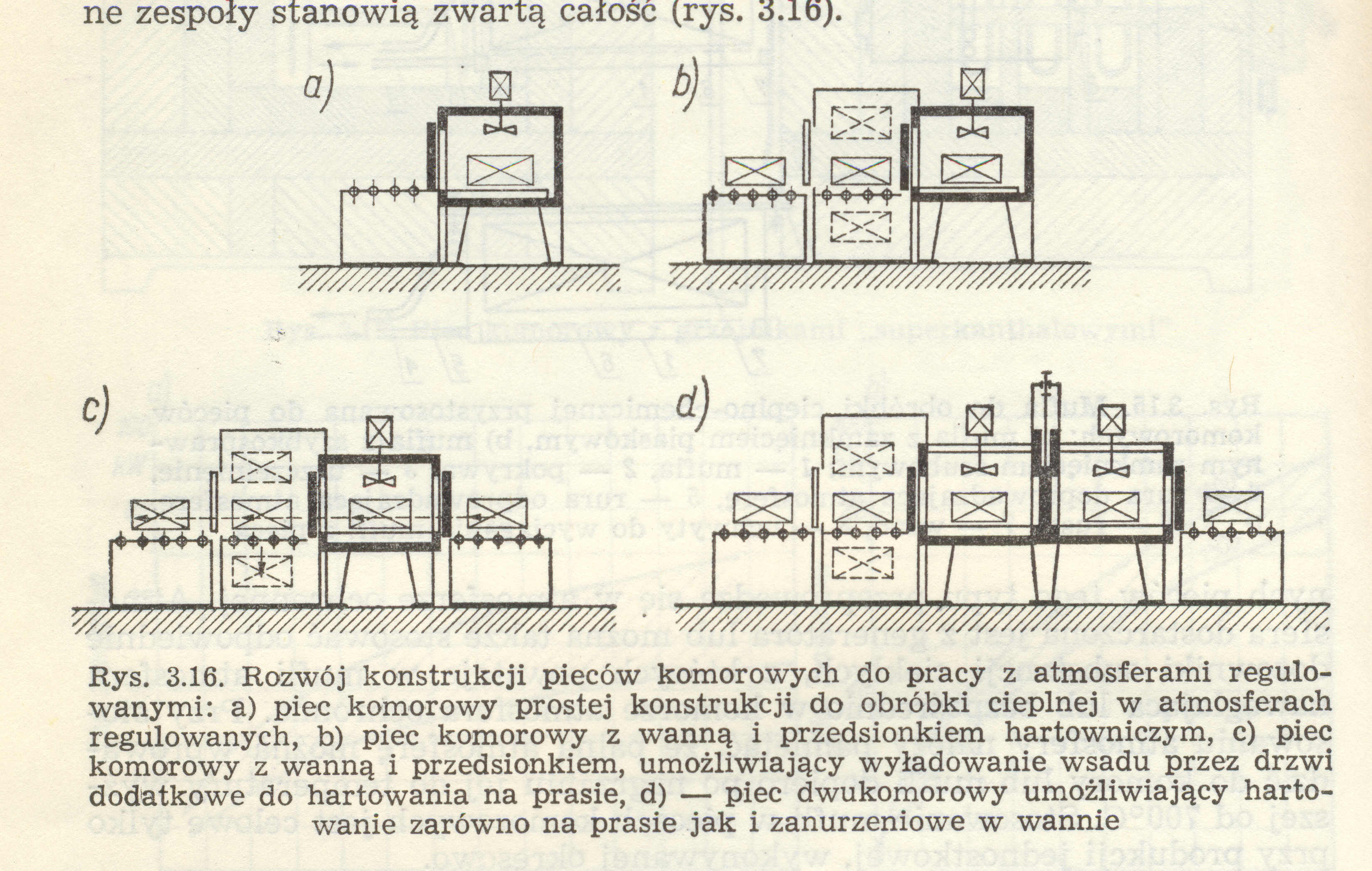
13. Piec komorowy
niskotemperaturowe do 700oC - wymiana ciepła na drodze konwekcji, ruch powietrza wymuszony jest przez specjalny wentylator. Energię grzejną stanowi elektryczność lub gaz opałowy
średniotemperaturowe 700-1000oC - wymiana ciepła przez promieniowanie, nie potrzeba wentylatorów. Stosowana jest atmosfera naturalna lub ochronna. Grzejniki rozmieszczone równomiernie na wszystkich ścianach oraz na drzwiach.
Wysokotemperaturowe 1000-1600oC - komory wykonanae tylko z materiałów zeramicznych, dwa rodzaje grzejników: sility (spiekane węgliki krzemu -1350-1400oC) lub superkanthal (spiekane krzemki molibdenu 1600oC)
Piec komorowy z wanną hartowniczą i przedsionkiem
Po kolei:
nowy element wjeżdża do przedsionka
następnie zostaje wywindowany do góry gdzie może zostać wstępnie ogrzany
rozgrzany już wcześniej element będący już w piecu wyjeżdża z pieca i trafia do przedsionka
następnie element będący niedawno w piecu zjeżdża do wanny z kąpielą w celu zahartowania
w między czasie zjeżdża na dół ten pierwszy element co był u góry i który czekał w kolejce do pieca
nowy element, który tyle czekał wjeżdża w końcu do komory pieca
schłodzony i zahartowany już element zostaje wywindowany do poziomu zero - przedsionka
zahartowany element wyjeżdża z przedsionka jako gotowy produkt
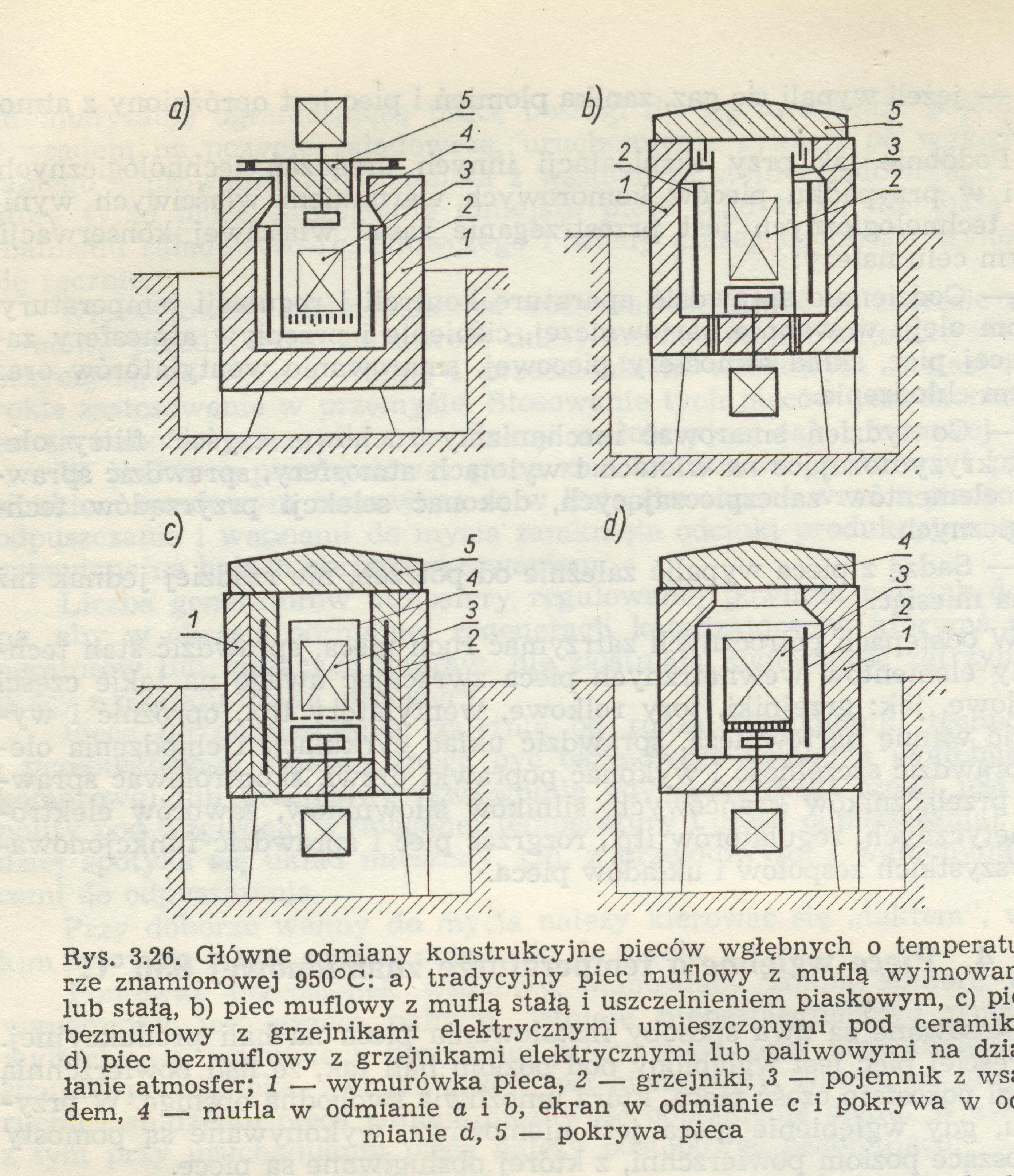
14. Piece wgłębne
Piec muflowy z muflą wyjmowaną lub stałą
1 - wymurówka
2 - grzejniki
3 - wsad
4 - mufla (retorta)
5 - pokrywa
Najczęściej piec jest wgłębiany pod poziom hali, nad powierzchnią podłogi pozostaje tylko taka część pieca, która konieczna jest do łatwej obsługi. Płaszcz zewnętrzny pieca wykonany jest z blachy cienkiej, ściany boczne i spód pieca wykonane są z ceramiki ognioodpornej i materiałów izolacyjnych. Buduje się dwie odmiany: bezmuflowe oraz z muflą.
15. Zasada konstrukcji pieca bębnowego
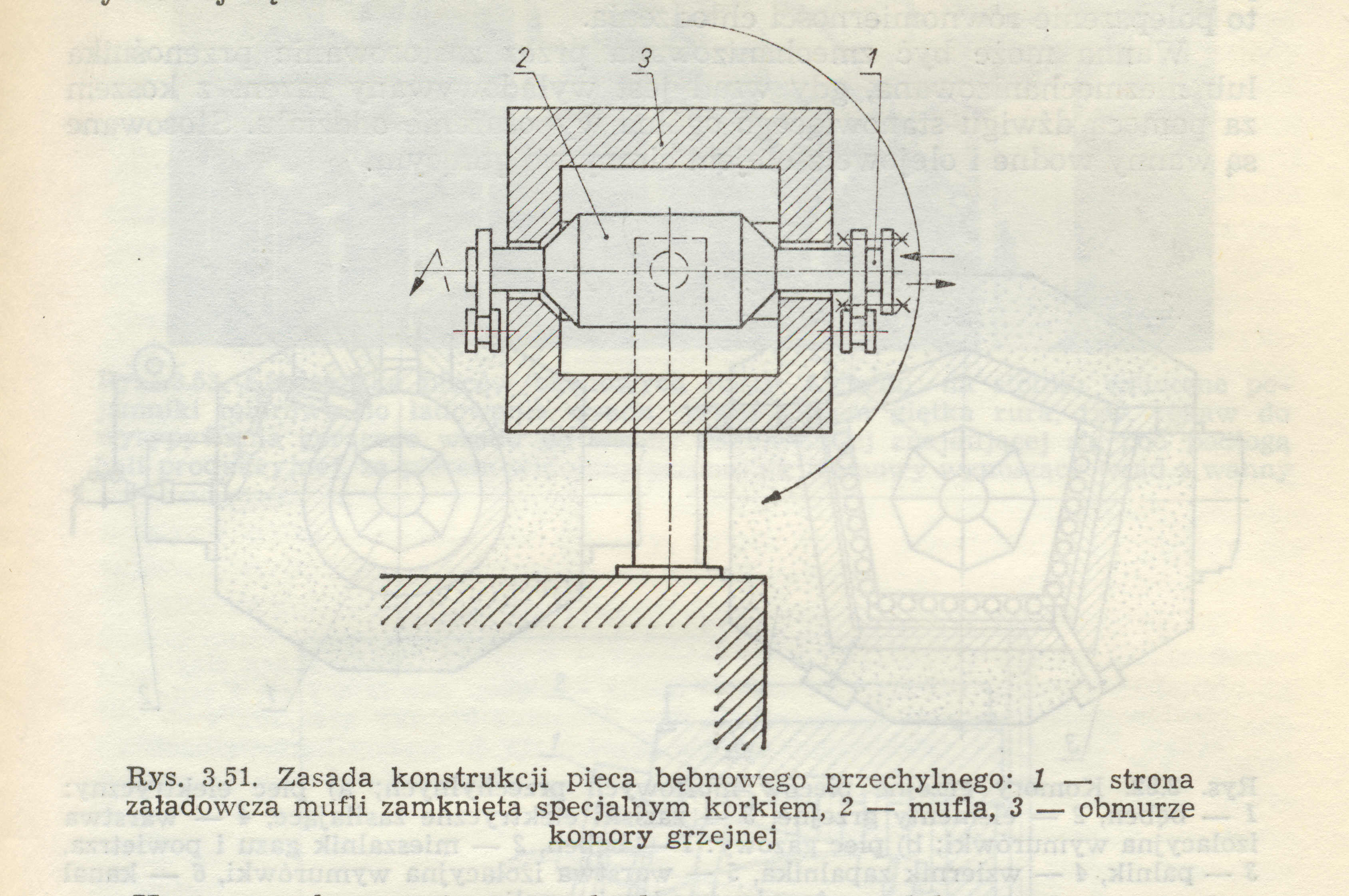
Piece bębnowe pracuja najczęściej w zakresie temp. 750-950oC. Komora pieca zbudowana jest w kształcie naczynia walcowego, lub wielobocznego. Na ścianach ułożyskowana jest obrotowa mufla-bęben. W trakcie pracy pieca mufla wykonuje ruch obrotowy, piece takie najczęściej są połączone z wanna hartowniczą, wsad jest wysypywany prosto do niej.
16. Piec przelotowy (przepychowy)
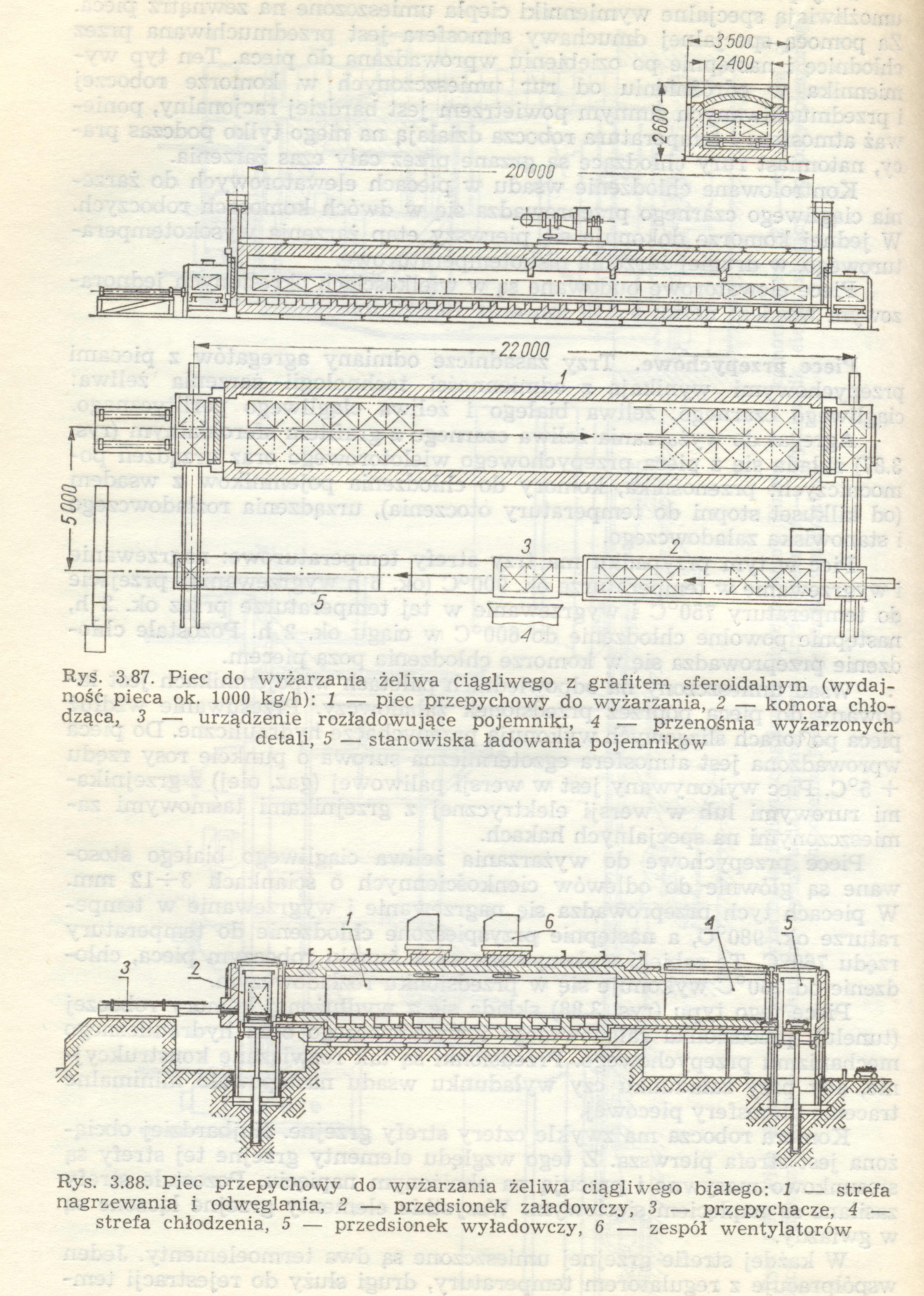
Piece przepychowe są stosowane do produkcji wielkoseryjnej i masowej. Sposób przenoszenia wsadu umożliwia obróbkę elementów o różnych kształtach i dużym zakresie mas. Głównymi elementami pieca przepychowego są przedsionek załadowczy z mechanizmem oteirania drzwi, wielostrefowa komora robocza pieca, przedsionek wyładowczy z wanna hartowniczą, mechanizm przepychowy przepychający wsad przez piec.
17. Piece z rusztem wstrząsowym
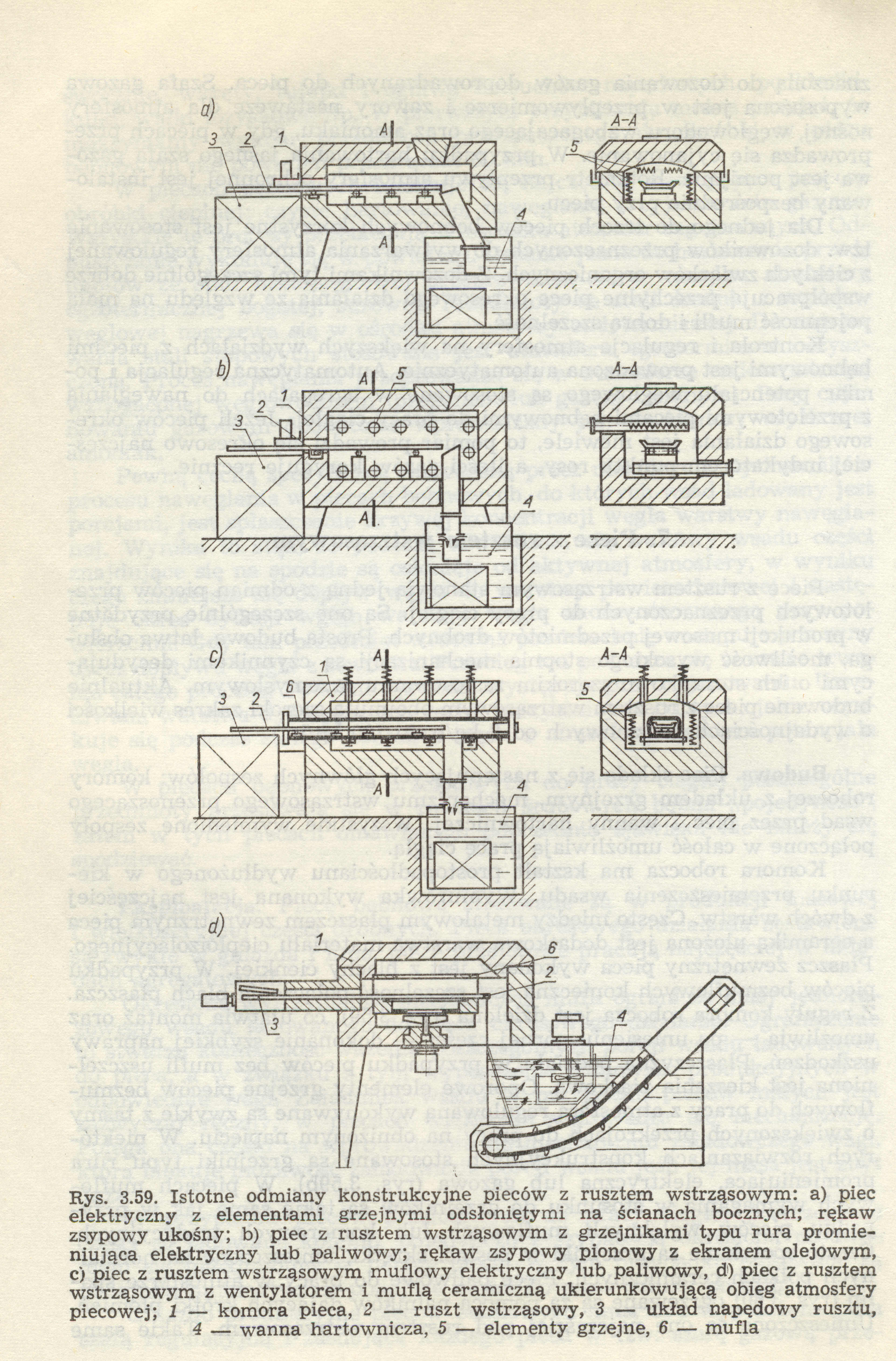
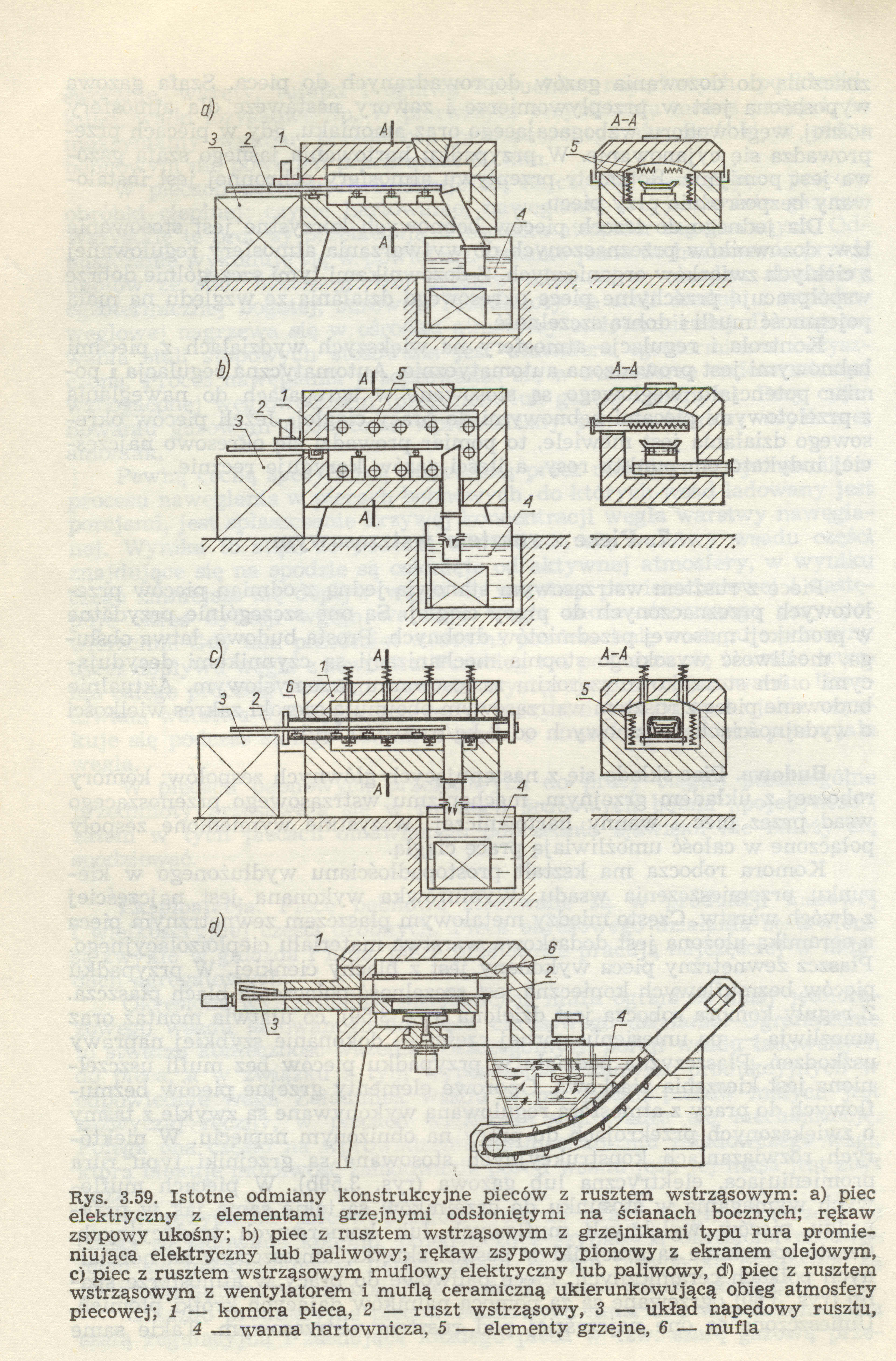
Piece z rusztem wstrząsowym stanowią jedną z odmian pieców przelotowych przeznaczonych do pracy ciągłej. Są przydatne do produkcji masowej drobnych przedmiotów. Piec składa się z: komory roboczej z układem grzejnym, mechanizmu wstrząsowego służącego do przenoszenia wsadu przez piec oraz wanny hartowniczej.
18. Piece taśmowe
Występują trzy rodzaje- nisko, średniotemperaturowe i o temperaturze znamionowej 1000-1150oC.
W piecach niskotemperaturowych mechanizm napędu przenośnika zamontowany jest pod piecem. Taśma prowadzona jest wewnątrz pieca na specjalnych prowadnicach. W piecach średniotemperaturowych przenośnik taśmowy znajduje się całkowicie w komorze pieca, współpracują z wannami hartowniczymi - są to typowe piece hartownicze.
19. Piec próżniowy
Zastosowanie pieców próżniowych w obróbce stali szybkotnących i innych stali narzędziowych rozwinęło się w ostatnim 10-leciu. Wprowadzenie czystych gazów (wodór, argon) jako gazy chłodzące oraz odpowiedni ich obieg w komorze pieca pozwala na hartowanie. Rozróżnia się piece muflowe oraz bezmuflowe. Buduje się je jako piece wgłębne lub piece komorowe z muflą poziomą. Do wytworzenia próżni służą specjalne pompy próżniowe.
20. Rola atmosfer ochronnych i próżni w obróbce cieplnej
Reakcje chemiczne podczas grzania metali i stopów w atmosferach ochronnych
Reakcje utleniania i redukcji w obecności tlenu
Reakcje redukcji wodorem i utleniania parą wodną
Reakcje redukcji tlenkiem węgla i utleniania dwutlenkiem węgla
Reakcje redukcji i utleniania metali w mieszaninie gazów H2, H2O, CO, CO2 i N2
Reakcje odwęglania i nawęglania stali w atmosferach: CO - CO2 , H2 - CH4, N2
a)rola atmosfer ochronnych:
-zapobiegają utlenianiu i odwęglaniu powierzchni przedmiotów obrabianych cieplnie
b)rola próżni:
Wymagania dotyczące jasnej i czystej powierzchni spełnia obróbka cieplna stali w próżni, polegająca na grzaniu w ośrodku gazowym o ciśnieniu znacznie mniejszym od atmosferycznego.
Próżnia:
Utlenianie stali tlenem
Utlenianie stali parą wodną
21. Napisz reakcję utleniania i redukcji stali tlenem
Utlenianie stali tlenem:
22. Napisz reakcję utleniania i redukcji stali parą wodną
Utlenianie stali parą wodną:
23. Z wykresu T - pO2 określ dla temperatury 600 oC ciśnienie pO2 przy którym nastąpi utlenianie lub redukcja Fe i Cu
HARTOWNOŚĆ
24. Co to jest hartowność, utwardzalność, przehartowalność
Hartowność - podatność stali na hartowanie, wyrażana zależnością przyrostu twardości w wyniku hartowania od warunków austenityzowania i szybkością chłodzenia;
Twardość zależy od stężenia C i udziału martenzytu.
Utwardzalność - podatność stali na hartowanie, której miarą jest zależność największej możliwej do uzyskania po hartowaniu twardości od warunków austenityzowania oraz stężenia węgla.
Przehartowalność - zależność przyrostu twardości w wyniku hartowania od szybkości chłodzenia. Zależy ona od stężenia węgla i pierwiastków stopowych w roztworze podczas austenityzowania, stopnia jednorodności austenitu oraz wielkość ziarna.
Miarą przechartowalności jest krytyczna szybkość hartowania lub średnica krytyczna Dn, tj. średnica pręta, w którym po hartowaniu w ośrodku o określonej intensywności chłodzenia w osi przekroju poprzecznego obrabianego elementu uzyskuje się złożoną strukturę z co najmniej n% martenzytu, np.: D80
25. Od czego zależy hartowność stali
O hartowności stali współdecydują: utwardzalność, przehartowalność,
Harowność stali zależy od:
• składu chemiczny stali; stale niestopowe mają niską hartowność; hartowność
zwiększa węgiel i dodatki stopowe (oprócz kobaltu) rozpuszczone w austenicie;
• wielkości ziarna austenitu ;stale gruboziarniste mają większą hartowność;
• jednorodności austenitu; bardziej jednorodny austenit zwiększa hartowność;
• nie rozpuszczonych cząstek węglików, tlenków, azotków — zmniejszają hartowność
Kobalt i chrom zwiększają hartowność stopów przez przesuwanie wykresu CTP w prawo.
26. Jakie są metody badania hartowności stali
Metoda Jominy'ego hartowania od czoła:
Jedna z najpowszechniej stosowanych metod określenia hartowności stali. Metoda ta polega na oziębianiu strumieniem wody, czołowej powierceni próbki walcowej o średnicy 25mm i długości 100mm. Zahartowaną próbkę należy przeszlifować w dwóch jednakowo oddalonych od osi próbki i równoległych do osi próbki płaszczyznach zdejmując warstwę 0,4 mm.
Następnie wykonuje się serie pomiarów twardości metodą Rockwella w skali C w odstępach licząc od czoła próbki: 2*1,5mm; 6*2mm i później co 5mm. Z uzyskanych wymiarów wykonujemy wykres HRC od mm otrzymując tym samym pasma hartowności.
Metoda krzywych „U”:
Polega na hartowaniu prętów z tego samego gatunku stali o róznych średnicach i wyznaczaniu rozkładu twardości na przekroju poprzecznym każdego pręta wzdłuż średnicy. Wyniki próby podaje się w postaci wykresu twardości w funkcji odległości od środka próbki wzdłuż średnicy.
Metody obliczeniowe.
27. Jaki jest wpływ hartowności stali na strukturę stali po hartowaniu i twardość na przekroju
poprzecznym.
??
28. Klasyfikacja stali
Stopowe, niestopowe i nierdzewne
29. Stal konstrukcyjna
Określenie stale konstrukcyjne jest stosowane głównie do stali C-Mn o strukturze ferrytyczno-perlitycznej.
Stale te są stosowane w dużych ilościach w inżynierii lądowej, wodnej oraz chemicznej zarówno w postaci blach, jak i kształtowników o grubości wielu centymetrów i granicy plastyczności (Re) zwykle do 500 MPa.
Do stali konstrukcyjnych zalicza się również niskostopowe gatunki stali, które są hartowane i odpuszczane w celu uzyskania granicy plastyczności do 700 MPa.
Zastosowanie:
Zakres zastosowań stali konstrukcyjnych niskowęglowych jest bardzo szeroki, a mianowicie:
konstrukcje nośne budynków, mosty, statki, platformy wiertnicze i wydobywcze ropy i gazu, pojazdy, ropo- i gazociągi oraz zbiorniki ciśnieniowe.
Titanic, wieża Eifla, rurociągi
Wymagania:
Dobra spawalność przy dostatecznych własnościach mechanicznych (głównie Re), oraz odporność na kruche pękanie (drobne ziarno)
Główną cechą większości konstrukcji jest duży udział spawania i duże wymagania stawiane połączeniom spawanym (Spawanie jako podstawowy proces łączenia zaczęło zastępować nitowanie na początku lat czterdziestych XX wieku)
Spełniają je stale o niskiej zawartości C i bardzo niskiej zawartości zanieczyszczeń (S, P)
30. Stale maszynowe
szeroki zakres stali zwykle obrabiany cieplnie w celu uzyskania wytrzymałości na rozciąganie powyżej 700 MPa.
Stale te są stosowane na elementy, od których wymaga się ściśle określonej sztywności, wytrzymałości, odporności na: pękanie, zmęczenie, pełzanie, korozję i zużycie.
Stale te powinny charakteryzować się dobrą hartownością, skrawalnością i niekiedy również dobrą zdolnością do kształtowania procesami odkształcenia plastycznego na zimno.
Zastosowanie:
Są one stosowa w przemyśle samochodowym, kosmicznym, wydobywczym, obronnym, chemicznym, rolnym oraz w transporcie kolejowym i w urządzenia przemysłowych.
Ponad połowa stali maszynowych znajduje zastosowanie w samochodach osobowych i ciężarowych, traktorach i ciężkim sprzęcie samojezdnym.
Podczas pracy elementy wykonane z tych stali są narażone na działanie dużych naprężeń.
31. Stale narzędziowe
Stale, z których wykonuje się narzędzia do kształtowania metali przez:
kucie (stemple, matryce),
Cięcie (piły, noże tokarskie)
Wyciskanie
Ciągnienie,
Walcowanie lub odlewanie do form metalowych (walce w walcarkach, formy do odlewania).
Do kształtowania polimerów, ceramik i kompozytów (matryce, stemple)
Wymagania:
Wytrzymałość i twardość narzędzi muszą być większe niż materiałów ciętych lub kształtowanych.
Stąd SN są twarde, odporne na działanie ciepła, zdolne do przenoszenia dużych naprężeń w temperaturze otoczenia jak i wyższej (do 700oC) przy małym zużyciu.
Ze względu na b. różnorodne wymagania istnieje duża grupa SN od tanich i prostych niestopowych (duża zaw. C) do drogich, stopowych stali szybkotnących, do pracy na gorąco.
Pierwiastki stopowe:
Dodaje się w celu zwiększenia hartowności i zwiększenia odporności na odpuszczające działanie ciepła.
Zwiększając hartowność - zwiększają wytrzymałość, stąd mniejsze przekroje i łagodniejsze ośrodki chłodzące.
Tworzą węgliki zwiększające twardość i odporność na ścieranie, hamujące rozrost ziarna - stąd większa udarność
Węgliki są trwałe w wysokich temperaturach (nie koagulują)
Rodzaje stali narzędziowych:
niestopowe do pracy na zimno
stopowe do pracy na zimno,
do pracy na gorąco
szybkotnące
32. Stale stopowe do pracy w podwyższonej temperaturze
Stale stopowe do pracy w temperaturze podwyższonej do ok. 600oC są stosowane w energetyce na urządzenia ciśnieniowe, głównie na: walczaki kotłów parowych,
rury kotłowe i przegrzewaczowe,
do budowy turbin parowych, wodnych i gazowych,
na armatury kotłów i turbin,
zbiorniki ciśnieniowe i inne urządzenia energetyki konwencjonalnej i jądrowej oraz przemysłu chemicznego.
Skład chemiczny stali stopowych pracy w podwyższonej temperaturze
Ze względu na skład chemiczny stale stopowe do pracy w podwyższonej temperaturze dzieli się na:
niskowęglowe, o stężeniu do 0,25% C,
średniowęglowe - o stężeniu węgla większym niż 0,25%,
niskostopowe - o małym i średnim stężeniu węgla i łącznym stężeniu pierwiastków stopowych nieprzekraczającym 3%,
średniostopowe - o średnim stężeniu węgla i stężeniu pierwiastków stopowych w zakresie 3-5%,
wysokostopowe - o dużym stężeniu pierwiastków stopowych, przekraczającym 5% - w tym głównie Cr powyżej 10%.
Pierwiastki stopowe
Do najważniejszych pierwiastków stopowych polepszających własności wytrzymałościowe w wysokiej temperaturze oraz odporność na pełzanie należą Cr, Mo i V.
Odporność na utlenianie w podwyższonej temperaturze polepsza głównie Cr.
Stale zawierające 1÷2,5% Cr mogą być stosowane w temperaturze do ok. 580·C.
Zwiększenie stężenia Cr nawet do 13% nie wpływa znacząco na zmianę czasowej wytrzymałości stali na pełzanie.
Dopiero dodatek węglikotwórczych pierwiastków stopowych, głównie Mo, a szczególnie V, a także W, Ti i Nb, przyczynia się do znacznego zwiększenia własności wytrzymałościowych oraz zwiększenia czasowej wytrzymałości na pełzanie.
33. Stale żaroodporne i żarowytrzymałe
Od stali i stopów pracujących w wysokiej temperaturze w zakresie powyżej 550°C wymaga się dużej żaroodporności i żarowytrzymałości.
Żaroodporność to odporność stopu na działanie czynników chemicznych, głównie powietrza oraz spalin i ich agresywnych składników w temperaturze wyższej niż 550°C. Żaroodporność jest ściśle związana ze skłonnością stali do tworzenia zgorzeliny.
Zgorzelina powinna stanowić ciągłą warstwę, dokładnie przylegającą do metalicznego rdzenia, co utrudnia dyfuzję utleniacza i jonów metalu.
Wymagania te spełniają niskowęglowe stale o jednofazowej strukturze ferrytu lub austenitu, o dużym stężeniu chromu i niklu oraz dodatkowo krzemu i aluminium.
34. Stale i stopy oporowe
Oddzielną grupę stopów żaroodpornych o szczególnych własnościach elektrycznych stanowią stopy oporowe, przeznaczone na elementy grzejne pieców i innych urządzeń nagrzewających do obróbki cieplnej.
Stale i stopy oporowe są produkowane w postaci drutów i taśm. Materiały te charakteryzują się następującymi własnościami:
b. dużą opornością właściwą, b. małym temperaturowym współczynnikiem oporności, b. małym temperaturowym współczynnikiem rozszerzalności,
małą przewodnością cieplną, wysokimi własnościami mechanicznymi w temperaturze pokojowej, dużą odpornością na pełzanie w wysokiej temperaturze, dużą odpornością na korozję gazową.
Odporność na pełzanie i odporność korozyjna decydują przede wszystkim o trwałości elementów grzejnych.
35. Nadstopy i stopy wysoko-żaro- wytrzymałe
Stopy żelaza zawierające więcej niż ok. 50% dodatków stopowych noszą nazwę nadstopów. Stopy te zawierają Cr, co zapewnia im żaroodporność, oraz Nb, Zr, Ti, Al i N, umożliwiające utwardzanie wydzieleniowe.
Nadstopy żarowytrzymałe dzieli się na następujące grupy:
II! stopy na osnowie Fe, zawierające Cr i Ni, 11II stopy złożone Fe-Cr-Ni-Co, lIII stopy na osnowie Co bez Fe, zawierające Cr, Ni, Mo, W, iIIII stopy na osnowie Ni, zawierające Cr, niekiedy Co, a także niewielkie dodatki Mo, Ti, Al, Zr, B.
Orientacyjny skład chemiczny niektórych zagranicznych gatunków nadstopów żarowytrzymałych podano w tablicy 6.61, natomiast znormalizowanych w kraju stopów Fe-Ni-Cr (według PN-ISO 9722:2000) - w tablicy 6.62.
Zastosowanie:
Nadstopy żarowytrzymałe są stosowane w temperaturze wyższej niż żarowytrzymałe stale austenityczne, tj. wyższej od 750°C, a nawet 1000°C (rys. 6.26).
Stopy te są stosowane głównie na łopatki, wirniki oraz dysze turbin parowych i silników odrzutowych.
36. Wpływ środowiska promieniotwórczego na materiały konstrukcyjne
Wobec materiałów stosowanych w energetyce jądrowej stawiane są specjalnie wyostrzone wymagania. Dotyczą one procesu ich wytwarzania, kontroli w czasie eksploatacji i oceny stanu sprawności eksploatacyjnej .
Pod wpływem promieniowania, w strukturze materiałów konstrukcyjnych, zachodzą przemiany sukcesywnie obniżające charakterystyki eksploatacyjne, materiałów. W pierwszym rzędzie pogarszają się właściwości mechaniczne i odporność korozyjna.
Spośród wszystkich rodzajów promieniowania najsilniejszy wpływ właściwości materiałów wywiera promieniowanie neutronowe. Dlatego do materiałów odpornych na promieniowanie zalicza się te, które zachowują trwałość struktury i właściwości właśnie w warunkach promieniowania neutronowego.
← Model Seegera
Neurony uderzają w atomy materiałów wybijając je z pozycji węzłowych.
Uderzony neuronem atom, podobnie jak kula bilardowa, uderza w sąsiedni atom, wywołując w sieci dodatkowe przesunięcia.
Takie kaskadowe - „bilardowe” zjawisko tworzy w strukturze przestrzenie o dużej gęstości dyslokacji z peryferyjnymi obszarami wysokiej koncentracji atomów międzywęzłowych.
Jeden neutron może wytworzyć w aluminium ponad 6000 wakansów, w berylu z dużą energią wiązań międzyatomowych - ponad 450.
37. Jaki jest wpływ niklu na pęcznienie stali.
Wraz z zawartością % niklu zmniejsza się wskaźnik pęcznienia
ΔV
V [%]
38. Materiały na elementy elektrowni jądrowych
1 - plater zewnętrzny obudowy betonowej
Stale niskowęglowe i węglowe
2 - plater wewnętrzny obudowy betonowej
Stale nierdzewne ferrytyczne
9 - korpus reaktora
Stale nierdzewne austenityczne
Materiały na pręty paliwowe
Wymagania:
materiał z małym przekrojem czynnym wychwytywania neutronów,
wysokie własności mechaniczne i antykorozyjne
Pierwsze materiały to stale chromowo-nikowe - wady: duży przekrój czynny wychwytywania elektronów, skłonność do pęcznienia
Materiały obecne: stopy cyrkonu Zircalloy. Zalety:
15 razy mniejszy przekrój czynny wychwytywania elektronów,
Mała rozszerzalność cieplna, wysoka plastyczność i odporność na pełzanie
Materiały na wymienniki ciepła
Przekazywanie ciepła z pierwotnego obwodu reaktora do drugiego obwodu - poprzez tysiące rur.
Wymagania: wysoka trwałość cieplna i korozyjna.
Początkowo: stale 18.8 (18%Cr i 8%Ni) i 18.12 (18%Cr i 12%Ni).
Obecnie stosuje się stopy niklu:
w USA stop inconel 600 (60,5%Ni, 23%Cr i 14%Fe)
w RFN stop inconel 800 (34%Ni, 21%Cr i 43%Fe)
39.Stale stopowe do pracy w podwyższonej temperaturze:
Wymagania stawiane stalą do pracy o podwyższonej temperaturze:
Ze względu na szczególne warunki pracy - oprócz określonych własności wytrzymałościowych
i ciągliwych w temperaturze pokojowej - stale te cechują się:
-wymaganymi własnościami w temperaturze podwyższonej. Zjawiska zachodzące w stali w temperaturze podwyższonej powodują z reguły zwiększenie plastyczności. W wyniku tego odkształcenie trwałe zależy od trzech czynników: naprężenia, czasu działania obciążenia i temperatury. Gdy czynnik czasu nie działa jeszcze istotnie na odkształcenie trwałe stali, podstawę do oceny właściwości stali stanowi: granica plastyczności
lub
albo wytrzymałość
, wyznaczane na próbce rozciągania w temperaturze t.
W temperaturze wyższej od temperatury granicznej stałe obciążenie powoduje ciągle postępujące odkształcenie stałe, obciążenie powoduje ciągle postępujące odkształcenie konstrukcji wskutek pełzania, aż do jej zniszczenia
Wiele elementów urządzeń energetycznych, np. łopatki turbin lub wirniki w podwyższonej temperaturze podlegają ponadto działaniu naprężeń zmęczeniowych.
Przeznaczenie: Stale stopowe do pracy w temperaturze podwyższonej do ok. 600°C są stosowane
w energetyce na urządzenia ciśnieniowe, głownie na walczaki kotłów parowych,
rury kotłowe i przegrzewaczowi, do budowy turbin parowych, wodnych i gazowych,
na armatury kotłów i turbin, zbiorniki ciśnieniowe i inne urządzenia energetyki
konwencjonalnej i jądrowej oraz przemysłu chemicznego.
Skład chemiczny i struktura stali stopowych do pracy w podwyższonej temperaturze
Ze względu na skład chemiczny stale stopowe do pracy w podwyższonej temperaturze
dzieli się na:
niskowęglowe- o stężeniu do 0,25% C,
średniowęglowe - o stężeniu węgla większym niż 0,25%,
niskostopowe - o małym i średnim stężeniu węgla i łącznym stężeniu pierwiastkow
stopowych nieprzekraczającym 3%,
średniostopowe - o średnim stężeniu węgla i stężeniu pierwiastkow stopowych
w zakresie 3÷5%,
wysokostopowe - o dużym stężeniu pierwiastkow stopowych, przekraczającym 5% - w tym głownie Cr powyżej 10%.
Ze względu na strukturę stale stopowe do pracy w podwyższonej temperaturze
można podzielić na:
-ferrytyczno-perlityczne,
-ferrytyczno-bainityczne,
-o strukturze martenzytu wysokoodpuszczonego.
40. Stale żaroodporne i żarowytrzymałe:
Wymagania stawiane tym stalom:
Od stali i stopów pracujących w wysokiej temp. (powyżej 550C) wymaga się dużej żaroodporności i żarowytrzymałości. Wymagania te spełniają niskowęglowe stale o jednofazowej strukturze ferrytu lub austenitu, o dużym stężeniu chromu i niklu oraz dodatkowo krzemu i aluminium.
Przeznaczenie:
Stale ferrytyczne są stosowane na nieobciążone mechanicznie elementy aparatury chemicznej, piecow i kotłow przemysłowych, elementy palników gazowych, skrzynie do nawęglania i inne.
Stale austenityczne o większej żarowytrzymałości są stosowane na podobne elementy, lecz obciążone mechanicznie.
41. Co to jest żaroodporność i żarowytrzymałość?
Żaroodporność- to odporność stopu na działanie czynników chemicznych, głownie powietrza oraz spalin i ich agresywnych składników w temperaturze wyższej niż550°C. Żaroodporność jest ściśle związana ze skłonnością stali do tworzenia zgorzeliny. Zgorzelina powinna stanowić ciągłą warstwę, dokładnie przylegającą do metalicznego rdzenia, co utrudnia dyfuzję utleniacza i jonow metalu. Wymagania te spełniają niskowęglowe stale o jednofazowej strukturze ferrytu lub austenitu, o dużym stężeniu chromu i niklu oraz dodatkowo krzemu i aluminium.
Pierwiastki wpływające na żaroodporność stali:
-korzystnie :chrom, dodatki Si i Al.,
-nie korzystnie V i Mo.
Żarowytrzymałością jest nazywana odporność stopu na odkształcenia, z czym wiąże się zdolność do wytrzymywania obciążeń mechanicznych w wysokiej temperaturze - powyżej 550°C. Żarowytrzymałość w temperaturze wyższej od 550°C jest uzależniona głownie od odporności na pełzanie. Dużą żarowytrzymałość wykazują więc stale o strukturze austenitycznej - ze względu na mniejsze współczynniki dyfuzji niż w ferrycie , o znacznej wielkości ziarn i z dyspersyjnymi wydzieleniami faz, głownie na granicach ziarn.
Pierwiastki wpływające na żarowytrzymałość stali: Nikiel i Cr
42. Stale i stopy oporowe, wymagania, skład chemiczny, struktura, własności, przeznaczenie
Przeznaczenie: Oddzielną grupę stopów żaroodpornych o szczególnych własnościach elektrycznych
stanowią stopy oporowe, przeznaczone na elementy grzejne pieców i innych
urządzeń nagrzewających do obróbki cieplnej. Stale i stopy oporowe są produkowane
w postaci drutów i taśm.
Skład chemiczny i struktura:
-niklowo-chromowe o strukturze austenitycznej (tzw. chromonikieliny lub nichromy) - z dodatkiem Fe, a także niedużymi dodatkami Mn i Si, zawierające kilka setnych części procentu węgla.
-żelazowo-chromowo-aluminiowe o strukturze ferrytycznej (tzw. ferchromale
lub fechrale), zawierające niewielkie dodatki Mn i Si oraz kilka setnych części
procentu węgla.
własności:
-dużą opornością właściwą,
-małym temperaturowym wspołczynnikiem oporności,
-małym temperaturowym wspołczynnikiem rozszerzalności,
-małą przewodnością cieplną,
-wysokimi własnościami mechanicznymi w temperaturze pokojowej,
-dużą odpornością na pełzanie w wysokiej temperaturze,
-dużą odpornością na korozję gazową.
-Odporność na pełzanie i odporność korozyjna decydują przede wszystkim
o trwałości elementow grzejnych.
43. Nadstopy i stopy wysoko żarowytrzymałe wymagania , skład chemiczny, struktura, własności, przeznaczenia:
Skład chemiczny, struktura:
Stopy żelaza zawierające więcej niż ok. 50% dodatkow stopowych noszą nazwę nadstopow. Stopy te zawierają Cr, co zapewnia im żaroodporność, oraz Nb, Zr, Ti, Al i N, umożliwiające utwardzanie wydzieleniowe.
Nadstopy żarowytrzymałe dzieli się na następujące grupy:
-stopy na osnowie Fe, zawierające Cr i Ni,
-stopy złożone Fe-Cr-Ni-Co,
-stopy na osnowie Co bez Fe, zawierające Cr, Ni, Mo, W,
-stopy na osnowie Ni, zawierające Cr, niekiedy Co, a także niewielkie dodatki
Mo, Ti, Al, Zr, B.
Właściwości i Przeznaczenia:
Nadstopy żarowytrzymałe są stosowane w temperaturze wyższej niż żarowytrzymałe
stale austenityczne, tj. wyższej od 750°C, a nawet 1000°C. Stopy
te są stosowane głownie na łopatki, wirniki oraz dysze turbin parowych i silnikow
odrzutowych.
Nadstopy żarowytrzymałe charakteryzują się dużymi własnościami wytrzymałościowymi
w wysokiej temperaturze, w szczegolności - dużą wytrzymałością na
pełzanie. W większości są one umacniane w wyniku wydzielania faz o dużej dyspersji.
Obrobka cieplna nadstopow żarowytrzymałych polega więc na przesycaniu
i starzeniu. Zwiększenie trwałości nadstopow uzyskuje się także w wyniku wytworzenia
na ich powierzchni powłok żaroodpornych.
Rola wentylatorów w piecu:
1. wyrównanie temperatury w całej objętości pieca
2. Wspomaganie w przekazywaniu ciepła od ogniw grzejnych do materiału wsadowego do momentu gdy osiągniemy na tyle wysoką temperaturę, że będzie występować promieniowanie
3. "skupianie" większej ilości ciepła w miejscu gdzie materiał wsadowy ma większe pole przekroju, w celu otrzymania równomiernej temperatury w całej jego objętości
Wyszukiwarka
Podobne podstrony:
Badanie widma promieniowania termicznego na przykładzie 01, promieniowanie termiczne
pytania na specjalizacje 01, MEDYCYNA, LEP
j polski praca na 24 01 2011
dużo przepisów na ryby 01, Ryby
Ściąga na kolokwium! 01
Fiz.Pol. cz. 2 - pytania na egz. 01.2012, fizyka polimerów, wykład
Fiz.Pol. cz. 2 - pytania na egz. 01.2012, Fizyka Polimerów WCh PŁ
Praca Domowa - Word - na 30.01.2008, Informatyka
wykład na 12 01 2007
16 18 Cellulit na celowniku 01
chirurgia pyt na egz 01 04 2006, Naika, stomatologia, Chirurgia
Kot na Rozdrożu, Kot Na Rozdrożu 01, Ohayo-o
Karty mBaku i MultiBanku program rabatowy na dzien 01 12 2010
Premier Iraku zakaz kandydowania nie wpłynie na frekwencję (01 03 2010)
Macomber Debbie Pora na romans 01 Pora na romans
Faria Laurie A Niebieski płomień na koszmary 01 Niebieski płomień na koszmary
Karol May A pokój na Ziemi 01 U stóp Sfinksa
więcej podobnych podstron