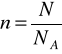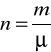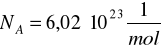Temat: Model gazu doskonałego
Cząsteczki gazu można traktować jak punkty materialne.
Ruch cząsteczek jest chaotyczny.
Liczba cząsteczek jest bardzo duża.
Poza momentami zderzeń cząsteczki nie oddziałują ze sobą.
Zderzenia są doskonale sprężyste.
Parametry stanu gazu: to mierzalne wielkości makroskopowe związane z układem, takie jak temperatura
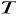
, ciśnienie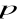
, objętość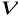
, a także liczby moli gazu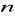
.Objętość gaz
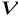
jest równa objętości naczynia w którym znajduje się gaz.
Temperatura jest miarą średniej energii kinetycznej cząsteczek gazu.
Średnia energia kinetyczna ruchu postępowego cząsteczek gazu zależy od temperatury T i jest do niej wprost proporcjonalna.
![]()
![]()
- stała Boltzmana; ![]()
- temperatura
Ciśnienie
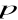
gazu wywierane przez cząsteczki gazu na ścianki naczynia możemy obliczyć z wyrażenia:
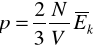
![]()
- liczba cząsteczek; ![]()
- objętość gazu ![]()
- średnia energia kinetyczna cząsteczek
Równanie to nosi nazwę podstawowego wzoru teorii kinetyczno-molekularnej gazu.
Liczby moli gazu
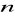
jest równa:
|
|
|
|
|
|
||
Równanie Clapeyrona:
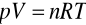
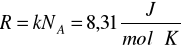
- stała gazowa
Równanie stanu gazu doskonałego - Dla danej masy gazu doskonałego stosunek iloczynu ciśnienia i objętości do temperatury bezwzględnej jest wielkością stałą.
![]()
Można zmieniać parametry gazu, ale wyrażenie pozostaje stałe. Wartość tego wyrażenia dla stanu początkowego (1) i końcowego (2) jest taka sama.
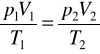
Wyszukiwarka
Podobne podstrony:
Fizyka-ściąga , Podstawowe równanie torii kinetyczno-cząsteczkowej gazu doskonałego
18. Energia potencjalna, Fizyka - Lekcje
24. Pole grawitacyjne, Fizyka - Lekcje
3. Wielkości charakteryzujące ruch, Fizyka - Lekcje
33. Kondensatory, Fizyka - Lekcje
9. Opory ruchu, Fizyka - Lekcje
29 Fale akustyczne cd, Fizyka - Lekcje
37. Praca i moc prądu stałego, Fizyka - Lekcje
36. Prawo Ohma dla obwodu zamkniętego, Fizyka - Lekcje
Przemiana izotermiczna, Fizyka - Lekcje
Model gazu id 304818 Nieznany
54, Biotechnologia PWR, Semestr 2, Fizyka 3.2
40b. Cyklotron Spektroskop masowy, Fizyka - Lekcje
34. Mechanizm przepływu prądu elektrycznego, Fizyka - Lekcje
CIEPLO WLASCIWE GAZU DOSKONALEGO
23. Prawo powszechnego ciążenia, Fizyka - Lekcje
52. Energia wewnętrzna, Fizyka - Lekcje
1. Wielkości fizyczne i ich jednostki, Fizyka - Lekcje
10. Ruch po równi pochyłej, Fizyka - Lekcje
więcej podobnych podstron