ZESTAW I -
SIŁA.Siłę określa się z II z drugiego równania Newtona jako iloczyn masy i przyśpieszenia
K= m*a
W układzie SI jednostką jest niuton.Jest to siła która masie 1 kg nadaje przyśpieszenie 1 m/s2 .jednostką wymiarową jest kg*m/s2.
Jednostką główna -podstawowa w układachrechnicznym i mieszanym jest kg.siła oznaczona jako kG . wzór na ciężar :
G= mg
2.MASA.Jednostką masy jest 1 kg(SI,mieszany) .w układzie technicznym jest jednostka techniczna masy-zwana INERTEM.
m=![]()
1kG*1n/s2=1 inter=9,80665 kg.
Przy przeliczaniu na układ SI lub mieszany
Gc=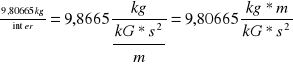
KILOMOL jest równy tylu kg substancji danego pierwiastka czy związku chemicznego ile wynosi jego względna masa cząsteczkowa.
Nm3jest to ilość substancji gazowej wypełniająca przestrzeń 1m3 przy ciśnieniu 1 atmosfery fizycznej przy temperaturze 0O C.
Równoważnik masy ![]()
3.OBJETOŚĆ.Wielkością charakteryzującą stan gazu jest objetość odniesiona do jednostki masy
![]()
objetość właściwa jest to objetość która zajmuje 1 kg substancji danego ciała.
Odwrotnością objetości właściwej jest gęstość.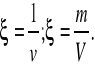
Gęstość jest również masą właściwą .
Ciężarem właściwynciała nazywamy cieżar przypadający na jednostkę objetości(jest to stosunek cieżaru ciała do jego objetość
![]()
ZESTAW 4
CHARAKTERYSTYCZNE PRZEMIANY GAZOWE
Przemiana politropowa - wielokierunkowa-
Politropa-określa równanie 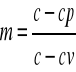
PVn=const m-wykładnik politropy
RÓWNANIE POISSONA
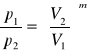
ciśnienie objetości
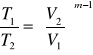
temperatura objetości
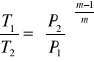
temperatura ciśnienia
w przeminie politropowej stałe jest ciepło własciwe c= const.
Równanie ogólne politropy 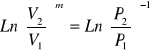
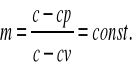
Przemiana politropowa jest przemianą uogólniona i zawiera w sobie jako przypadki szczególne wszystkie rozpatrywane poprzednio przemiany. dopuszcza zmianę wszystkich trzech parametrów.
Praca bezwzględna
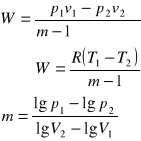
Praca techniczna -rzut danej przemiany na oś p.
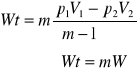
ciepło przemiany
![]()
zmiana entropii
![]()
Przemiana izotermiczna
W tej przemianie stała jest temp.czynnika T= const. M=1
Parametry stanu czynnika zmieniają się zgodnie z zależnością p1v1= p2v2 =RT= const.
Ponieważ stała jest temp. czynnika więc jego energia wewnętrzna nie ulega zmianie .z I zas.dynamiki wynika że jednostkowe ciepło przemiany jest równe pracy zewnętrznej właściwej q1,2 =l1,2
Praca bezwzględna
![]()
praca techniczna
![]()
praca bezwzględna
ciepło przemiany
![]()
zmiana entropii
![]()
przemiana izobaryczna
w tej przemianie stałe jest ciśnienie p= const. , m=0
![]()
ciśnienie stałe bez względu na różnice objetości.
Praca bezwzględna jest to pole przed krzywa rzutowaną na oś objętości
![]()
praca techniczna WT=0
ciepło przemiany
![]()
G - ilość
zmiana entropii
![]()
Przemiana izochoryczna
Objętość właściwa czynnika jest stała v=const. ![]()
Kompresja -zwiększa ciśnienie
Równanie Poissona
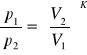
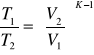
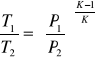
praca bezwzględna W=0
Praca tech. ![]()
Ciepło przemiany
![]()
zmiana entropii
![]()
Przemiana adiabatyczna
W niej nie zachodzi wymiana ciepła z otoczeniem. układ jest odizolowany całkiem od otoczenia .nie ma zmienności ciepła. Q1,2 =0 , S= const. , dQc=0 , m=K .
Praca przemian
![]()
praca tech.=zmiana entropi
![]()
u=q-l , q=0 , u=1 , 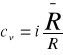
PRZEMIANY NIEODWRACALNE
Dławienie adiabatyczno -izoenergijne
T1=T2 , U1=U2
dwa zbiorniki ,jeden pusty a drugi zawiera gaz o parametrach p1V1T1 połaczone izolowanym cieplnie przewodem z zaworem.po otwarciu następuje wyrównanie temperatur i ciśnień.Rozpatrywany układ nie wykonuje pracy nie pobiera ani nie oddaje ciepła ,całkowita energia wewnętrzna gazu jest jednakowa na poczatku i na końcu.(OPISANE ZJAWISKO JEST NIEODWRACALNE) .
Dławienie adiabatyczno - izentalpowe
Zjawisko występuje gdy w rurociągu występuje przeszkoda.na wykresie widać że ciśnienie przed samą przeszkodą lekko wzrasta przy przezkodzie maleje i za przeszkodą wzrasta,lecz już nie noszaca tej samej wartości.Przeszkoda powoduje stały spadek ciśnienia
![]()
po zdławieniu strugi czynnika przepływa z niewielka prędkościa .ENTALPIA po zdławieniu = ENTALPI przed zdławieniem i1 =i2.
Adiabata nieodwracalna - pośrednia między izentropą a dławieniem.
![]()
W1<W rozpręż. ![]()
spręż.
Wyszukiwarka
Podobne podstrony:
Technika cieplna - Spalanie, Skrypty, UR - materiały ze studiów, III semsestr, Technika Cieplna
Przemiany gazowe wzory i wykresy, Skrypty, UR - materiały ze studiów, III semsestr, Technika Cieplna
76576, Skrypty, UR - materiały ze studiów, III semsestr, Ekonomia
word, Skrypty, UR - materiały ze studiów, III semsestr, infa
Word ćw.1.obiekt painbrush+funkcje, Skrypty, UR - materiały ze studiów, III semsestr, infa
Korzyści skali, Skrypty, UR - materiały ze studiów, III semsestr, Ekonomia
ekon[1].sciaga-1, Skrypty, UR - materiały ze studiów, III semsestr, Ekonomia
TERMOMETRY TERMOELEKTRYCZNE, Skrypty, UR - materiały ze studiów, studia, studia, Studia, ROK V, TECH
Kopia Opis techniczny B, Skrypty, UR - materiały ze studiów, studia, studia, 4 STASZEK, Semestr II,
Opis techniczny B, Skrypty, UR - materiały ze studiów, studia, studia, 4 STASZEK, Semestr II, Budown
Opis techniczny-Ania, Skrypty, UR - materiały ze studiów, studia, studia, 4 BOGDAN, Semestr II, Wiej
Ania ksztaltowanie srod. sprawozdanie techniczne, Skrypty, UR - materiały ze studiów, studia, studi
SPRAWOZDANIE TECHNICZNE, Skrypty, UR - materiały ze studiów, studia, studia, 4 BOGDAN, Semestr II, W
Kopia Opis techniczny B, Skrypty, UR - materiały ze studiów, studia, studia, 4 STASZEK, Semestr II,
dom0, Skrypty, UR - materiały ze studiów, studia, studia, Bastek, Studia, Rok 3, SEMESTR VI, Woiągi
hydrologia ćwiczenia terenowe 4, Skrypty, UR - materiały ze studiów, IV semestr, hydrologia, terenó
KOSZULKA, Skrypty, UR - materiały ze studiów, studia, studia, 3 STASZEK, Mechanika budowli
więcej podobnych podstron