|
INSTYTUT INŻYNIERII ŚRODOWISKA
UNIWERSYTET ZIELONOGÓRSKI
|
|
LABORATORIUM Z TECHN. WODY I ŚCIEKÓW
|
III ROK INŻYNIERII ŚRODOWISKA
STUDIA DZIENNE GRUPA 36 B
|
|
CHARAKTERYSTYKA WÓD PODZIEMNYCH, POWIERZCHNIOWYCH I UZDATNIONYCH
|
Woda występująca w warunkach naturalnych, tj. w przyrodzie, nie jest związkiem chemicznie czystym, lecz jest mieszaniną wieloskładnikową i wielofazową, która zawiera roztwory różnych soli, gazów oraz ciał pochodzenia zarówno mineralnego jak i organicznego. Domieszki te dostają się do wody podczas jej krążenia w przyrodzie. W związku z tym skład fizyczno-chemiczny wód naturalnych jest bardzo złożony i ściśle związany z wędrówką wody oraz środowiskiem, z którego ona pochodzi. Skład wody naturalnej można ogólnie zapisać: H2O +x,
gdzie x - to domieszki, czyli składniki naturalne i obce.
Współczesna gospodarka człowieka i przemysł zanieczyszczają wody naturalne rozmaitymi substancjami i dlatego większość wód nie nadaje się do picia i potrzeb gospodarczych, gdyż nie odpowiada podstawowym wymaganiom sanitarnym.
Zasada oznaczenia mętności polega na wizualnym porównaniu mętności badanej próbki wody w świetle czarnym z wzorcami przygotowanymi według skali wzorcowej określającej mętność wody. Wzorce zostały wcześniej przygotowane laboratoryjnie. Jednostki mętności podaje się w mgSiO2/dm3.
Zasada oznaczenia barwy polega na wizualnym porównaniu barwy badanej próbki wody w świetle białym z wzorcami przygotowanymi według skali platynowo - kobaltowej lub dwuchromianowo - kobaltowej. Jednostki barwy przyjęto oznaczać w mg Pt/dm3.
Odczyn wody w sposób przybliżony określa się za pomocą papierków wskaźnikowych. Do dokładnego oznaczenia pH stosuje się metodę kolorymetryczną i elektrometryczną.
Zasada oznaczenia żelaza: zasada oznaczenia polega na utlenianiu żelaza dwuwartościowego do trójwartościowego, które pod wpływem rodanku amonowego w środowisku kwaśnym daje czerwono krwiste zabarwienie, którego intensywność jest proporcjonalna do stężenia żelaza w badanej wodzie.
Zasada oznaczenia manganu: zasada oznaczania polega na utlenianiu związków manganowych do nadmanganianu wobec azotanu srebra jako katalizatora i siarczanu rtęciowego jako czynnika kompleksującego chlorki. Intensywność powstałego zabarwienia 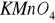
określa się fotokolorymetrycznie.
Zasada oznaczenia fosforanu polega na tworzeniu się w roztworze kwaśnym kwasu fosforomolibdenowego o żółtym zabarwieniu, który ulega redukcji pod wpływem chlorku cynawego, tworząc związek kompleksowy - błękit molibdenowy - o intensywnym niebieskim zabarwieniu. Intensywność zabarwienia jest proporcjonalna do zawartości fosforanów. Oznacza się ją wizualnie lub fotokolorymetrycznie.
Zasada oznaczenia azotu amonowego metodą bezpośredniej Nessleryzacji: amoniak reaguje z odczynnikiem Nesslera tworząc związek o żółtym zabarwieniu, którego intensywność jest proporcjonalna do stężenia amoniaku.
Zasada oznaczania utlenialności: Zasada oznaczania polega na utlenianiu związków organicznych i niektórych łatwo utleniających się nieorganicznych, np. soli żelazowych, azotynów, siarkowodoru i innych reduktorów, za pomocą nadmanganianu potasowego w roztworze kwaśnym w temperaturze wrzenia wody. Nadmiar dodanego roztworu nadmanganianu potasowego odmiareczkowuje się kwasem szczawiowym.
Ekstynkcja badanej wody wyniosła 0,174. Dla takiej ekstynkcji zawartość fosforanu wynosi 0,16 mgP043-/dm3 .
Ekstynkcja badanej wody wyniosła 0,082. Dla takiej ekstynkcji zawartość azotu amonowego wynosi 0,513 mgNH4+/dm3 .
Ekstynkcja badanej wody wyniosła 0,121. Dla takiej ekstynkcji zawartość żelaza wynosi 1,997 mgFe/dm3 .
Ekstynkcja badanej wody wyniosła 0,008. Dla takiej ekstynkcji zawartość żelaza wynosi 0,132 mgFe/dm3 .
Ekstynkcja badanej wody wyniosła 0,001. Dla takiej ekstynkcji zawartość żelaza wynosi 0,020 mgMg/dm3 .
Ekstynkcja badanej wody wyniosła 0,0001. Dla takiej ekstynkcji zawartość żelaza wynosi 0,002 mgMn/dm3 .
Utlenialność - oblicza się wg wzoru:
a-ilość roztworu KmnO4 zużyta na zmiareczkowanie próbki wody;3,5; 2,3; 1,7cm3
b- ilość roztworu KmnO4 zużyta na utlenienie związków organicznych zawartych w 100 cm3 wody destylowanej; 0,3 cm3
V- objętość próbki wody użyta do oznaczenia; 100 cm3
X = 3,5 - 0,3 = 3,2 mgO2/dm3
X = 2,3 - 0,3 = 2,0 mgO2/dm3
X = 1,7 - 0,3 = 1,4 mgO2/dm3
Zestawienie badań wody w tabelce
FOSFOR: Związki fosforu w ilościach występujących w wodach do picia nie są szkodliwe dla zdrowia i z tego powodu nie są limitowane. Jednak duże ilości fosforanów, ponad 14 - 15 mgP043-/dm3, buforują kwasy soku żołądkowego.
Ze względu na właściwości eutrofizacyjne fosforu przepisy sanitarne w Polsce regulują dopuszczalne ilości fosforanów w wodach powierzchniowych. W I klasie czystości zawartość fosforanów może wynosić 0,2 mgP043-/dm3 . Badana woda mieści się w tym przedziale.
ŻELAZO I MANGAN: Znaczenie higieniczne żelaza nie jest dokładnie znane, jednak ze względu na to, że obecność żelaza pogarsza właściwości organoleptyczne wody, należy je z wody usunąć. Żelazo jest organizmowi ludzkiemu niezbędne jako składnik krwiotwórczy, jednak wydalanie żelaza z organizmu jest niewielkie i wskutek tego jego zapasy wystarczają na dłuższy czas. Zwiększone ilości żelaza mogą powodować występowanie plam przy praniu bielizny.
Ilości manganu spotykane w wodach naturalnych stanowią zazwyczaj od 1/6 do 1/10 zawartości żelaza. Znaczenie higieniczne w wodzie jest podobne jak żelaza. Nie zostało udowodnienie jakoby mangan zawarty w wodzie oddziaływał szkodliwie na niektóre narządy człowieka.
Woda do picia nie powinna przekraczać 0,2 mgFe/dm3, natomiast manganu nie powinno być więcej niż 0,05 mgMn/dm3. Badana woda podziemna zawiera 1,997 mgFe/dm3 , natomist woda uzdatniona mieści się w granicy jakiej powinna odpowiadać woda do picia. Zawartość manganu również spełnia określone wymagania.
AMONIAK: W wodach naturalnych związki azotowe występują jako produkty biochemicznego rozkładu białek roślinnych i zwierzęcych lub są pochodzenia mineralnego.
Amoniak (azot amonowy ) może pochodzić z procesów redukcji azotynów i azotanów, z rozkładu biochemicznego związków białkowych oraz z odprowadzanych ścieków miejskich i przemysłowych. Amoniak może być pochodzenia mineralnego, czyli powstaje w wodach podziemnych wskutek redukcji azotynów i azotanów przez siarkowodór, substancje humusowe. O zanieczyszczeniu wody, świadczy obecność amoniaku pochodzącego z procesów rozkładu biochemicznego produktów organicznych zawierających azot. O jakości wody świadczy pochodzenie amoniaku. W wodach naturalnych występuje on w postaci jonu NH4+, a w wodach podziemnych amoniak mineralny występuje od dziesiątych do kilku mg/dm³. W wodach użytkowych obecność amoniaku jest niepożądana. Amoniak jest związkiem korozyjnym w stosunku do żelaznych rur wodociągowych.
Według WHO azot amonowy może pogorszyć jakość wody już przy stężeniu powyżej 0,05 mgNH4+/dm3 Nasza badana woda powierzchniowa ma stężenie rzędu 0,513mgNH4+/dm3.
UTLENIALNOŚĆ: Zawarte w wodach naturalnych związki organiczne utleniają się za pomocą nadmanganianu potasowego średnio w 60-70%. Oznaczenie utlenialności ma duże znaczenie dla charakterystyki stopnia zanieczyszczenia wód naturalnych związkami organicznymi zarówno pochodzenia zwierzęcego jak i roślinnego. Pod względem sanitarnym utlenialność wody ma istotne znaczenie, gdy jest ona wywołana związkami organicznymi pochodzenia zwierzęcego, w takiej wodzie mogą również znajdować się bakterie chorobotwórcze. Wody, które badaliśmy nie przekraczają 5 mgO2/dm3, w związku z tym spełniają wymogi sanitarne.
Wnioski: wodę bada się w celu ustalenia jej składu fizyczno - chemicznego, a na tej podstawie określa się jej przydatność do picia, potrzeb gospodarczych i przemysłowych, zgodnie z ustalonymi wymaganiami. Zakres badania wody ma dać odpowiedź na postawione pytanie, tj. czy badana woda nadaje się do ściśle określonego celu, czy odpowiada wymaganiom higieniczno - sanitarnym oraz jaki jest jej skład fizyczno - chemiczny. W praktyce sanitarnej rozróżnia się trzy następujące rodzaje badania fizyczno - chemicznego wody do picia:
W nawiązaniu do obowiązujących norm stwierdziliśmy, że woda uzdatniona, którą badaliśmy jest wodą klarowną, bezbarwną. Ocena zawartości żelaza i manganu - w normie, utlenialności - w normie, w związku z tym nadaje się na spożycie.
Natomiast badana woda powierzchniowa ma dopuszczalne stężenie fosforaów, jest w wystarczającym stopniu natleniona.
Woda podziemna kilkakrotnie przekracza zakres barwy i mętności. Spowodowane może to być 10-krotnym przekroczeniem dopuszczalnej zawartości żelaza w tej wodzie.
