1. Oblicz objętość zbiornika potrzebnego do magazynowania m=90kg gazu świetlnego o temp.T= 10°C pod ciśnieniem p=1 Mpa=1000000Pa , jeżeli dany jest objętościowy procentowy skład tego gazu; H2=46% CH4=32% CO=15% N2=7%.Uniwersalna stała gazowa B=8315 J/(kmol ⋅ K).
pV=mRT---V=mRT/p
R=B/M
M=2*0,46+(12+4)*0,32+(12+16)*0,15+(2*14)*0,07=12,2kg/kmol
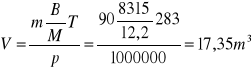
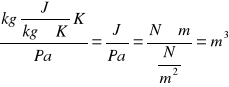
2.Wynalazca twierdzi ,że zbudował silnik cieplny, który w określonym czasie pobiera 100MJ ciepła ze źródła o temp. 327C, oddaje ciepło do źródła o temp. 27C, wykonując pracę 20kWh. Oceń poprawność tego twierdzenia.
Dane:
Q=100MJ=100000kJ
L=20kWh
T=327C=600K
T0=27C=300K
Obliczenia:
1J=Ws
1kJ=1kWs
1kJ=1/3600=0,00027kWh
100000kJ=27,78kWh
100MJ=27,78kWh
η=L/Q=20/27,78=0,71![]()
To twierdzenie jest niepoprawne.
3.Oblicz ile kg pary wodnej wilgotnej znajduje się w zbiorniku o objętości 2m3, jeżeli ciśnienie tej pary wynosi 5MPa, a jej entalpia właściwa równa jest 2465KJ/kg. Potrzebne dane odczytaj z załączonej tabeli.
Dane:
V=2m3
P=5Mpa
i=2465KJ/kg
Obliczenia:
v=V/m
m=V/v
m=V/[v'+x(v''-v')]
i=i'+x(i''-i')
x=(i-i')/(i''-i')=(2465-1154)/(2793-1154)=0,79
m=2000/[1,2858+0,79(39,4102-1,2858)]=63,69kg
[dm3/(dm3/kg)=kg]
1. Oblicz gęstość azotu, którego ciśnienie wynosi 200kPa, a temp. 310C.Uniwersalna stała gazowa B=8315J/kmol*K
Dane:
P=200kPa=200000Pa
T=310C=583K
B=8315J/kmol*K
M=28kg/kmol
Obliczenia:
pV=mRT
pV/RT=m
p/RT=m/V
m/V=ρ
R=B/M
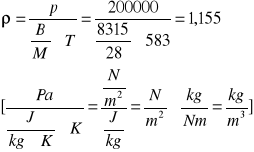
2.Objętość tlenu zawierającą masę 2kg przy temp. 13C zwiększono 2 razy w wyniku podgrzewania przy stałym ciśnieniu. Oblicz ilość ciepła zużytego na ogrzewanie. Ciepło właściwe tlenu przy stałej objętości 0,66kJ/kg*K. Stała tlenu R=0,26kJ/kg*K
Dane:
M=2kg
T1=13C=286K
V2=2V1
Cv=0,66kJ/kg*K
R=0,26kJ/kg*K
Obliczenia:
R=Cp-Cv⇒Cp=R+Cv
Q=mCp(T2-T1)
V1/V2=T1/T2
T2=T1*V2/V1
T2=2T1=572K
Q=m(R+Cv)(2T1-T1)=2(0,26+0,66)(2*286-286)=514,8
[kg*kJ/kg*K*K=kJ]
1. Obrazem pewnej krzywej przemiany w układzie współrzędnych T-S jest odcinek linii prostej. Parametry czynnika na początku przemiany : temp. 205C, entropia 4J/K, a na końcu przemiany :temp. 349C, entropia 6J/K. Oblicz ilość ciepła , którą pochłonął czynnik podczas przemiany.
T1=205C
S1=4J/K
T2=349C
S2=6J/K
S2-S1=Q/(T2-T1)
Q=(S2-S1) (T2-T1)=2*144=288J
2. Ze zbiornika o pojemności 8m3wypompowano 9kg powietrza aż do osiągnięcia ciśnienia 1 kPa przy temp. 10C . Oblicz temp. Powietrza przed wypompowaniem, jeżeli początkowe ciśnienie wynosiło 1bar. Stała gazowa powietrza R=287J/kg*K.
Dane:
V=8m3
M=9kg
P2=1kPa=1000Pa
T2=10C=283K
P1=1bar=100kPa=100000Pa
R=287J/kg*K
P1V=mRT1
P2V=mRT2
P2V-P1V=mRT2-mRT1
T1=[mRT2-(p2V-p1V)]/mR [K]
3.3 kg powietrza o temp. 20C sprężono izotermicznie do objętość 0,1dm3. Podczas sprężania odprowadzono 125kJ ciepła. Oblicz objętość powietrza przed sprężaniem. Stała gazowa powietrza R=287J/kg*K .
m=3kg
T=20C=293K
V2=0,1dm3
Q=125kJ
R=287J/kg*K
p2V2=mRT
p2=mRT/V2
Q=p2V2lnV2/V1
Q/p2V2=ln V2/V1
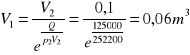
Wyszukiwarka
Podobne podstrony:
pat sciąga chemia zerówka, NAUKA, chemia, lab
sciąga z techniki, NAUKA, chemia, lab
technika cieplna3 - ściąga, NAUKA, chemia, lab
technika cieplna2 - ściąga, NAUKA, chemia, lab
chemia1 - sciaga, NAUKA, chemia, lab
chemia10, NAUKA, chemia, lab
miareczkownie, NAUKA, chemia, lab
Równowaga w roztworach elektrolitów, NAUKA, chemia, lab
Masa atomowa i cząsteczkowa, NAUKA, chemia, lab
Na ciała poruszające się w cieczy, NAUKA, chemia, lab
Oznaczenie miedzi, NAUKA, chemia, lab
grupy pierwsiatkow chemia, NAUKA, chemia, lab
adsorp, NAUKA, chemia, lab
chemia7, NAUKA, chemia, lab
więcej podobnych podstron