Odgazowanie wody
Woda zawiera przede wszystkim składniki powietrza (02, N2, CO2, N2S) przy czym CO2 dodatkowo może pochodzić z rozkładu kwaśnych węglanów oraz przemian biochemicznych.
W przypadku obecności w wodzie gazów agresywnych, które powodują korozję konieczne jest ich usunięcie w trakcie procesów uzdatniania wody. Najbardziej agresywny jest tlen i CO2.
Odgazowanie mechaniczne
Sposoby mechaniczne polegają na odpędzeniu rozpuszczonych gazów czemu sprzyja rozwinięcie powierzchni zwiększającej szybkość wymiany mas pomiędzy fazą ciekłą i gazową. Uzyskać to można poprzez: rozpylanie wody; intensywne mieszanie; przedmuchiwanie powietrzem.
Powyższymi metodami można skutecznie usuwać z wody: CO2 i H2S.
Niniejsze gazy wypierane są z wody przez tlen zawarty w powietrzu. W celu maksymalnego rozwinięcia powierzchni w desorbentach CO2 stosuje się wypełnienie kolumn pierścieniami Raschiga lub specjalnymi kształtkami z tworzywa.
Równanie kinetyki wymiany gazów ma postać: dc/dt = KL∙α (ct - cS); dc - zamiana stężenia gazu w wodzie w czasie dt ; KL∙α - całkowity współ. przenikania masy
Ct, Cs - stężenie gazu w wodzie odpływ i dopływ do areatora.
Odgazowanie termiczne
Odgazowanie termiczne jest podstawową metodą usuwania z wody rozpuszczonych. gazów w układach przemysłowych. Jest to proces desorpcji przebiegający w wyniku: tworzenia się pęcherzyków gazu i ich konwekcji z fazy wodnej do formy gazowej; dyfuzja gazu przez graniczną powierzchnię faz.
Rozpuszczalność danego gazu w wodzie jest uzależniona od ciśnienia i temperatury [ prawo Henriego Ar = K x Pa].
Przy podgrzaniu wody obniża się cząstkowe ciśnienie rozpuszczonych w niej gazów, wskutek czego maleje również ich rozpuszczalność w wodzie. W stanie wrzenia prężność pary wodnej równa jest ciśnieniu panującemu nad wodą, a ciśnienie cząstkowe gazów i ich rozpuszczalność spada do zera.
Całkowite odgazowanie wody może być dokonane przy dowolnej temperaturze lub przy dowolnym ciśnieniu, ........... temperaturze odgazowania odpowiada temperatura wrzenia wody pod ciśnieniem przy którym prowadzi się odgazowanie.
Temperaturę wrzenia konieczną do przeprowadzenia odgazowania osiąga się w odgazowaczu dwoma sposobami: przez ogrzanie wody parą w przeciwprądzie,
przez wprowadzenie do odgazowywacza wody podgrzanej. Odgazowywacze mogą pracować przy ciśnieniach wyższych lub niższych od atmosferycznych.
W celu przyśpieszenia desorpcji niezbędne jest maksymalne rozwinięcie powierzchni rozdziału między parą, a wodą oraz zmniejszeniu grubości warstwy wrzącej wody
rozdeszczanie i rozbryzgiwanie, przepływ wody przez złoże, harbortaż (przepływ przez wodę paty)
Metoda termicznego odgazowania pozwala na usunięcie z niej gazów do wartości poniżej 0,1mggazu/l.
Odgazowanie chemiczne (Usuwanie O2)
Chemiczne metody odtleniania wody stosuje się przede wszystkim do wody obiegu ciepłowniczego lub jako uzupełnienie odgazowania termicznego. Polegają one na wprowadzeniu reduktorów, które utleniają się tlenem obecnym w wodzie. Stosuje się najczęściej: siarczyn sodu Na2SO3, dwutlenek siarki SO2, hydrazyna (N2H4 H2O [zwiększa zasolenie wody], fosforyn sodu Na3PO3, chlorek żelazowy FeCl2
Szybkość wiązania tlenu zależy od: zawartości tlenu w wodzie, dawki reduktora, temperatury, pH wody
W celu zagwarantowania ilościowego przebiegu reakcji w możliwie najkrótszym czasie, z reguły wymagane jest podwyższanie temperatury wody i zapewnienie nadmiaru środka odtleniającego.
Powstałe produkty reakcji mogą stanowić niekorzystne zanieczyszczanie wody i dlatego odtlenianie chemiczne jest zalecane jako uzupełnienie odgazowania termicznego (ma wówczas na celu wiązanie szczątkowych ilości tlenu).
Mechanizm działania poszczególnych reduktorów jest następujący: 2Na2SO4 + O2 →2Na2SO4
Stechiometryczne zapotrzebowanie na bezwodny siarczyn sodowy wynosi 8 mg Na2SO3 na 1 mg związanego tlenu, co odpowiada 16 mg produktu.
Dla potrzeb praktycznych dawkę bezwodnego siarczynu oblicza się ze wzoru: D Na2SO4 = 8Co2+ ... [mg/dm3] Co2 - stężenie tlenu w wodzie [mg/dm3]
Należy pamiętać, iż przy odtlenianiu wody powyższym środkiem wzrasta zasolenie wody ( o 9mg/dm3 na każdy 1 mg/dm3 rozpuszczonego tlenu).
Dodatkową wadą odtleniania wody przy Na2SO3 jest możliwość przebiegu dodatkowych reakcji, których produkty są szkodliwe dla urządzeń.
Nadmiar siarczynu np. w kotłach pracujących pod ciśnieniem powyżej 0,7 MPa może ulegać rozkładowi i hydrolizie: Na2So3 + H2O → 2NaOH + SO2
Szczególnie niebezpieczny jest SO2, który przedostaje się z parą do dalszych części układu; zakwaszając kondensat i wywołuje intensywną korozję przewodów.
Inne szkodliwe reakcje to redukcja tlenków żelaza i miedzi: 3Fe2O3 + Na2SO3 → 2Fe3O4 + Na2SO4 2CuO + Na2SO3 → Cu2O + Na2SO4
Odtlenianie hydrazyną:
2NH2 + O2 → N2↑ + 2H2O
Powstający azot utlenia się z parą, nie wchodząc w żadne reakcje w warunkach obiegu wodno-parowego.
Do odtleniania stosuje się hydrazynę lub jej wodzian [N2H4 H2O] zawierający 64% czystej substancji.
Produkty handlowe zawierają wodzian hydrazyny o stężeniu 24-100%.
Handlowy produkt stanowi zwykle stężony roztwór (ok. 25%) z którego po rozcieńczeniu wodą przygotowuje się roztwór roboczy o stężeniu 1 - 2,5% (ciecz toksyczna).
Odtlenianie hydrazyną wymaga pewnego nadmiaru reagentu, podgrzania wody do temperatury T>100°C i pH>8,7.
Całkowite związanie tlenu w wodzie do temperatury 103 ÷ 115°C, pH=9÷9,5 i nadmiarze hydrazyny 0,02 mg/dm3 zachodzi w czasie.
Dla umożliwienia odtleniania w niższych temperaturach konieczne jest stosowanie katalizatorów: jony Ca2+ i Mn2+.
Do związania 1mgO2 potrzeba 1mg hydrazyny, zaś 1,6 mg w przypadku wodzianu hydrazyny.
Dawkę hydrazyny dla okresu normalnej eksploatacji wylicza się : D N2H2 = 1,5C1 + 1,5C2 + 0,1C3
C1, C2, C3 - stężenie w wodzie O2, Fe2O3, CuO [mg/dm3] Obecnie w wodzie lub na powierzchni metalu tlenki żelaza i miedzi również reagują z hydrazyną:
6Fe2O3 + N2H4 → N2↑ + 2H2O + 4Fe3O4 // 2Cu2O + N2H4 → 4Cu + 2H2O + N2↑
nadmiar hydrazyny w wodzie nie powinien przekraczać 0,1mg/dm3 wyższe stężenie jest nieekonomiczne oraz może powodować niekorzystne skutki wywołane reakcjami wtórnymi. Do nich należy rozkład hydrazyny w temp. do 269oC // 3N2H4 → 4NH3 + N2↑
powstający amoniak, choć w niewielkich ilościach oddziałuje korzystnie - alkalizując wodę. Ma to szczególne znaczenie w kotłach parowych, w których amoniak oraz parą wodna przedostają do dalszej części układu i zabezpiecza przewody przed korozją. W temperaturze > 269oC rozkład hydrazyny zachodzi z wydzieleniem wodoru (proces niekorzystny): 3N2H4 → 2NH3 + 3N2↑ + 2H2O
Odtlenianie żelazem i jego związkami
Praktyczne zastosowanie znalazło odtlenianie za pomocą żelaza metalicznego, które w postaci stalowych wiórków umieszcza się w filtrze. Przepływająca przez filtr woda zawierająca tlen rozpuszcza wiórki, a reakcja ma charakter elektrochemiczny
proces anodowy: Feo → Fe2+ + 2e proces katodowy: O2 + 4e + 2H2O → 4(OH)-
Powstające pierwotne produkty korozji Fe2+, (OH)- dają wtórny produkt Fe(OH)2, który pod wpływem tlenu w wodzie ulega dalszym przemianom:
4 Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3↓
Powstający Fe(OH)3↓ wytrąca się w postaci galaretowatego osadu. Związek ten jest zatrzymywany w warstwie filtracyjnej, stąd konieczność czyszczenia filtru (do płukania wstecznego z dołu do góry).
Do związania 1mgO2 potrzebne jest 2,4mgFe.
zalety: + prosta obsługa; + możliwość usuwania tlenu z zimnej wody
wady: możliwość obniżenia sprawności filtru na skutek pasywacji wiórków stalowych; trudności z usunięciem z filtrów osadu Fe(OH)3↓; znaczne zużycie wody na płukanie filtru; niebezpieczeństwo (przy zbyt krótkim czasie kontaktu) wytrącania się osadu Fe(OH)3↓ w kotłach i elementach instalacji.
Usuwanie CO2
Odgazowywanie polega na chemicznym wiązaniu CO2, nazywane często odkwaszaniem.
Do najczęściej stosowanych sposobów wiązania CO2 zalicza się:
filtrowanie wody przez rozkruszony marmur CaCO3 + CO2 + H2O → Ca(HCO3)2
Wzrasta twardość węglanowa wody ok. 0,46mval/m3 na każde 10g związanego CO2, dodatkowo wzrasta zasadowość i pH)
filtrowanie przez filtry wypełnione materiałem alkalicznym (np. masa MAGNO) MgO + 2CO2 + H2O → Mg(HCO3)2
Wzrasta twardość węglanowa, zasadowośc i pH wody) //
wiązanie CO2 za pomocą wody wapniowej Ca(OH)2 + CO2 → CaCO2 + H2O
Wytrąca się osad: sodu - Na2CO3 + CO2 + 2H2O → 2NaHCO3 + H2O// ługu -NaOH + CO2 → NaHCO3 // wzrasta zasadowość i pH wody.
Techniki membranowe
są to techniki pozwalające na separację zanieczyszczeń na poziomie molekularnym lub jonowym; są to procesy nowe, a ich szybki rozwój obserwuje się w ciągu ostatnich 10 lat; procesy te wykorzystywane są najczęściej do odsalania wody, natomiast rzadziej do zmiękczania wody oraz usuwania z niej substancji organicznych, w tym związków refrakcyjnych oraz kursorów halogenowych połączeń chloroorganicznych, jak również bakterii i wirusów;
W technologii uzdatniania wody wykorzystuje się następujące metody membranowe:
mikrofiltracje - (MF) - do usuwania zawiesin (<1μm) oraz części koloidów; bazują na mechanizmie sitowym, a siłą napędową tych procesów jest różnica ciśnień po obu stronach membrany
ultrafiltrację - (UF) - do usuwania zawiesiny (<1μm), wszystkich koloidów, bakterii, pewnej ilości rozpuszczonych zw. organicznych; bazuje na mechanizmie dyfuzyjno - sitowym.
nanofiltrację - (NF) - do zmiękczania i częściowego odsalania, usuwane są wszystkie zanieczyszczenia poza solami jednowartościowymi (np. NaCl), bazuje na mechanizmie dyfuzyjno - sitowym.
odwróconą osmozę (RO) - usuwane są wszystkie zanieczyszczenia oraz domieszek zawartych w wodzie w tym gazowym, produktem jest woda odmineralizowana, polega na dyfuzji cząstek przez półprzepuszczalną membranę pod wpływem ciśnienia wyższego od ciśnienia atmosferycznego
elektrodializę (EDR) - usuwane są wszystkie zanieczyszczenia oraz domieszek zawartych w wodzie w tym gazowym, produktem jest woda odmineralizowana, opiera się na dyfuzji jonów przez membrany jonowymienne wymuszonej potencjałem elektrycznym.
Czynnikiem decydującym o uzyskaniu stopnia separacji jest rodzaj membrany oddziaływującej na przepływ jonów lub cząstek przez membranę. Membrana jest cienką przegroda pozwalającą na selektywny transport masy.
ZJAWISKO OSMOZY
Osmoza - zjawisko polegające na jednokierunkowym przenikaniu cząsteczek rozpuszczalnika (np. wody) do roztworu (solanki) przez błonę półprzepuszczalną
oddzielającą rozpuszczalnik od roztworu. Na skutek różnicy potencjałów chemicznych obu cieczy rozpuszczalnik przechodzi od roztworu bardziej rozcieńczonego
do roztworu bardziej stężonego, to jest w kierunku wyższego stężenia, aż do uzyskania równowagi potencjałów chemicznych.
Zgodnie z prawem vaint Hoffa ciśnienie osmotyczne: Π = cRT [Pa] T - temperatura [K] c - stężenie substancji rozpuszczonych [kmol/m3]
R - stała gazowa [kJ/kmolK]
Przyłożenie ciśnienia zewnętrznego (większego od ciśnienia atmosferycznego) po stronie roztworu bardziej stężonego powoduje przepływ rozpuszczalnika z roztworu bardziej stężonego do roztworu rozcieńczonego, a więc w kierunku przeciwnym do naturalnego - zjawisko to nosi nazwę odwróconej osmozy.
Parametry określające przebieg procesu odwróconej osmozy:
![]()
współczynnik eliminacji substancji rozpuszczonych (stopień zatrzymania), który określa w jakim stopniu membrana eliminuje substancje rozpuszczone
c1 - stężenie substancji rozpuszczonych w wodzie
c2 - stężenie substancji rozpuszczonych w substracie
stopień konwersji (odzysku)
![]()
Qp - natężenie przepływu parametru (produktu)
Qt - natężenie przepływu produktu zasilającego
przepuszczalność membrany (miara wydajności hydraulicznej procesu)
![]()
Vv - objętość roztworu t - czas sm - powierzchnia membrany
Δp - różnica ciśnień po obu stronachmembrany
4
![]()
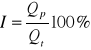
![]()
Wyszukiwarka
Podobne podstrony:
Was2, Inżynieria Środowiska, mgr 1 semestr, Uzdatnianie wody do celów przemysłowych, wykłady, opraco
Was1, Inżynieria Środowiska, mgr 1 semestr, Uzdatnianie wody do celów przemysłowych, wykłady, opraco
Egzamin-Woda-2006, Inżynieria Środowiska, mgr 1 semestr, Uzdatnianie wody do celów przemysłowych, wy
Wasowski wykłady, Inżynieria Środowiska, mgr 1 semestr, Uzdatnianie wody do celów przemysłowych, wyk
24a UZDATNIANIE WODY DO CELÓW PRZEMYSŁOWYCH
24a UZDATNIANIE WODY DO CELÓW PRZEMYSŁOWYCH
Sprawko2, Inżynieria środowiska, inż, Semestr V, Oczyszczanie wody, laboratorium
ściąga pyt 1, Inżynieria środowiska, inż, Semestr V, Oczyszczanie wody
Analiza systemowa, Inżynieria Środowiska, mgr 2 semestr, Analiza systemowa, wykłady, przodki, opraco
HES wykłady 2009, Inżynieria Środowiska, mgr 1 semestr, Ekonomika przedsiębiorstw komunalnych
Analiza systemowa - egzamin, Inżynieria Środowiska, mgr 2 semestr, Analiza systemowa, wykłady, przod
AS-1, Inżynieria Środowiska, mgr 2 semestr, Analiza systemowa, wykłady, prezentacje
Sprawko3, Inżynieria środowiska, inż, Semestr V, Oczyszczanie wody, laboratorium
więcej podobnych podstron