ŻABICKA AGATA dnia 9.04.2002r.
WTŻ gr.10.
22. WYZNACZANIE CIEPŁA WŁAŚCIWEGO CIAŁ STAŁYCH.
Celem mojego ćwiczenia jest wyznaczenie ciepła właściwego ciała stałego.
Ilość ciepła Q pobranego przy ogrzaniu ciała od temperatury T1 do temperatury T2 (lub oddanego przy jego stygnięciu od T2 do T1) zależy od rodzaju ciała i jest proporcjonalna do jego masy i uzyskanej zmiany temperatury:
![]()
, gdzie
c- współczynnik proporcjonalności nazywany średnim ciepłem właściwym w zakresie temperatur odT1 do T2.
Wzór definiujący ciepło właściwe otrzymujemy z przekształcenia wzoru na ilość ciepła:
![]()
Ciepło właściwe jest to ilość ciepła potrzebna do ogrzania jednostki masy o jednostkę temperatury.
Jednostką ciepła właściwego jest ![]()
.
WYZNACZANIE CIEPŁA WŁAŚCIWEGO CIAŁA STAŁEGO:
Przy wyznaczaniu ciepła właściwego ciała stałego posługujemy się kalorymetrem.
Aby dokonać pomiaru ciepła właściwego c ciała, ogrzewamy go do temperatury t1 i umieszczamy w kalorymetrze z wodą o temperaturze początkowej t0. kontakt ciała z wadą powoduje szybką wymianę ciepła, dzięki czemu ustala się wspólna temperatura t wody, kalorymetru i badanego ciała. Ciało oddaje przy tym ilość ciepła Q1:
Q1=m1c(t1-t)
Woda i kalorymetr pobierają ciepło w ilości Q2:
Q2=(mwcw+mkck)(t-t0), gdzie:
mw- masa wody w kalorymetrze
mk- masa kalorymetru
cw i ck- ciepło właściwe wody i kalorymetru.
Ponieważ układ jest izolowany cieplnie, to:
Q1=Q2
Z powyższych trzech wzorów wynika, że szukane ciepło właściwe ciała stałego jest wyrażone wzorem:
-1-
![]()
WYKONANIE ĆWICZENIA:
Na wadze laboratoryjnej ważę badane ciało- jego masę oznaczam m1:
POMIAR I POMIAR II
m1=0,0227kg m1=0,0255kg
Ważę suchy kalorymetr właściwy z mieszadełkiem- mk:
mk=0,2200kg
Do kalorymetru wlewam wodę (ok.1/3 jego objętości) i ważę go- m2. następnie obliczam masę wody wlanej do kalorymetru ze wzoru:
mw=m2-mk.
POMIAR I POMIAR II
m2=0,3278kg m2=0,3325kg
mw=0,1078kg mw=0,1124kg
Wsypuję badane ciało do probówki, i umieszczam probówkę w pojemniku z gorącą wodą.
Notuję temperaturę t1 jaka się ustaliła, a następnie mierzę temperaturę wody w kalorymetrze- t0. Po zmierzeniu temperatury wsypuję ciało do kalorymetru.
POMIAR I POMIAR II
t1=50,2°C t1=48,4°C
t0=20,6°C t0=17°C
Wodę w kalorymetrze mieszam, a następnie mierzę jej temperaturę t, jaka się ustali:
POMIAR I POMIAR II
t=21,6°C t=18,8°C
Obliczam ciepło właściwe ciała.
Obliczam średnią wartość ciepła właściwego ciała stałego.
OBLICZENIA:
Liczę ciepło właściwe ciała z pierwszego pomiaru korzystając ze wzoru:
![]()

-2-
Liczę ciepło właściwe z drugiego pomiaru:

Obliczam średnią wartość ciepła właściwego ciała stałego:

RACHUNEK BŁĘDÓW:
Błąd obliczam dla jednego z dwóch pomiarów- dla pomiaru I.
tx≡t-t0=1°C
ty≡t1-t=28,6°C
W celu uproszczenia zapisów do wzoru wprowadzone zostały oznaczenia i wówczas:
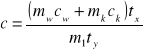
Błąd bezwzględny Δc liczę na podstawie powyższego wzoru metodą różniczki zupełnej.
Zakładamy, że cw i ck nie są obarczone błędem.
Wówczas:
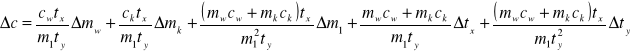
gdzie:
Δm1=Δmk=Δm, Δm- dokładność ważenia:
Δm=0,0001kg
Δmw=2Δm=0,0002kg
Δtx=Δty=2Δt=0,2°C
Δc=tx/(m1ty)(cwΔmw+ckΔmk)+c(Δm1/m1+Δtx/tx+Δty/ty)
Δc=1°C/(0,0227kg·28,6°C)(4,19·103J/kg·K·0,002kg+896J/kg·K·0,0001kg)+ +1,29·103J/kg·K(0,0001kg/0,0227kg+0,2°C/1°C=0,2°c/28,6°C)
Δc=274,005J/kg·K
-3-
Bp=Δc/c·100%=274,005/1,29·103·100%
Bp=21,24%
WNIOSKI:
Ciepło właściwe ciała stałego nie zgadza się z wartością tablicową. Różnica pochodzi głównie z niedokładności pomiarów. Błąd powstały w obliczeniach może być wynikiem niedokładności przyrządów pomiarowych: wagi i termometru (przy ważeniu badanego ciała, kalorymetru z mieszadełkiem- pustego i z wodą). Na procent błędu mogło również wpłynąć niedokładne określenie wspólnej temperatury wody, kalorymetru i badanego ciała. Tak duży błąd może być również wynikiem nieuwzględnienia udziału ciepła z otoczenia. Błąd pomiaru związany jest również z utratą ciepła ciała stałego podczas przesypywania go do kalorymetru.
-4-
Wyszukiwarka
Podobne podstrony:
sprawozdanie cwiczenie 22, studia, agrobiotechnologie
ćwiczenia i wykłady - 22 i 23 maja 2010r, Postępowanie cywilne
22. Kroki ustalania ceny, Materiały PSW Biała Podlaska, ZiPM- ćwiczenia
mechana, ruch-plaski-wahadlo3, Data wykonania ćwiczenia: 22
Cwiczenie 22 i
chemia fizyczna-ćwiczenie 22, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczn
Ćwiczenie Chemia 2 (18 10 22 10 2010 r )
cwiczenie nr 1 2011 10 02 13 35 22
mechana, ruch-plaski-wahadlo, Data wykonania ćwiczenia: 22
45 Arkuszy ćwiczeniowych Matura angielski rozmowy sterowane, Arkusz ćwiczeniowy 22, Arkusz ćwiczenio
mechana, ruch-plaski-wahadlo, Data wykonania ćwiczenia: 22
45 Arkuszy ćwiczeniowych Matura angielski rozmowy sterowane, Arkusz ćwiczeniowy 22, Arkusz ćwiczenio
Ćwiczenie Chemia 2 (18.10., 22.10.2010 r.)
Ekonometria-ćwiczenia z 22-10-2000
Ćwiczenie1 22, TiR UAM II ROK, Informatyka
Biochemia 22.01.2012 2 cwiczenia, Biochemia
cwiczenie 22
więcej podobnych podstron