Numer ćwiczenia VI |
Dział analizy i temat ćwiczenia: Rozdzielenie na składniki mieszaniny złożonej z acetonu, wody i siarczanu (VI) miedzi (II) |
Data wykonania: 24.02.2013 |
Grupa 1 |
Imię nazwisko Konrad Nowak |
Nazwisko sprawdzającego |
Uwagi |
|
Ocena |
Wstęp:
Destylacja to rozdzielanie ciekłej mieszaniny wieloskładnikowej poprzez odparowanie, a następnie skroplenie jej składników. Stosuje się ją w celu wyizolowania lub oczyszczenia jednego lub więcej związków składowych.
W destylacji wykorzystuję się różnice prężności par różnych rozpuszczalników w danej temperaturze nad roztworem. W miarę podnoszenia się temperatury prężność par rośnie aż do osiągnięcia wartości ciśnienia otoczenia. Każda ciecz osiąga tę wartość w innej temperaturze i dlatego każda ciecz ma inną temperaturę wrzenia. Powstałe podczas wrzenia pary można schłodzić, co powoduje ich skroplenie.
Rozróżnia się destylację zwykłą i destylację frakcyjną.
Destylację zwykłą stosuje się gdy z mieszaniny różnych substancji trzeba wydzielić jeden składnik o najniższej temperaturze wrzenia lub gdy trzeba zbadać czystość danej substancji poprzez oznaczenie jej temperatury wrzenia.
Destylację frakcyjną stosuje się w przypadku oddzielania kilku lotnych substancji tworzących mieszaninę.
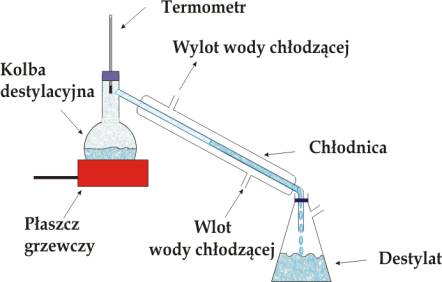
Zestaw do destylacji składa się z trzech części: kolby okrągło dennej destylacyjnej, chłodnicy Liebiega i odbieralnika do zbierania destylatu. Do podgrzewania używa się palnika z siatką azbestową lub płaszcza grzejnego.
W szyjce kolby destylacyjnej umieszcza się termometr (na wysokości wylotu do chłodnicy), a do kolby dodaje się kilka kamyczków wrzennych zapobiegających przegrzaniu cieczy. Mieszanina którą chcemy rozdzielić nie powinna przekraczać połowy objętości kolby.
Ogólny wygląd zestawu destylacyjnego:
Wykonanie ćwiczenia:
Cel doświadczenia: rozdzielenie na składniki mieszaniny złożonej z acetonu, wody i siarczanu (VI) miedzi (II)
Wykorzystany sprzęt: zestaw do destylacji (kolba 250ml, chłodnica Liebiega, zlewki na destylat, płaszcz grzejny, termometr.
Odczynniki: mieszanina CuSO4 wody i acetonu do rozdzielenia.
Wykonanie ćwiczenia:
Do kolby przelano 100ml mieszaniny przeznaczonej do rozdzielenia, następnie wrzucono kilka kamyczków wrzennych by zapobiec przegrzaniu się cieczy. Kolbę umieszczono w płaszczu grzejnym, a następnie zmontowano zestaw do destylacji wraz z termometrem (termometr umieszczono na wysokości wylotu chłodnicy) Po sprawdzeniu szczelności podłączono wodę do chłodnicy i prąd w płaszczu grzejnym.
Po pewnym czasie zauważono, że temperatura zatrzymała się w okolicach 56°C. W tej temperaturze wrze aceton. W odbieralniku zaczął zbierać się destylat. Po pewnym czasie temperatura znowu zaczęła rosnąć (cały aceton już odparował). Zmieniono odbieralnik. Temperatura zatrzymała się ponownie przy ok. 100°C (wrzenie wody). W odbieralniku zebrał się destylat.
Pojawienie się kryształków substancji jest znakiem, że należy zakończyć destylację.
Wnioski:
Temperatury wrzenia wody, acetonu i CuSO4 różnią się znacznie i dlatego można z powodzeniem rozdzielić te substancje poprzez destylację.
Destylacja nie sprawdzi się w przypadku chęci rozdzielenia substancji o podobnych temperaturach wrzenia.
Numer ćwiczenia V |
Dział analizy i temat ćwiczenia: Rozdzielenie na składniki mieszaniny złożonej z węglanu wapnia (CaCO3) i di chromianu (VII) potasu (K2Cr2O7) |
Data wykonania: 24.02.2013 |
Grupa 1 |
Imię nazwisko Konrad Nowak |
Nazwisko sprawdzającego |
Uwagi |
|
Ocena |
Wstęp:
Krystalizacja to proces wydzielania się ciał stałych z ich roztworów w postaci krystalicznej. Krystalizację można wykorzystać do oddzielenia mieszaniny.
Rozpuszczanie substancji w temp. Wrzenia rozpuszczalnika wykonuje się w zestawie przedstawionym na rysunku:
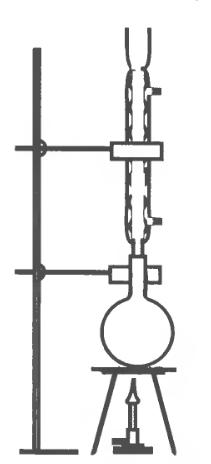
W przypadku oddzielania substancji łatwopalnej można zastosować płaszcz grzejny zamiast palnika.
Na kolbę w której znajduje się mieszanina nakłada się chłodnicę zwrotną, której dolny wylot podłącza się do źródła wody a górny służy do wylewania wody.
Naczynia szklane nie powinny być montowane na sztywno a tylko przytrzymywane przez łapy.
W tak zmontowanym zestawie można przez długi czas ogrzewać substancję w temperaturze wrzenia rozpuszczalnika bez utraty go.
Sączenie wykrystalizowanych substancji odbywa się przeważnie na zestawie do sączenia pod zmniejszonym ciśnieniem.
Wykonanie ćwiczenia:
Cel ćwiczenia: rozdzielenie na składniki mieszaniny złożonej z węglanu wapnia (CaCO3) i dichromianu (VII) potasu (K2Cr2O7)
Wykorzystany sprzęt: kolba okrągłodenna, płaszcz grzejny, chłodnica, łapy podtrzymujące, zestaw do sączenia pod zmniejszonym ciśnieniem, karbowany sączek.
Odczynniki: mieszanina CaCO3 i K2Cr2O7.
Wykonanie ćwiczenia:
Do kolby okrągłodennej (250cm3) umieszczonej na łapie wlano 60cm3 wody destylowanej (odmierzono za pomocą cylindra), a następnie dodano 6 łyżeczek mieszaniny przeznaczonej do rozdzielenia i dwa kamienie wrzenne (zapobiegające przegrzaniu roztworu). Następnie kolbę umieszczono w płaszczu grzejnym i założono na nią chłodnicę. Po sprawdzeniu zestawu uruchomiono ogrzewanie kolby i podłączono wodę do chłodnicy.
Po pewnym czasie stopniowo dodano przez chłodnicę 5ml wody destylowanej, utrzymując wrzenie.
Po rozpuszczeniu się dichromianu (VII) potasu gorący roztwór z kolby przesączono przez sączek karbowany. Na sączku pozostał osad nierozpuszczonego węglanu wapnia, a w przesączu znalazł się dichromian potasu (przesącz koloru pomarańczowego).
Przesącz pozostawiono do ostudzenia. Po ostudzeniu zaczęły krystalizować pomarańczowe kryształy dichromianu potasu, które sączono następnie na Lejku Büchnera pod zmniejszonym ciśnieniem.
Wnioski:
W ćwiczeniu wykorzystano zjawisko zwiększania rozpuszczalności w skutek zwiększenia temperatury.
Wykorzystując to można z dość dużą dokładnością oddzielić od siebie składniki mieszanin.
Numer ćwiczenia
|
Dział analizy i temat ćwiczenia: Rozdzielenie na składniki mieszaniny złożonej z opiłków żelaza i siarki |
Data wykonania: 24.02.2013 |
Grupa 1 |
Imię nazwisko Konrad Nowak |
Nazwisko sprawdzającego |
Uwagi |
|
Ocena |
Wykonanie ćwiczenia:
Celem ćwiczenia było rozdzielenie mieszaniny opiłków żelaza od siarki.
Do rozdzielenia użyto magnesu.
Magnes ma właściwości przyciągające inne metale (np. żelazo)
Po zbliżeniu go do mieszaniny opiłki żelaza zaczęły się na nim zbierać, a siarka pozostała na kartce.
W ten sposób szybko i łatwo można oddzielić metale od innych substancji.
Wyszukiwarka
Podobne podstrony:
9098
9098
9098
9098
więcej podobnych podstron