DIOKSYNY - NOMENKLATURA, POCHODNE I ZWIĄZKI DIOKSYNOPODOBNE
M.R. Dudzińska
Polichlorowane dibenzo-p-dioksyny i polichlorowane dibenzofurany (PCDD/Fs) w odróżnieniu od wcześniejszych polichlorowanych związków chemicznych, jak np. chloro-insektycydy, które znalazły zastosowanie praktyczne, nie były nigdy produkowane komercyjnie i nie znaleziono dla nich żadnego praktycznego wykorzystania. Znalazły się one w środowisku człowieka jako nie zamierzone zanieczyszczenia śladowe, produkt przemian zachodzących w procesach technologicznych i reakcji ubocznych w środowisku.
Potoczna nazwa „dioksyny” oznacza grupę związków będących polichlorowymi pochodnymi dioksyny lub furanu (Rys.1.), czyli polichlorodibenzo-p-dioksyny (PCDDs) i polichloro-dibenzofurany (PCDFs). Są to dwie serie planarnych, tripolicyklicznych, aromatycznych związków o podobnych właściwościach chemicznych i dużej trwałości termodynamicznej. Ze względu na ilość i miejsce podstawienia chloru wyróżniamy 75 izomerów PCDDs i 135 izomerów PCDFs (tzn. kongenerów). Prawie wszystkie z 210 kongenerów zostały odnalezione w próbkach środowiskowych (Hagenmaier i Linding, 1994). Ze względu na toksyczność dla człowieka za najbardziej niebezpieczne uważa się jedynie 17 kongenerów (7 dioksyn i 10 furanów) i zwykle tylko te 17 oznacza się w próbkach środowiskowych. Stąd w potocznym rozumieniu nazwa „dioksyny” funkcjonuje tylko dla tych 17 związków. Na rysunku 1.2 przedstawiono wzór najbardziej znanej (i najbardziej niebezpiecznej) 2,3,7,8-tetradibenzo-p-dioksyny czyli 2,3,7,8-TCDD.
Rys.1. Wzór ogólny: a) dibenzo-p-dioksyny i b) dibenzo-p-furanu wraz z numeracją węgli.
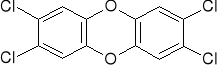
Rys. 2. Wzór 2,3,7,8-TCDD.
Dibenzo-p-dioksyna i dibenzofuran mogą być także podstawione innymi chlorowcami: bromem, jodem, fluorem. Istnieją także pochodne mieszane. Z tego względu ogólna ilość indywiduów, które możemy sklasyfikować jako „dioksyny” sięga kilku-kilkunastu tysięcy.
Omawiając wpływ dioksyn na środowisko, uwzględnia się ostatnio tzw. „dioksyn like PCBs” czyli komplanarne polichlorowane bifenyle, wykazujące toksyczność zbliżoną do toksyczności dioksyn. PCBs to w sumie 209 kongenerów, z czego cztery z non-orto PCBs i osiem z mono-orto jest uwzględnianie w nowej klasyfikacji toksykologicznej, zalecanej przez WHO i uwzględniane w sumarycznej toksyczności polichlorowanych dioksyn, furanów i bifenyli przy ocenie ryzyka dziennego pobrania przez człowieka.
Rys. 3. Wzór bifenylu i jego chloropochodnych.
Między PCBs a PCDD/Fs istnieją dwie zasadnicze różnice. Po pierwsze we właściwościach - PCBs wykazują wyższą prężność par i są wobec tego bardziej lotne. Wykazują także wyższe stopnie biokumulacji w łańcuchu troficznym, głównie wodnym. Druga zasadnicza różnica występuje w źródłach obu grup związków chloroorganicznych do środowiska. PCDD/Fs ciągle powstają (nieintencjonalnie) i są ciągle, jakkolwiek w mniejszych ilościach, wprowadzane do środowiska. Natomiast od kiedy produkcja i stosowanie PCBs zostało zakazane, a produkty je zawierające są stopniowo wycofywane, polichlorowane bifenyle nie powstają jako niechciane zanieczyszczenie.
Do PCDD/Fs podobne są także związki zawierające w swej strukturze zamiast tlenu - siarkę, czyli polichlorowane tiantreny i dibenzotiofeny. Mogą one powstawać w podobnych reakcjach termicznych, jak PCDD/Fs w obecności siarki. Niewiele wiadomo o toksyczności tych związków, jednak przeważa opinia są znacznie mniej toksyczne niż ich analogi zawierające tlen.
Fizyczne, chemiczne i toksykologiczne właściwości PCDD/Fs
Polichlorowane dibenzo-p-dioksyny i dibenzofurany, podobnie jak sama dibenzo-p-dioksyna i dibenzofuran, są bezbarwnymi ciałami stałymi, o temperaturach topnienia powyżej 1000C, niskich prężnościach par i wysokich temperaturach wrzenia. Zebrane dane literaturowe na temat właściwości fizycznych dioksyn można znaleźć w Dudzińska i Kozak (2001). Ze względu na zachowanie w biotycznych i abiotycznych elementach środowiska przyrodniczego, najważniejsze są ich właściwości lipofilne - słaba rozpuszczalność w wodzie, względnie dobra rozpuszczalność w rozpuszczalnikach apolarnych i dobra rozpuszczalność w tłuszczach. Skutkiem lipofilowych właściwości dioksyn oraz niskich prężności par nasyconych jest ich sorpcja na apolarnych powierzchniach ciał stałych - np. popiołów lotnych czy węgla aktywnego, a także na skórze ludzkiej, odzieży, etc.
Tabela 1. Właściwości fizykochemiczne PCDDs i PCDFs
(Hedlund i Rodhe 2004, Dudzińska i Kozak, 2001)
Kongener |
Stała Henry'ego [Pa×m3×mol-1] |
Rozpuszczal-ność w wodzie [ng/dm3] |
log KO/W |
Prężność pary [Pa]
|
Dibenzo-p-dioksyny 2,3,7,8-TCDD TCDDs PeCDDs HxCDDs HpCDDs OCDD |
0,71 0,13 ÷ 0,71 0,12 ÷ 1,48 0,63 ÷ 1,45 0,76 ÷ 1,28 0,68 |
19,3 ÷ 320 118 ÷ 664 4,42 ÷ 167 2,4 (20oC) 0,4 (20oC) |
6,8 6,8 ÷ 7,45 6,64 ÷ 7,45 7,30 ÷ 7,98 8,00 ÷ 8,20 8,20 ÷ 8,60 |
6,27 × 10-5 5,79×10-5 ÷ 6,27 × 10-5 4,31 × 10-6 ÷ 1,20 × 10-5 2,69 × 10-6 ÷ 4,45 × 10-6 1,77 × 10-7 1,19 × 10-7
|
Dibenzofurany 2,3,7,8-TCDF 5.82 ÷ 6.10 2 × 10-8 TCDFs 5.6 ÷ 6.79 1.5 × 10-8 ÷ 4.0 × 10-8 PeCDFs 6.19 ÷ 6.92 1.5 × 10-9 ÷ 4.3 × 10-9 HxCDFs 7.0 5.8 × 10-11 ÷ 1.80 × 10-10 HpCDFs 3.53 × 10-11 ÷ 5.8 × 10-11 OCDF |
1,40 1,46 ÷ 1,50 0,63 ÷ 1,45 0,74 ÷ 1,01 1,41 ÷ 1,42 0,192
|
419
1,35 |
5.82 ÷ 6.10 5,6 ÷ 6,79 6,19 ÷ 6,92 7,0 7,40 ÷ 8,0 8,0 ÷ 8,8 |
2 × 10-8 1,5 × 10-8 ÷ 4,0 × 10-8 1,5 × 10-9 ÷ 4,3 × 10-9 5,8 × 10-11 ÷ 1,80 × 10-10 3,53 × 10-11 ÷ 5,8 × 10-11 3,75 × 10-12
|
Właściwości chemiczne
Polichlorowane dibenzo-p-dioksyny i dibenzofurany, są substancjami wyjątkowo trwałymi i stabilnymi termodynamicznie. Podobnie jak chloropochodne bifenyli, są odporne na działanie czynników środowiskowych. Nie ulegają biodegradacji, czyli są odporne na przemiany biochemiczne i hydrolizę. Są także odporne na działanie umiarkowanych kwasów i zasad oraz czynników utleniających innych niż tlen. Szczególną odporność na degradację biochemiczną wykazują kongenery zawierające chlor w pozycjach 2,3,7,8 (bocznych).
PCDD/Fs ulegają utlenieniu dopiero w ostrych warunkach, w wysokiej temperaturze - powyżej 8500C. Znalazło to zastosowanie w procesach destrukcji termicznej odpadów, gdzie wysoka temperatura i nadmiar tlenu sprzyja obniżaniu emisji dioksyn do atmosfery. Duże znaczenie, zarówno przy formowaniu się dioksyn w procesach termicznych, jak i przy ich termicznej destrukcji mają katalizatory. Do katalizatorów wspomagających powstawanie PCDD/Fs zaliczyć możemy jony miedzi(II), żelaza(III), ołowiu(II) i cynku (Huang i Bueckens, 1996), a do katalizatorów przyśpieszających ich rozkład związki chromu lub tytanu (Choi i in., 2000).
Oprócz mechanizmu destrukcji termicznej w wysokich temperaturach, innym znanym mechanizmem rozkładu jest fotoliza i fotodysocjacja przy pomocy promieniowania ultrafioletowego. Proces ten znalazł zastosowanie przy niszczeniu pozostałości PCDD/Fs w laboratoriach chemicznych. Może mieć także znaczenie w obniżaniu stężenia PCDD/Fs obecnych w powietrzu atmosferycznym, jak i zalegających w zapadliskach ekosystemu, jako że dioksyny mogą ulegać fotolizie w fazie gazowej, w roztworach, jak i w formie zaadsorbowanej na powierzchni ciał stałych, w czasie ekspozycji na niektóre długości fali obecne w promieniowaniu słonecznym (Atkinson, 1991, Miller i in.,1989). O ile jednak rozkład termiczny zachodzi do związków prostych, o tyle degradacja fotolityczna to głównie reakcje odszczepienia chloru (dechlorowania), czyli przemiana wyżej chlorowanych kongenerów do niżej chlorowanych.
Odłączanie atomów chloru od wyżej chlorowanych dioksyn i powstawanie niżej chlorowanych może prowadzić do powstawania różnych produktów. Fotodegradacja PCDD/Fs silnie zależy od stanu występowania w środowisku. PCDD/Fs zaadsorbowane na powierzchni gleby lub popiołów lotnych są odporne na degradację i wyjątkowo stabilne w środowisku, natomiast w fazie gazowej fotodegradacja zachodzi w większą prędkością.
Obserwacje degradacji zarówno w naturalnym świetle słonecznym, jak i w lampach rtęciowych wykazały, że wyżej chlorowane kongenery są bardziej wrażliwe na fotodegradację niż niżej chlorowane, a PCDDs są nieznacznie bardziej stabilne niż PCDFs. Oba efekty są lepiej widoczne dla rzeczywistego światła słonecznego (Schuler, Schmid, Schlatter, 1998).
Podstawowe właściwości PCDD/Fs - trwałość, lipofilowość powodują silną sorpcję PCDD/Fs na glebie i pyłach zwieszonych oraz słabą biodegradację, a w związku z tym kumulację PCDD/Fs w osadach dennych, osadach ściekowych i biokumulacja w organizmach wodnych i ziemnych (tkance tłuszczowej) - głównie izomerów tetra-, penta-, hexa- hepta i okta.
Właściwości toksykologiczne
Polichlorowane dibenzo-p-dioksyny i dibenzofurany uważane są za wysoce toksyczne, przy czym stopień toksyczności zależy od ilości i miejsca podstawników chlorowych. Wykazują one różnorodne działanie toksykologiczne: embriotoksyczne, immunotoksyczne, histopatologiczne, endokrynotoksyczne, neurotokyczne, oraz rakotwórcze. Działanie na organizm ludzki jest przedmiotem rozpraw z dziedziny medycyny i nie może być tutaj szczegółowo omawiane. W przypadkach katastrofalnych skażeń środowiska nie odnotowano jednak wyraźnego wzrostu liczby zgonów, gdyż działanie dioksyn jest powolne, niekiedy objawiające się dopiero w pewnych okolicznościach, lub jak w przypadku nowotworów, po kilkunastu - kilkudziesięciu latach. Ostatnie badania wykazują, że właśnie długofalowe skutki działania bardzo niskich dawek PCDD/Fs mogą mieć bardziej znaczący wpływ na zdrowie ludzkie niż początkowo zakładano na podstawie toksyczności ostrej dla niektórych gatunków ssaków. W 1997 roku PCDD/Fs zostały uznane przez Międzynarodową Agencję do Badań nad Nowotworami (IARC) za kancerogen grupy A. Z tego względu trwałość i przemieszczanie PCDD/Fs w środowisku powinno być przedmiotem stałego zainteresowania.
Każdy z 210 kongenerów PCDD/Fs ma inną toksyczność. Zazwyczaj przyjmuje się, że kongenery mające od 1 do 3 podstawników nie wykazują toksyczności, albo tak znikomą, że nie oznacza się ich stężenia w elementach środowiska. Za najbardziej toksyczne uważa się kongenery posiadające podstawniki w pozycjach 2, 3, 7 i 8 (w sumie 17) i tylko 17 najbardziej toksycznych się oznacza. Przyporządkowano im wartości współczynników równoważnych toksyczności - TEF (toxicity equivalent factor). Normowana zawartość dioksyn jest podawana jako TEQ - toxicity equivalent quontity. Parametr TEQ oblicza się sumując zawartości masowe 17 kongenerów pomnożone przez odpowiednie, przyporządkowane im TEF, wg wzoru:
TEQ = (m x TEF)
W ciągu kilkudziesięciu lat badań i pomiaru poziomów dioksyn w środowisku zaproponowano kilka skal przyporządkowujących danym kongenerom wartości TEF, np. proponowane przez NATO, niemieckie, skandynawskie. Najbardziej rozpowszechniła się tzn. skala międzynarodowa, oznaczana jako I-TEQ. W 1998 roku WHO zweryfikowało niektóre wartości, obniżając TEF dla OCDD i OCDF (TEF=0,0001) a podwyższając dla PeCDD (TEF=1). Wtedy także współczynniki TEF przyporządkowano niektórym polichlorowanym bifenylom (non-orto i mono-orto), wykazującym podobny mechanizm oddziaływania na organizmy żywe jak dioksyny.
Kolejna weryfikacja nastąpiła w roku 2005, kiedy to ponownie zmieniono współczynniki dla OCDD i OCDF (podwyższając je trzykrotnie w stosunku do korekty z 1998 r.), obniżono współczynniki dla PeCDF oraz zmieniono współczynniki dla większości PCB (Van de Berg i in., 2006).
Tabela 2. Wartości współczynników TEF wg. (I-TEF) oraz WHO (z roku 1998 i 2005) dla 17 najbardziej toksycznych kongenerów PCDD/Fs
Kongener |
I-TEF |
WHO-TEF (1998) |
WHO-TEF (2005) |
2,3,7,8-TCDD |
1,0 |
1,0 |
1,0 |
1,2,3,7,8-PeCDD |
0,5 |
1,0 |
1,0 |
1,2,3,4,7,8-HxCDD |
0,1 |
0,1 |
0,1 |
1,2,3,6,7,8-HxCDD |
0,1 |
0,1 |
0,1 |
1,2,3,7,8,9-HxCDD |
0,1 |
0,1 |
0,1 |
1,2,3,4,6,7,8-HpCDD |
0,01 |
0,01 |
0,001 |
OCDD |
0,001 |
0,0001 |
0,0003 |
2,3,7,8-TCDF |
0,1 |
0,1 |
0,05 |
1,2,3,7,8-PeCDF |
0,05 |
0,05 |
0,03 |
2,3,4,7,8-PeCDF |
0,5 |
0,5 |
0,3 |
1,2,3,4,7,8-HxCDF |
0,1 |
0,1 |
0,1 |
1,2,3,6,7,8-HxCDF |
0,1 |
0,1 |
0,1 |
1,2,3,7,8,9-HxCDF |
0,1 |
0,1 |
0,1 |
2,3,4,6,7,8-HxCDF |
0,1 |
0,1 |
0,1 |
1,2,3,4,6,7,8-HpCDF |
0,01 |
0,01 |
0,01 |
1,2,3,4,7,8,9-HpCDF |
0,01 |
0,01 |
0,01 |
OCDF |
0,001 |
0,0001 |
0,0003 |
Ponieważ w pracach często porównuje się wartości zmierzone przez różnych badaczy, należy zwracać uwagę kiedy badania przeprowadzono i którą skalę użyto przy przeliczaniu. Jest to szczególnie istotne dla badań w osadach ściekowych, gdzie dominującym kontenerem jest OCDD. Trzy skale przedstawiono w tabeli 2.
Poza toksycznością substancji ulegających biokumulacji, bardzo istotny jest czas ich życia w organizmie. Czasy życia (określane zwykle jako t1/2) zależą od wielu biotycznych i abiotycznych czynników, między innymi metabolizmu, a także ze względu na wysoką lipofilność dioksyn - zawartości tkanki tłuszczowej w organizmie. Dla trwałych lipofilnych chemikaliów zaobserwowano także tym dłuższe czasy życia w organizmie im niższa masa ciała (Geyer i in., 2002).
Zwykle szacuje się, że czas połowicznego trwania PCDD/Fs w organizmie ludzkim wynosi średnio około 8 lat (Sullivan i in. 1991), jednak Geyer i in. (2002) podaje dłuższe czasy połowicznego trwania - np. dla 1,2,3,7,8-PeCDD - 12,6 lat, dla 1,2,3,4,7,8-HxCDD od 26 do 45 lat, dla 1,2,3,4,6,7,8-HpCDD - 80-102 lata, a dla OCDD aż 112-132 lata (zależnie od metody liczenia).
Zmieniając wartości współczynników TEF, Światowa Organizacja Zdrowia zmieniła też dopuszczalne pobrania dzienne dioksyn - TDI (Tolerable Daily Intake). W roku 1998 wprowadzono zalecenie od 1 do 4 pg WHO-TEQ/kg/dzień. Należy jednak pamiętać, że ostatnie zalecenia WHO obejmują także non-orto PCBs. W roku 2001 połączone Komitety Ekspertów FAO i WHO zaleciły jako tymczasowe dopuszczalne pobory: TMI = 70 pg WHO-TEQ/kg masy ciała / miesiąc (Verstraete, 2002).
Drogi pobierania przez organizm człowieka
Różne dane literaturowe dla pomiarów populacji ludzkiej wykazują zawartość PCDD/Fs w tkance ludzkiej na poziomie 5-20 ng-TEQ/kg tłuszczu. Wartość ta oczywiście może się różnić, zależnie od ekspozycji na PCDD/Fs. Żyjemy w ekosystemie, w którym występowało w przeszłości i występuje nadal “tło” dioksyn, co oznacza, że PCDD/Fs występują także w organizmie człowieka - pobierane drogą:
kontaktową (przez skórę),
oddechową,
pokarmową (woda, żywność).
Za najbardziej niebezpieczną dla człowieka uważa się drogę pokarmową. Nawet przyjmując wartości maksymalne dla pobierania drogą oddechową i kontaktową, ponad 90% PCDD/Fs przenika do organizmu ludzkiego z żywnością (Dudzińska i Kozak, 2001). W krajach wysoko rozwiniętych, gdzie spożywa się żywność przetworzoną, a dieta zawiera więcej mięsa i jego przetworów, z żywności pochodzi nawet powyżej 95% pobieranych PCDD/Fs (Winters, D., 2002).
Ponieważ ogólne stężenie PCDD/Fs od lat 80-tych spada, dane literaturowe odnośnie dziennego pobierania z pożywieniem różnią się - zależnie do roku badania oraz uwzględnianej diety. Dane mogą się znacznie różnić zależnie od kraju. I tak może to być od poniżej 100 do nawet 200 pg I-TEQ/ dzień dla osoby o masie ciała około 80 kg. Najnowsze badania w krajach Unii Europejskiej wykazały, że średni pobór dioksyn i PCBs wynosił od 1,2 do 3,0 pg WHO-TEQ /kg masy ciała/ dzień, czyli znaczna część populacji jest narażona na pobrania wyższe niż dopuszczalne (Verstraete, 2002).
Zagrożeniem dla łańcucha troficznego jest bezpośrednia depozycja atmosferyczna oraz skażenia pośrednie, w wyniku których wprowadza się ponownie do środowiska PCDD/Fs skumulowane w zapadliskach biotycznych i abiotycznych, jak np. osady ściekowe.
Ze względu na kumulację w łańcuchu troficznym niezwykle istotne są przemiany i transport PCDD/Fs w poszczególnych elementach środowiska oraz pomiędzy nimi. Na przemiany w elementach ekosystemu mają wpływ przede wszystkim właściwości fizyczne i chemiczne PCDD/Fs, ale także warunki panujące w środowisku i obecność innych substancji, tzn. współzanieczyszczeń.
ŹRÓDŁA PCDD/FS W ŚRODOWISKU.
Źródła PCDD/Fs w środowisku możemy rozpatrywać z dwóch punktów widzenia: mechanizmu - reakcji, prowadzącego do powstania dioksyn albo procesu technologicznego, powodującego ich emisję lub zrzut do środowiska jako produktu ubocznego. Reakcje prowadzące do powstawania dioksyn możemy podzielić na chemiczne, termiczne, enzymatyczne i fotochemiczne (Rappe i in.,1991). Jeśli chodzi o procesy technologiczne, do głównych źródeł należy zaliczyć: produkcję i wykorzystanie chlorofenoli, głównie tri- i pentachlorofenolu, spalanie odpadów komunalnych i przemysłowych, bielenie papieru, przerób wtórny metali kolorowych, produkcję miedzi, magnezu i stali.
Rozróżniamy także tzw. źródła pierwotne - czyli procesy i/lub reakcje, w wyniku których dioksyny powstają z pierwiastków (synteza „de novo”) lub prekursorów oraz źródła wtórne - czyli wtórne zanieczyszczanie środowiska przez produkty i substancje zawierające PCDD/Fs na poziomie śladowym, np. przerób odpadów, wykorzystanie osadów ściekowych.
Reakcje pierwotne były przedmiotem wielu lat badań, przegląd syntez mogących prowadzić do powstawania pierwotnego PCDD/Fs opisano między innymi w Dudzińska i Kozak (2001) oraz Dudzińska (2003). Zasadniczo wyróżnia się powstawanie „de novo” - syntezę z substancji prostych - węgla, tlenu i chloru, zachodzącą najczęściej w wysokich temperaturach, czyli w procesach termicznych, oraz powstawanie z prekursorów - związków chloroorganicznych, które w wyniku prostych reakcji mogą prowadzić do PCDDs lub PCDFs. Tego typu reakcje możemy zaliczyć do termicznych, chemicznych oraz, według ostatnich doniesień także enzymatycznych. Zachodzą one w przemyśle syntez chemicznych, gdzie dioksyny są zanieczyszczeniem śladowym wielu związków chloroorganicznych, jak polichlorowane bifenyle (PCBs), polichlorofenole (PCP), etc. oraz np. w kompoście z osadów lub odpadów.
Każdy proces spalania - od odpadów, poprzez papierosy do drewna - prowadzi do powstawania dioksyn, czy będzie to ognisko rozpalone przez człowieka, czy też naturalny pożar lasu w wyniku uderzenia pioruna.
Do procesów, w których występują szczególnie sprzyjające warunki, a zatem w wyniku których do środowiska mogą być emitowane znaczące ilości PCDD/Fs zaliczamy:
- spalarnie odpadów komunalnych,
- produkcję i przetwórstwo metali,
- spalanie węgla,
- spalanie odpadów szpitalnych i przemysłowych,
- produkcję i wykorzystanie chlorofenoli, głównie tri- i penta-chlorofenolu,
- bielenie papieru,
- recykling metali,
- motoryzację (emisje z silników samochodowych).
Te gałęzie przemysłu wprowadzają do atmosfery emisje zawierające PCDD/Fs, do odbiorników ścieki skażone dioksynami, albo, jak w przypadku przemysłu chemicznego, pestycydów, barwników, itp., ich produkty mogą zawierać ślady dioksyn powstałe w wyniku reakcji ubocznych. Emisje wprowadzone do atmosfery mogą przemieszczać się na duże odległości i w wyniku depozycji atmosferycznej stanowić źródło zanieczyszczenia wód i gleby. Niezwykle istotne jest zatem, w jakich produktach przemysłu chemicznego znajdują się PCDD/Fs. Niektóre z tych produktów dobrze znamy, jak np. herbicydy chloroorganiczne, pestycydy, mieszaniny polichlorowanych fenoli (PCP). Wiele z tych substancji zostało wycofanych z użytku i produkcji w krajach Europy i w USA, ale często są jeszcze stosowane w Azji, a gotowe wyroby sprowadzane do UE. Do najbardziej spektakularnych przykładów należy pentachlorofenol (PCP), wycofany w użytkowania w Europie, ale stosowany do zwalczania szkodników bawełny w Chinach i trafiający w bawełnianych wyrobach i surowej bawełnie importowanej z Chin na rynki USA i UE.
Lista substancji może się zmieniać, bo w dalszym ciągu odkrywamy nowe źródła. W Japonii stwierdzono ostatnio, że istnieją procesy przemysłowe, w których nie intencjonalnie powstają dioksyny jako zanieczyszczenie śladowe, a które do tej pory nie zostały zidentyfikowane i zinwentaryzowane jako źródła dioksyn (Kawamoto, 2002). Do procesów tych należą: produkcja kaprolaktanu (produktu pośredniego w produkcji nylonu), chlorobenzenu, surowych pigmentów, acetylenu i włókien aluminiowych. Z procesów tych dioksyny były wprowadzane do wód powierzchniowych ze ściekami.
W ostatnich latach, ze względu na wprowadzenie szeregu ograniczeń w emisjach ze spalarni odpadów zanotowano dwa zjawiska. Po pierwsze ogólne skażenie środowiska dioksynami w krajach wysoko uprzemysłowionych spadło, po drugie - zmieniły się „główne” źródła emitujące do atmosfery największe ilości PCDD/Fs. Maleje udział spalarni odpadów, rośnie udział emisji z rafinerii metali (głównie miedzi i ołowiu), cementowni, krematoriów, a także niekontrolowanych procesów spalania - wypalanie traw, spalanie domowe. Wycofano z produkcji i stosowania wiele związków chloroorganicznych, ograniczono dawki chloru stosowane w procesach bielenia. Zmalał zatem udział źródeł pierwotnych, a wzrósł udział źródeł wtórnych w skażeniu środowiska dioksynami.
Obecnie niepokój może budzić obieg wtórny dioksyn wyemitowanych do środowiska w latach 70. i 80., gdyż ogólne skażenie środowiska prowadzi do dalszego zanieczyszczania ze źródeł wtórnych - w wyniku recyklingu, przerobu odpadów i osadów ściekowych.
Jednym z trudniejszych aspektów oceny depozycji atmosferycznej jest określenie jaka dawka TEQ może pochodzić z tzw. „nowych” lub „świeżych” dioksyn, wyemitowanych właśnie do atmosfery, a jaki jest udział tzw. dioksyn „starych”, zalegających i krążących w środowisku od lat. Ten wtórny obieg pyłów zanieczyszczonych PCDD/Fs może mieć wpływ zarówno na poziom i rozkład PCDD/Fs w powietrzu atmosferycznym, jak i na efektywność usuwania w wyniku depozycji atmosferycznej.
Pierwotne źródła PCDD/Fs emitują dioksyny głównie do atmosfery (procesy spalania czyli źródła termiczne) oraz do wody - ze ścieków zawierających dioksyny z syntez chemicznych lub produkcji papieru. Do środowiska wodno-glebowego PCDD/Fs mogą być wprowadzane bezpośrednio - ze źródeł wtórnych, takich jak ścieki, osady ściekowe, odpady, kompost z odpadów, chemikalia zanieczyszczone, oraz pośrednio - w wyniku uwalniania do atmosfery (reakcje pierwotne) a następnie depozycji suchej i mokrej.
Gleba zatrzymuje dioksyny i pełni ważną rolę w ich magazynowaniu. Istotna jest też jej rola w zmianie paternu środowiskowego, ponieważ różne kongenery ulegają w różnym stopniu sorpcji na cząstkach gleby. Ze względu na mechanizmy emisji wtórnej z gleby do atmosfery (ulatnianie w fazie gazowej oraz porywanie cząstek gleby) - gleba może być także wtórnym źródłem zanieczyszczenia atmosfery - choć w niewielkim stopniu, a w czasie np. powodzi - także źródłem wtórnego zanieczyszczenia wód (Duarte-Davidson i in., 1997). Jeśli przyjmie się za potwierdzoną hipotezę o naturalnych mechanizmach powstawania dioksyn, to w glebie mogą znajdować się także dioksyny pochodzenia nie-antropogenicznego. W takim przypadku należałoby glebę uznać za źródło pierwotne. Wody powierzchniowe pełnią rolę w transporcie dioksyn odbieranych bezpośrednio ze ściekami, lub opadłymi na powierzchnię w wyniku depozycji atmosferycznej. Do oceanu światowego zanieczyszczenia trafiają w wyniku depozycji atmosferycznej i spływów powierzchniowych. Rolę ostatecznego zapadliska pełnią osady denne.
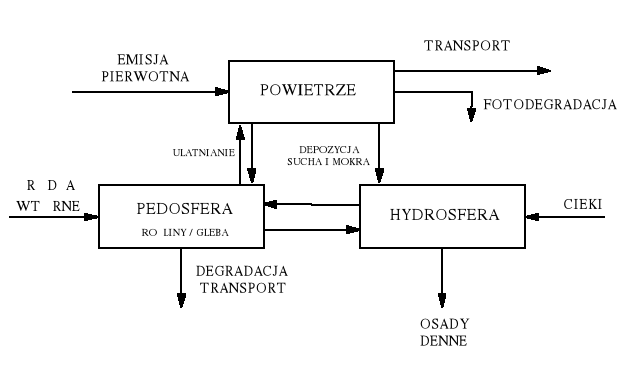
Rys. 4. Emisje i zrzut PCDD/Fs do środowiska oraz możliwe interakcje.
Na powierzchni gleby zachodzi kumulacja dioksyn w warstwie powierzchniowej - o ile degradacja przebiega wolniej niż dopływ ze źródeł. W osadach dennych kumulacja raczej nie zachodzi - nowe warstwy powstają sukcesywnie, i stąd osady stanowią istotne źródło informacji na temat depozycji atmosferycznej w poszczególnych okresach historycznych. Schemat takiego podziału pomiędzy elementy środowiska przedstawiono na rysunku 4.
Źródła PCDDs i PCDFs w Polsce
W Polsce nigdy nie przeprowadzono na szerszą skalę badań skażenia środowiska naturalnego dioksynami, ani obecności tych związków w tkankach ludzkich i mleku karmiących matek. Nie podjęto do tej pory próby sporządzenia, opartego na rzeczywistych pomiarach emisji i tła, bilansu dioksyn.
Ze względu na wymagania aparaturowe, kwalifikacje do pomiaru dioksyn posiadają nieliczne laboratoria, głównie laboratoria badawcze, związane z uczelniami (Kraków, Lublin, Łódź).
Pomiary dokonane w latach 1996-1999 w Krakowie (Grochowalski, 2000), wykazały, że poziom PCDD/Fs w powietrzu atmosferycznym Krakowa był znacznie podwyższony w stosunku do dużych miast Europy Zachodniej. W Krakowie zimą poziom przekraczał 5 pg-TEQ/m3, podczas gdy średnio w Europie Zachodniej notuje się 0,3 pg-TEQ/m3. Pomiary w osadach ściekowych w Lublinie także wykazały wyższe stężenia niż w osadach z Niemiec czy Hiszpanii, jakkolwiek poziom w glebach na terenie miasta był porównywalny z poziomami w glebach z terenów zurbanizowanych w Europie (Dudzińska, 2003).
Główny Urząd Statystyczny podaje roczną emisję dioksyn w oparciu o obliczenia szacunkowe na podstawie ilości i rodzaju źródeł. Według obliczeń w roku 2004 emisja wyniosła ponad 388,7 g I-TEQ (GUS, Ochrona Środowiska, 2006). Ponieważ w Polsce spalanie odpadów nie jest popularną metodą uznaje się, że 48,8% tej emisji pochodzi z procesów spalania w gospodarce komunalnej i mieszkaniowej, czyli ze spalania węgla i innych nośników energii.
Literatura
Adriaens P., Fu Q.Z., Grbic-Galic D., 1995, Bioavailability and transformation of highly chlorinated dibenzo-p-dioxins and dibenzofurans in anaerobic soils and sediments, Environ. Sci. Technol., 29, 2252-2260.
Atkinson, R., 1991, Atmospheric lifetimes of dibenzo-p-dioxins and dibenzofurans, Sci. Total Environ., 104, 17-33.
Barkovskii A.L., Adriaens P., 1996, Microbial dechlorination of historically present and freshly spiked chlorinated dioxins and diversity of dioxin-dechlorinating populations, Appl. Environ. Microbiol., 62, 4556-4562.
Braga A.M.C.B., Krauss T., 2000, PCDD/F-concentrations in soil and cows' milk from a hexachlorocyclohexane contaminated area in Rio de Janeiro-Brasil, Organohalogen Compounds, 46, 354-357.
Broman D., Naf C., Rolff C., Zebuhr Y., 1990, Analysis of PCDD and PCDF in soil and digested sludge from Stockholm, Sweden, Chemosphere 21, 1213-1220.
Bunge M., Ballerstedt H., Lechner U., 2001, Regionspecific dechlorination of spiked tetra- and trichlorodibenzo-p-dioxins by anaerobic bacteria from PCDD/F-contaminated Spittelwasser sediments, Chemosphere 43, 675-681.
Butzkamm-Erker R., Mach R.E., 1990, Neuere Daten uber Dixingehalte in Klarschlammen, Korrespondenz Abwasser 37, 161-168.
Choi W., Hong S-J., Chang Y-S, Cho Y., 2000, Photocatalytic degradation of polychlorinated dibenzo-p-dioxins on TiO2 film under UV or solar light irradiation, Environ. Sci. Technol., 34, 4810-4815.
Clark B., Henry J.G., MacKay D., 1995, Fugacity analysis and model of organic chemical fate in a sewage treatment plant, Environ. Sci. Technol., 29, 1488-94.
Czerwiński J., Dudzińska M.R., Rut B., 2003, GC MS/MS screening of dioxin-like compounds on the example of polychlorinated dibenzothiophene - thio-analogues of polychlorinated dibenzofuranes, Organohalogen Compounds, 60, 462-465.
Czerwiński J., Dudzińska M.R., Rut B., 2002, Determination of polychlorinated dibenzo-p-dioxins and dibenzofurans in the fly ashes from the Hoval type medical waste incinerator, Organohalogen Compounds, 56, 237-239.
Dudzińska M.R., 2003, Występowanie i przemiany polichlorowanych dibenzo-p-dioksyn i dibenzofuranów w układach: osady ściekowe-gleba, Monografie Komitetu Inżynierii Środowiska PAN, vol.14 , Lublin, ISBN 83-80293-15-3.
Dudzińska M.R., 2002, Polichlorowane dibenzo-p-dioksyny i dibenzofurany w osadach ściekowych oczyszczalni ścieków komunalnych - źródła, stężenia i skutki dla środowiska, Monografie Komitetu Inżynierii Środowiska PAN, vol. 11, 545-554.
Dudzińska M.R., Kozak Z., 2001, Polichlorowane dibenzo-p-dioksyny i dibenzofurany - właściwości i oddziaływanie na środowisko, Monografie Komitetu Inżynierii Środowiska PAN, nr 6, stron 159, ISBN 83 915874-4-4.
Engwall M., Schnurer A., 2002, Fate of Ah-receptor agonist in organic household waste during anaerobic degradation-estimation of levels using EROD induction in organ cultures of chick embryo livers, Sci. Tot. Environ., 297, 105-108.
European Dioxin Inventory. 1999: Report for European Commission, DG XI.
Fiedler H., 1993, Formation and sources of PCDD/PCDF, Organohalogen Compounds, 11, 221-228.
Fiedler H., 1996, Sources of PCDD/PCDF and impact on the environment, Chemosphere 32, 55-64.
Geyer H.J., Schramm K.-W., Feight E.A., Behechti A., Steinberg C., Bruggemann R., Poiger H., Henkelmann B., Kettrup A., 2002, Half-lives of tetra-, penta-, hexa-, hepta-, and octachlorodibenzo-p-dioxin in rats, monkeys, and humans - a critical review, Chemosphere 48, 631-644.
Grochowalski A., 2000, Badania nad oznaczaniem polichlorowanych dibenzodioksyn, dibenzofuranów i bifenyli, Monografia 272, Seria Inżynieria i Technologia Chemiczna, Politechnika Krakowska, Kraków.
GUS, Ochrona środowiska 2006, Informacje i opracowania statystyczne, Warszawa 2006.
Hagenmaier, H., Linding, C., She J., 1994, Correlation of environmental occurrence of polychlorinated dibenzo-p-dioxins and dibenzofurans with possible sources, Chemosphere 29, 2163-2174.
Hagenmaier H., She, J., Benz, T., Davidowsky N., Dusterhoft L, Linding C., 1992, Analysis of sewage sludge for polyhagenated dibnezo-p-dioxins, dibenzofurans and diphenylethers, Chemosphere 25, 1457-1462.
Hagenmaier, H., She J., Linding, C., 1992, Persistence of PCDDs and PCDFs in contaminated soil at Maulach and Rastatt in Southwest Germany, Chemosphere 25, 1449-1456.
Hosoya K., Kimata K., Fukunishi K., Tanaka N., 1995, Photodecomposition of 1,2,3,4- and 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD) in water-alcohol media on a solid support, Chemosphere 31, 3687-3698.
Huang H., Buekens A., 1996, De novo synthesis of polychlorinated dibenzo-p-dioxins and dibenzofurans. Proposal of a mechanistic scheme, The Science of the Total Environment 193, 121-141.
Lamparski, L.L., Nestrick T.J., Stenger V.A., 1984, Presence of chlorodibenzodioxins in sealed 1933 sample of dried municipal sewage sludge, Chemosphere 13, 361-365.
Molina L., Diaz-Ferrero J., Coll M., Marti R., Broto-Puig F., Comellas L., Rodriguez-Larena M.C., 2000, Study of evolution of PCDD/F in sewage sludge-amended soils for land restoration purposes, Chemosphere 40, 1173-1178.
Oberg, L., Wagman N., Andersson R., Rappe C., 1993, De novo formation of PCDD/Fs in compost and sewage sludge - a status report, Organohalogen compounds 11, 297-302.
Releases of Dioxins and Furans to Land and Water in Europe, 1999, Raport opracowany na zlecenie Dyrekcji Generalnej ds. Środowiska, Komisji Europejskiej.
Rappe C., 1993, Sources of exposure, environmental concentrations and exposure assessment of PCDDs and PCDFs, Chemosphere 27, 211-225.
Rappe, C., 1994, Dioxin, patterns and source identification, Fresenius J. Anal. Chem., 348, 63-75.
Rappe C., Kjeller L-O., Kulp S-E., de Wit C., Hasselsten I., Palm O., 1991, Levels, profile and pattern of PCDDs and PCDFs in samples related to the production and use of chlorine, Chemosphere 23, 1629-1636.
Rappe C., Anderson R., Karlaganis G., Bonjour R., 1994, PCDDs and PCDFs in samples of sewage sludge from various areas in Switzerland, Organohalogen Compounds 20, 79-84.
Schuler F., Schmid P., Schlatter C., 1998, Photodegradation of polychlorinated dibenzo-p-dioxins and dibenzofurans in cuticular waxes of laurel cherry, Chemosphere 36, 21-34.
Tysklind M., Carey A.E., Rappe C., Miller G.C., 1992, Photolysis of OCDF and OCDD on soil, Organohalogen Compounds 8, 293-296.
Van den Berg M., Birnbaum L.S., Denison M., De Vito M., Farland W., Feeley M., Fiedler H, Hakansson H., Hanberg A., Haws L., Rose M., Safe S., Schrenk D., Tohyama C., Tritscher A., Tuomisto J., Tysklind M., Walker N., Peterson R.E., 2006, The 2005 World Health Organization Reevaluation of Human and Mammalian Toxic Equivalency Factors for Dioxins and Dioxin-Like Compounds, Toxicological Sciences 93(2), 223-241.
Verstratee F., 2002, Development and implementation of an EC strategy on dioxins, furans and dioxin-like PCBs in food and feed, Organohalogen Compounds, 55, 1-4.
Winters D., 2002, Risk management implications of emerging dioxin sciences, Organohalogen Comp. 57, 261-264.
1
Wyszukiwarka
Podobne podstrony:
diox nacodz, WSEiZ, WSEiZ, Diox
Prof R Zuber poprawki 09.12.2012, WSEiZ, WSEiZ
odpowiedzi 2007, WSEIZ, Budownictwo, Semestr III, 3. Materiały do izolacji cieplnej
UKŁAD ODDECHOWY, WSEiZ, WSEiZ, PIELEGNIARSTWO
Zasady komunikacji i metody pozyskiwania informacji o pacjencie, WSEiZ, WSEiZ, PIELEGNIARSTWO
WSEIZ STATYSTYKA W 03 new kopia
ZM II WSEiZ zad 3
ZM II WSEiZ zad 3 wersja poprawiona
WYKŁAD I - Kopia, WSEiZ, WSEiZ, PIELEGNIARSTWO
Diox
TERMINY ZJAZDÓW NA ROK AKADEMICKI 2012-2013 lato, WSEiZ, WSEiZ
pytania demografia więckowska, WSEiZ, WSEiZ, Demografia
WSEIZ STATYSTYKA W 02
Pytania kontrolne do egzaminu z PW, WSEIZ, ZOM1 owizo, Polityka wodna
więcej podobnych podstron