Nanotechnologia sem. III
grupa 3:
Głąbała Konrad
Gniewaszewska Monika
Kowalski Kamil
Lewicka Magdalena
Majkowska Justyna
Rembowska Aleksandra
Szadkowska Karolina
Szejgis Witold
Wiktorowski Kamil
Polimery i materiały funkcjonalne - laboratorium
Ćwiczenie 2
Alkaliczna polimeryzacja kaprolaktamu
data wykonania ćwiczenia: 13 X 2010
Cel ćwiczenia:
Przeprowadzenie procesu polimeryzacji na przykładzie alkalicznej polimeryzacji kaprolaktamu z wytworzeniem poliamidu 6, a także obserwacja efektu egzotermicznego reakcji.
Wstęp teoretyczny:
![]()
Poliamid 6 (PA 6) to termoplastyczny polimer znany także jako nylon 6, Tarnamid lub Steelon.
Ma postać elastycznej masy kolorem zbliżonej do kości słoniowej, może być przezroczysty, jeśli jego warstwa jest wystarczająco cienka. Charakteryzuje się dobrą odpornością na ścieranie, dużą twardością, dobrymi zdolnościami tłumiącymi, udarnością i wysoką ciągliwością, również w niskich temperaturach. Temperatura topnienia waha się w granicach 215-218˚C.
Poliamid 6 znajduje zastosowanie głównie jako tworzywo konstrukcyjne oraz w produkcji włókien syntetycznych. Wytwarza się z niego również elementy takie jak koła zębate, wirniki pomp, detale techniczne, a także folie, rury i pręty.
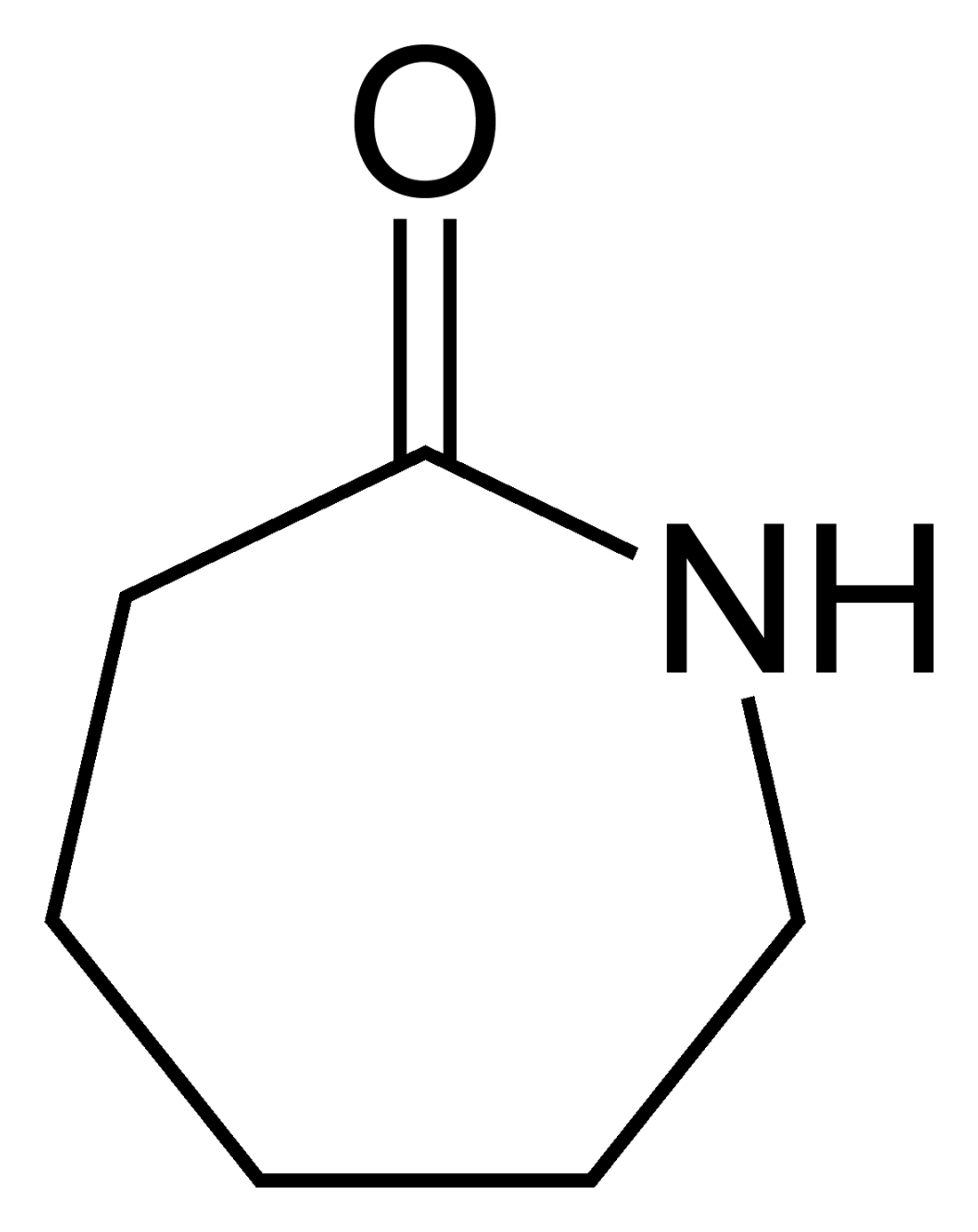
Podstawowym surowcem do produkcji poliamidu 6 jest ε-kaprolaktam czyli laktam kwasu ε-aminokapronowego.
Jest to biała krystaliczna substancja o właściwościach higroskopijnych. Odznacza się charakterystycznym słabym zapachem i gorzkim smakiem. Topi się w temperaturze 69˚C, stając się bezbarwną klarowną cieczą. Kaprolaktam rozpuszcza się zarówno w wodzie, jak
i w rozpuszczalnikach organicznych takich jak benzen, etanol, chloroform, eter etylowy czy octan etylu. Słabo rozpuszcza się natomiast w lekkich węglowodorach parafinowych (n-heksan, n-heptan itp.)
Poliamid 6 otrzymuje się w wyniku polikondensacji lub polimeryzacji anionowej ε-kaprolaktamu. Katalizatorami polimeryzacji anionowej są związki o charakterze zasadowym - metale alkaliczne, ich wodorotlenki, amidy i inne związki. Obecnie stosuje się powszechnie syngrid, dilaktamat i tetralaktamat, które są mniej wrażliwe na obecność zanieczyszczeń i łatwiejsze w dozowaniu.
Wprowadzenie niewielkiej ilości aktywatora - acylolaktamu (lub substancji reagującej z laktamem z utworzeniem acylolaktamu) pozwala znacznie obniżyć temperaturę reakcji. Stosowane są także związki zawierające 3-rzędowe atomy azotu: monocykloalkany, pochodne karbamidowe kaprolaktamu, a także mono- i diizocyjaniany, głównie aromatyczne.
Alkaliczna polimeryzacja laktamów może być prowadzona w rozpuszczalniku (zwykle niepolarnym) lub w bloku (powyżej lub poniżej temperatury topnienia wytwarzanego poliamidu). Polimeryzację poniżej temperatury topnienia poliamidu prowadzić można w sposób pseudoizotermiczny lub adiabatyczny. W metodzie pseudoizotermicznej formę ogrzewa się w stałej temperaturze, wytwarza się gradient temperatury w przekroju bloku. W metodzie adiabatycznej formę ogrzewa się z taką szybkością, aby nie powstawał gradient temperatury, co zapobiega powstawaniu naprężeń w wytwarzanym polimerze.
Na ćwiczeniach laboratoryjnych alkaliczną polimeryzację kaprolaktamu prowadzimy metodą odlewu swobodnego - wyłączamy ogrzewanie, gdy temperatura w reaktorze osiągnie 160˚C, co zapewnia jednorodny rozkład temperatury w całej masie powstającego polimeru. Proces wykonuje się w atmosferze gazu obojętnego - azotu, który zapewnia odpowiednie środowisko reakcji (już 0,65 % wilgoci w powietrzu zahamowałoby reakcję).
Aparatura składa się z formy szklanej umieszczonej w łaźni grzejnej z olejem silikonowym, zaopatrzonej w układ regulacji temperatury, nasadki szklanej umożliwiającej dozowanie katalizatora i aktywatora, zamontowanie mieszadła i kapilary z termoelementem umożliwiającym pomiar temperatury mieszaniny reakcyjnej oraz podłączenie dopływu gazu obojętnego.
Przebieg doświadczenia:
Odważyliśmy 100 g ε-kaprolaktamu i przenieśliśmy do reaktora szklanego umieszczonego w łaźni z olejem silikonowym. Po stopieniu kaprolaktamu wymieniliśmy nasadkę i wprowadziliśmy mieszadło centralne i termoelement w kapilarze, po uszczelnieniu aparatury podłączyliśmy dopływ azotu. Włączyliśmy mieszadło, po osiągnięciu temperatury 110˚C dodaliśmy katalizatora, którym jest dilaktamat (C18H34N2O6AlNa - dikaprolaktaminian bis-(2-metoksy)glino-sodowy) w ilości 0,3 % mol.
Obliczenie wymaganej ilości katalizatora dla 100 g kaprolaktamu:
![]()
Obliczoną ilość katalizatora odmierzyliśmy strzykawką i wprowadziliśmy do reaktora. Następnie zwiększyliśmy temperaturę łaźni. Gdy temperatura w reaktorze wzrosła do 160˚C, dodaliśmy aktywatora „B” (C21H25N4O4 - tolilenokarboamollo-bis-kaprolaktam).
Obliczenie wymaganej ilości aktywatora dla 100 g kaprolaktamu:
![]()
Odważoną ilość aktywatora wprowadziliśmy do reaktora i wyłączyliśmy grzanie. Po 40 s wyłączyliśmy mieszadło i wyjęliśmy je z reaktora, pozostawiając tylko kapilarę z termoparą umożliwiającą monitorowanie temperatury. Dalej obserwowaliśmy efekt termiczny reakcji oraz zmiany zachodzące w reaktorze.
Obserwacje:
Po dodaniu aktywatora i wyłączeniu łaźni zaobserwowaliśmy dalszy wzrost temperatury w reaktorze. Maksymalna zarejestrowana temperatura wyniosła 179,1˚C, po czym zaczęła powoli maleć. W wyniku tworzenia się polimeru zawartość reaktora zaczęła powoli tężeć, a następnie przyjmować mlecznobiałą barwę i obkurczać się. W miarę postępu reakcji obserwowaliśmy coraz większą ilość powstającego polimeru. Po zastygnięciu i wyjęciu z formy otrzymaliśmy produkt - poliamid 6 w postaci białego walca.
Tabela wyników:
czas [min:s] |
temp. [°C] |
0 |
160,6 |
00:23 |
161,2 |
00:46 |
162,0 |
01:09 |
162,3 |
01:33 |
162,5 |
01:56 |
163,0 |
02:19 |
163,9 |
02:42 |
164,8 |
03:05 |
165,6 |
03:28 |
166,3 |
03:51 |
167,1 |
04:14 |
167,9 |
04:37 |
168,9 |
05:00 |
170,2 |
05:23 |
171,7 |
05:46 |
173,4 |
06:09 |
174,9 |
06:32 |
176,3 |
06:55 |
177,2 |
07:18 |
177,8 |
07:41 |
178,3 |
08:04 |
178,8 |
08:27 |
179,0 |
czas [min:s] |
temp. [°C] |
08:50 |
179,1 |
09:13 |
179,1 |
09:36 |
178,9 |
09:59 |
178,5 |
10:23 |
177,9 |
10:46 |
177,6 |
11:09 |
177,9 |
11:32 |
178,2 |
11:55 |
178,4 |
12:18 |
178,5 |
12:41 |
178,3 |
13:04 |
178,1 |
13:27 |
177,6 |
13:50 |
177,1 |
14:13 |
176,9 |
14:36 |
176,8 |
14:59 |
176,8 |
15:22 |
176,8 |
15:45 |
176,8 |
16:08 |
176,6 |
16:31 |
176,3 |
16:54 |
176,2 |
17:17 |
176,0 |
Wnioski:
Polimeryzacja kaprolaktamu jest procesem egzotermicznym. Po zainicjowaniu reakcji pomimo wyłączenia ogrzewania temperatura układu wzrasta aż do osiągnięcia 179,1˚C - maksymalnej temperatury polimeryzacji. Następnie maleje ilość ciepła wydzielana podczas reakcji, w wyniku czego temperatura zaczyna spadać. Drugi pik na wykresie odpowiada prawdopodobnie temperaturze skurczu: 178,5˚C.
Po osiągnięciu wartości maksymalnej temperatura powinna łagodnie opadać. W naszym przypadku jest inaczej, prawdopodobnie dlatego, że środowisko reakcji nie było do końca wolne od wody - mogły pojawić się nieszczelności w instalacji. Przy tym obecność termopary i innych aparatów w reaktorze mogła mieć wpływ na przebieg procesu.
4
![]()
Tmax polimeryzacji = 179,1˚C
Wyszukiwarka
Podobne podstrony:
spr2-kaprolaktam(1), studia, nano, 2rok, 3sem, polimery i materiały funkcjonalne, lab
zabor, studia, nano, 2rok, 3sem, polimery i materiały funkcjonalne, zaliczenie
pytania 1 wykład, studia, nano, 2rok, 3sem, polimery i materiały funkcjonalne, zaliczenie
polimery2010, studia, nano, 2rok, 3sem, polimery i materiały funkcjonalne, zaliczenie
konspekt prezentacji czapor www.przeklej.pl, studia, nano, 2rok, 3sem, polimery i materiały funkcjon
nanomat.pol.6-8, studia, nano, 2rok, 3sem, nanomateriały polimerowe, wykład, opracowanie zagadnień
odp13 łańcuch polimerowy, studia, nano, 2rok, 3sem, nanomateriały polimerowe, wykład, opracowanie za
p rodnikowa odp3, studia, nano, 2rok, 3sem, nanomateriały polimerowe, wykład, opracowanie zagadnień
superabsorbery, studia, nano, 2rok, 3sem, nanomateriały polimerowe, lab
nanopolimery 14-16, studia, nano, 2rok, 3sem, nanomateriały polimerowe, wykład, opracowanie zagadnie
Pytania kol czast NPol 2010 NT, studia, nano, 2rok, 3sem, nanomateriały polimerowe, wykład, opracowa
TSP cz2, studia, nano, 2rok, 4sem, technologie syntezy polimerów, wykład
spr rurki, studia, nano, 3rok, 6sem, polimery w medycynie
spr Chromatografia, studia, nano, 2rok, 4sem, analiza instrumentalna, lab, 11-GC
spr enkapsulacja, studia, nano, 3rok, 6sem, polimery w medycynie
masówka sprawko, studia, nano, 2rok, 4sem, analiza instrumentalna, lab, 4-MS
ai - chromatografia lab, studia, nano, 2rok, 4sem, analiza instrumentalna, lab, 11-GC
spr rurki, studia, nano, 3rok, 6sem, polimery w medycynie
czesc I, studia, nano, 3rok, 6sem, projektowanie wyrobów z materiałów polimerowych
więcej podobnych podstron