Tomasz Świątek
Wydział Biotechnologii i Nauk o Żywności
Kierunek: biotechnologia
Grupa B2
Ćwiczenie nr 53
Tytuł ćwiczenia : Miareczkowanie pehametryczne
Data wykonania ćwiczenia 12.12.2005
Data oddania sprawozdania 19.12.2005
Data zwrotu sprawozdania....................
Data ponownego oddania sprawozdania..............
Słaby kwas |
|
VNaOH [ml] |
pH |
0 |
2,02 |
0,5 |
2,05 |
1 |
1,90 |
1,5 |
1,95 |
2 |
1,98 |
2,5 |
2,07 |
3 |
2,15 |
3,5 |
2,30 |
4,0 |
2,52 |
4,5 |
3,00 |
4,7 |
3,36 |
4,9 |
4,14 |
5,1 |
4,30 |
5,3 |
4,44 |
5,5 |
4,50 |
5,7 |
4,58 |
6,0 |
4,70 |
6,3 |
4,81 |
6,5 |
4,90 |
7,0 |
5,04 |
7,5 |
5,21 |
8,0 |
5,38 |
8,5 |
5,55 |
9,0 |
5,78 |
9,5 |
6,22 |
9,7 |
6,43 |
10,0 |
9,34 |
10,1 |
9,85 |
10,2 |
9,86 |
10,3 |
10,19 |
10,4 |
10,46 |
10,5 |
10,46 |
10,7 |
10,80 |
10,9 |
10,95 |
11,2 |
11,11 |
11,5 |
11,20 |
12,0 |
11,36 |
Tabela wyników
Mocny kwas |
|
VNaOH [ml] |
pH |
0 |
1,86 |
0,5 |
1,87 |
1 |
1,92 |
1,5 |
1,95 |
2 |
2,00 |
2,5 |
2,08 |
3 |
2,16 |
3,5 |
2,28 |
4 |
2,45 |
4,5 |
2,63 |
4,7 |
3,38 |
4,9 |
3,42 |
5,0 |
3,46 |
5,2 |
6,67 |
5,3 |
8,79 |
5,4 |
9,86 |
5,5 |
10,26 |
5,6 |
10,50 |
5,7 |
10,70 |
5,8 |
10,88 |
5,9 |
10,96 |
6,0 |
11,13 |
6,1 |
11,20 |
6,3 |
11,25 |
6,5 |
11,39 |
6,7 |
11,41 |
7,0 |
11,48 |
7,5 |
11,55 |
8,0 |
11,62 |
8,5 |
11,68 |
9,0 |
11,72 |
9,5 |
11,76 |
10,0 |
11,80 |
10,5 |
11,81 |
11,0 |
11,82 |
11,5 |
11,83 |
12,0 |
11,85 |
12,5 |
11,87 |
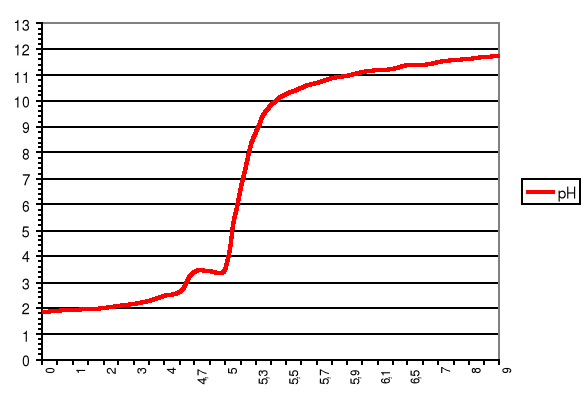
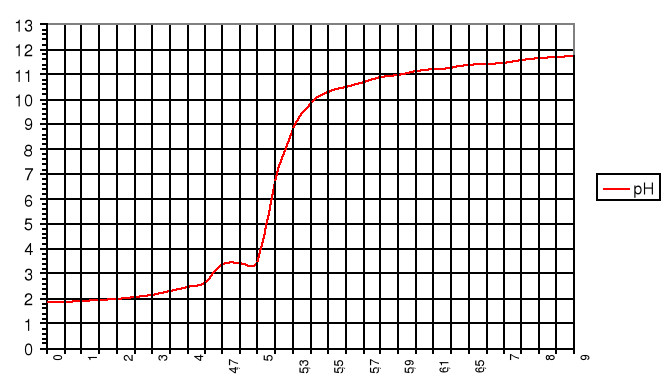
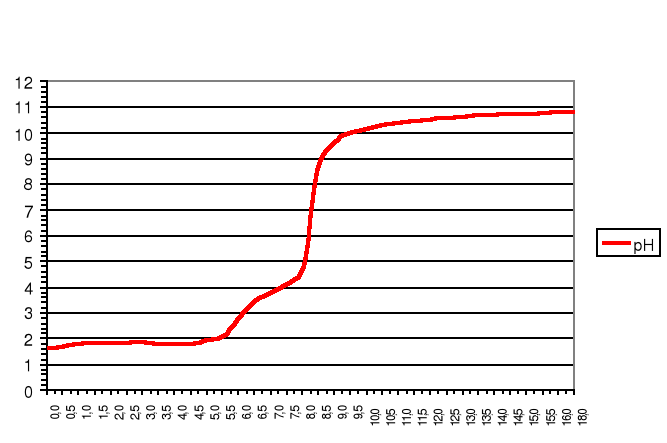
Wykres zmiany pH od objętości zasady
pH
VNaOH [cm3]
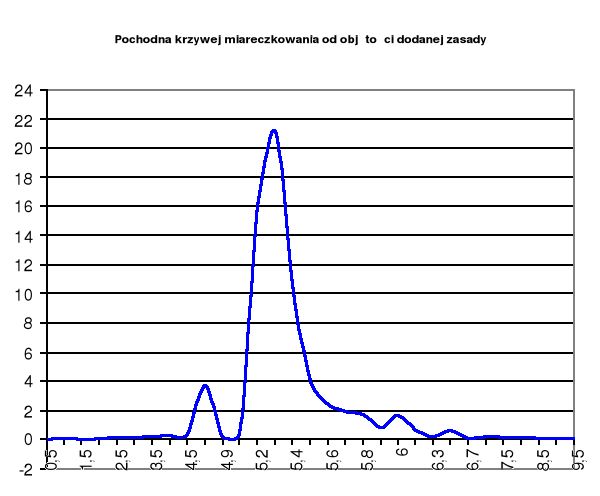
ΔpH
ΔVNaOH
Obliczam liczbę moli mocnego kwasu i stężenie molowe roztworu wyjściowego
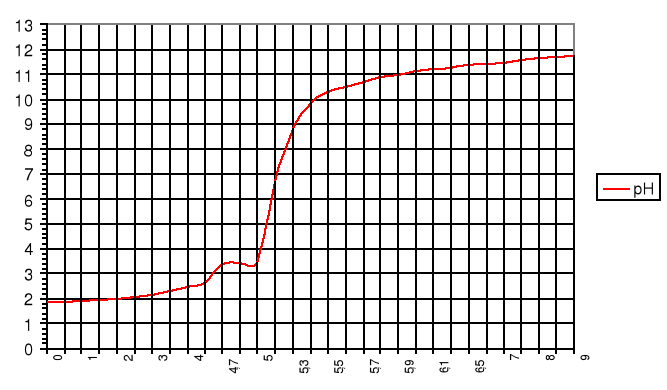
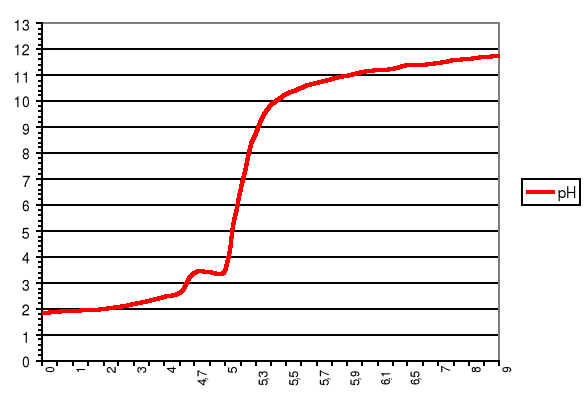
Wykres zmiany pH podczas miareczkowania mocnego i słabego kwasu od objętości zasady
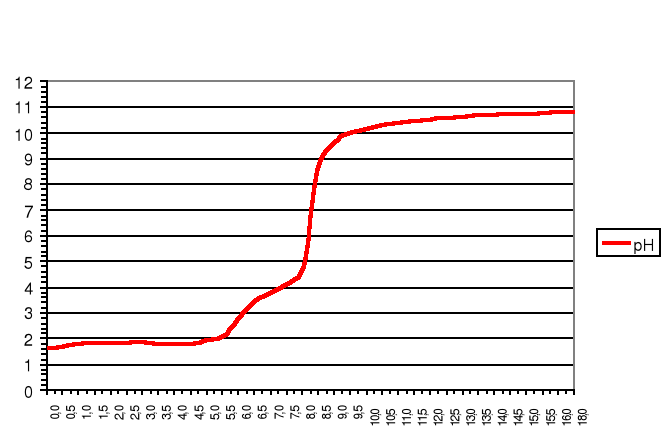
pH
VNaOH [cm3]
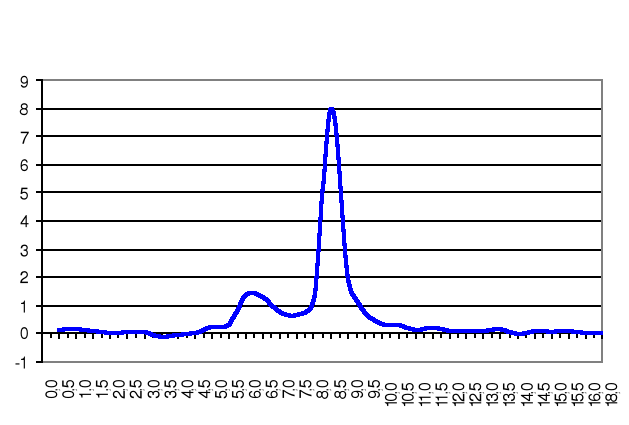
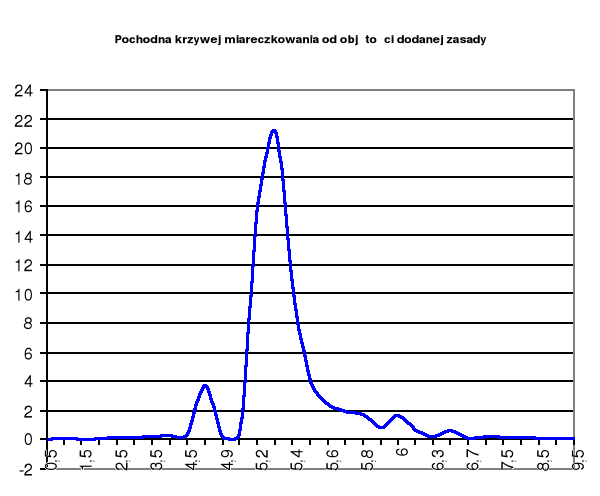
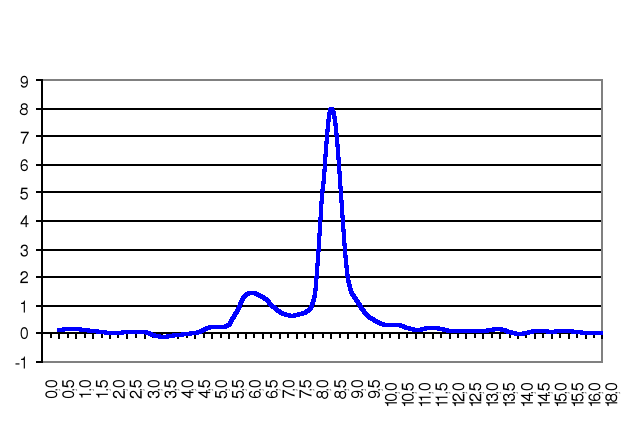
Wykres pochodnej krzywej miareczkowania od objętości dodanej zasady
ΔpH
ΔVNaOH
Obliczam liczbę moli obu kwasów oraz stężenie molowe wyjściowe roztworów kwasów
Uwagi i wnioski
Metodą miareczkowania pehametrycznego wyznaczyć można zarówno stężenie pojedynczego kwasu, jak również stężenie kwasów słabego i mocnego w mieszaninie W przypadku miareczkowania mieszaniny słabego i mocnego kwasu konieczne jest dodanie acetonu, ze względu na istnienie zjawiska rozdziału słabego kwasu organicznego między fazę wody i acetonu. Ma to na celu częściowy rozdział mieszaniny kwasów, w wyniku, czego można wyznaczyć dwa punkty równoważnikowe
Wyszukiwarka
Podobne podstrony:
Moje sprawozdanie nr 45 koniec + wnioski, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
Sprawozdanie moje 44 koniec, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
Moje sprawozdanie nr 45 koniec bez wnioskow, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
Tabelka pomiarowa do 21, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
obliczenia i wnioski, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
konsp15, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
konspekt 53, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
sprawozdanie 45miki, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
Ch.f.44, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
hasz, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
SPRAWOZDANIE 54, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
Cwiczenie 5, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
lab chem fiz 23, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
sprawko 77, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
Ćwiczenie 45 kula, BIOTECHNOLOGIA POLITECHNIKA ŁÓDZKA, CHEMIA FIZYCZNA
więcej podobnych podstron