CCF20121201�000

Ćwiczenie 10<
Temat: Wykrywanie hemoglobiny i jej pochodnych. Identyfikacja produktów rozpadu hemu. Ilościowe oznaczanie hemoglobiny we krwi metodą kolorymetryczną Drabkina.
Hemoglobina
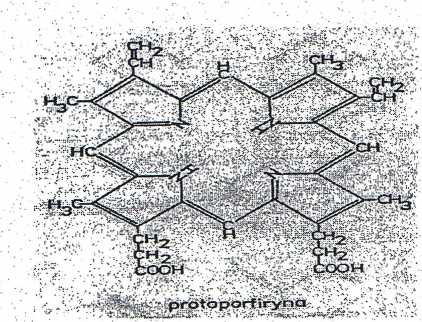
Warunkiem wiązania tlenu przez hemoglobinę .białka należącego d ogrupy hemoprotein jest obecność jednostki niebiałkowej, a mianowicie grupy hemowej.; Składa się ona z części organicznej i atomu żelaza. Część organiczna protoporflryna, zbudowana jest z czterech pierścieni pirolowych, połączonych mostkami • metinowymi. w pierścień tetrapirolowy. Do tego pierścienia przyłączone są łańcuchy boczne, z których cztery są grupami metylowymi, dwa- grupami winylowymi i dwa - resztami kwasu propionowego
Atom żelaza w grupie hemowej, umieszczony w centrum pierścienia protoporfiryny, wiąże się z czterema atomami azotu wiązaniami koordynacyjnymi, piąte wiązanie — z tlenem (zachodzi proces utlenowania), a szóste wiązanie koordynacyjne służy do połączenia z białkiem przez pierścień imidazolowy histydyny.
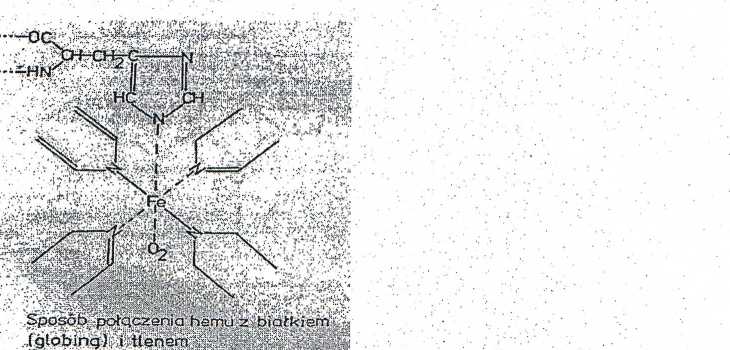
W procesie utlenowania stopień utlenienia żelaza nie zmienia się, powstaje oksyhemoglobina (Hb-02). W przypadku utleniania żelazo zmienia swój stopień utlenienie z Fe+2 do Fe+3 z jednoczesnym przyłączeniem cząsteczki H20, powstaje methemoglobina (Met-IIb).
Hemoglobina jest przenośnikiem tlenu w organiźmie w postaci oksyhemoglobiny tj. hemoglobiny utlenowanej. Cząsteczka hemoglobiny może przyłączyć 4 cząsteczki tlenu atmosferycznego, lg hemoglobiny wiąże 1,36 ml tlenu. Proces utlenowania hemoglobiny i trwałość powstałej oksyhemoglobiny zależy od Ciśnienia parcjalnego tlenu, tzn. od jego stężenia.
Oksyhemoglobina pod działaniem kwasów, zasad i rozpuszczalników organicznych, jak etanol lub aceton, przechodzi w parahematynę, inaczej nazywaną hemichromogenem. Część białkową jest tu denaturowana, a żelazo - w postaci Fe+3. Redukując hemichromogen otrzymuje się hemochromogen, zbudowany z hemu i globiny zdenaturowanej.
Wyszukiwarka
Podobne podstrony:
8
I Rok Wydział Lekarski - „Biologia Medyczna” - Rok Akad. 2015/2016 Ćwiczenie 10 Temat: Genetyka medy
CCF20121201�007 Ćwiczenie 12 Temat: Reakcje barwne charakterystyczne dla wybranych enzymów: katalaza
CCF20121201�006 Ćwiczenie 11 Temat: Witaminy - reakcje barwne. Ilościowe oznaczanie kwasu askorbinow
Ćwiczenie 9 Temat: Ćwiczenie 10 Temat: Ćwiczenie 11 Temat: Ćwiczenie 12 Temat: Ćwiczenie
Rok Wydział Lekarski - „Biologia Medyczna” - Rok Akad. 2013/2014 Ćwiczenie 10 Temat: Genetyka medycz
CCF20120509�006 Ćwiczenie 10 Zróżnicowanie przestrzenne biocenoz 1. Na schematach przekroju oceanu,
temat V (8) 90 saprofitycznych pałeczek pochodzenia jelitowego w produktach żywnościowych wskazuje n
10
13
1a PJWSTKLaboratorium techniki cyfrowej Sprawozdanie z ćwiczeń nr: 10 Temat: System przerwań Imię
015 4 Rys.1.10. Zwarte warstwy heksagonalne w sieci A3 wg [2] 1.3. Zadania do ćwiczenia ZADAKIE 1 Te
więcej podobnych podstron