lepkości
Tablica VI
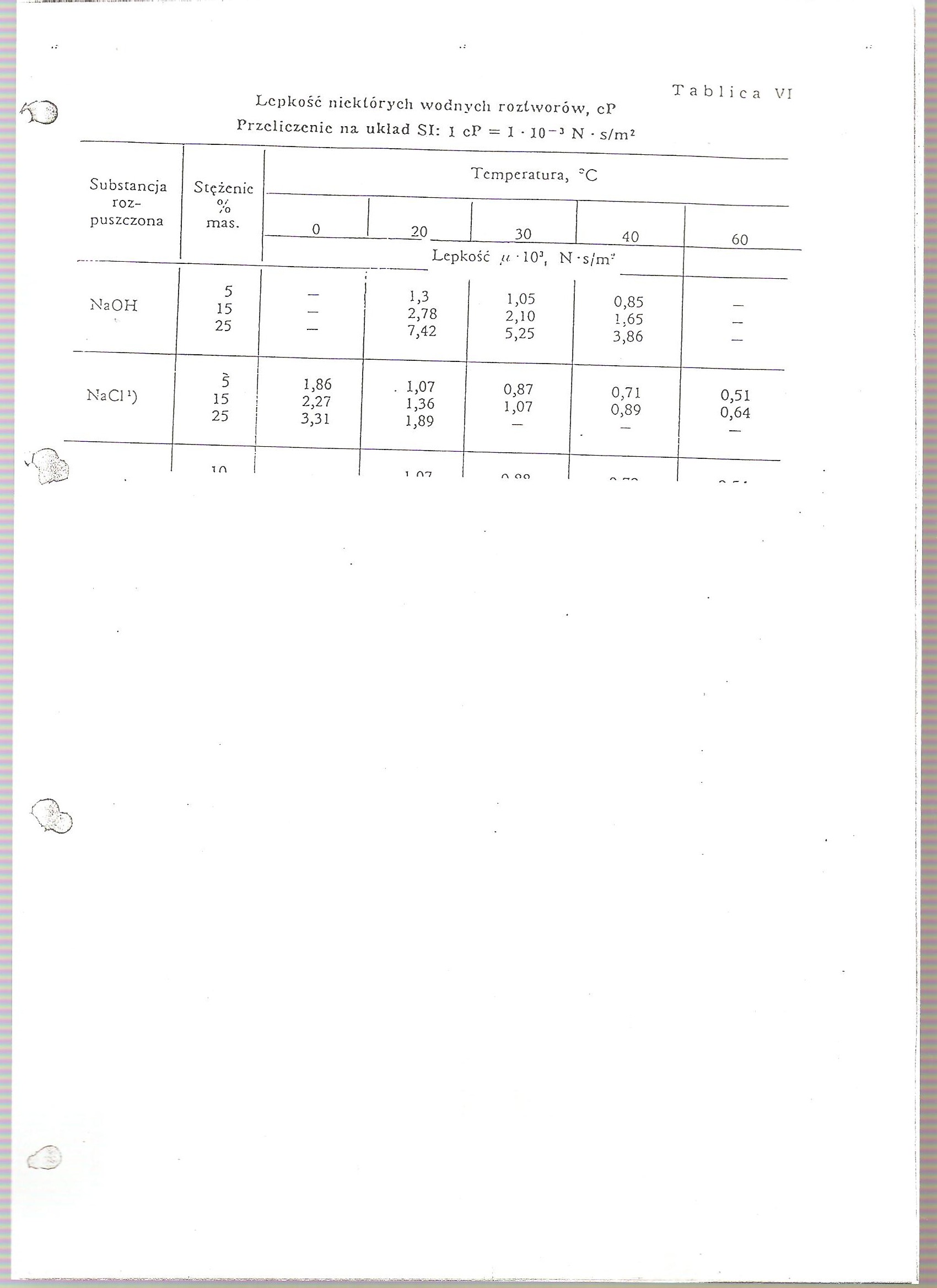
Lepkość niektórych wodnych roztworów, cP Przeliczenie na układ SI: 1 cP = 1 • 10~3 N • s/m2
|
Temperatura, | ||||||
|
Substancja |
Stężenie | |||||
|
roz- |
Ot /O | |||||
|
puszczona |
mas. |
0 |
20 |
30 |
40 |
60 |
|
Lepkość u TO3, N |
•s/m'-’ | |||||
|
5 |
1,3 |
1,05 |
0,85 | |||
|
NaOH |
15 |
— |
2,78 |
2,10 |
1,65 |
— |
|
25 |
— |
7,42 |
5,25 |
3,86 |
— | |
|
5 |
1,86 |
. 1,07 |
0,87 |
0,71 |
0,51 | |
|
NaCl1) |
15 |
2,27 |
1,36 |
1,07 |
0,89 |
0,64 |
|
25 |
3,31 |
1,89 |
— |
• | ||
|
i n 1 |
i m |
r\ oo | ||||


msggammgSSmmSSm
Wyszukiwarka
Podobne podstrony:
własności fizyczne NaCl Tablica 30 Własności fizyczne wodnych roztworów JTaCl (przeliczono wg [7] )
Program zajęć laboratoryjnych, cd, AGH Laboratorium VI -Równowagi jonowe w wodnych roztworach
w3( Przeliczanie stężeń Stężenie molowe roztworu można przeliczyć na stężenie procentowe i odwrotnie
DSC00074 (19) 4,1 cP /4,1.10"^ m 2,7 cP /2,7.10“3 lepkość w 80°C ,u = lepkość w 100°C ąłs= Temp
DSC02122 VI. Właściwości związków nieorganicznych w roztworach wodnych: 1. Zwykle
skanuj0062 (16) 120 5. Równowagi Jonowe w rozclortesonych roztworach wodnych5.1. Roztwory mocnych kw
8 TABLICA VI.Linia Małopolska(i początki Linii Kujawskiej i Mazowieckiej). 1. N. N
SL371935 GRUPA "A" H Obliczyć pH wodnych roztworów 0,01 M NaOH -*lnMHCiOfilM Na3PO«
więcej podobnych podstron