skanuj0070

140
140
(4.7)
(4.8)
dę=_jw_
dr ^+^,1+^,2
Przyrównując stronami (4.6) i (4.7) otrzymujemy równanie: T.-T dT
---= cm—.
Rk+Rsi+R, 2
Po rozdzieleniu zmiennych w równaniu (4.8) i wycałkowaniu go dostajemy, że różnica temperatur pomiędzy grzejnikiem a odbiornikiem zanika w czasie według wzoru:
__T_
AT - ATQ e (RSl+Ksi+Kt)cm _
Gdy powierzchnie grzejnika, odbiornika oraz próbki są polerowane, a badany materiał jest izolatorem cieplnym, wówczas mamy podstawy, aby przyjąć, że: 1
| Rsi + Rs2 « R/c
i wówczas:!
AT s AT0 e’ = AT0 e* r“ . (4.9)
Literatura!
i
[1] S.Wiśniewski: Wymiana ciepła. PWN, Warszawa 1979.
[2] M.Hering: Termokinetyka dla elektryków. Wydawnictwo Naukowo-Techniczne, Warszawa 1980.
Ćwiczenie 11 1
Wyznaczanie równoważnika elektrochemicznego wodoru i miedzi
1. Wprowadzenie
Substancje o wiązaniu jonowym lub cząsteczki polarne (niektórych kwasów, zasad i soli) rozpuszczane w cieczy o dużej względnej przenikalności elektrycznej (np. w wodzie o er = 81) ulegają rozpadowi na jony, czyli dyso-cjacji elektrolitycznej. Roztwory takie nazywamy elektrolitami.
Rozpad cząsteczek obojętnych na jony następuje w wyniku oddziaływania na te cząsteczki dipolowych cząsteczek wody, co prowadzi do rozerwania wiązań chemicznych (patrz rys.l, ćw.15).
W elektrolitach, równolegle do dysocjacji, przebiega proces rekombinacji jonów. W wyniku tych procesów ustala się równowaga dynamiczna pomiędzy liczbą cząsteczek rozpadających się i powstających. W roztworze istnieje zatem pewien stopień dysocjacji a, określony jako stosunek liczby moli cząsteczek zdysocjowanych n, do ogólnej liczby moli cząsteczek n0 zawartych w roztworze:
(1)
n
a - —
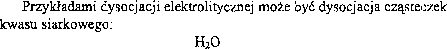
H2S04 2H+ + S04”,.
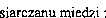
(2)
(3)
Cu SO4 <- '>- Cu++ + SO4
Opracował A.Kubisz.
Wyszukiwarka
Podobne podstrony:
45026 skanuj0025 (140) 5. Międzynarodowe aspekty ochrony przyrody 176 © Grzegorz i Przykłady gatunkó
Skanuj0070 140 Lekcja dwudziesta pierwsza Un dia de julio, nuestros protagonistas se cruzan otrą vez
52108 skanuj0050 (46) 4. Naukowe podstawy prawnej ochrony przyrody 140 ■ zmiany st
38454 skanuj0026 (140) 2. Człowiek i przyroda: od zarania dziejów do współczesności 50 nieoczyszczon
skanuj0012 (140) E. Michlom :cz: B.uidr.ia operacyjne i eksploatacyjne - PodstawyZadania przepływów
więcej podobnych podstron