DSCN4681
Entalpia dowolnych ciał prostych jest funkcją ciśnienia i temperatury.
Podczas wykonywania doświadczeń z adiabatycznym dławieniem gazu doskonałego nie zmienia się entalpia właściwa i temperatura, mimo zmian ciśnienia. Wynika stąd, źe entalpia właściwa gazów doskonałych jest wyłączną funkcją temperatury.
Zjawisko jest nieodwracalne, ponieważ, jak wynika z obserwacji, przepływ przez przewężenie lub przegrodę porowatą jest skierowany zgodnie ze spadkiem ciśnienia.
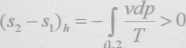
Ponieważ objętość właściwa i temperatura są dodatnie, a ciśnienie maleje, więc entropia w rozważanym nieodwracalnym zjawisku adiabatycznym wzrasta.
Wyszukiwarka
Podobne podstrony:
PB040170 UKŁADY WIELOSKŁADNIKOWE Rozważmy układ dwuskładnikowy. Entalpia swobodna G takiego układu j
skan0105 108 Termodynamika chemiczna 3d:2. Temperatura topnienia [°C] naftalenu jest funkcją ciśnien
66060 PB040170 UKŁADY WIELOSKŁADNIKOWE Rozważmy układ dwuskładnikowy. Entalpia swobodna G takiego uk
DSCN4678 Podczas wykonywania doświadczeń wyrównywania ciśnień w adiabatycznym układzie zamkniętym z
1tom166 7. ELEKTRONIKA 334 Ponieważ iloczyn koncentracji dziur i elektronów (7.1) jest funkcją tylko
skanuj0060 • v rm źle dobranej dawki jest ból pojawiający sit; podczas wykonywania il mi
46584 skanuj0060 • v rm źle dobranej dawki jest ból pojawiający sit; podczas wykonywania il mi
CCI00217 l.Ceł projektu: Określenie zmiany ciśnienia i temperatury podczas przepływu polietylenu mał
II& 350 °C Orientacyjna temperatura wody zasilającej w funkcji ciśnienia pary świeżej; 1 — obieg pro
IMAG0043 Właściwości entalpii 1 nlalpin jest funkcjii stanu Układ ma nkrcśloni
IMAG0064 Afut-iH — Agoyjł + Krótkie w nioski: 1. Ponieważ entalpia jest funkcją st
DSCN4610 Do najczęściej spotykanych rodzin przemian o jednej niezależnej zmiennej dla ciał prostych
ARCHITEKTURA WNĘTRZ Najważniejsza jest funkcjonalność i czytelny prosty układ przestrzenny.
DSCN4610 Do najczęściej spotykanych rodzin przemian o jednej niezależnej zmiennej dla ciał prostych
DSCN4618 Energia wewnętrzna jest funkcją addytywną. czyli energia wewnętrzna układu jest równa sumie
więcej podobnych podstron