img102
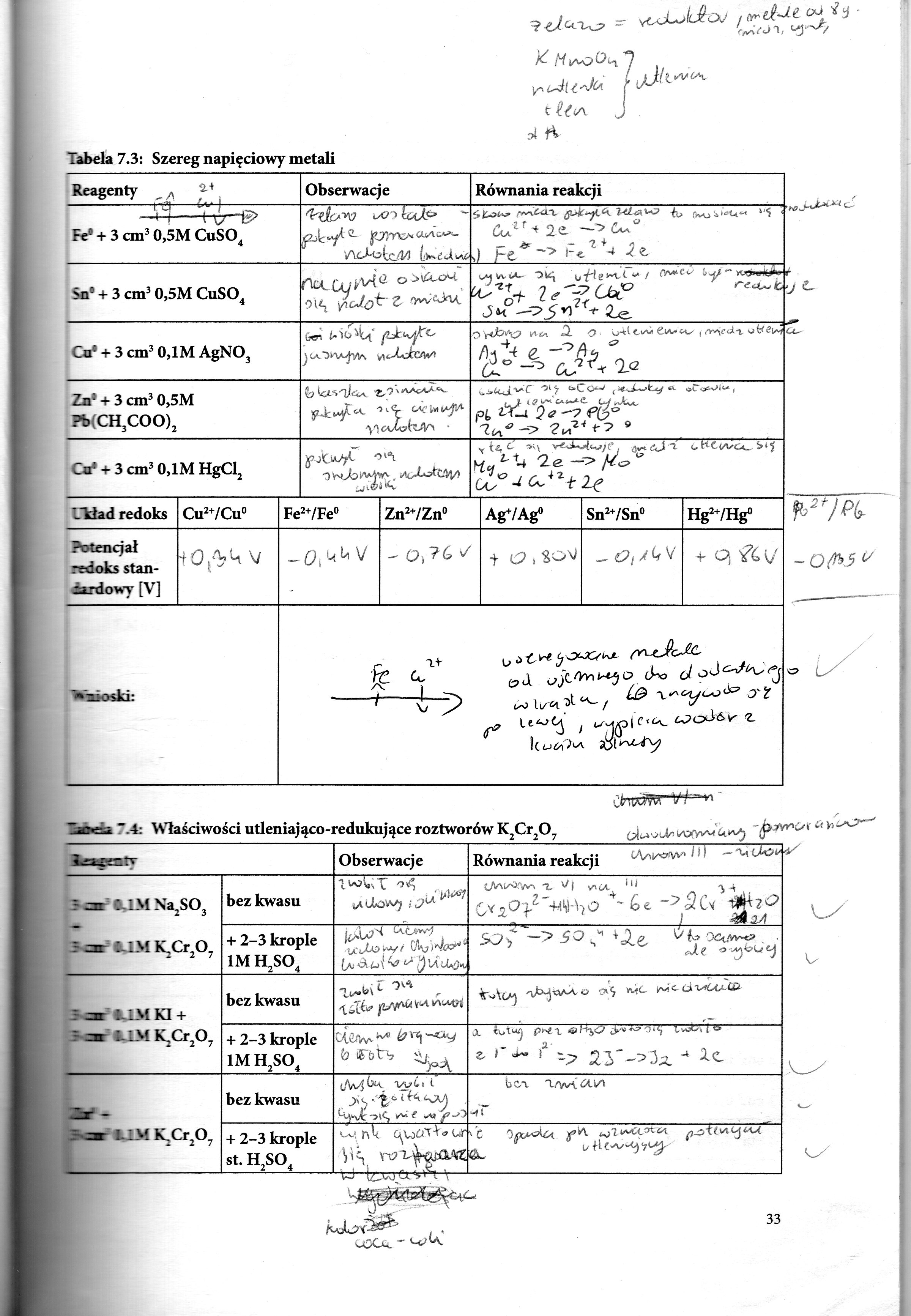
Tabela 7.3: Szereg napięciowy metali
at
Reagenty „A
-hS)-W-
-H-t-X7~®>
Fe0 + 3 cm3 0,5M CuSO
Sn* + 3 cm3 0,5M CuSO
Ca* + 3 cm3 0,1M AgN03
Zn! + 3 cm3 0,5M Pb{CH3COO)2
Obserwacje
t ^<f<A 5I fi
Równania reakcji
^lia^o ijoo hśjp1 ~
iAcT-ol^/M |
ncuu/Md oMa-cM,
9 U* Z ^
«r, i. to ''tf fUc^jto jCOkvy>/V\ w<.-kckcAnA
')vłr
'V^cvMx4''> ■
fr^iCdrL fi.
uCr + 2e -pe ^ I- e
Klą^o {x> ‘“5
— > CA
^ .u
-y
---r Ł y -
^ <f <-Tv ł
um w jA- ">U^ *+ i (^mC
\Ć*l+ le~?< CbP
0ytbi*e? *.*, Ił o- o-Ut-i/we***-*^ 1 t*Ącdi. oć^ew
/)^4 e 47
«j[v>'r oi^ ••co*-' «■ *rwi<-,
#-1 Qe-yeB°
pt
TĄ ~> ?A' t?_
v tą c' r€.J~.fi^JC , HC </Vła_ i1 ■)'
V C-
Ca5 + 3 cm3 0,1M HgCl2
, ^Ł>totC4v?
|
LTdad redoks |
Cu2+/Cu° |
Fe2+/Fe° |
Zn2+/Zn° |
Ag+/Ag° |
Sn2+/Sn° |
Hg2+/Hg° |
|
Potencjał redoks standardowy [V] |
■łO^M V |
-oyu V |
- Oi 76 M |
t C? i sod |
- c?/ d U v |
3- q f 4 q |
|
'"•aioski: |
Yf (*, 4/ —ł—ir5> ^ >^l huo,')^ &l ^ | |||||
oIła u iA*w\4 4 *q /j>> y^u *
p/ypfr
- 0/^.5 ^
".4: Właściwości utleniająco-redukujące roztworów K2Cr2Oy
.Łstisnts"
Obserwacje
Równania reakcji
c/W^w* W-
: nr I lMNa2S03
3 car I IM K.Cr20.
—
r nr ! IM KI +
' nr i- IM K,Cr20_
LIM K,Cr O
bez kwasu
+ 2-3 krople IM H.SO.
_2 4
bez kwasu
+ 2-3 krople IM H SO,
_2 4
bez kwasu
+ 2-3 krople st. ELSO.
T^wc oną ~
CaĆ^-w-/
«//
wJ*>,
l/j ÓlCj'\ ^0 ^ W U*Qaj
IiA L ^ r
to r&H
t/W4 w. yAi t
Ca hU <^votft -V« ur 'jA rtf"M
U tzTCTfctA^t

-U3<A ' W
tMlA^Vvs T. V/| vn,A IM ,
+'će ~yt9.CH 2O
Jr
SCif 50 10 ł^e u‘l> 0Ct/VVtu
9>S «fc iMt dvo<.a> T t,.\uj (!•<! 4i )4jó* iS>“ '3‘ £i ’. -••'-•• i “
ł r ^ 2y->x
boa a/yvióAvi
Ic
M
-fi
f Oa^oCt f^v jTTT7TKj^u‘
fi ^-A/^ *7^^-
CA
33
Wyszukiwarka
Podobne podstrony:
Tabela 2 Tabela 2. Szereg napięciowy metali ELEKTRODA P0™CJAL ELEKTRODA P0™CJAL ELEKTRODA
szereg napieciowy metali SZEREG NAPIĘCIOWY METALI ^IPbłOgnlwró Reakcja elektrodowa np^ mm* Li* +
Zdjęcie0127 Jpgp Wydz. 15l_Itowto, IM
SZEREG NAPIĘCIOWY METALI ^IPbłOgnlwró Reakcja elektrodowa np^ mm* Li* + e ?=*
3. Szereg napięciowy metali Metale uszeregowane według rosnących wartości potencjału normalnego twor
SZEREG NAPIĘCIOWY METALI ^IPbłOgnlwró Reakcja elektrodowa np^ mm* Li* + e ?=*
Szereg napięciowy metali (inaczej szereg elektrochemiczny, szereg aktywności metali) to zestawi
Wnioski wynikające z szeregu napięciowego metali Każdy metal o niższym potencjale normalnym wypiera
SZEREG NAPIĘCIOWY METALI. OGNIWA GALWANICZNE Opracowanie: dr inż. Krystyna Moskwa, dr inż. Bogusław
39639 str058 (4) 115 Praktyczny szereg napięciowy metaliĆWICZENIE NR 13PRAKTYCZNY SZEREG NAPIĘCIOWY
DSCN4174 (2) ^ __. Szereg napięciowy metali J , n O Cs K Ca Na Mg Al Mn Cr Zn .Fe Co Ni Sn Pb H C
DSCN4175 (2) Szereg napięciowy metali Rozpuszczanie metali w kwasach Zn + H2S04 = ZnS04 + H2t 3Cu +
Szereg elektrochemiczny (napięciowy) metali VoIta uszeregował metale pod względem malejącej aktywnoś
więcej podobnych podstron