DSCF6588

132
Jednocześnie powierzchnia styku z powietrzem zewnętrznej ścianki kapiiary i wewnętrznej naczynia wzrosła o AS2:
Ostatni wzór wygodnie jest przepisać w innej postaci, korzystając z 10:
2n(R2 — rj)8h 2nr2(Ah-8h)
Jgl R-ri R-r, W
Wypadkowemu przyrostowi powierzchni:
AS = ASl-AS2 = 2nr^l-jj^-'j(Ah~dh) (14)
odpowiada zgodnie z wzorem 1 następujący przyrost energii potencjalnej: AU2 = er AS = 2kto^1 -jJ—^Ah - 8h) (15)
Z zasady prac wirtualnych AU^ = AU2, czyli:
Ze związku tego można wyznaczyć współczynnik napięcia powierzchniowego er:
a =
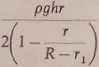
(17)
W przypadku, gdy promień naczynia jest znacznie większy od promienia kapiiary, wzór 17 upraszcza się do 8.
4. Zastosowanie
Ciśnienie występujące w rurkach kapilarnych odgrywa ważną rolę przy dostarczaniu glebie wilgoci. Wprawdzie korzenie roślin sięgają w głąb na nie więcej niż 30 § 40 cm, jednak dzięki porowatej strukturze gleby (pory spełniają rolę kapilar) zapas wody w górnych warstwach może być uzupełniany.
Zjawiska napięcia powierzchniowego odgrywają rolę także w procesach piania, flotacji, przy produkcji tkanin nie przepuszczających wody itp.
Interesujący jest związek napięcia powierzchniowego z molowym ciepłem palowania oraz takimi wielkościami jak rozmiary cząsteczek cieczy i liczba apteczek w 1 molu (Waterson, 1858). Wyobraźmy sobie mol cieczy •r postaci sześcianu o krawędzi a = Nd, gdzie d oznacza średnicę pojedynczej apteczki, N - liczbę cząsteczek tworzących krawędź:
M
N*d* = Vm = — (18)
y - oznacza objętość molową, M — masę cząsteczkową, p - gęstość.
Jeśli rozetniemy sześcian na warstwy o grubości jednej cząsteczki, otrzymamy N warstw o grubości d każda. Powtarzając tę operację w pozostałych wymiarach otrzymamy N3 = NA oddzielnych cząsteczek, gdzie NA oznacza liczbę cząsteczek w 1 molu (liczba Avogadro).
Ponieważ każde rozcięcie sześcianu odpowiada przyrostowi powierzchni 2a2 = 2N2d2, a na każdy z trzech wymiarów przypadło N rozcięć, wobec tego łączny przyrost powierzchni wyniósł:
S = 6 N3d2 (19)
Zgodnie z wzorem 1 odpowiada temu przyrost energii potencjalnej:
Upm. = 6 erN3d2 (20)
Z drugiej strony, energia potrzebna do tego, aby mol cieczy rozdzielić na pojedyncze cząsteczki, jest to po prostu molowe ciepło parowania L=Mcp, gdzie cp oznacza ciepło parowania odniesione do jednostki masy. Ostatecznie więc otrzymujemy z wzorów 18 i 20 następujące wyrażenia na wielkość i liczbę cząsteczek w jednym molu:

5. Pomiary
Pomiar wysokości słupa cieczy dokonywany jest przy użyciu katetometru, średnicę kapilar mierzymy za pomocą mikroskopu.
Wyszukiwarka
Podobne podstrony:
4 (225) Tarciem nazywa się zjawisko powstawania sit stycznych do powierzchni styku dwóch ciał Tarcie
skanuj0085 (35) d Ci, c2 średnica nominalna, równa w przybliżeniu średnicy walcowej powierzchni styk
Badania SEM powierzchni styków z kompozytu WC-Ag... powierzchni styku. Tam, gdzie na powierzchni będ
skanowanie0015 URSA GLASSWOOL*Stropodachy dwudzielne, wentylowane powietrzem zewnętrznym • 153. Okap
2162 Bartosz Kaźmierczak powierzchni rdzenia powietrznego osiągnąć ciśnienie otoczenia. Wytwarzający
IMG311 • temperatura powietrza zewnętrznego (tj • wilgotność
INSTRUKCJA PUG@5 ■ Posmarować cienko gwint oraz powierzchnię styku śrub głowicy
Instrukcja obslugi COLT CZ5 3 Komfort jiuih Pobieranie powietrza zewnętrznego inrannn Aby podczas
skanowanie0008 Naprężenia ścinające kołek na powierzchni styku czopa i piasty.
skanowanie0023 3 Minimalna ilość powietrza zewnętrznego: • Dla wszystkich pomieszc
więcej podobnych podstron