3582300479
I 1P- 1
m Zaznacz wzór sumaryczny i masę cząsteczkową wodorotlenku żelaza(III).
A. Fe3OH, 185 u B. Fe(OH)3, 107 u C. Fc3OH, 87 u D. Fe(OH)3, 73 u
\ 2P. 1

Odpowiedź:
ni Oblicz zawartość procentową (procent masowy) metalu w wodorotlenku glinu i stosunek mas pierwiastków chemicznych w tym wodorotlenku.
m Zaznacz numery probówek, w których w wyniku zachodzącej reakcji chemicznej powstaną wodorotlenki. Zapisz równania reakcji otrzymywania tych wodorotlenków i określ, jaką barwę w ich roztworach przyjmie fenoloftaleina. | 2p. |
|
Schemat doświadczenia |
Sr h2o — |
ił i |
S2i h2o — |
ił 2 |
NaC NaOH — |
jł 3 O |
CaO h2o- |
ił 4 | ||||
|
Równanie reakcji otrzymywania wodorotlenku | ||||||||||||
|
Barwa fenoloftaleiny | ||||||||||||
2i~l
IB Oblicz, ile gramów sodu oraz ile gramów wody należy użyć, aby otrzymać 20 g wodorotlenku sodu. Obliczeń dokonaj na podstawie odpowiedniego równania reakcji chemicznej.

Odpowiedź:
Ba
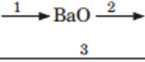
Ba(OH)2
IB Napisz równania reakcji chemicznych przedstawionych na schemacie. 1.
2.
3._
IB
Zaprojektuj doświadczenie, w którym otrzymasz wodorotlenek miedzi(II). Narysuj schemat, zapisz obserwacje_
i sformułuj wniosek. Napisz równanie reakcji chemicznej. | 2p. |
Obserwacje:
Wniosek:
Równanie reakcji chemicznej:
•03 Oblicz, ile gramów wodorotlenku cyny(II) powstało, gdy do roztworu zawierającego 5 g chlorku cyny(II) dodano roztworu wodorotlenku potasu, w którym rozpuszczono 2,24 g tego wodorotlenku.
Wyszukiwarka
Podobne podstrony:
45 (189) Wodorotlenek żelaza(III) Fe(OH)3 Wodorotlenek żelaza(III) jest to brunatny proszek o gęstoś
rozpuszczonym w elektrolicie tlenem daje brunatną rdzę, będącą mieszaniną wodorotlenków żelaza(III)
str (156) 7. W celu otrzymania osadu wodorotlenku żelaza(III) należy: a) użyć bezb
11. Napisz wzór sumaryczny i strukturalny oraz oblicz masę cząsteczkową siarkowego (IV) 12. Wybierz
Wodorotlenek sodu 1) Budowa Wzór sumary czny 2) Otrzymywanie 2H-.Ó 2 NaOH NaOH Dwie cząsteczki wody
11. Napisz wzór sumaryczny i strukturalny oraz oblicz masę cząsteczkową kwasu fosforowego (V) 12. Wy
test TEST: Woda i roztwory wodne (wersja II) I. Napisz wzór sumaryczny, elektronowy i kreskowy cząst
47529 testy, zielone str 85 28. Jaki jest wzór sumaryczny substancji, której cząst
test 4 rEST: Woda I roztwory wodne (wersja II) I. Napisz wzór sumaryczny, elektronowy i kreskowy czą
i n H2S H s H• ••• wzór sumaryczny wzór strukturalny model cząsteczki
test TEST: Woda i roztwory wodne (wersja II) 1. Napisz wzór sumaryczny, elektronowy i kreskowy cząst
więcej podobnych podstron