8873811733
Zadanie 7. (0-2) ■ ■■■■■■■ m
Na rysunku przedstawiono fragment układu okresowego pierwiastków.
liczba atomowa masa atomowa, u
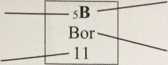
symbol pierwiastka
nazwa pierwiastka
|
1 |
iH Wodór 1 |
2 |
13 |
14 |
15 |
16 |
17 |
2He Hel 4 | |
|
3Li |
4Be |
5B |
6C |
?N |
bO |
9F |
loNe | ||
|
2 |
Lit |
Beryl |
Bor |
Węgiel |
Azot |
Tlen |
Fluor |
Neon | |
|
7 |
9 |
11 |
12 |
14 |
16 |
19 |
20 | ||
|
uNa |
12Mg |
13AI |
uSi |
15P |
ióS |
17CI |
18 Ar | ||
|
3 |
Sód |
Magnez |
Glin |
Krzem |
Fosfor |
Siarka |
Chlor |
Argon | |
|
23 |
24 |
27 |
28 |
31 |
32 |
35,5 |
40 | ||
|
19K |
2oCa |
3iGa |
32Ge |
33AS |
34Se |
35Br |
3óKr | ||
|
4 |
Potas |
Wapń |
Gal |
German |
Arsen |
Selen |
Brom |
Krypton | |
|
39 |
40 |
70 |
73 |
75 |
79 |
80 |
84 | ||
Nadtlenek wodoru to związek o wzorze H2O2. Pod wpływem różnych czynników, np. temperatury, nadtlenek wodoru ulega reakcji rozkładu przebiegającej według równania.
2H2O2 —► 2H20 + O2
7.1. Dokończ zdanie. Wybierz właściwą odpowiedź spośród podanych.
Z powyższego równania reakcji rozkładu wynika, że z 2 cząsteczek nadtlenku wodoru otrzymano
A. 2 cząsteczki tlenu.
B. 1 cząsteczkę tlenu.
C. 3 atomy tlenu.
D. 1 atom tlenu.
7.2. Oceń prawdziwość podanych zdań. Wybierz P, jeśli zdanie jest prawdziwe, albo F - jeśli zdanie jest fałszywe.
|
Masa cząsteczkowa H2O2 jest równa 34 u. |
P |
F |
|
Stosunek masowy wodoru do tlenu w nadtlenku wodoru wynosi 1 :8. |
P |
F 1 |
Wyszukiwarka
Podobne podstrony:
Zadanie 7. (0-2) Na rysunku przedstawiono fragment układu okresowego pierwiastków..H liczba
Zadanie 15. (3 pkł) Na rysunku przedstawiono fragment układu pokarmowego człowieka. a)
skanuj0010 Zadanie 14. (3 pkl) Na rysunku przedstawiono fragment wykresu pewnej funkcji parzystej/.
Zadanie 35. Na rysunku przedstawiono fragment A. połączenia gwintowanego wałka i
zadania Gajerski2 i. Produkcja polipropylenu (PP) Na rysunku przedstawiono fragment instalacji do pr
BYT e) 01 2006 4 NC_ Na rysunku przedstawiono fragment modleu aplikacji, której zadaniem jest rysow
Zadanie 29. (2 pkt) Na rysunku przedstawiono fragment wykresu funkcji/ który powstał w wyniku przesu
popr (2) Zadanie 10 Na rysunku przedstawiono fragment dwóch blach połączonych czterema śrubami ciasn
Zadanie 1. Na rysunku przedstawiono sieć o topologii A. siatki. B.
Moduł 3. Wymagania egzaminacyjne z przykładami zadań Przykładowe zadanie 2. Na rysunku przedstawiono
IMG 77 34. Na rysunku U 5 przedstawiono fragment przekroju przez chloroplast. Wskaźniki przedstaw wi
IMAG0092 (6) 1 .Na rysunku przedstawiono schemat układu elektrycznego, Vrą6 o jakim natężeniu / płyn
IMAG0093 (5) 2.Na rysunku przedstawiono schemat układu elek moc wydzieli się na rezystorze R ?
Zadanie 1. Na schemacie przedstawiono fragment cząsteczki białka o strukturze Hl-rzędowej oraz warun
Zadanie 7. Na rysunku przedstawiono budowę skóry płazów, która u tych zwierząt pełni istotną funkcj
UCZNIA GM-M1-192RMSPnHHHHHHHHOHHHHHHi Na rysunku przedstawiono fragment siatki graniastosłupa
Zadanie 1. (0-1) Na rysunku przedstawiono kartkę z kalendarza na rok
więcej podobnych podstron