107718

Przewodność elektrolityczna zależy od:
- rodzaju elektrolitu, ponieważ wpływa on na ruchliwość elektrolityczną jonów
- rodzaju rozpuszczalnika
- temperatury - przewodność rośnie o 1 -2% wraz ze wzrostem temperatury o IK
- stężenia elektrolitu - dla rozcieńczonych roztworów obserwujemy wprost proporcjonalną zależność między stężeniem a przewodnością, ale dla roztworów elektrolitów mocnych, wzrost stężenia powoduje spadek przewodności ze względu na oddziaływania między jonami, łącznie się w pary i tworzenie kompleksów, które wpływają na spadek ruchliwości.
• Przewodność molowa elektrolitu - wprowadzona ją, ale wyeliminować ujemny wpływ zmian stężenia na przewodność elektrolityczna.
Molowa przewodność odpowiada przewodności warstwy elektrolitu o gmbości lm i takiej powierzchni, że w ogr aniczonej bryle jest 1 mol elektrolitu.
K
A = lOOOc
Przy nieskończenie rozcieńczonym roztworze istnieje graniczna wartość przewodności molowej, którą oznaczamy A00.
• Zgodnie z teorią Debye’a Hiickela - Onsagera, opisującą zależność A od stężenia i cliarakteru elektrolitu, graniczna wartość przewodności molowej wyznaczamy w funkcji pierwiastka z stężenia:
f(/i) = vć
A
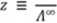
• Stosunek przewodnictw - definiuje się to pojęcie dla roztworów elektrolitów słabych:
Zależy on od ruchliwości elektr olitycznej jonów w roztworze a także stopnia dysocjacji. Jeśli elektrolit jest bardzo slaby, to rzeczywiste stężenie jonów jest niewielkie i wpływ ruchliwości na stosunek przewodnictw jest znikomy - można go pominąć. Przy tym założeniu otrzymujemy zależność:
z = a
Z tej zależności można szacować stopień dysocjacji elektrolitów słabych rozcieńczonych za pomocą pomiarów przewodności molowych.
2. Aparatura i odczynniki:
- konduktometr ScvcnEasy Mettler Toledo
- roztwór wzorcowy 0,01 M KC1
- roztwory: 0,0IM HCI i 0,1M CH3COOH
- termostat
- zlewki, kolbki stożkowe, bnrrety, lejki, tryskawki z wodą destylowaną
3. Czynności pomiarowe:
- uruchomiliśmy termostat i ustawiliśmy temperaturę 25‘C
- zmierzyliśmy przewodność roztworu wzorcowego KC1 i dokonaliśmy kalibracji konduktometru według wskazówek
- przygotowaliśmy roztwrory elektrolitów o odpowiednich stężeniach
- zmierzyliśmy przewodność wody destylowanej, roztworów przygotowanych oraz wyjściowych
4. Obliczenia i błędy pomiarowe:
Przewodność molową liczymy ze wzoru:
K
A = lOOOc
Dokonaliśmy także pomiaru przewodności wody destylowanej, która wynosi: k = 4,75 ps*cm ', i stwierdziliśmy, że ma ona marginalne znaczenie i nie wpływa na wyniki.
2
Wyszukiwarka
Podobne podstrony:
Slajd59 (2) Wartość przewodności elektrycznej poszczególnych tkanek zależy od s rodzaju jonów&n
DSC02164 (3) stopień dvsociacii zależy od: - Rodzaju elektrolitu - &nb
Stopień dysocjacji zależy od rodzaju rozpuszczalnika, koncentracji (stężenie elektrolitu) oraz
S6003445 elektrycznych lania zależy od Okres sygnału V? uakieiystykę: częstotliwości fey na sygnał t
IMAG1596 Czas trwania zespołu uprawek pożniw sposób jego wykonania zależy od: r rodzaju przedplonu i
skanuj0060 (7) ROZSZERZALNOŚĆ CIEPLNA zależy od rodzaju wiązań
SL275456 Zawartość mioglobiny zależy od • Rodzaju mięsa (ciemne wołowe,
Slajd15 (101) Podział wapieni organicznych 1. Zależy od rodzaju masy podst. i proporcji masa podstaw
więcej podobnych podstron