60828

Wracając do wzoru na energię wewnętrzną: AU—AnRA T .
Podstawiając wszystko do bilansu cieplnego: AQ-AnRAT + 11 RAT -5tiRAT . Porównując ze wzorem na pracę otrzymujemy: AQ-5A\V-5-2A5J-\225J^5\2^kcal .
W przemianie izotermicznej temperatura się nie zmienia, więc energia wewnętrzna:
AU-n cpA T-0
Wobec tego z bilansu cieplnego wynika, że:
AU=AQ-AW = 0=>AQ-AW = 2A5J**\026kcal .
3. W wyniku rozszerzania adiabatycznego tlenu, o masie 3,2 g i temperaturze początkowej
6 N 5 N
20 C , jego ciśnienie zmniejszyło się od 10—; do 3,8-10—- . Określić jak będzie temperatura końcowa gazu.
W przemianie adiabatycznej zachodzi związek: pV*~const Z równania Clapeyrona: pV-tiRT .

Ostatecznie wzór na końcową temperaturę:
/ 1 *-i
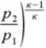
7,,=20°C=193,15 AT
*=— - bo tlen występuje w dwuatomowych cząsteczkaclr, które mają 5 stopni swobody (mchy w
trzech kienuikach i obroty względem dwóch osi prostopadłych do prostej przechodzącej przez atomy).
Podstawiając:
3,8-10
N
7\= 193,15 K
193,15A'-
7^145,5A
Uwraga: nigdzie w obliczeniach nie używałem masy, dlatego zastanawiam się, czy nie ma błędu...
4 Podczas izobarycznego sprężania tlenu o masie 10 kg i temperaturze początkowej 100 C objętość jego zmniejszyła się 1,25 razy. Znaleźć pracę wykonaną podczas sprężania oraz ilość
Wyszukiwarka
Podobne podstrony:
spektro EGZAMIN - SPEKTROSKOPIA termin I ł. Jakie rodzaje energii składają się na energię wewnętrzna
243 [1024x768] 250 PODSTAWY TERMODYNAMIKI CHEMICZNEJ oraz wyrażeniem na energię wewnętrzną (3.170) I
ENERGIA WEWNĘTRZNA CIAŁAr Energią wewnętrzną ciała nazywamy sumę wszystkich
Energia wewnętrzna to jedno z podstawowych pojęć termodynamiki. W ramach mechaniki Newtona pojęcie e
III. Podsumowanie Na podstawie wszystkich dostępnych bilansów i sprawozdań finansowych omawianej
img169 169 Podstawiane otrzymane wyrażenie do wzoru na zmianę energii kinetycznej strumienia między
Zdjęcie054 (15) I zasada termodynamikiQ = AU + W O - ciepło dostarczone do układu. AU - zmiana energ
AU=AQ+ AW0 + AWno AU=AQ+ AWno-pAV AU zmiana energii wewnętrznej układu AQ ciepło dostarczone do ukła
35456 Zdjęcie054 (15) I zasada termodynamikiQ = AU + W O - ciepło dostarczone do układu. AU - zmiana
35456 Zdjęcie054 (15) I zasada termodynamikiQ = AU + W O - ciepło dostarczone do układu. AU - zmiana
fizyczna egzamin001 Chemia fizyczna I (termodynamika) 1. Zmiana energii wewnętrznej układu AU w ogól
więcej podobnych podstron