Część I: Podstawy chemoterapii
1
1. CHEMOTERAPIA
1.1. Definicja chemoterapii
W/g Encyklopedii Powszechnej PWN1
chemoterapia to: zwalczanie chorób przez zniszczenie
drobnoustrojów chorobotwórczych środkami chemicznymi
wprowadzonymi do organizmu chorego. W tej klasycznej
definicji należy zwrócić uwagę na dwa aspekty. Po pierwsze,
nie każdy lek jest chemoterapeutykiem. Jedynie ten, którego
mechanizm działania polega na zwalczaniu drobnoustrojów
chorobotwórczych. Po drugie, chemoterapeutyk wprowadzany
jest do organizmu chorego i walczy z czynnikiem
chorobotwórczym niejako "od środka". Należy więc wyraźnie
odróżnić chemoterapeutyki od środków dezynfekcyjnych
(antyseptyków). Te ostatnie powodują również śmierć
czynników chorobotwórczych (patogenów), ale dokonują tego
poza organizmem pacjenta lub w najlepszym razie na jego
skórze.
Coraz
częściej definicję chemoterapii poszerza się
poprzez objęcie nią również innych niż drobnoustroje
czynników chorobotwórczych. Przede wszystkim obiektami
zainteresowania chemoterapii stały się z jednej strony wirusy,
a z drugiej pierwotniaki i robaki. Ponadto jako czynnik
chorobotwórczy traktuje się również pewne komórki własne
chorego. Dotyczy to głównie komórek zmienionych
nowotworowo, ale również niektórych elementów
komórkowej odpowiedzi immunologicznej skierowanych
przeciwko prawidłowym komórkom pacjenta. Szczególnego
rodzaju patogenem okazały się priony: czynniki wywołujące
rzadkie, choć znane od dawna choroby zakaźne ludzi i
zwierząt2. Tak szeroki zakres pojęcia patogenu (czynnika
chorobotwórczego) wynika z bardzo podobnej strategii
działania chemoterapeutyków (patrz punkt 2). W niniejszym
skrypcie stosować
będziemy poszerzoną definicję
chemoterapii traktując jako patogeny:
♦
priony
♦
wirusy
♦
bakterie
♦
grzyby i drożdże
♦
pierwotniaki
♦
robaki
♦
komórki nowotworowe.
1.2. Początki współczesnej chemoterapii
Podwaliny pod chemoterapię położył lekarz
szwajcarski Paracelsus (1493-1541). Przekonany, że na każdą
dolegliwość musi istnieć jakiś odrębny lek, wnikliwie badał i
poszukiwał takich specyficznie działających środków.
Wypróbowując rozmaite związki chemiczne wprowadził do
lecznictwa m.in. związki rtęci (niegdyś jedyny skuteczny lek
przeciwko kile) oraz związki antymonu przez długi czas
bardzo popularne w medycynie.
Początek współczesnej chemoterapii stanowią prace
lekarza i biologa niemieckiego Paula Ehrlicha (1854-1915). W
roku 1891 wysunął on koncepcję zastosowania związków
chemicznych do zwalczania chorób zakaźnych. Jego prace
badawcze uwieńczone zostały pełnym sukcesem.
1Encyklopedia Powszechna PWN, Państwowe Wydawnictwo
Naukowe, Warszawa 1973.
2M. FIKUS: Niekonwencjonalny zabójca, Wiedza i Życie
1995(9), str.22-24.
N
S
(CH
3
)
2
N
N ( C H
3
)
2
+
Cl
-
Błękit metylenowy
NH
2
A s
O
O H
O N a
Atoksyl (1904)
A s
HO
H
2
N
A s
OH
NH
2
Salwarsan (1909)
As
HO
H
2
N
A s
OH
N H C H
2
SO
2
Na
Neosalwarsan
Rys.1-1.
Budowa chemiczna pierwszych współczesnych
chemoterapeutyków wprowadzonych do lecznictwa przez
Ehrlicha.
Chemoterapia zawdzięcza mu takie preparaty jak (Rys.1-1.):
♦
błękit metylenowy
♦
czerwień trypanową
♦
atoksyl
♦
salwarsan i neosalwarsan.
Błękit metylenowy stosowano w leczeniu malarii, czerwień
trypanową i atoksyl przy zwalczaniu zakażeń trypanosomami
(np. śpiączki afrykańskiej) a salwarsan i neosalwarsan przy
leczeniu kiły.
Następnym krokiem milowym w historii
chemoterapii stało się wprowadzenie do lecznictwa przez
lekarza niemieckiego Domagka barwnika dwuazowego o
nazwie Prontosil Rubrum w roku 1934 (Rys.1-2.). Związek
ten nie działał na bakterie w hodowli, ale wprowadzony do
organizmu skutecznie zwalczał zakażenia wywoływane przez
szereg bakterii. Wyjaśnienie mechanizmu jego działania
otworzyło e r ę s u l f o n a m i d ó w .
N
N
NH
2
NH
2
S
O
O
NH
2
Rys.1-2.
Budowa chemiczna preparatu Prontosil Rubrum -
prekursora sulfonamidów przeciwbakteryjnych wprowadzonego
do lecznictwa przez Domagka w roku 1934.
Przełomowym momentem w historii chemoterapii
stało się odkrycie i zastosowanie antybiotyków przeciw-
bakteryjnych. Oto krótki kalendarz ważnych momentów
historii tej dziedziny:
Część I: Podstawy chemoterapii
2
1928 r
Fleming stwierdza, że pleśń Penicillium
notatum
wydziela do podłoża coś, co silnie
hamuje wzrost niektórych bakterii.
Hipotetyczna substancja nazwana penicyliną
przez szereg lat nie daje się wyizolować
1942 r
Florey, Chain i Abraham izolują po raz
pierwszy penicylinę. Rozpoczyna się e r a
a n t y b i o t y k ó w .
1944 r
Waksman izoluje streptomycynę: pierwszy lek
przeciwgruźliczy
1947 r
Burkholder odkrywa chloromycetynę
1948 r
Duggar izoluje aureomycynę
1950 r
Finlay znajduje terramycynę
Od roku 1944 (odkrycie streptomycyny) rozpoczyna
się atak chemoterapeutyczny na gruźlicę. Poza antybiotykami
pojawiają się syntetyczne chemoterapeutyki przeciwgruźlicze
takie jak PAS, Conteben i Rimifon (Rys.1-3.).
NH
2
OH
O
OH
PAS (1946)
NHCOCH
3
N
NH
S
NH
2
Conteben (1947)
N
HO
O
NH
NH
2
Rimifon (1951)
Rys.1-3.
Budowa chemiczna pierwszych syntetycznych
chemoterapeutyków przeciwgruźliczych.
Niezależnie trwa poszukiwanie leków
przeciwpierwotniakowych (głównie przeciwmalarycznych.
Do lecznictwa wchodzą (Rys.1-4.): plazmochina, atebryna,
proguanil i chlorochina.
Te sukcesy w leczeniu zakażeń bakteryjnych i
niektórych chorób wywoływanych przez pierwotniaki
kontrastują z sytuacją obserwowaną w zakresie chemoterapii
przeciwgrzybowej, przeciwwirusowej i
przeciwnowotworowej. Okazuje się bowiem, że:
♦
nie znany jest ani jeden związek skuteczny w chorobach
wywoływanych przez priony
♦
brak jest skutecznych i nieszkodliwych
chemoterapeutyków przeciwnowotworowych
♦
wśród chemoterapeutyków przeciwwirusowych istnieją
jedynie leki o bardzo wąskim spektrum działania
♦
w zatrważającym tempie rośnie oporność bakterii
chorobotwórczych na stosowane dotychczas chemo-
terapeutyki, w tym przede wszystkim antybiotyki
♦
szereg chemoterapeutyków przeciwgrzybowych i
przeciwwirusowych indukuje pojawianie się szczepów
opornych.
W tej sytuacji ciągle aktualne jest poszukiwanie nowych,
skuteczniejszych i mniej szkodliwych chemoterapeutyków.
N
H3O
NH
N
+
N
CH3O
NH
N
Plazmochina (1926)
C
N
Cl
OCH
3
NH
N
Atebryna (1930)
Cl
NH
NH
NH
NH
NH
Proguanil (1940)
N
Cl
NH
N
Chlorochina (1946)
Rys.1-4.
Budowa chemiczna niektórych klasycznych
chemoterapeutyków przeciwpierwotniakowych.
2. SELEKTYWNA TOKSYCZNOŚĆ.
Możliwość zastosowania pewnych związków
chemicznych jako chemoterapeutyków opiera się na zjawisku
tzw. s e l e k t y w n e j t o k s y c z n o ś c i . Ze
zjawiskiem tym mamy do czynienia wtedy, gdy związek
chemiczny zastosowany w określonym stężeniu wywiera
silniejsze działanie szkodliwe w stosunku do patogenu niż w
stosunku do komórek gospodarza. Dobry chemoterapeutyk
powinien charakteryzować się możliwie dużą selektywną
toksycznością Należy zdać sobie sprawę,
że
chemoterapeutykami nie mogą być ani trucizny o działaniu
ogólnym (np. cyjanki lub siarczki) ani antyseptyki o działaniu
niszczącym (np. H
2
O
2
, KMnO
4
, J
2
). Muszą to być związki
możliwie nieszkodliwe dla organizmu gospodarza, a
jednocześnie toksyczne dla patogena (pasożyta). Zjawisko
selektywnej toksyczności występuje wtedy, gdy potencjalny
chemoterapeutyk wykorzystuje istniejące różnice w budowie i
funkcjach patogenu i komórek gospodarza.

Część I: Podstawy chemoterapii
3
2.1. Układy patogen - gospodarz
Zgodnie
ze
współczesną definicją chemoterapii
możemy rozróżnić 7 układów gospodarz-patogen. Są to
układy:
1. człowiek : bakteria
2. człowiek : grzyb (drożdżak)
3. człowiek : robak
4. człowiek : pierwotniak (ameba, rzęsistek{Trichomonas})
5. człowiek : wirus
6. człowiek : nowotwór
człowiek : prion
Kolejność, w jakiej wykaz ten został zbudowany nie jest
przypadkowa. Wraz ze wzrostem numeru wzrasta również
trudność leczenia chemoterapeutykami. Wynika to z dwóch
przyczyn. Pierwszą z nich jest wzrastające podobieństwo
biochemiczne i fizjologiczne pomiędzy patogenem i
gospodarzem, a drugą wzrastające zdolności przystoso-
wawczych niektórych patogenów. Wypadkową obu tych
przyczyn jest powyższa kolejność. Nie bez znaczenia jest
również zasób naszej wiedzy o patogenie.
Omówimy teraz pokrótce sytuację występującą przy
stosowaniu chemoterapii w każdym z tych układów.
Człowiek : bakteria.
W okresie początków chemoterapii był to
najgroźniejszy patogen. W chwili obecnej nie zdajemy już
sobie sprawy, jakie ofiary zbierało kiedyś bakteryjne
zapalenie płuc czy bakteryjne zakażenia przyranne. Do czasu
zastosowania sulfonamidów i antybiotyków
przeciwbakteryjnych bakterie należały do groźnych i
powszechnie występujących patogenów. W początkowym
okresie chemoterapii układowi człowiek : bakteria
poświęcono wiele uwagi i nakładów finansowych i w chwili
obecnej można sytuację uznać za opanowaną: istnieje szeroka
gama możliwych do zastosowania klinicznego
chemoterapeutyków w zasadzie przeciwko wszystkim znanym
typom bakterii chorobotwórczych. Jest to niewątpliwie
skutkiem występowania istotnych różnic biochemicznych
pomiędzy patogenem i gospodarzem. Dzięki temu w
przypadku niektórych chemoterapeutyków przeciw-
bakteryjnych występuje prawie idealna selektywna
toksyczność.
Jednakże bakterie należą do patogenów o wręcz
niewiarygodnych zdolnościach przystosowawczych i
obronnych. W efekcie ciągle powstają nowe szczepy bakterii
chorobotwórczych charakteryzujących się coraz większą
opornością w stosunku do stosowanych
chemoterapeutyków3 4.Wymaga to wprowadzania do
lecznictwa, co 5
÷7 lat kolejnego leku o nowym, odmiennym
od dotychczas wykorzystywanego mechanizmie działania5
Człowiek : komórka grzybowa
Komórki grzybów i drożdżaków chorobotwórczych,
(np. Candida albicans) były przez wiele lat uważane za
stosunkowo niegroźny patogen. Wynikało to niewątpliwie z
faktu, że najczęstszymi grzybicami w tym okresie były
grzybice skórne, które zwalczać można stosunkowo prostymi
środkami. Ponadto są to choroby nie stwarzające zwykle
zagrożenia dla życia pacjenta. Sytuacja zmieniła się
dramatycznie ok. 30 lat temu, gdy na skutek lekkomyślnego
stosowania antybiotyków przeciwbakteryjnych o szerokim
3T. BEARDSLEY: Raj utracony?, Świat Nauki, 1993(1), str.8.
4T. BEARDSLEY: Opór wobec oporności, Świat Nauki, 1996(3),
str.13.
5Z.A. KWIATKOWSKI: Nie przegrać z bakteriami, Wiedza i Życie,
1994(9), str.10-16.
spektrum działania stwierdzono gwałtowny wzrost
zachorowań na grzybice układowe (np. wątroby lub płuc).
W chwili obecnej groźne dla życia grzybice układowe
występują przede wszystkim w krajach o wysokim poziomie
opieki medycznej. Szerokie i często beztroskie stosowanie
antybiotyków przeciwbakteryjnych prowadzi do
wyeliminowania z organizmu pacjenta również bakterii
obojętnych lub wręcz niezbędnych dla zdrowia, np. tzw. flory
bakteryjnej przewodu pokarmowego, która jest dla człowieka
istotnym źródłem niektórych witamin. W tej sytuacji
opuszczone nisze ekologiczne zajmowane są przez grzyby i
drożdżaki. Ich nadmierny rozwój na błonach śluzowych jamy
ustnej lub górnych dróg oddechowych stwarza sytuację
sprzyjającą wystąpieniu zakażenia grzybowego narządów
wewnętrznych. Na ile jest to sprawa ważna świadczyć mogą
wyniki badań prof. Sameta z AMG wykazujące, że przyczyną
ok. 70% zakończonych śmiercią powikłań pooperacyjnych
były infekcje grzybowe.
Dodatkowym czynnikiem zwiększającym ryzyko wystąpienia
grzybicy układowej jest kontakt potencjalnego chorego z
czynnikami obniżającymi odporność immunologiczną
organizmu. Z jednej strony mogą to być świadomie stosowane
w przypadku przeszczepów lub niektórych chorób
autoimmunologicznych leki immunosupresyjne. Z drugiej,
szereg chemoterapeutyków przeciwnowotworowych wywiera,
jako jeden z podstawowych efektów ubocznych, działanie
immunosupresyjne. Nie bez znaczenia jest również
występowanie wśród substancji zanieczyszczających
środowisko coraz większej liczby związków uszkadzających
układ immunologiczny.
Szczególnie dramatyczna stała się sytuacja z infekcjami
grzybowymi w momencie wybuchu epidemii AIDS: wirus
HIV uszkadza przecież układ odpornościowy chorego. W
sytuacji, gdy dzięki skutecznym chemoterapeutykom
przeciwbakteryjnym bakterie nie stanowią największego
zagrożenia, na czoło wysunęły się grzyby i drożdżaki. Według
niektórych danych statystycznych ok. 80% chorych na AIDS
umiera na skutek różnorakich grzybic.
Grzyby i drożdżaki, pomimo wieloletnich badań, są
ciągle jeszcze patogenami stosunkowo mało poznanymi. Przy
bardzo znacznym podobieństwie biochemicznym do komórek
gospodarza są patogenem trudnym z punktu widzenia
chemoterapii. W chwili obecnej nie ma w zasadzie
skutecznego i mało szkodliwego leku przeciw grzybicom
układowym (narządowym). Należy tu wyraźnie zaznaczyć, że
mówimy cały czas o grzybicach narządów wewnętrznych, a
nie skóry. W tym ostatnim przypadku wymogi dotyczące
selektywnej toksyczności są dużo mniejsze i istnieje wiele
skutecznych preparatów dermatologicznych.
Człowiek : robak.
Jest to patogen niedoceniany przez przemysł
farmaceutyczny i "zaniedbany" przez klinicystów i
biochemików. Ten brak zainteresowania wynika po części z
faktu, że zarobaczenie z reguły nie prowadzi do śmierci
chorego. Są to tzw. choroby brudnych rąk, których
występowanie związane jest z niskim poziomem higieny.
Zwykle jednym z etapów zakażenia jest dostanie się do
przewody pokarmowego człowieka jaj lub form niedojrzałych
patogenu wraz z brudem lub kurzem. Tak więc odpowiedni
poziom higieny stanowi znaną od lat dosyć skuteczną
profilaktykę.
Medycyna ludowa zna wiele prostych i często całkiem
skutecznych środków naturalnych przeciwko tego typu
patogenom. Badania kliniczne wykazały np., że pestki dyni są
skutecznym i praktycznie nieszkodliwym środkiem
leczniczym w przypadku robaczycy u dzieci. Dodatkową

Część I: Podstawy chemoterapii
4
zaletą tego "lekarstwa" jest to, że może ono być stosowane
profilaktycznie, a potencjalni "pacjenci" chętnie godzą się na
taką "kurację"; dużo chętniej niż na łykanie tabletek, nie
mówiąc już o zastrzykach.
Dużo większe zainteresowanie tym patogenem wykazuje
weterynaria. Wynika to nie tylko z faktu, że zarobaczone
zwierzęta hodowlane wolniej rosną w hodowli lub ich mięso
nie nadaje się jako surowiec dla przemysłu spożywczego. W
ostatnich latach obserwuje się intensywny postęp w zakresie
zwalczania tego typu patogenów u zwierząt domowych, w
tym szczególnie u psów.
Z punktu widzenia biochemii robaki są patogenem
bardzo podobnym do gospodarza. Na szczęście jednak,
według posiadanej dotychczas wiedzy, robaki wykazują
bardzo słabe zdolności przystosowawczych. Istotne znaczenie
ma również fakt, że walczymy z nim praktycznie na zewnątrz
organizmu: w świetle przewodu pokarmowego. Błona
śluzowa przewodu pokarmowego, podobnie jak skóra,
stanowi skuteczną barierę dla szeregu klas związków
chemicznych. Można więc stosować związki o małej
selektywnej toksyczności, o ile tylko nie są one wchłaniane z
przewodu pokarmowego. Przykładem mogą tu być omawiane
powyżej pestki dyni: za działanie odrobaczające
odpowiedzialna jest grupa silnie toksycznych związków
praktycznie całkowicie niewchłanialnych z przewodu
pokarmowego.
Człowiek : pierwotniak.
Pierwotniaki jako patogeny są w warunkach
polskich patogenami "egzotycznymi". Na stałe w Polsce
spotykamy się w zasadzie tylko z dwiema chorobami
wywoływanymi przez pierwotniaki. Jest to lamblioza i
rzęsistkowica. Pozostałe tzw. "ameby" nie mają w naszych
warunkach klimatycznych szans na rozprzestrzenianie się.
Choroby przez nie wywoływane są odosobnionymi
przypadkami, gdy pacjent uległ infekcji w krajach o dużo
cieplejszym klimacie, a objawy choroby wystąpiły po jego
powrocie do Polski. Jednakże ostatnio, ze względu na
nasilający się ruch turystyczny ryzyko wystąpienia chorób
wywoływanych przez pierwotniaki wzrasta.
Do najbardziej znanych chorób wywoływanych przez
pierwotniaki należą:
∗
malaria
∗
śpiączka afrykańska
∗
leiszmanioza
∗
lamblioza
∗
rzęsistkowica jelit lub pochwy
∗
czerwonka pełzakowata
Właściwie trudno mówić o pierwotniakach jako o jednym
typie patogenu. Praktycznie każdy z nich ma swoiste cechy
czy to biochemiczne czy to fizjologiczne i wymaga
indywidualnego podejścia.
Przy znacznym podobieństwie biochemicznym do komórek
gospodarza pierwotniaki wykazują stosunkowo duże
zdolności przystosowawcze polegające np. na możliwości
przejścia w niekorzystnych warunkach w różnorodne formy
przetrwalnikowe nie poddające się leczeniu. Jednakże
stosunkowo skomplikowany cykl życiowy większości
patogennych pierwotniaków, wymagający dla
rozprzestrzeniania się patogenu życia, w co najmniej dwóch
środowiskach (np. w przypadku malarii są nimi organizm
owada i ssaka), pozwala znaleźć takie etapy rozwoju, w
których funkcje komórki istotnie odbiegają od typowych
funkcji komórek gospodarza. Różnice te stanowią podstawę
selektywnej toksyczności szeregu znanych
chemoterapeutyków przeciwpierwotniakowych. Niestety,
praktycznie wszystkie one wykazują, zwłaszcza przy
dłuższym stosowaniu, szereg efektów ubocznych.
Człowiek : wirus.
Wirus jest patogenem bardzo trudnym z punktu
widzenia chemoterapii. Poza komórką nie wykazuje żadnych
przejawów życia: jest kompozycją różnych składników
chemicznych. Nie zachodzą w nim żadne reakcje
biochemiczne. Z kolei po wniknięciu do komórki gospodarza
wirus jako taki znika modyfikując przy tym mechanizmy
biochemiczne komórki gospodarza. Praktycznie jako patogen
należy traktować nie wirusa, lecz k o m ó r k ę
g o s p o d a r z a zakażoną wirusem. W tej sytuacji jedyne
różnice biochemiczne sprowadzają się do występowania w
zakażonej komórce jednego lub kilku enzymów
zsyntetyzowanych przez komórkę w oparciu o dostarczoną
przez wirusa informację genetyczną.
Większość typowych chorób wirusowych człowieka
wywoływana jest przez wirusy od dawna pasożytujące na
organizmach ludzi. Przebieg tych chorób jest względnie
łagodny i jedynie sporadycznie stanowią one zagrożenie dla
życia chorego. Taki obraz choroby wskazuje, że organizm
gospodarza wypracował sposoby ograniczające szkodliwość
infekcji. Sytuacja wygląda zdecydowanie inaczej, gdy
dochodzi do infekcji organizmu ludzkiego wirusem, z którym
przodkowie nasi nie mieli do czynienia. Sztandarowym
przykładem może tu być AIDS6. Jeszcze bardziej
dramatyczny przebieg mają przypadki infekcji
wywoływanych przez tzw. wirusy krwotoczne7. U
zaatakowanych nimi pacjentów pojawia się wysoka
temperatura ciała i następuje pogorszenie ogólnego stanu
zdrowia, któremu często towarzyszą krwawienia. W ciężkich
przypadkach zgon pacjenta jest następstwem silnych
krwotoków lub niewydolności wielonarządowej. Najbardziej
znanym wirusem tego typu jest wirus Ebola.
Do chwili obecnej brak jest chemoterapeutyków
przeciwwirusowych o zadawalającej skuteczności i
selektywnej toksyczności.
Człowiek : komórka nowotworowa.
W
układzie tym występuje całkowity brak
jakościowych różnic w biochemii patogenu i gospodarza.
Można wprawdzie wykazać istnienie pewnych różnic
ilościowych (głównie kinetycznych), lecz jest to słaby punkt
zaczepienia dla selektywnego oddziaływania i stąd w zasadzie
brak skutecznych chemoterapeutyków przeciwnowo-
tworowych. Komórki nowotworowe traktowane jako
patogeny wykazują ogromną różnorodność: praktycznie u
każdego pacjenta są inne. Odnosi się to do:
6
W.C. GREENE: AIDS - choroba układu
odpornościowego, Świat Nauki, 1993(11), str.66-74.
7
B. LeGUENNO: Odradzające się wirusy, Świak Nauki,
1995(12), str. 36-44.
Część I: Podstawy chemoterapii
5
♦
różnic narządowych w zakresie komórek macierzystych,
z których powstały komórki nowotworowe
♦
różnic osobniczych pomiędzy poszczególnymi chorymi
♦
różnic w stopniu i miejscu uszkodzenia materiału
genetycznego, którego wynikiem była transformacja
nowotworowa.
W chwili obecnej jest to z punktu widzenia
chemoterapii najbardziej "niewdzięczny" układ, w którym
brak jak dotychczas spektakularnych sukcesów.
Człowiek : prion.
Układ ten jest w chwili obecnej terra incognita
chemoterapii. Nie tylko nie znany jest ani jeden związek
chemiczny, który hamowałby rozwój chorób prionowych, ale
brak jest nawet koncepcji jak związek taki miałby działać.
Priony są naturalnymi białkami występującymi w komórkach
wielu narządów. Z klinicznego punktu widzenia szczególnie
istotne jest ich występowanie w komórkach mózgu. Choroby
prionowe są efektem nagromadzenia się w tkance mózgowej
białka prionowego o nieprawidłowej konformacji. Znamy
obecnie trzy podstawowe przyczyny chorób prionowych:
i. dziedziczne choroby prionowe – mutacja w genie
kodującym to białko powoduje taką zmianę sekwencji
aminokwasów, że białko w trakcie biosyntezy
przyjmuje nieodpowiednią konformację
ii. samoistne przypadki chorób prionowych –
przypadkowa zmiana konformacji pod wpływem
czynników zewnętrznych
iii. „infekcja” białka prionowego – wprowadzenie do
organizmu nieprawidłowej postaci białka np. drogą
pokarmową
Szczególnie ciekawe jest jak dochodzi do „rozmnażania się”
nieprawidłowej konformacji białka. W warunkach
fizjologicznych białka prionowe występują w postaci
homodimerów. Dimery takie znajdują się jednak w stanie
równowagi z pulą formy monomerycznej. Możliwe jest
powstanie dimeru, którego jeden ze składników ma
nieprawidłowa konformację. Co więcej w dimerze takim po
pewnym czasie dochodzi do zmiany konformacji
prawidłowego składnika – powstaje dimer zawierający dwie
formy nieprawidłowe. Nastąpiło więc „rozmnożenie się”
formy nieprawidłowej. Wielokrotne powtarzanie tego procesu
doprowadza po odpowiednio długim czasie (zwykle kilka lub
kilkanaście lat) do nagromadzenia się dużej ilości form
nieprawidłowych – powstaje choroba prionowa.
2.2. Biochemiczne podstawy selektywnej
toksyczności.
Chcąc dokonać czegoś nowego w chemoterapii
układów "trudnych" nie możemy już, jak za czasów Ehrlicha,
działać na oślep metodą prób i błędów. Wiadomo, że
podstawą selektywnej toksyczności jest istnienie różnic
pomiędzy komórkami gospodarza i patogenu. Warunkiem
racjonalnych działań w zakresie poszukiwania nowych,
lepszych chemoterapeutyków jest właśnie znalezienie,
zrozumienie i wykorzystanie tych różnic.
2.2.1. Typy różnic biochemicznych możliwych do
wykorzystania jako podstawa selektywnej
toksyczności
Rozważmy teraz, najpierw teoretycznie, jakiego
typu różnice biochemiczne lub fizjologiczne mogą być
wykorzystane jako podstawa selektywnej toksyczności. Znane
są jak dotychczas 4 klasy różnic pomiędzy gospodarzem i
patogenem mogące stanowić podstawę selektywnej
toksyczności. Są to różnice:
∗
targetowe
∗
metaboliczne
∗
transportowe
∗
konsekwencyjne.
Najłatwiejsze do wykorzystania są r ó ż n i c e
t a r g e t o w e . Obiektem docelowym (targetem) leków są
najczęściej biopolimery (białka, kwasy nukleinowe) lub błony
biologiczne. W najbardziej sprzyjającej sytuacji w komórce
patogena istnieje target (np. enzym) nie mający swego
odpowiednika w komórce gospodarza. Mówimy wtedy o
jakościowej różnicy targetowej. Potencjalnym
chemoterapeutykiem może być wtedy każdy związek wiążący
się z takim obiektem docelowym. Standardowym przykładem
chemoterapeutyków wykorzystujących ten typ różnic są
Tabela II-I.: Podstawowe różnice pomiędzy komórkami pro- i eukaryotycznymi.
Struktura Eukaryoty
Procaryoty
jądro i chromosomy
obecne
jądro zawierające szereg
chromosomów zbudowane z DNA i
białek
brak jądra, jeden chromosom
zawierający tylko DNA
aparat mitotyczny
obecne centriole i wrzeciono
brak aparatu mitotycznego, jego rolę
pełni w pewnym stopniu błona
komórkowa
błona komórkowa
zawiera sterole
brak steroli
ściana komórkowa
zwierzęta: brak
jednokomórkowce i rośliny: obecna;
zbudowana z polisacharydów
obecna we wszystkich komórkach i
posiadająca złożoną strukturę (peptydo-
glikan)
rybosomy
80 s (60 s + 40 s)
za wyjątkiem mitochondriów i
chloroplastów
70 s (50 s + 30 s)
system oddechowy
wyspecjalizowane
organelle:
mi-
tochondria
zlokalizowany w błonie komórkowej
inne organelle
obecne
brak
wewnątrzkomórkowe
zbliżone do środowiska istotnie
wyższe od środowiska
ciśnienie osmotyczne
Część I: Podstawy chemoterapii
6
penicyliny i cefalosporyny. Antybiotyki te blokują syntezę
ważnego składnika ściany komórkowej bakterii, a w
komórkach ssaków ściana komórkowa nie istnieje.
Półjakościowe różnice targetowe występują wtedy, gdy w
komórce gospodarza i w patogenie występują układy
spełniające te same funkcje, lecz układy te (np. rybosomy)
różnią się istotnie swoim składem i/lub strukturą. Przykładem
chemoterapeutyków wykorzystujących ten typ różnic mogą
być antybiotyki tetracyklinowe lub erytromycyna.
O
r ó ż n i c a c h m e t a b o l i c z n y c h
mówimy wtedy, gdy pomiędzy gospodarzem i patogenem
występują różnice w spektrum substratowym lub
inhibicyjnym enzymów albo też, gdy różna jest w obu typach
komórek zawartość tego samego enzymu. Różnice
metaboliczne są różnicami tylko ilościowymi. Powoduje to, że
chemoterapeutyki oparte o takie różnice wykazują zwykle
istotne efekty uboczne.
Zjawisko selektywnej toksyczności oparte może być
również na r ó ż n i c a c h we właściwościach
t r a n s p o r t o w y c h błon komórkowych. Różnice te
polegać mogą na różnej selektywności transportu ułatwionego
lub różnej szybkości dyfuzji przez błony lipidowe
wynikającej z ich różnego składu lipidowego.
Różnice transportowe mają ze swej natury charakter ilościowy
wraz ze wszystkimi tego konsekwencjami.
W trakcie poszukiwania nowych
chemoterapeutyków przeciwgrzybowych w Katedrze
Technologii Leków i Biochemii PG stwierdzono, że podstawą
selektywnej toksyczności może być również fakt, że
zahamowanie tego samego enzymu może mieć różne
konsekwencje dla komórki patogenu i gospodarza. Wykazano
również,
że te tzw. r ó ż n i c e
k o n s e k w e n c y j n e stanowić mogą podstawę
zjawiska selektywnej toksyczności. Np. inaktywacja syntazy
glukozamino-6-fosforanu przejawiająca się zahamowaniem
biosyntezy glikoprotein powoduje w przypadku grzybów w
ciągu godziny zaprzestanie podziałów komórkowych. W
organizmach ssaków istnieje pula glukozaminy wystarczająca
do zaspokojenia potrzeb organizmu na przeciąg kilku dni.
Zastanówmy
się teraz, czym tak na prawdę, w
sensie biochemicznym, różnią się komórki poszczególnych
patogenów od komórek gospodarza. Należy jednak przedtem
odpowiedzieć sobie na pytanie czy trzeba rozpatrywać każdy
z patogenów oddzielnie czy też można je połączyć w pewne
klasy. Wiąże się to z generalnym problemem klasyfikacji
organizmów żywych.
Od wieków istnieje podział świata żywego na
królestwa zwierząt i roślin. Podział ten powstał jeszcze w
starożytności, a we współczesnej nauce ugruntowany został
przez wielkiego szwedzkiego przyrodnika
Linneusza (1707-78), twórcę nowożytnej systematyki świata
ożywionego. Jednakże zastosowanie w biologii mikroskopu i
odkrycie tzw. "mikrobów" spowodowało pojawienie się
pewnych wątpliwości, co do zasadności i zupełności takiego
podziału. Wielki i różnorodny świat organizmów
jednokomórkowych nie bardzo pasował do prostego podziału
na cudzożywne zwierzęta i samożywne rośliny. Nie ma
wątpliwości, że zielone jednokomórkowe glony ciążą w
kierunku roślin, a aktywnie poruszające się ameby do świata
zwierząt. Co jednak zrobić z takim np. pantofelkiem
(Paramecium caudatum), który w zależności od okoliczności
może zjadać zielone glony albo też asymilować je w swej
cytoplazmie i wykorzystywać ich zdolności syntetyzujące? A
nie jest to wcale najdziwniejszy z jednokomórkowców. Nie
powinno więc dziwić, że powstało wiele mniej lub bardziej
Komórka
eukariotyczna
prokariotyczna
Komórka
Gram +
Gram -
zwierzęca
roślinna
mitichondrium
chloroplast
retikulum
endoplazmatyczne
błona
jądrow
kolisty
DNA
polisom
błona
cytoplazmatyczna
ściana
komórkowa
otoczka
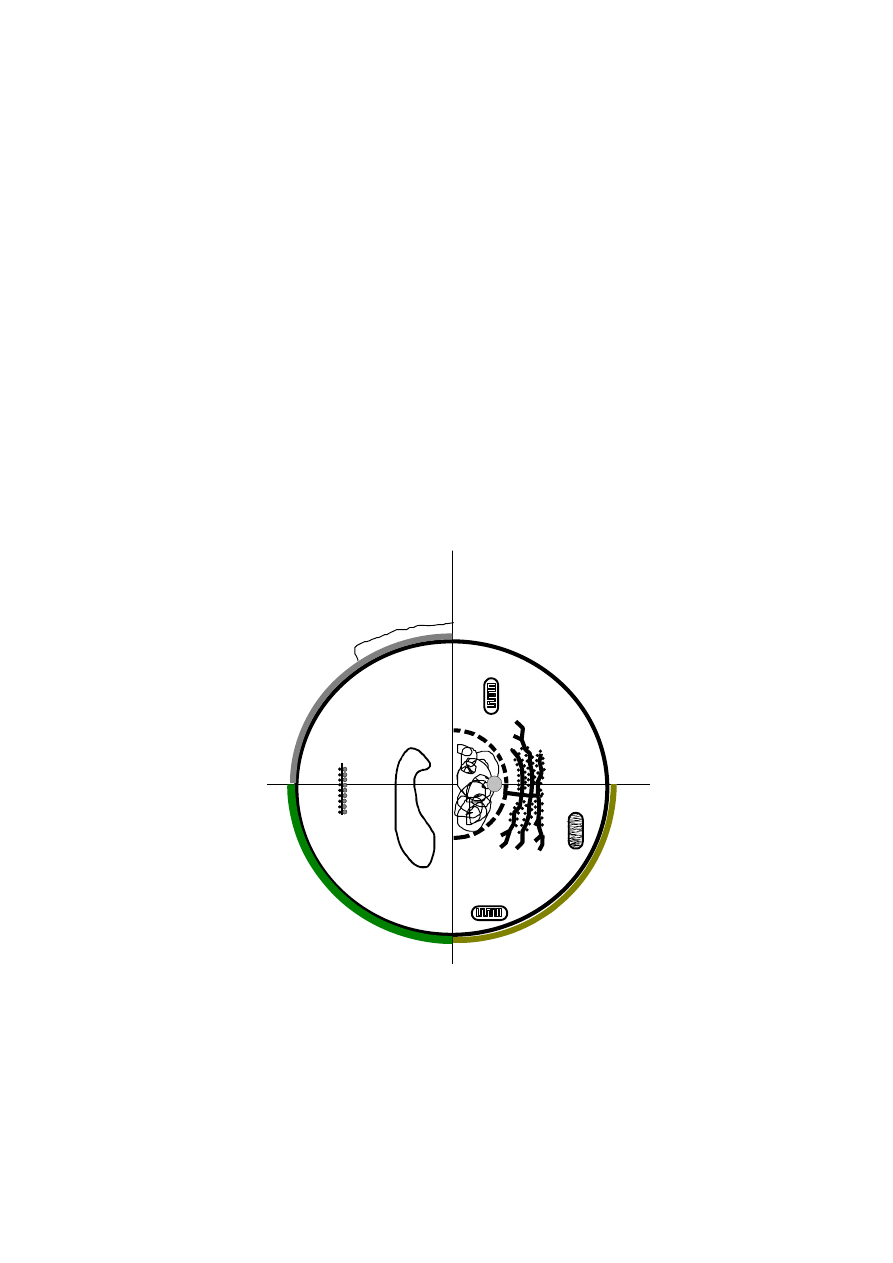
Rys.2-1.
Podstawowe różnice biochemiczne i strukturalne pomiędzy różnymi typami komórek.

Część I: Podstawy chemoterapii
7
oryginalnych systemów podziału świata ożywionego. W
chwili obecnej przyjęty jest w biologii podział na 5 królestw:
∗
jednokomórkowce bezjądrzaste (Monera)
∗
jednokomórkowce jądrzaste (Protista)
∗
grzyby
∗
rośliny
∗
zwierzęta
Nie w nim jednak miejsca na niektóre czynniki
chorobotwórcze np. wirusy.
Z punktu widzenia chemoterapii szczególnie
przydatny okazał się podział nie tyle ze względu na cechy
całego organizmu, co ze względu na strukturę materiału
genetycznego. Podział taki obejmuje:
i. priony: białkowe czynniki chorobotwórcze nie
zawierające materiału genetycznego. Te niedawno
odkryte patogeny wywołują szereg chorób ludzi i
zwierząt, m.in. chorobę curu, zespół Creuzfeldta-
Jakoba, chorobę wściekłych krów i scrapie (S.B.
PRUSINER: Choroby prionowe, Świat Nauki
1995(3),46. M. FIKUS: Niekonwencjonalny zabójca,
Wiedza i Życie
1995(9),22.).
ii. wirusy: kwas nukleinowy (DNA lub RNA) w otoczce
białkowej lub białkowo-lipidowej; brak cytoplazmy
iii. komórki prokaryotyczne: DNA w formie cyklicznej
w cytoplazmie (bakterie, sinice)
iv. komórki eukaryotyczne: DNA zamknięte w jądrze i
przez większość cyklu komórkowego zorganizowane
w formie chromosomów (grzyby, pierwotniaki, rośliny
i zwierzęta)
Okazuje się przy tym, że różnice pomiędzy komórkami pro- i
eukariotycznymi nie ograniczają się tylko do organizacji
materiału genetycznego, ale obejmują również szereg
ważnych struktur komórkowych:
∗
ścianę komórkową
∗
błonę komórkową (błony komórkowe prokaryotów nie
zawierają steroli)
∗
mechanizm i organizację syntezy białka
∗
organizację systemu oksydatywnej fosforylacji (łańcucha
oddechowego).
Najważniejsze dla chemoterapii różnice pomiędzy komórkami
pro- i eukaryotycznymi przedstawia Tabela II-I. i Rys.2-1. Po
zapoznaniu się z jej zawartością nie dziwi nas już fakt, że w
przypadku patogenu prokaryotycznego chemoterapia odniosła
najbardziej spektakularne i najpoważniejsze sukcesy.
Tabela II-II. Różnice biochemiczne wykorzystywane przez typowe chemoterapeutyki.
Patogen Różnica Chemoterapeutyki
bakteria
synteza ściany komórkowej (różnica
jakościowa)
cykloseryna, wankomycyna, bacy-
tracyna, penicyliny, cefalosporyny
replikacja DNA (inhibitory girazy DNA
- różnica półjakościowa)
kwas nalidiksynowy, chinolony
synteza DNA (inhibitory DNA-zależnej
polimerazy DNA)
rifamycyna, rifampicyna
synteza białka (podjednostka 50s)
erytromycyna, chloramfenikol
synteza białka (podjednostka 30s)
tetracykliny, streptomycyna, genta-
mycyna
błona cytoplazmatyczna (różnice tylko
ilościowe)
polimyksyny
metabolizm kwasu foliowego
sulfonamidy, biseptol
grzyby
błona cytoplazmatyczna
(sterole)
antybiotyki polienowe: nystatyna,
amfoterycyna B
biosynteza ergosterolu
pochodne imidazolu i tiazolu: mico-
nazol, clotrimazol, ketoconazol
biosynteza chityny i mannoproteidu
analogi strukturalne UDP-NAcGlu
biosynteza glukozaminy substratu do
syntezy chityny i mannoproteidu
analogi glutaminy: antykapsyna,
FMDP, DON, azaseryna
komórki nowo-
tworowe
szybkość podziałów komórkowych
(cecha wybitnie ilościowa - wysoka
toksyczność)
związki alkilujące, zw. sieciujące, inter-
kalatory, inhibitory topoizomerazy
2.2.2. Różnice gospodarz - patogen wykorzystywane
przez znane chemoterapeutyki
Moglibyśmy teraz przejść do omawiania
poszczególnych typów chemoterapeutyków i
wykorzystywanych przez nie różnic biochemicznych. Nie
stanowi to jednak przedmiotu niniejszego opracowania.
Czytelników zainteresowanych tym tematem odsyłam do
dostępnych opracowań innych autorów. Chciałbym za to
skupić uwagę na krótkim podsumowaniu, dla wybranych
typów patogenów, typowych różnic biochemicznych
wykorzystywanych przez najpopularniejsze chemoterapeutyki
(Tabela II-II).
Literatura uzupełniająca:
Mała Encyklopedia Zdrowia, wyd.IV, PWN, Warszawa
1967.
W.BRUHL i R.BRZOZOWSKI: Vademecum Lekarza
Ogólnego, PZWL, Warszawa 1979.
Document Outline
- 1. CHEMOTERAPIA
Wyszukiwarka
Podobne podstrony:
Podstawy Zarzdzania id 368860 Nieznany
Podstawowe zagadnienia id 36653 Nieznany
zestaw podstawowych drgan id 58 Nieznany
P1 podstawowe pojecia id 344421 Nieznany
Podstawy Turystyki id 368525 Nieznany
PODSTAWY TECHNOLOGII 1 id 36842 Nieznany
podstawy zarzadzania 5 id 36863 Nieznany
podstawy programowania id 36797 Nieznany
podstawy budownictwa id 366813 Nieznany
podstawy piel id 367783 Nieznany
6 Podstawy Projektowania id 43 Nieznany (2)
Podstawy automatyki id 366718 Nieznany
dod podstawy pomiarow id 138636 Nieznany
PODSTAWY BIOTECHNOLOGII id 3668 Nieznany
5 1 NIESTAC PODSTAWY 2011 id 39 Nieznany
podstawy marketingu id 367552 Nieznany
28 10 Podstawy Prawa id 31911 Nieznany (2)
więcej podobnych podstron