
I Z O M E R I A
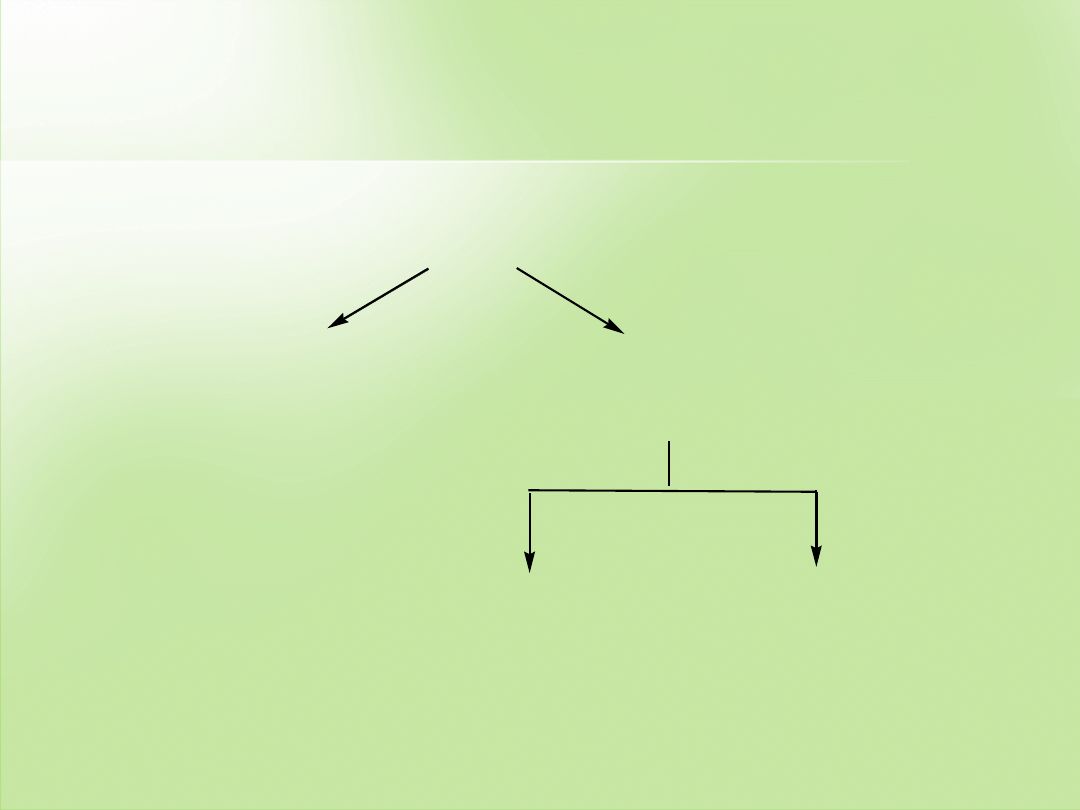
I Z O M E R Y
zwi
ązki o takim samym
wzorze sumarycznym
IZOMERY
KONSTYTUCYJNE
STEREOIZOMERY
zwi
ązki różniące się rodzajem
wiązań i rozmieszczeniem atomów
w cząsteczce
stereoizomery, które s
ą
odbiciami lustrzanymi
ENANCJOMERY
DIASTEREOIZOMERY
stereoizomery, które nie s
ą
odbiciami lustrzanymi
zwi
ązki o takiej samej konstytucji; różnią się
rozmieszczeniem atomów w przestrzeni
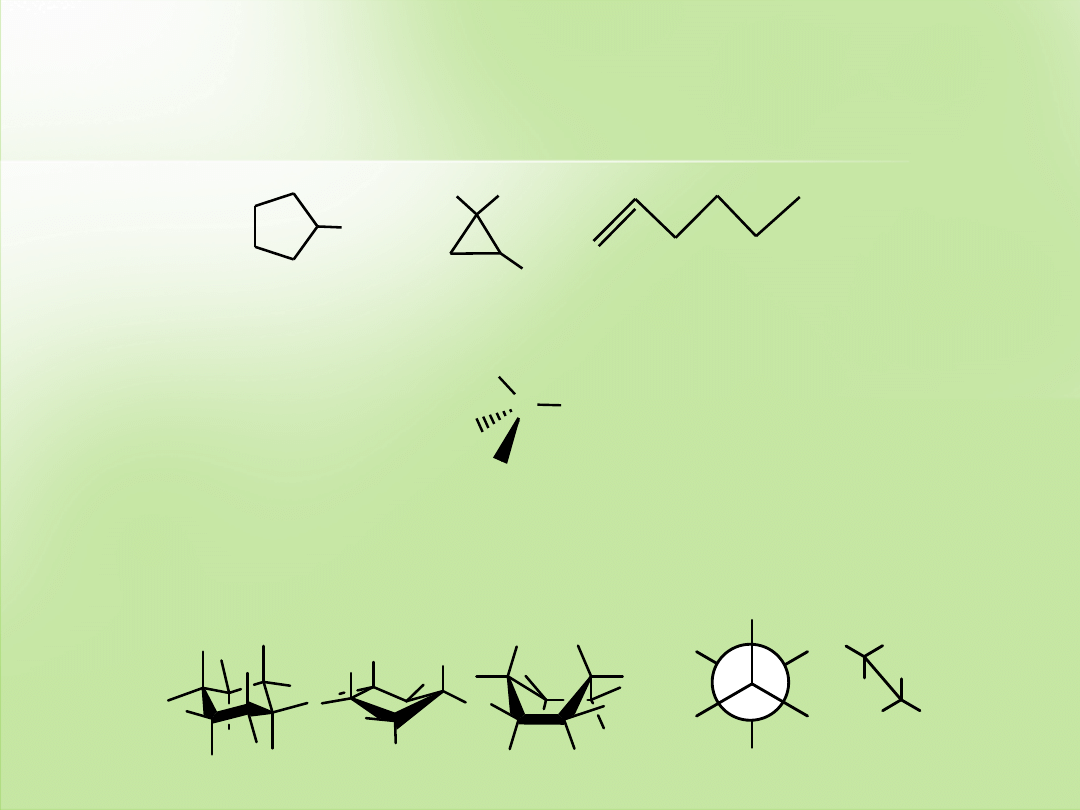
Konstytucja
–
sposób połączenia atomów ze sobą w cząsteczce.
Konfiguracja
–
przestrzenne ułożenie atomów lub grup atomów
w cząsteczce.
Konformacja
–
określone ułożenie atomów cząsteczki w przestrzeni
wynikające z obrotu wokół wiązań pojedynczych lub inwersji pierścienia.
CH
3
CH
3
H
3
C
CH
3
C
H
CH
2
Cl
CICH
2
CH
2
CH
3
*
(
S
)-1,4-dichloro-2-metylobutan
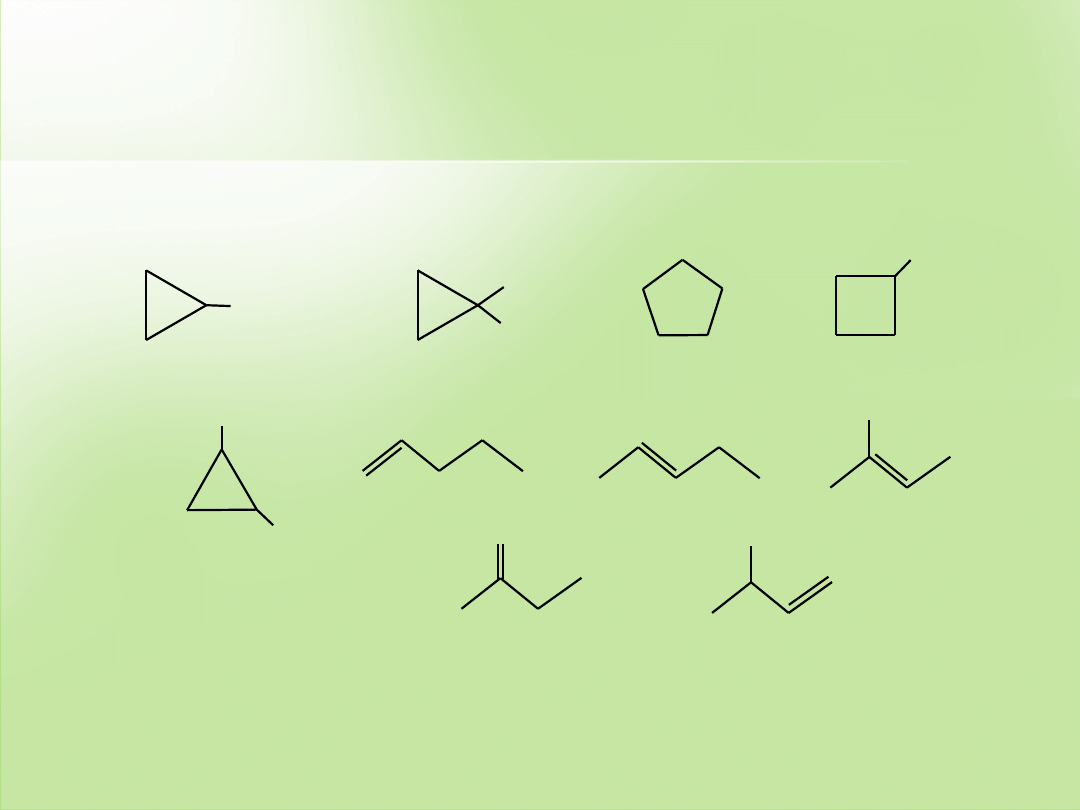
Izomery konstytucyjne
C
5
H
10
CH
2
CH
3
CH
3
CH
3
etylocyklopropan 1,1-dimetylocyklopropan cyklopentan
CH
3
CH
3
CH
3
1,2-dimetylocyklopropan
metylocyklobutan
pent-1-en
pent-2-en
2-metylobut-1-en
2-metylobut-2-en
3-metylobut-1-en
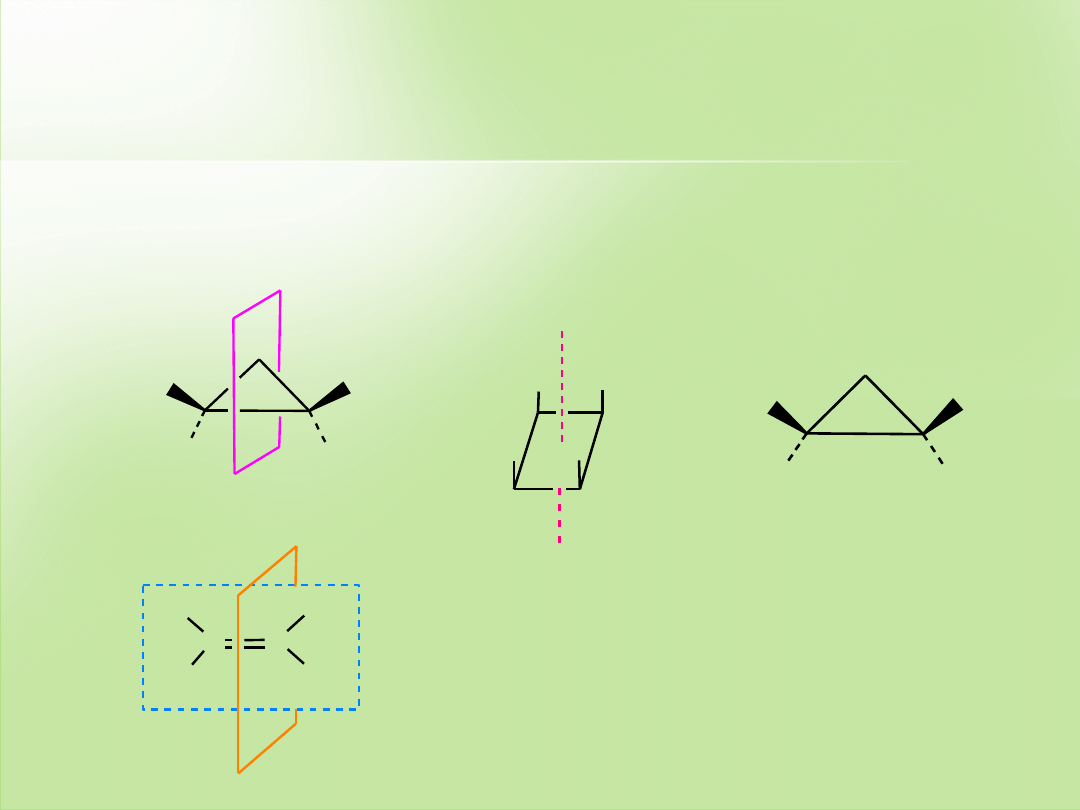
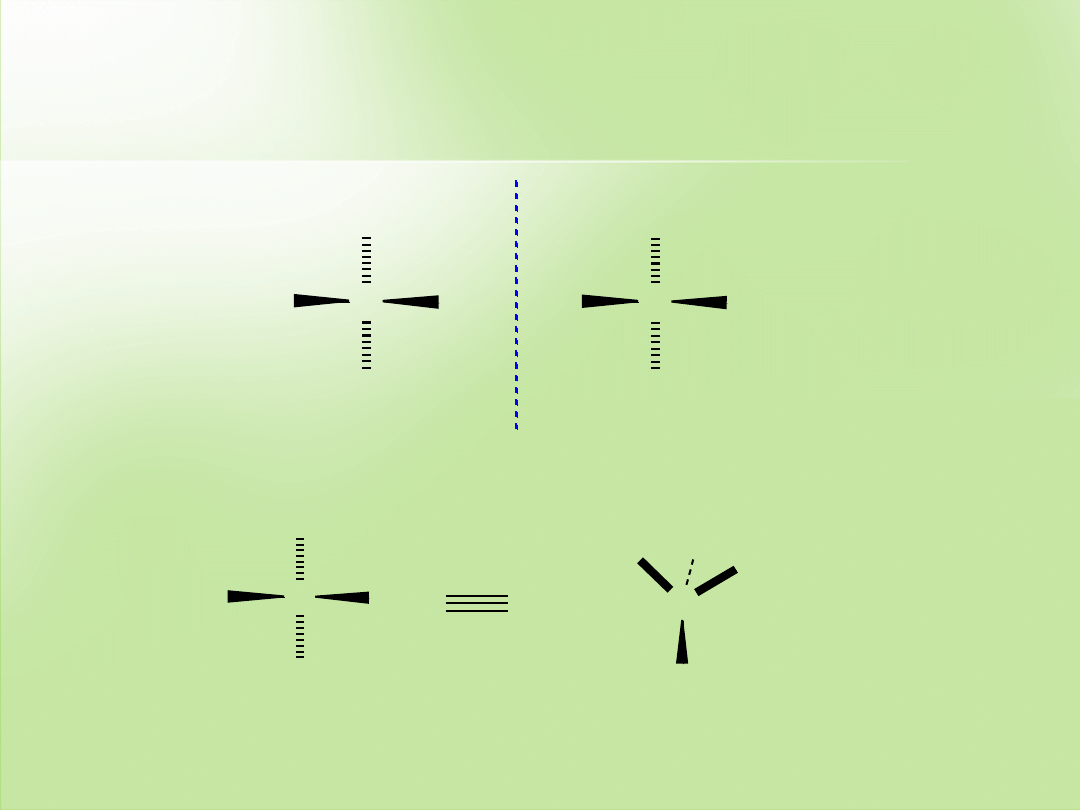
Elementy symetrii występujące
w związkach organicznych
a.
Płaszczyzna symetrii
b.
Środek symetrii
c.
Brak płaszczyzny symetrii i środka symetrii
a.
b.
c.
H
CH
3
H
H
3
C
trans
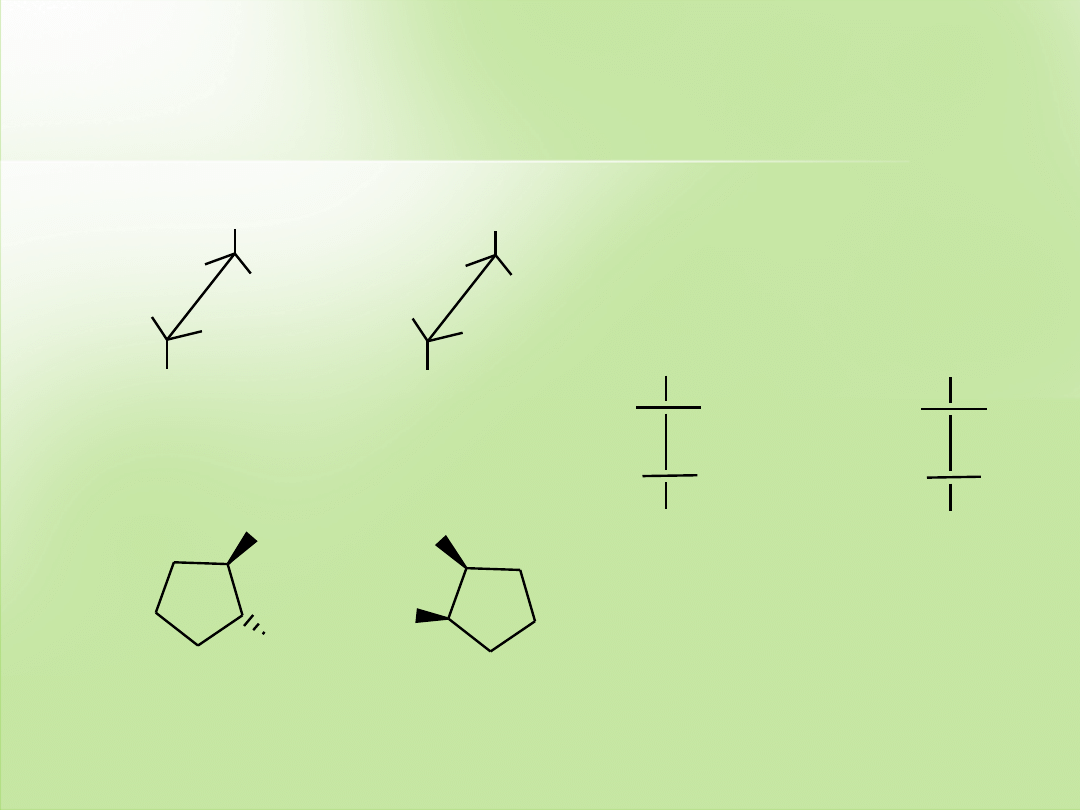
-1,2-dimetylocyklopropan
zwi
ązek chiralny
1,2-dietylo-3,4-dimetylocyklobutan
zwi
ązek achiralny
Et
Me
Me
Et
C
C
Br
Br
H
H
H
H
Cl
Cl
cis
-
1,2-dichlorocyklopropan
zwi
ązek achiralny

Enancjomery
-
są odbiciami lustrzanymi; w środowisku
achiralnym mają takie same właściwości fizyczne i chemiczne, np.
temp. top. i wrzenia, gęstość, moment dipolowy, energię
wewnętrzną, wartość bezwzględną skręcalności [
a
], różnią się
kierunkiem (znakiem
-
[
a
] lub
+
[
a
])
skręcania płaszczyzny światła
spolaryzowanego).

Atom węgla związany z czterema różnymi podstawnikami nazywany jest
atomem chiralnym
lub
centrum stereogenicznym
, dzięki
niemu cząsteczka nabiera właściwości związanych z chiralnością.
Litery (
R
) i (
S
) pisane kursywą określają
konfigurację absolutną
enancjomerów, którą się ustala w oparciu o reguły pierwszeństwa
podstawników wg
Cahna
,
Ingolda
i
Preloga
(1960 r.)
.
Konfiguracja absolutna
– rzeczywiste ułożenie atomów lub grup
atomów w przestrzeni.
C
Br
Cl
CH
3
CH
2
H
C
Br
Cl
CH
2
CH
3
H
(
R
)-1-bromo-1-chloropropan
(
S
)-1-bromo-1-chloropropan
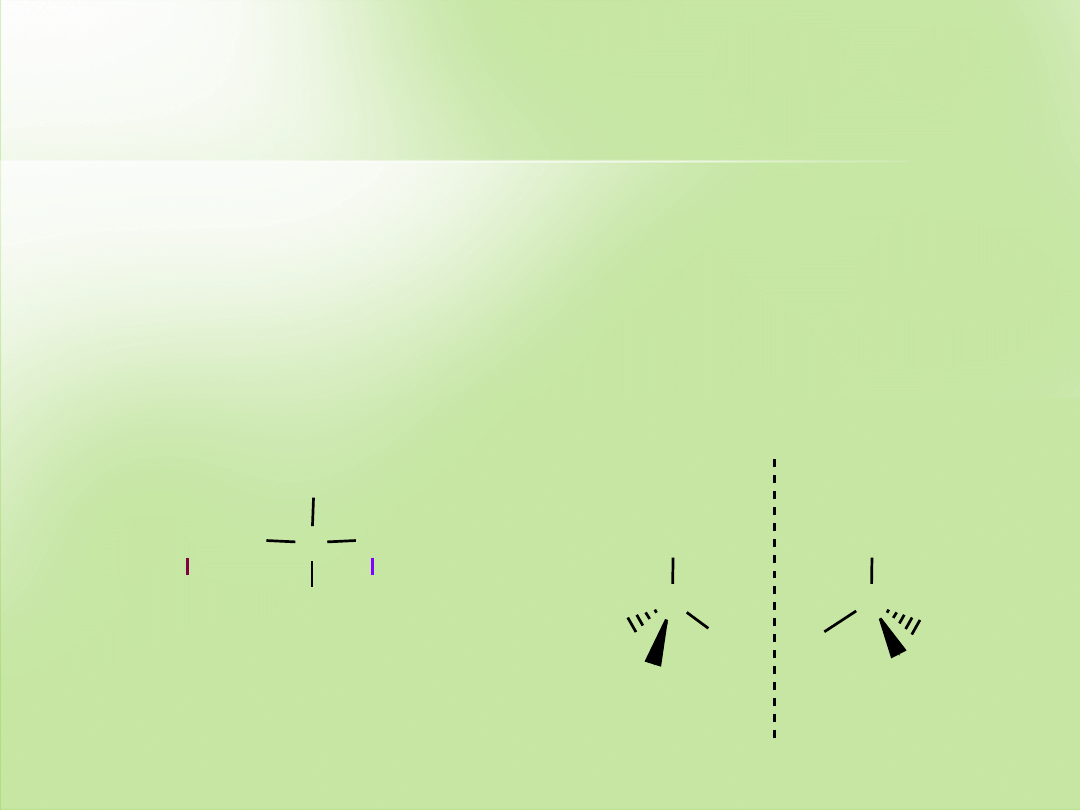
Reguły wg
Cahna, Ingolda i Preloga
1.
W celu przypisania centrum chiralnemu konfiguracji
R
lub
S
należy
ustalić kolejność pierwszeństwa podstawników według liczby atomowej
przyłączonych do atomu stanowiącego centrum stereogeniczne (od
podstawnika o największej liczbie atomowej do podstawnika o mniejszej
liczbie atomowej).
W przypadku występowania
izotopów
, o
pierwszeństwie decyduje ich liczba masowa.
C
Br
T
D
H
1
4
3
2
*
C
Br
T
D
H
1
4
3
2
*
4-bromo-3-chloro-1-fluoropentan
(mo
że zaistnieć w dwóch formach
przestrzennych)
C
Cl
H
CHCH
3
H
2
CCH
2
Br
F
1
*
2
3
4

2.
Jeżeli atomy związane bezpośrednio z centrum stereogenicznym są
takie same to o ważności podstawników decydują atomy z drugiego szeregu,
ewentualnie dalszych szeregów, tak żeby można było wyznaczyć
starszeństwo, musi ono zaistnieć (trzeba dojść do takiej pary atomów, z
których jeden ma większą liczbę atomową od drugiego).
Jeden atom o większej liczbie atomowej
jest ważniejszy od dwóch, a nawet trzech
atomów o mniejszych liczbach atomowych.
2-bromo-3-chloro-4-metylopentan
C
Cl
H
CHCH
3
CH
3
CH
Br
1
*
2
3
4
H
3
C
3-bromo-2-metylopentan
C
Br
H
CH
2
CH
3
CH
3
CH
1
*
2
3
4
H
3
C
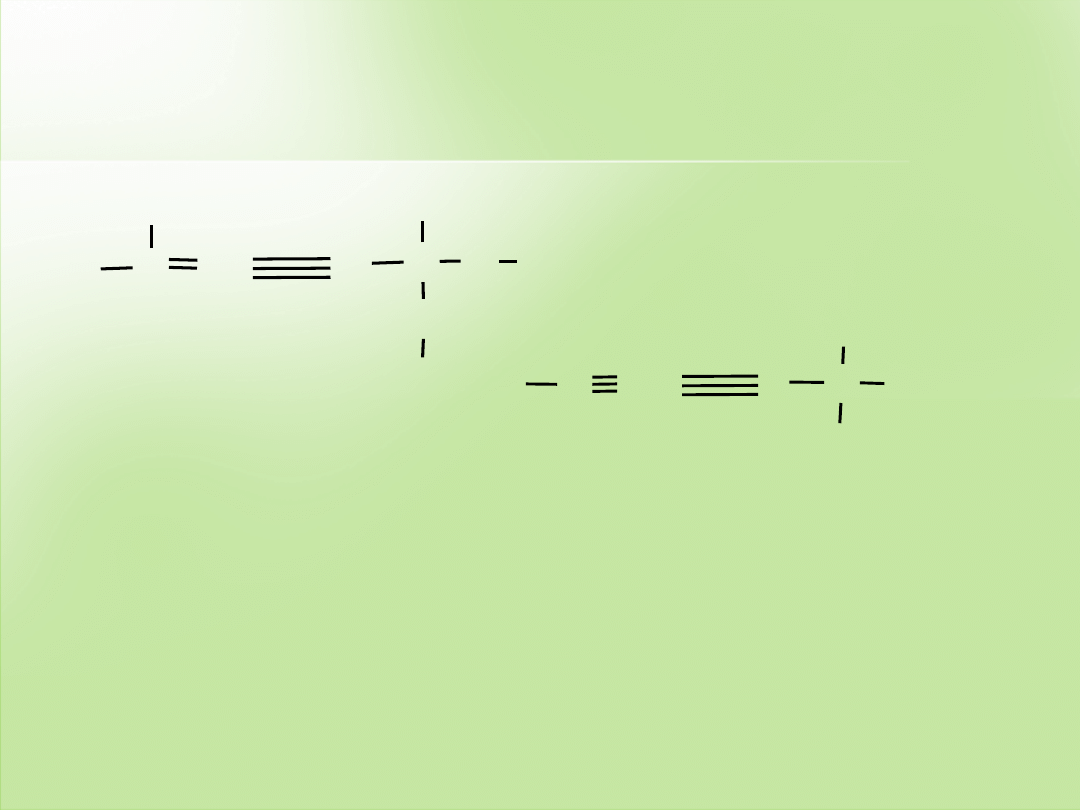
3.
W związkach zawierających wiązania wielokrotne oba atomy
powiązane w ten sposób liczy się podwójnie lub potrójnie.
C N
C N
N
N
C
O
C O
O
C
C
4.
Gdy asymetria cząsteczki zależy od różnic stereochemicznych
między podstawnikami, przyjmuje się:
dla izomerów geometrycznych
cis
>
trans
dla podstawników enancjomerycznych
R
>
S
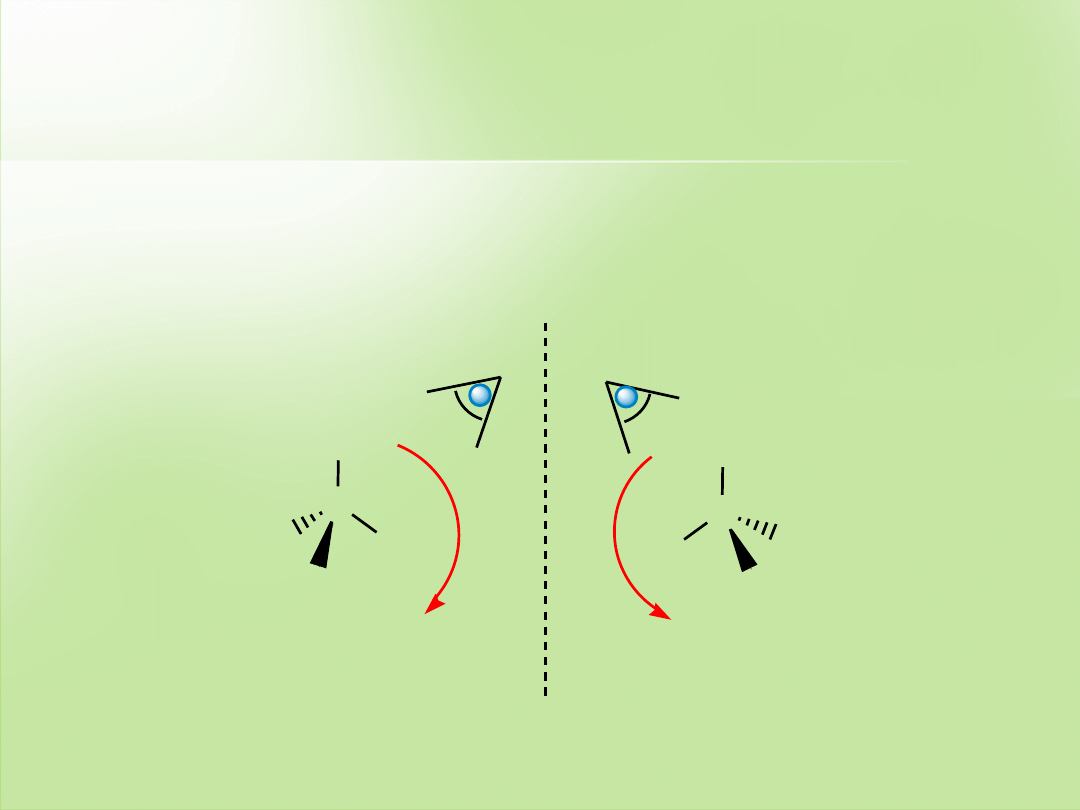
W przypadku enancjomeru z jednym centrum stereogenicznym zawierającym
podstawniki
1
,
2
,
3
i
4
, których kolejność pierwszeństwa jest
1
>
2
>
3
>
4
,
należy go ustawić w przestrzeni tak, aby podstawnik o najniższej liczbie atomowej
4
znalazł się dla obserwatora za chiralnym atomem węgla, a potem patrząc od frontu
zatoczyć łuk od podstawnika najstarszego poprzez średni do młodszego.
Łuk
zgodny
z ruchem wskazówek zegara (w prawo) - konfiguracja
R
.
Łuk
niezgodny
z ruchem wskazówek zegara (w lewo) - konfiguracja
S
.
C
Br
Cl
CH
3
H
C
Br
Cl
CH
3
H
(
R
)-1-bromo-1-chloroetan
(
S
)-1-bromo-1-chloroetan
1
4
2
1
3
*
*
4
2
3
Obserwator
Obserwator

Pierwszeństwo podstawników
Br
CH
3
H
I
C
I
Br
CH
3
H
1
2
3
C
F
Br
Cl
H
Br
F
Cl
H
1
2
3
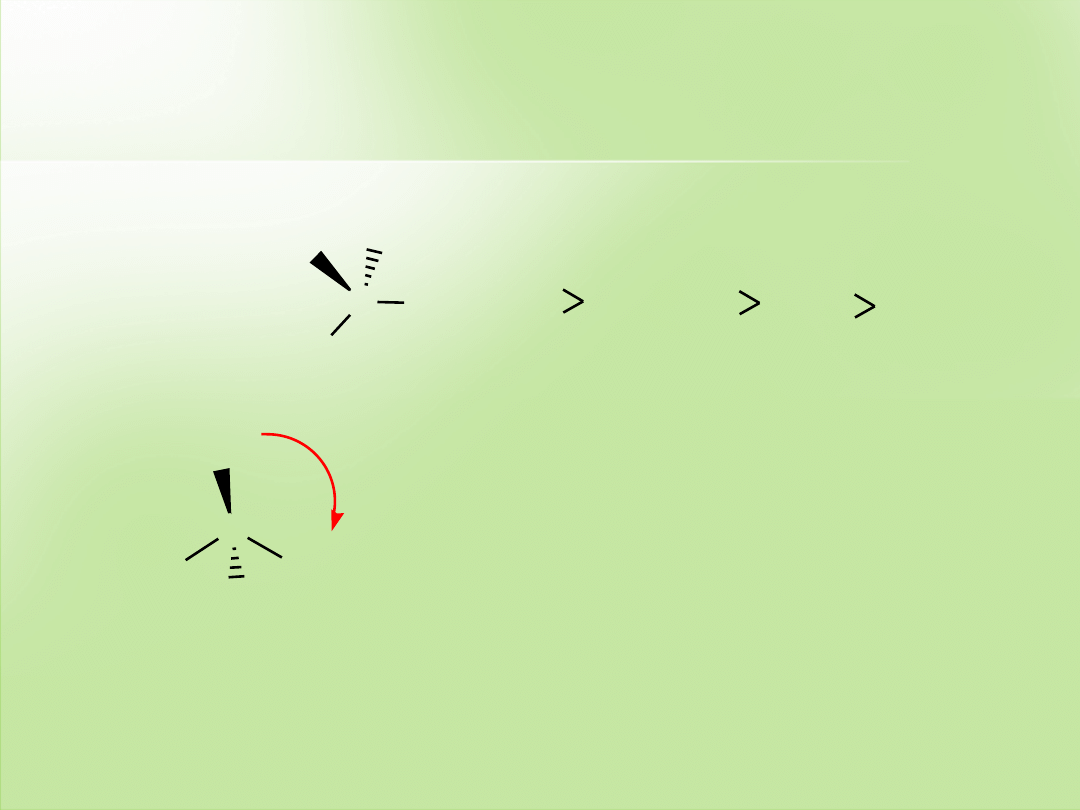
Pierwszeństwo podstawników
C
H
H
3
C
CH
3
CH
2
NH
2
NH
2
CH
3
CH
2
CH
3
H
C
CH
2
CH
3
H
3
C
H
2
N
H
1
2
3
(
R
)-1-metylopropyloamina
zorientowanie cz
ąsteczki tak, aby podstawnik
najm
łodszy był najbardziej oddalony od obserwatora
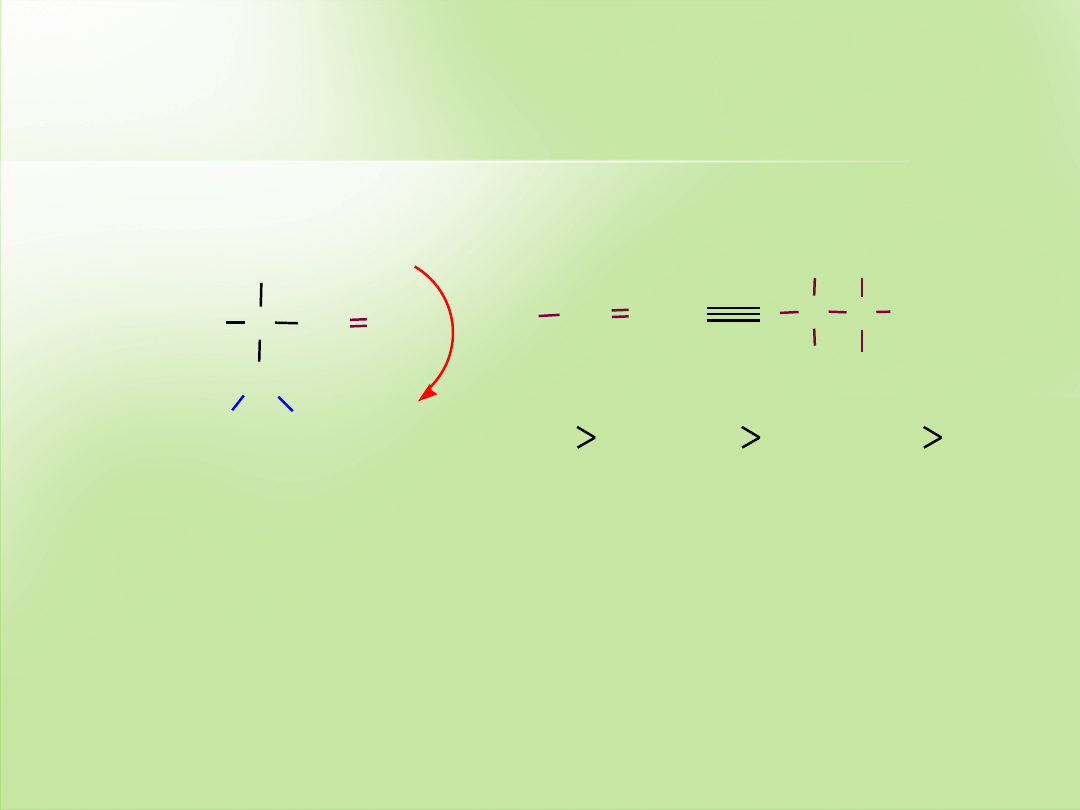
Pierwszeństwo podstawników
(
S
)-3-fluoro-4-metylopent-1-en
C
F
CH
CH
H
1
*
2
3
4
CH
2
H
3
C
CH
3
CH CH
2
C C
H
C
C
F
CH=CH
2
CH(CH
3
)
2
H
upo
rządkowane podstawniki
powiązane z centrum stereogenicznym
zgodnie ze starszeństwem
We wzorze
atom wodoru (najmłodszy podstawnik) zapisany jest poziomo czyli
znajduje się nad płaszczyzną, a nie pod płaszczyzną, należy oznaczoną
konfigurację (
R
) odwrócić i przyjąć jako rzeczywistą.

Często spotyka się (zwłaszcza w biochemii) oznaczenie enancjomerów
(
+
) i (
-
). Oznaczenie takie związane jest z kierunkiem skręcania
płaszczyzny światła spolaryzowanego (skręcalnością właściwą) i nie
można go bezpośrednio utożsamiać z konfiguracją absolutną.
Enancjomery (
+
) skręcają płaszczyznę światła spolaryzowanego
w
prawo
, zaś (
-
)
w lewo
.
C
H
CH
2
Cl
CH
3
CH
2
CH
3
*
(
S
)-(
+
)-1-chloro-2-metylobutan
*
(
R
)-(
-
)-oktan-2-ol
HO
H
Mieszanina racemiczna
(lub racemat) –
równomolowa mieszanina enancjomerów, nie
skręca płaszczyzny światła spolaryzowanego.
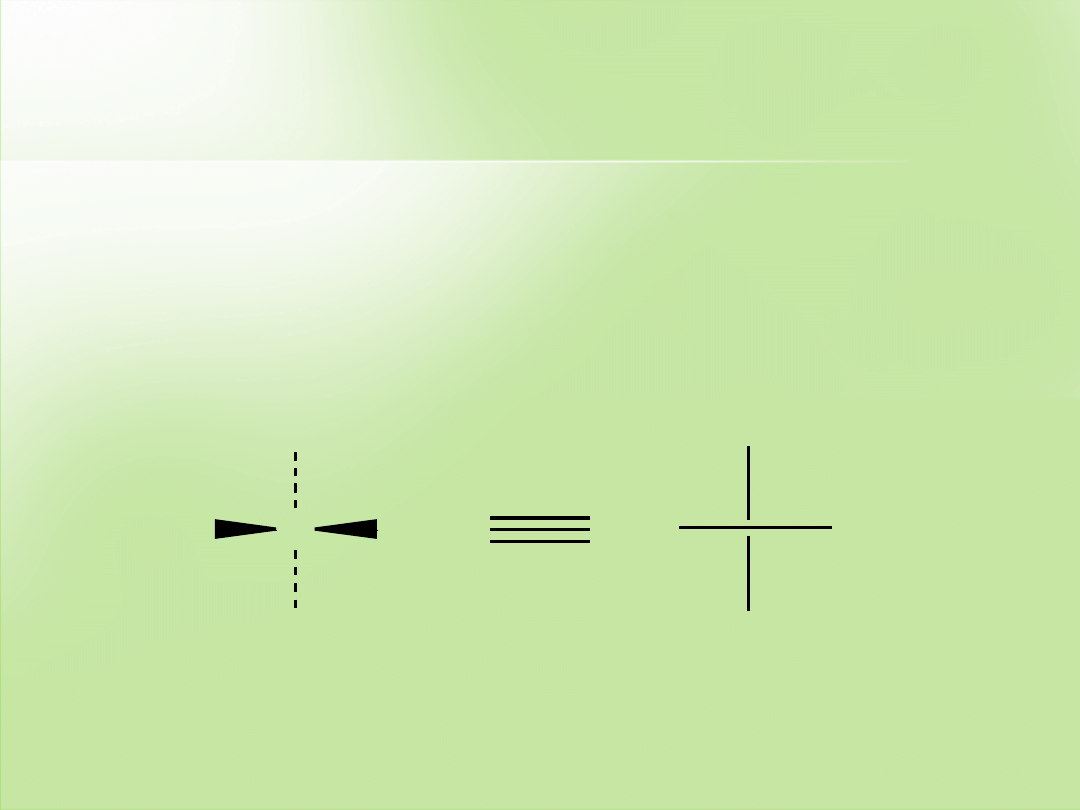
Projekcja Fischera
(rzutowanie wzoru płaskiego
cząsteczki na płaszczyznę)
–
cząsteczkę ustawia się tak, żeby
najdłuższy łańcuch węglowy znalazł się w jednej płaszczyźnie.
Następnie robi się jej pionowy rzut, np. na kartkę papieru;
wiązania pionowe są pod płaszczyzną, a poziome nad płaszczyzną
.
*
C
CH
3
CH
2
CH
3
H
Br
CH
3
CH
2
CH
3
H
Br
4
3
2
1
1
2
3
4
*
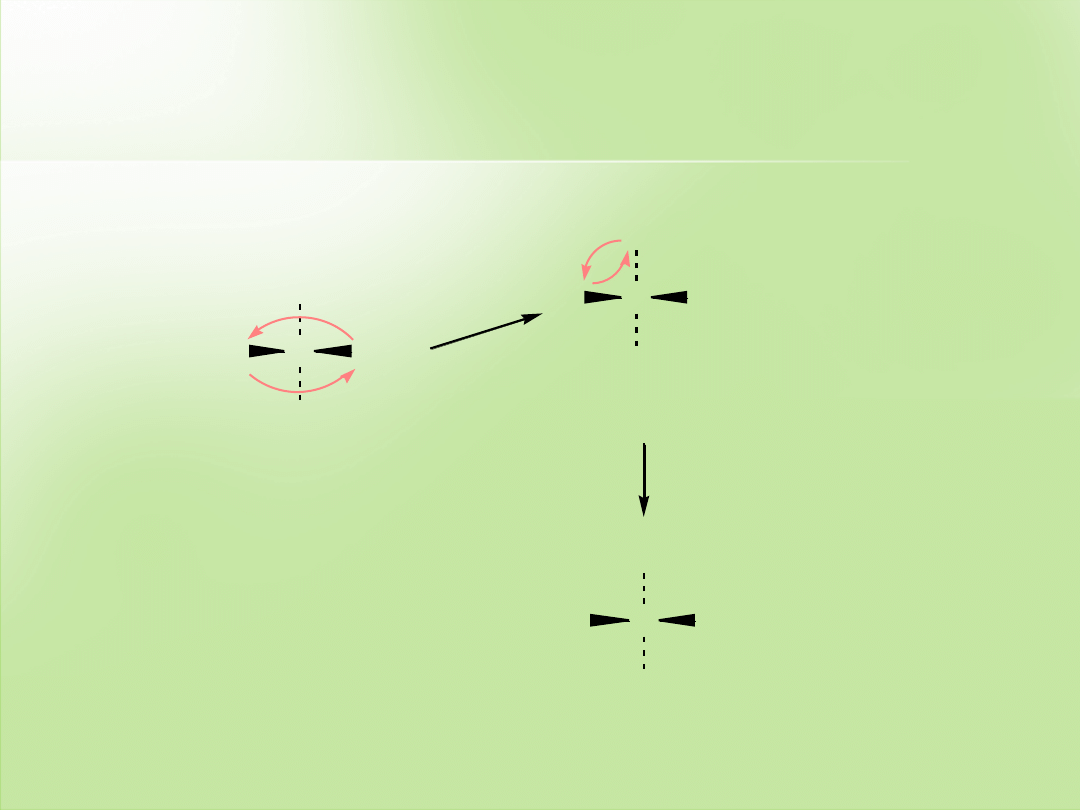
Nieparzysta (pojedyncza) zamiana podstawników na
projekcji Fischera
powoduje zmianę konfiguracji z (
R
) na (
S
) lub (
S
) na (
R
),
a parzysta zamiana podstawników zachowuje pierwotną konfigurację.
*
C
CH
2
CH
3
CH
2
CH
2
CH
3
H
F
4
3
2
1
(
S
)- 3-fluoroheksan
*
C
CH
2
CH
3
CH
2
CH
2
CH
3
F
H
4
3
2
1
(
R
)- 3-fluoroheksan
(
S
)- 3-fluoroheksan
*
C
F
CH
2
CH
2
CH
3
CH
3
CH
2
H
4
3
2
1
pojedyncza
zamiana podstawników
parzysta
zamiana podstawników
Cząsteczki zawierające dwa centra chiralne
Oznaczanie konfiguracji 2,3-dichlorobutanu
1
*
C
CH
3
C
CH
3
Cl
H
H
Cl
*
2
3
4
1
*
C
CH
3
C
CH
3
H
Cl
Cl
H
*
2
3
4
Stereoizomery
2,3-dichlorobutanu
1
*
C
CH
3
C
CH
3
Cl
H
Cl
H
*
2
3
4
1
*
C
CH
3
C
CH
3
H
Cl
H
Cl
*
2
3
4
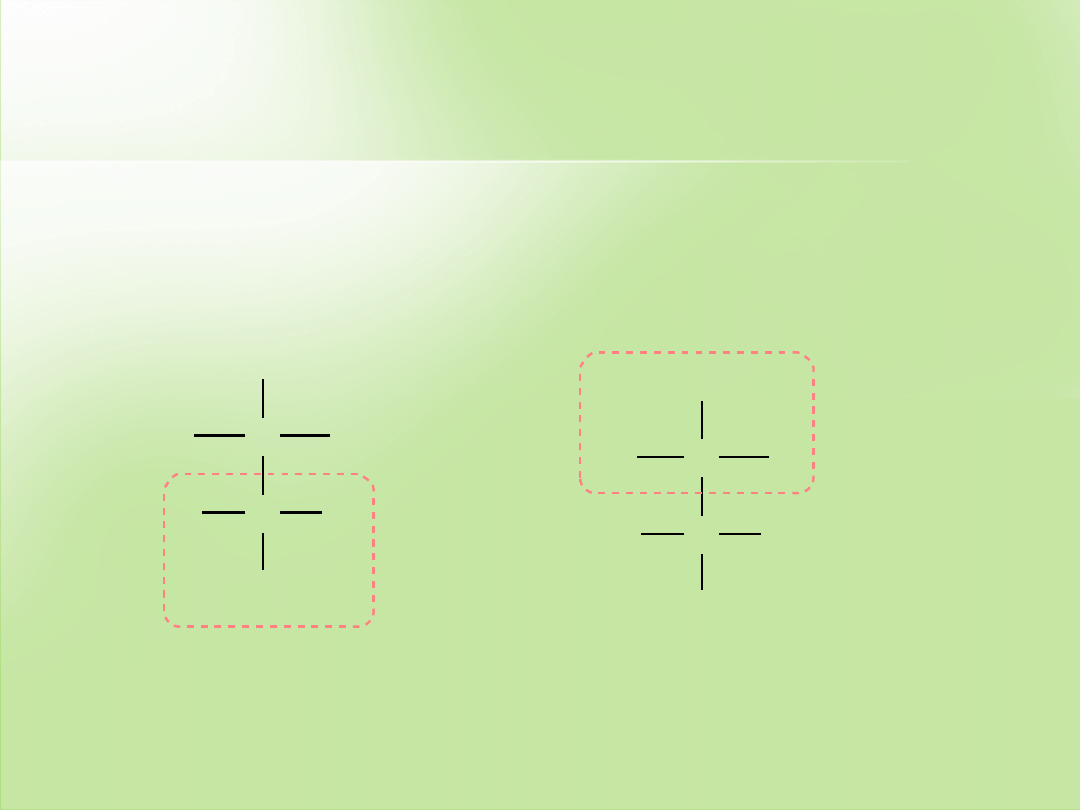
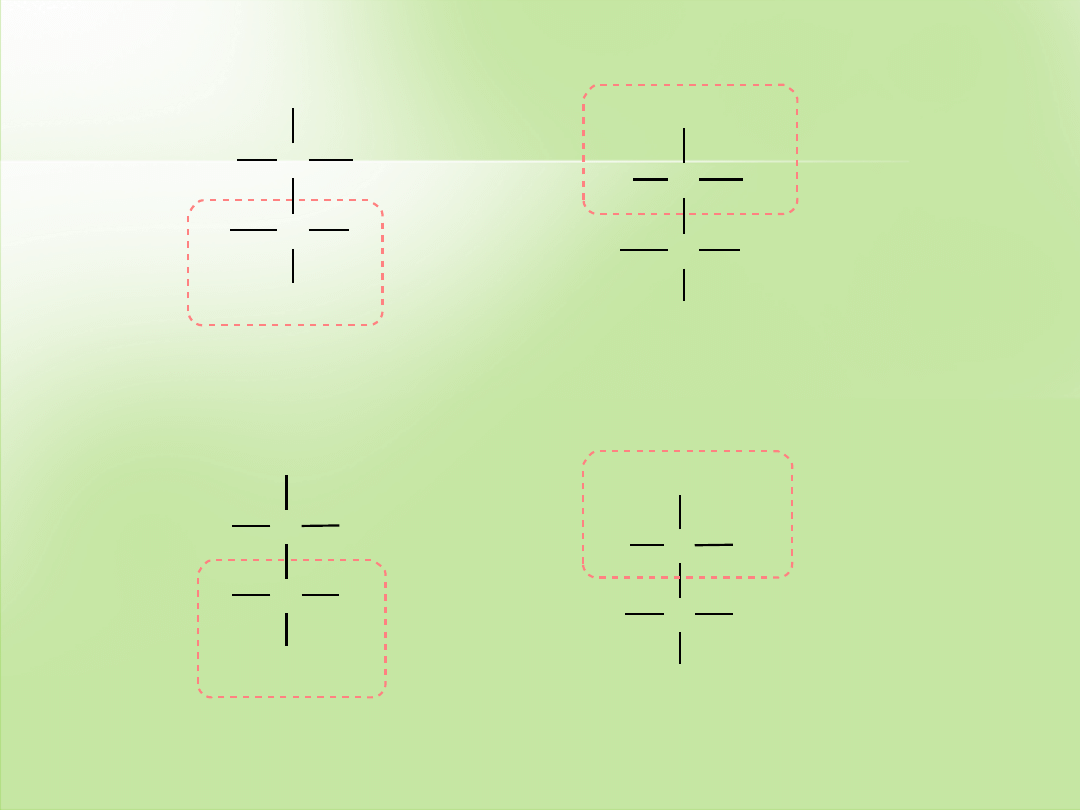
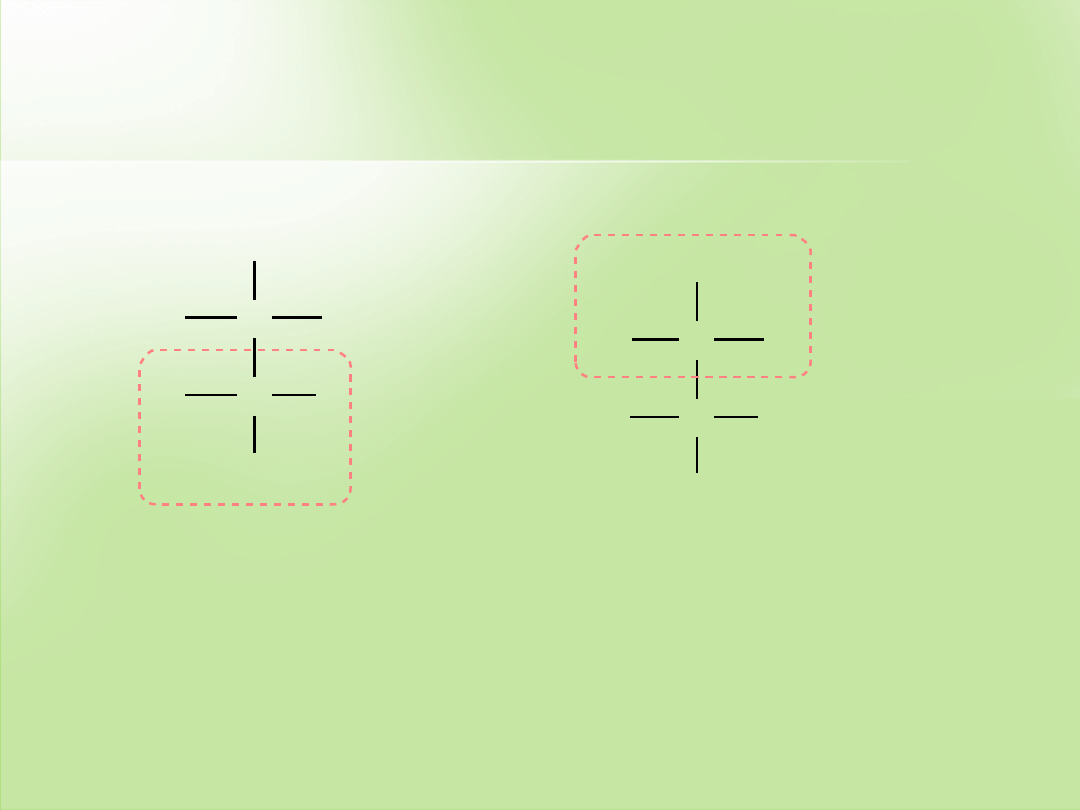
Po narysowaniu wzoru w projekcji Fischera przypisujemy konfigurację
poszczególnym centrom chiralnym. W 2,3-dichlorobutanie są dwa
centra chiralne
C
2
i
C
3
. Ponieważ we wzorach atom wodoru znajduje się
nad płaszczyzną (zapisany jest poziomo), a nie pod płaszczyzną
(zapis pionowy), a więc po oznaczeniu konfiguracji dla
C
2
i
C
3
należy oznaczoną
konfigurację odwrócić i przyjąć ją jako rzeczywistą.
*
C
CH
3
C
CH
3
Cl
H
H
Cl
2
konfiguracja
dla
C
2
:
(
R
)
4
3
2
1
*
C
CH
3
C
CH
3
Cl
H
H
Cl
3
4
3
2
1
konfiguracja
dla
C
3
:
(
S
)
(2
R
,3
S
)- 2,3-dichlorobutan
*
C
CH
3
C
CH
3
H
Cl
Cl
H
2
konfiguracja
dla
C
2
:
(
S
)
1
3
2
4
*
C
CH
3
C
CH
3
H
Cl
Cl
H
3
4
3
2
1
konfiguracja
dla
C
3
:
(
S
)
(2
S
,3
S
)- 2,3-dichlorobutan
*
C
CH
3
C
CH
3
Cl
H
Cl
H
2
konfiguracja
dla
C
2
:
(
S
)
4
3
2
1
*
C
CH
3
C
CH
3
Cl
H
Cl
H
3
4
3
2
1
konfiguracja
dla
C
3
:
(
R
)
(2
S
,3
R
)- 2,3-dichlorobutan
*
C
CH
3
C
CH
3
H
Cl
H
Cl
2
konfiguracja
dla
C
2
:
(
R
)
4
3
2
1
*
C
CH
3
C
CH
3
H
Cl
H
Cl
3
4
3
2
1
konfiguracja
dla
C
3
:
(
S
)
(2
R
,3
S
)- 2,3-dichlorobutan

Związki chiralne
1.
Chiralność cząsteczki jest warunkiem koniecznym
i wystarczającym do zaistnienia enancjomerów;
2.
Obecność chiralnego atomu węgla nie jest warunkiem
koniecznym ani wystarczającym do wystąpienia
enancjomerów;
3.
Liczba enancjomerów zależy od liczby centrów
asymetrii w cząsteczce i wynosi
LS=2
n
, gdzie
n
– liczba chiralnych atomów.
Diastereoizomery
- nie są odbiciami lustrzanymi;
różnią się właściwościami fizycznymi i chemicznymi.
1
*
C
CH
3
C
CH
3
Cl
H
H
Cl
*
2
3
4
1
*
C
CH
3
C
CH
3
H
Cl
Cl
H
*
2
3
4
Stereoizomery parami
A
-
B
,
A
-
D
,
B
-
C
,
C
-
D
są diastereoizomerami
(stereoizomery nie będące odbiciami lustrzanymi)
1
*
C
CH
3
C
CH
3
Cl
H
Cl
H
*
2
3
4
1
*
C
CH
3
C
CH
3
H
Cl
H
Cl
*
2
3
4
A
B
C
D
C
C
Br
H
Br
H
C
C
Br
H
H
Br
diastereoizomery
(izomery geometryczne)
cis
-1,2-dibromoetan
trans
-1,2-dibromoetan
OH
H
3
C
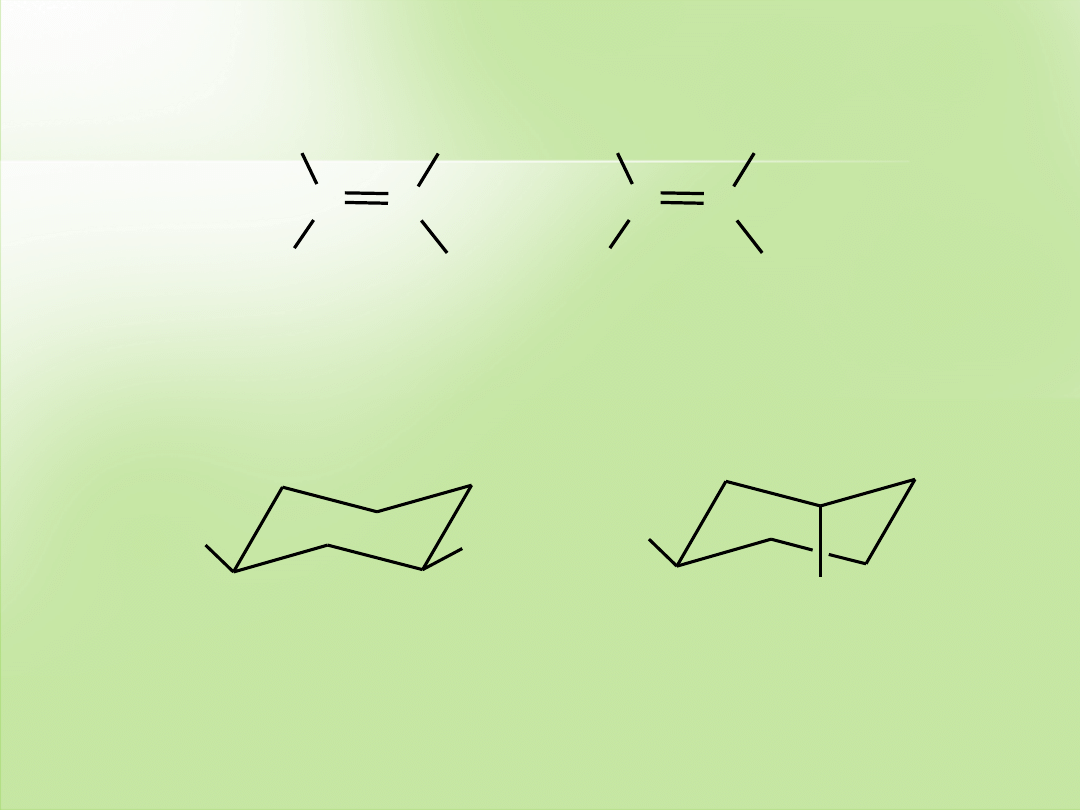
cis
-3-metylocykloheksanol
H
3
C
trans
-3-metylocykloheksanol
OH
diastereoizomery
(izomery konformacyjne)

3
2
*
COOH
CH
3
H
Br
H
Br
3
2
COOH
CH
3
Br
H
H
Br
*
*
*
kwas
(2
R
,3
R
)-2,3-dibromobutanowy
kwas
(2
S
,3
R
)-2,3-dibromobutanowy
diastereoizomery
(izomery konfiguracyjne)

Związki
mezo
–
stereoizomery zawierające
centra chiralne oraz płaszczyznę symetrii
1
*
C
CH
3
C
CH
3
Cl
H
Cl
H
*
2
3
4
1
*
C
CH
3
C
CH
3
H
Cl
H
Cl
*
2
3
4
(
2
S
,
3
R
)-2,3-dichlorobutan
(
2
R
,
3
S
)-2,3-dichlorobutan
mezo
-2,3-dichlorobutan
(związek achiralny)
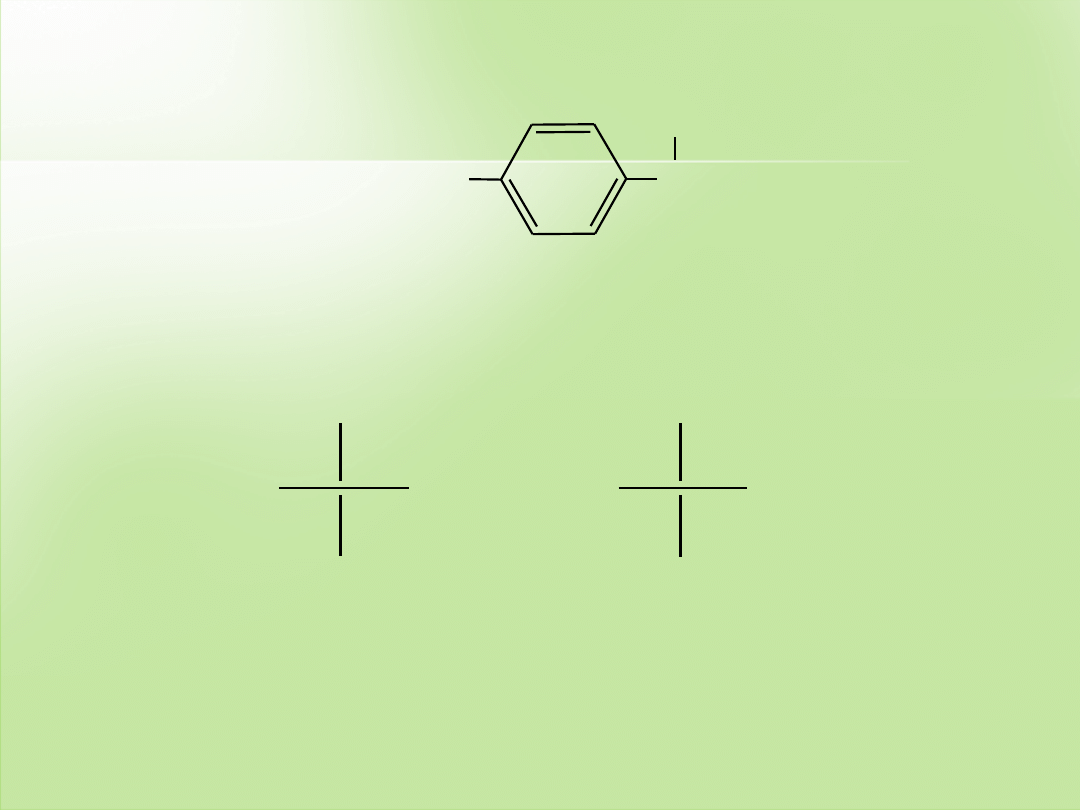
COOH
CH
3
Ar
H
1
3
2
4
(
R
)-ibuprofen
*
COOH
H
Ar
CH
3
1
3
2
4
(
S
)-ibuprofen
*
CHCOOH
CH
3
(CH
3
)
2
CHCH
2
ibufrofen
*
CH
2
OAr
H
HO
CH
2
NHCH(CH
3
)
2
1
3
2
4
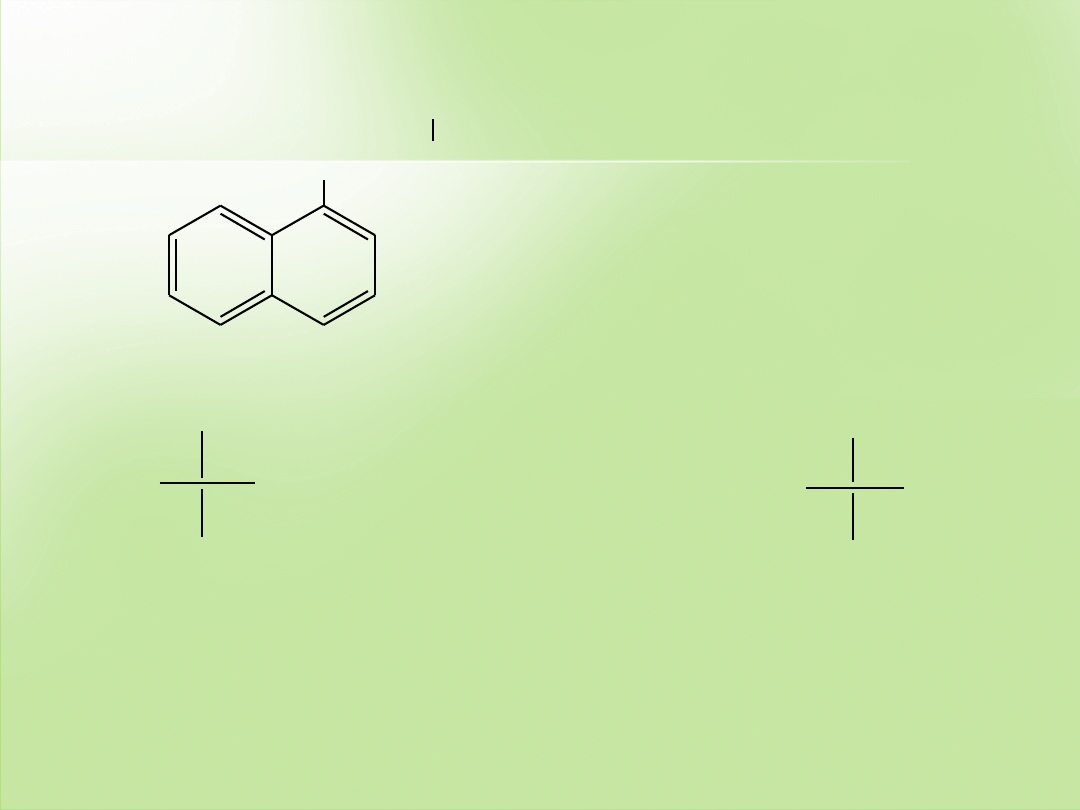
(R)-propranolol
(nieaktywny)
*
CH
2
OAr
H
(CH
3
)
2
CHNHCH
2
OH
1
3
2
4
(S)-propranolol
(blokuje receptory
)
*
OCH
2
CHCH
2
NHCH(CH
3
)
2
OH
*
propranolol
Konfiguracja względna
–
konfiguracja
stereoizomeru wyznaczona względem wzorca, np. aldehydu
glicerynowego przyjętego za modelowy związek.
atom
węgla na najwyższym
stopniu utlenienia
CHO
CH
2
OH
HO
H
aldehyd
L
-glicerynowy
*
CHO
CH
2
OH
H
OH
aldehyd
D
-glicerynowy
*
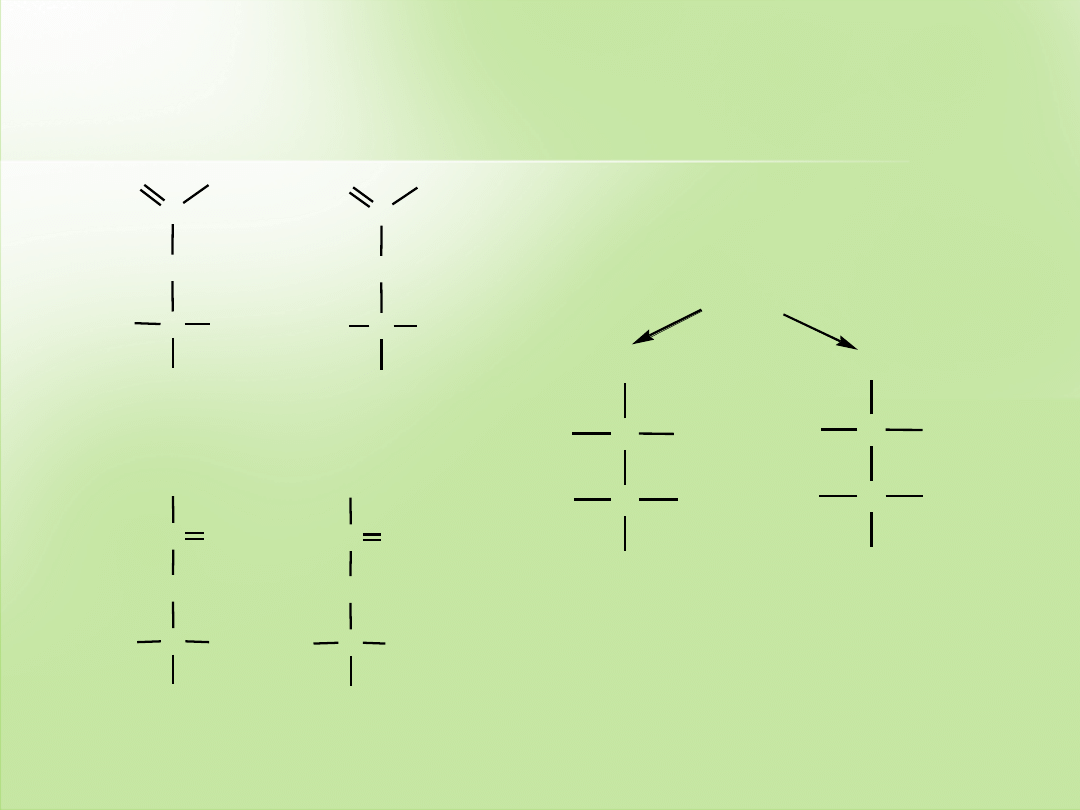
(CHOH)
n
D
-aldozy
C
C
CH
2
OH
OH
H
H
O
(CHOH)
n
L
-aldozy
C
C
CH
2
OH
H
HO
H
O
CH
2
OH
(CHOH)
n
D
-ketozy
C
O
C
CH
2
OH
OH
H
CH
2
OH
(CHOH)
n
L
-ketozy
C
O
C
CH
2
OH
H
HO
Cukry
(węglowodany) szeregu
L
i
D
.
C
CHO
C
CH
2
OH
H
HO
OH
H
L
-treoza
C
CHO
C
CH
2
OH
OH
H
H
HO
D
-treoza
atom
węgla na najwyższym
stopniu utlenienia
Aminokwasy białkowe
(oprócz
Gly
) są chiralne i mają
konfigurację
L
na
C
α
.
C
COO
CH
2
SH
NH
3
H
+
-
C
HSH
2
C
COO
H
NH
3
-
+
2
3
1
L
-Cysteina
ma konfigurację absolutną (
R
).
C
COO
CH
3
NH
3
H
C
COO
CH
3
H
NH
3
+
+
L
-alanina
D
-alanina
-
-
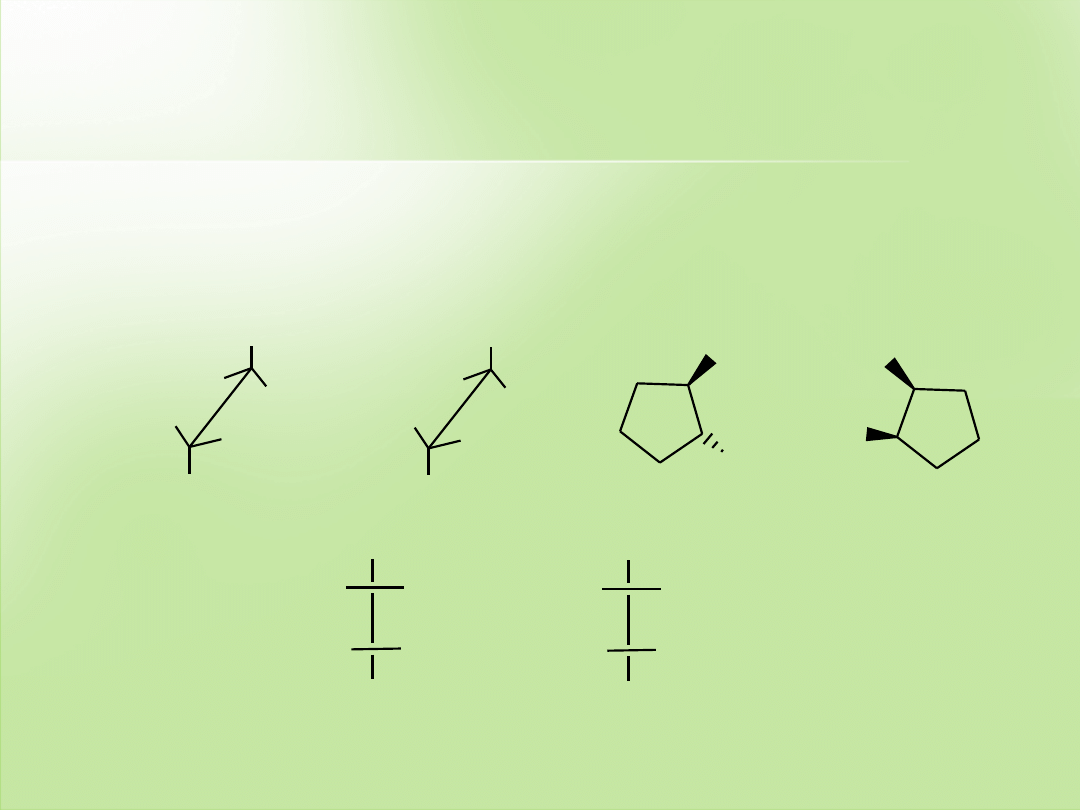
Pytanie
W każdej z następujących par związków zaznacz czy są to
związki identyczne, enancjomery czy diastereoizomery.
H
Br
H
CH
3
H
3
C
H
a.
H
Br
H
CH
3
H
3
C
H
b.
OH
OH
HO
HO
Cl
CH
2
CH
3
H
3
C
H
H
Cl
Cl
Cl
H
CH
2
CH
3
H
3
C
H
c.
Odpowiedź
Cl
CH
2
CH
3
H
3
C
H
H
Cl
Cl
Cl
H
CH
2
CH
3
H
3
C
H
c.
związki chiralne -
diastereoizomery
H
Br
H
CH
3
H
3
C
H
a.
H
Br
H
CH
3
H
3
C
H
związki chiralne -
enancjomery
b.
OH
OH
HO
HO
związki achiralne (
mezo
) -
diastereoizomery
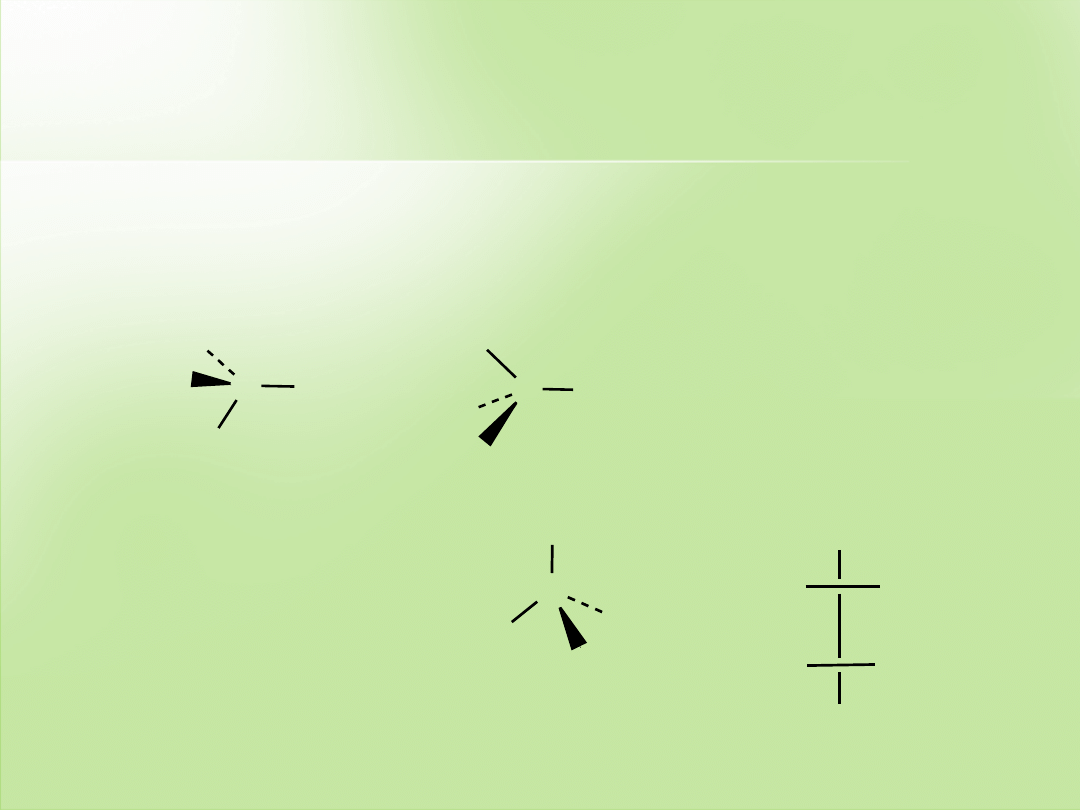
Pytanie
Określ konfigurację chiralnych atomów węgla oraz podaj
nazwy związków.
a.
C
Cl
H
H
3
C
H
13
C
6
b.
C
OH
C
3
H
7
H
3
C
C
2
H
5
CH
3
CH
3
H
Br
H
Br
d.
c.
C
CH
3
Ph
OH
H
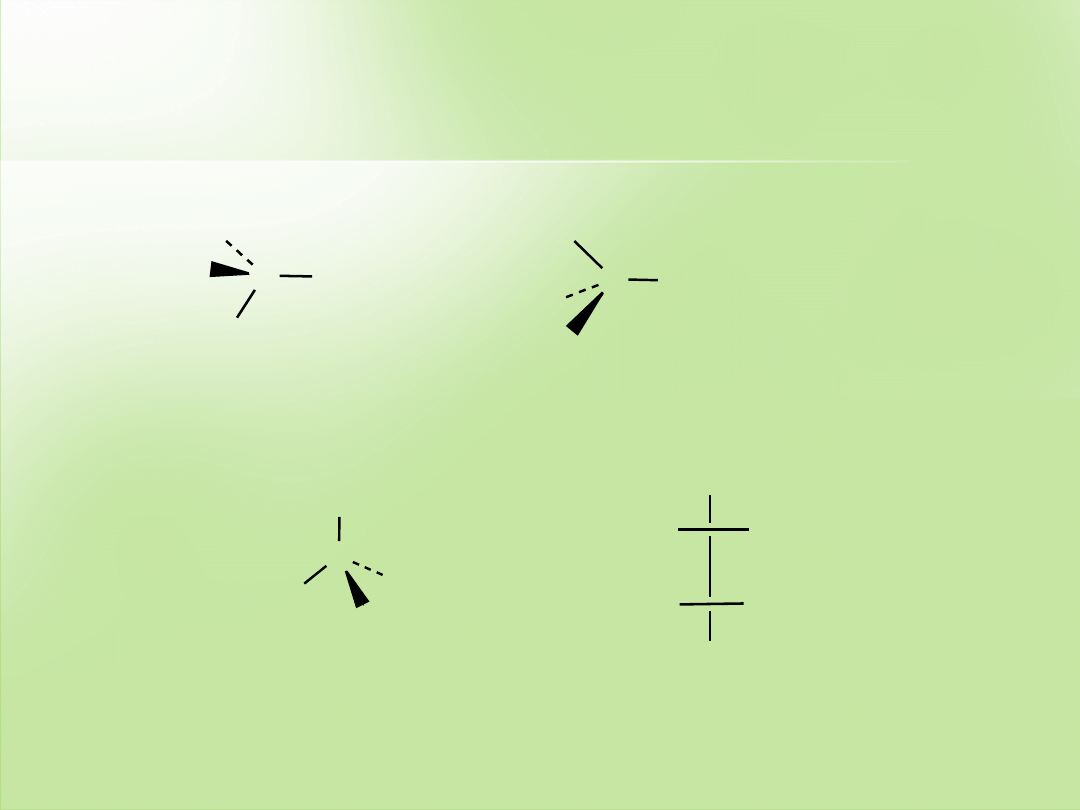
Odpowiedź
a.
C
Cl
H
H
3
C
H
13
C
6
4
3
2
1
*
(2
R
)-2-chlorooktan
b.
C
OH
C
3
H
7
H
3
C
C
2
H
5
1
2
3
4
*
(3
S
)-3-metyloheks-3-ol
c.
C
CH
3
Ph
OH
H
*
1
2
3
4
(
R
)-1-fenyloetanol
CH
3
CH
3
H
Br
H
Br
d.
*
*
(2
S
,3
R
)-2,3-dibromobutan

1. Przedstaw każdy z niżej podanych związków w jego najtrwalszej
konformacji:
a.
trans
-2-bromo-1-izopropylocykloheksan
b.
cis
-1-
tert
-butylo-3-fluorocykloheksan
c.
cis
-1-chloro-4-metylocykloheksan
d.
trans
-4-
tert
-butylocykloheksanol
2. Narysuj najtrwalszą konformację poniższego związku i podaj
jego nazwę. Czy jest on chiralny?
COOH
COOH
Br
Pytania
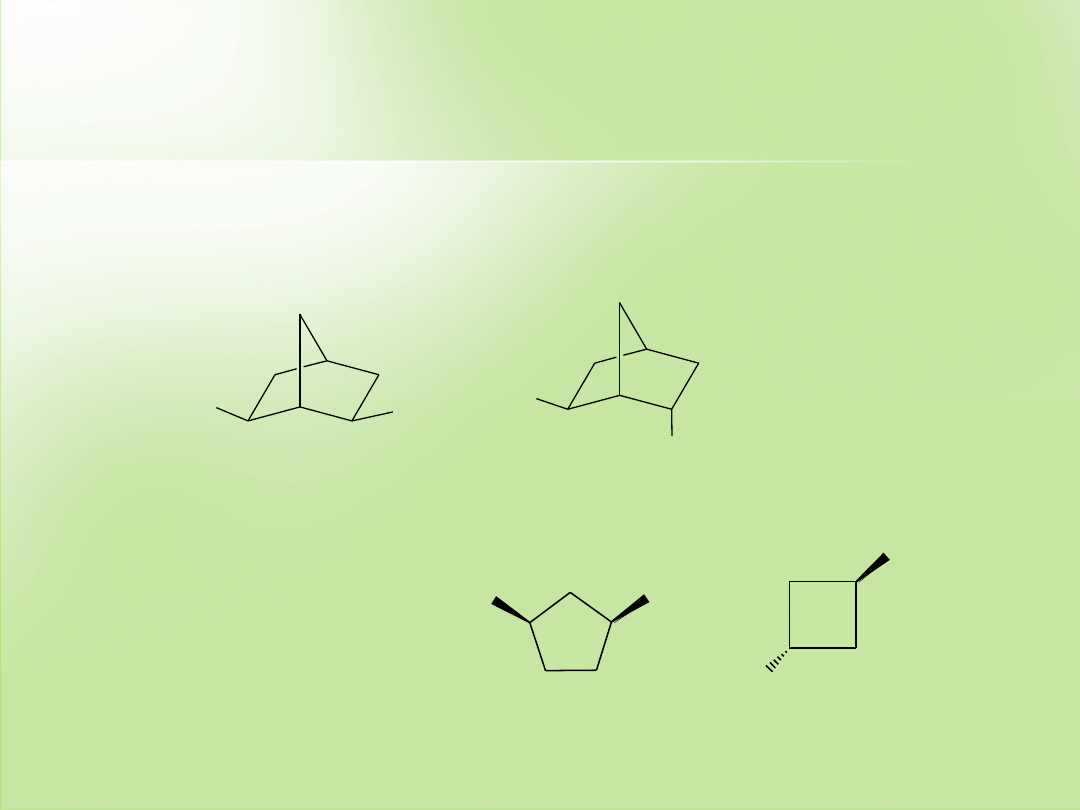
3. Określ konfigurację centrów stereogenicznych w następujących
związkach. Które z nich są formami
mezo
.
HO
OH
HO
OH
4
3
2
1
1
7
6
5
7
4
3
2
5
6
a.
b.
Br
Br
Cl
CI
c.
d.

Dziękuję za uwagę
Wyszukiwarka
Podobne podstrony:
izomeria optyczna
izomeria zwiazkow organicznych
Izomeria związków organicznych
Izomeryzacja ostateczna wersja
Izomeria 4 id 221207 Nieznany
Izomeria konformacyjna
Izomeria monosacharydów, Ratownicto Medyczne, BIOCHEMIA
Wyznaczanie stałych równania kinetycznego reakcji izomeryzacji D – glukozy do D fruktozyx
Ksylen (mieszanina izomerów)
Izomeria, IZOMERIA
Chemia wykłady, koło II sem v.3.0 - do nauki, Izomeria optyczna
Do prezentacji izomeria konfiguracyjna
koło 2 izomeria
Izomeria[1] id 221209 Nieznany
5 IZOMERIA wyklad
izomeria alkenow i alkinow ppt
Izomeria optyczna id 221213 Nieznany
więcej podobnych podstron