
Drogi szerzenia się zakażeń
szpitalnych w OIT
Oporność na antybiotyki
Monitorowanie mikrobiologiczne
Drogi szerzenia się zakażeń
szpitalnych w OIT
Oporność na antybiotyki
Monitorowanie mikrobiologiczne

Drogi szerzenia się zakażeń w OIT
A.
Kontakt
Patogeny przenoszone są głównie na rękach
personelu.
W ten sposób dochodzi do 80% Z.SZ. !
Patogeny przenoszone są głównie na rękach
personelu.
W ten sposób dochodzi do 80% Z.SZ. !
• ręce
• materiały opatrunkowe, narzędzia
• duże krople (z dróg oddechowych)

Drogi szerzenia się zakażeń w OIT
B.
Droga powietrzna
•
od chorych lub personelu (małe
krople, komórki naskórka)
•
z otoczenia (aerozole, urządzenia
klimatyzacyjne, kurz)

Drogi szerzenia się zakażeń w OIT
C.
Droga kałowo-ustna (ang.
fecal-oral)
Głównym rezerwuarem patogenów
jest przewód pokarmowy
chorego, a zakażenie następuje
przez jego usta.

Drogi szerzenia się zakażeń w OIT
D.
Krew
•
Podanie krwi lub preparatów
krwiopochodnych jako leku
•
Przypadkowe zakażenie krwią w relacji
pacjent-pacjent lub pacjent-pracownik
służby zdrowia

Oporność na antybiotyki
Oporność na antybiotyki

RYZYKO ZAKAŻEŃ SZCZEPAMI
WIELOOPORNYMI W OIT
•
szerokie stosowanie antybiotyków, zwłaszcza
-laktamowych (
cefalosporyny!
)
•
wcześniejsza hospitalizacja chorych
•
długotrwały okres leczenia
•
procedury inwazyjne - np.sztuczna wentylacja,
cewniki
naczyniowe, cewnik moczowy

Czynniki ryzyka rozwoju
oporności na antybiotyki w VAP
•Stosowanie antybiotyków przez 15 dni
1
•
Czas hospitalizacji
2
•
Czas prowadzenia sztucznej wentylacji >
7 dni
1
1
Trouillet J-L et al. Am J Respir Crit Care Med 1998;157:531-539.
2
Lautenbach E et al. Clin Infect Dis 2001;32:1162-1171.
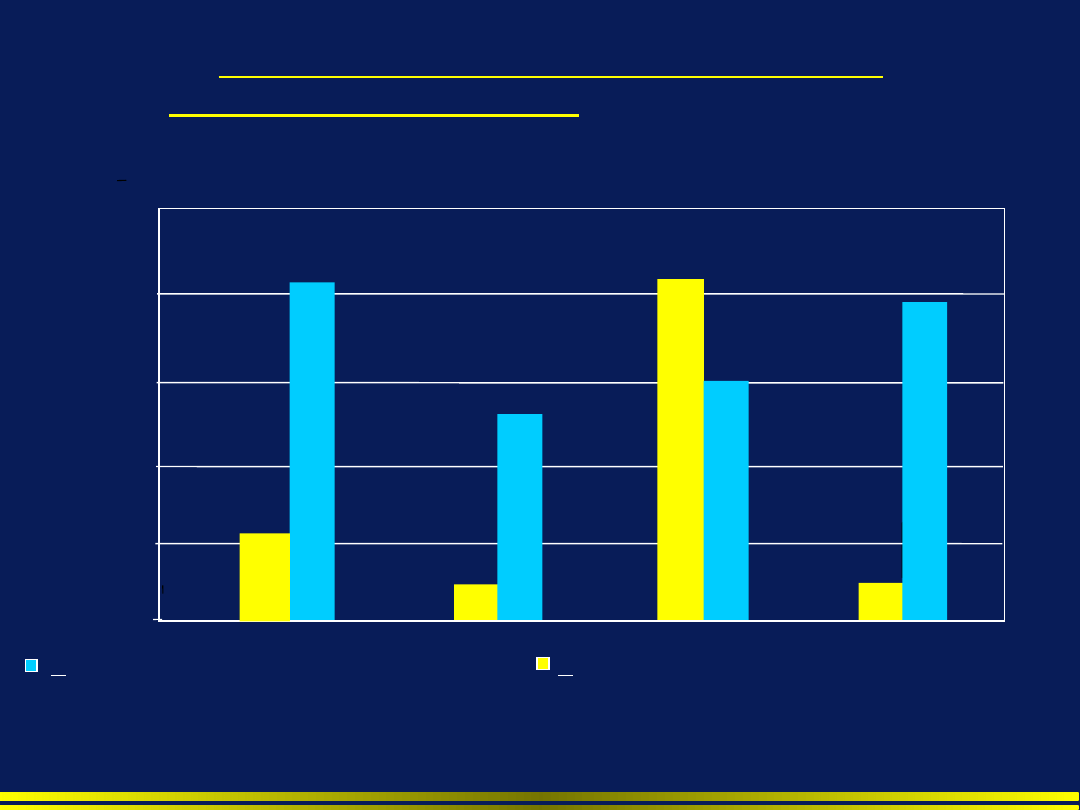
Wpływ
wcześniejszej antybiotykoterapii
oraz
sztucznej wentylacji
na rodzaj flory
bakteryjnej odpowiedzialnej za rozwój VAP
MV-wentylacja mechaniczna MRSA=metycylinooporny Staphylococcus aureus
Trouillet J-L et al. Am J Respir Crit Care Med 1998;157:531-539.
6.3
%
21.7%
3.1%
13.2%
21.9%
15.1%
3.1%
19.7%
0%
5%
10%
15%
20%
25%
P. aeruginosa
A. baumannii
Enterobacteriace
ae
MRSA
MV > 7 dni, bez wcześniejszej antybiotykoterapii
MV > 7 dni, wcześniejsza antybiotykoterapia
Pa
to
g
e
n
y
o
d
p
o
w
ie
d
zi
a
ln
e
z
a
r
o
zw
ó
j
V
A
P
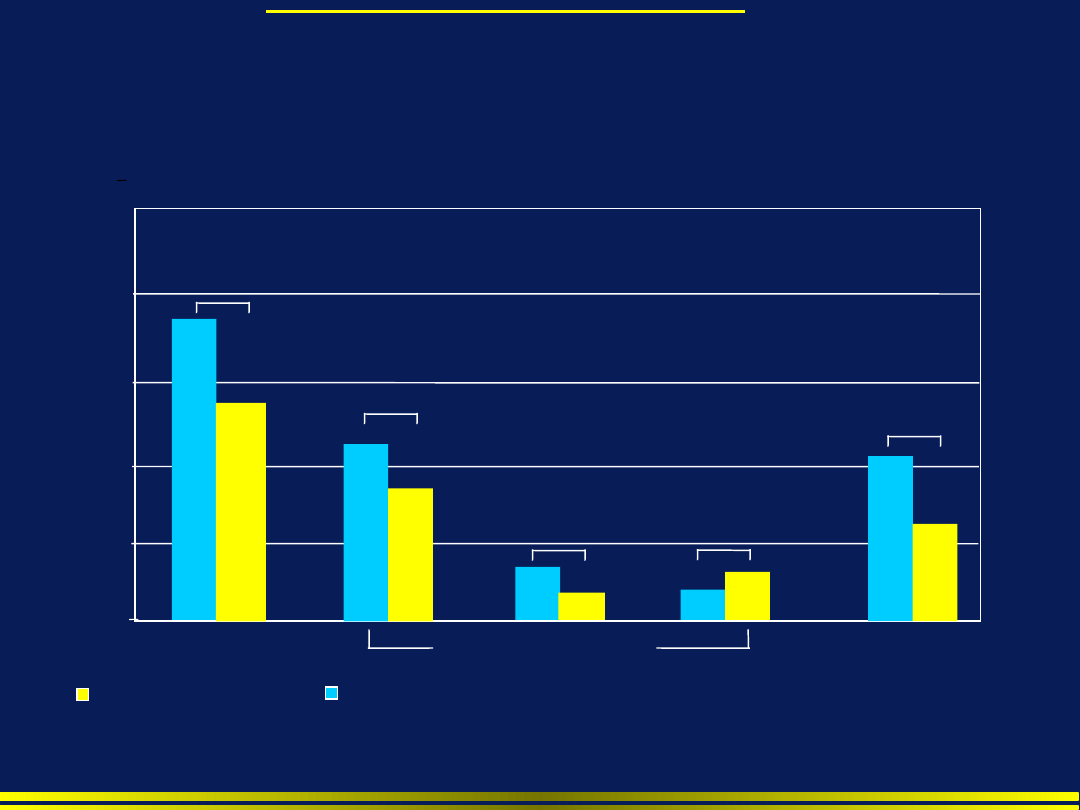
Wpływ
technik inwazyjnych
na rozwój
oporności patogenów wywołujących
zakażenia szpitalne
Kollef MH et al. Clin Inf Dis 2000;31(Suppl. 4):S131-S138.
Coagulase-negative
Staphylococci
P= .001
0
10
20
30
40
50
Zakażenia
krwi
Szpitalne zapalenie płuc
Zakażenia dróg
moczowych
Techniki inwazyjne
P
ro
ce
n
t
w
y
st
ę
p
o
w
a
n
ia
P. aeruginosa
P= .002
A. baumannii
P= .006
E. coli
P= .023
C. albicans
P= .009
Bez technik inwazyjnych

SZCZEPY WIELOOPORNE W OIT
• MRSA
• MRCNS
• Enterococcus faecalis-HLAR, VRE
• pałeczki Gram-ujemne – ESBL, oporność
na aminoglikozydy, fluorochinolony

Wyniki leczenia w zakażeniach wywołanych
szczepami Klebsiella pneumoniae
produkującymi ESBL
Leczenie
Leczenie
%
%
Śmiertelności
Śmiertelności
Nieaktywne
antybiotyki
71
Betalaktamy
44
Chinolony
36
Imipenem
8
Paterson DL. IDSA 1998.

Mechanizmy oporności krzyżowej
bakterii Pseudomonas
Jedne antybiotyki mogą ułatwiać rozwój oporności na inne
grupy antybiotyków:
–
fluorochinolony
mogą ułatwiać rozwój oporności na karbapenemy
–
cefalosporyny 3 generacji
mogą ułatwiać rozwój oporności na inne
antybiotyki
.
•
System efflux (MexAB-OprM)
czynnego wypompowywania
antybiotyków (meronem) indukuje oporność krzyżową na inne
leki przeciwdrobnoustrojowe, jak fluorochinolony, penicyliny,
cefalosporyny, makrolidy i sulfonamidy.
•
Utrata poryn OprD prowadzi do nieskuteczności karbapenemów
(
niemożność wniknięcia
do wnętrza komórki bakteryjnej).
Kohler T i wsp. Clin Microbiol Infect 2001;7(Suppl 5):7-10.
Livermore DM. Clin Infect Dis 2002;34:634-640.
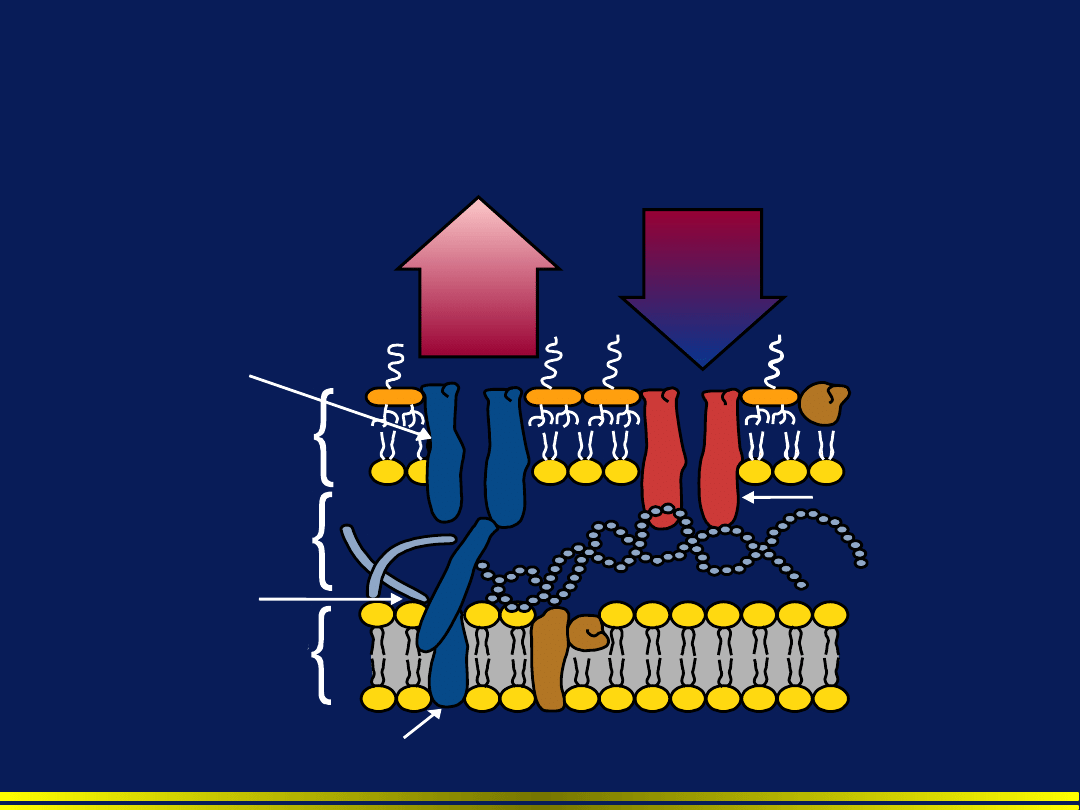
Mechanizmy oporności
Pseudomonas i system efflux
Za zgodą Livermore DM. Clin Infect Dis 2002;34:634-
640.
Meropenem
jest usuwany z
komórki,
( imipenem
nie )
System efflux
(OprM)
Błona
zewnętrzn
a
Przestrzeń
peryplazmatycz
na
Lipoproteiny
(MexA)
Błona
cytoplazmatyczn
a
System efflux (MexB)
Miejsce
wnikania
imipenemu I
meropenemu
do komórki
Białka porynowe

Metody obniżania oporności
na antybiotyki
Metody obniżania oporności
na antybiotyki
RACJONALIZACJA ANTYBIOTYKOTERAPII
RACJONALIZACJA ANTYBIOTYKOTERAPII
Wskazówki w postaci schematów
(guidelines)
Rotacja antybiotyków
Metoda polegająca na ustaleniu
Metoda polegająca na ustaleniu
schematu
schematu
stosowania antybiotyków w określonej
stosowania antybiotyków w określonej
grupie pacjentów i w określonym czasie
grupie pacjentów i w określonym czasie
ROTACJA ANTYBIOTYKÓW
ROTACJA ANTYBIOTYKÓW
KONCEPCJA:
KONCEPCJA:
Czasowe wyłączenie ze stosowania pewnych antybiotyków
Czasowe wyłączenie ze stosowania pewnych antybiotyków
(zwłaszcza
(zwłaszcza
o mniejszej skuteczności z powodu oporności drobnoustrojów)
o mniejszej skuteczności z powodu oporności drobnoustrojów)
i zastąpienie ich innymi może przywrócić skuteczność tych
i zastąpienie ich innymi może przywrócić skuteczność tych
wcześniej
wcześniej
stosowanych.
stosowanych.
specyfika szpitala
specyfika szpitala
monitorowanie mikrobiologiczne
monitorowanie mikrobiologiczne
ocena oporności drobnoustrojów
ocena oporności drobnoustrojów
które antybiotyki?
które antybiotyki?
na jak długo?
na jak długo?
SCHEMAT ROTACJI
SCHEMAT ROTACJI

ROTACJA ANTYBIOTYKÓW
ROTACJA ANTYBIOTYKÓW
Gerding DN, Larson TA, Hughes RA, et al: Aminoglycoside resistance and
Gerding DN, Larson TA, Hughes RA, et al: Aminoglycoside resistance and
aminoglycoside usage: Ten years of experience in the hospital. Antimicrob
aminoglycoside usage: Ten years of experience in the hospital. Antimicrob
Agents
Agents
Chemother, 1991; 35: 1284-1290
Chemother, 1991; 35: 1284-1290
-
rotacja antybiotyków z grupy aminoglikozydów
rotacja antybiotyków z grupy aminoglikozydów
(amikacyna/gentamycyna)
(amikacyna/gentamycyna)
-
dziesięć lat obserwacji
dziesięć lat obserwacji
-
czas wyłączania antybiotyku – od 3. do 51. miesięcy
czas wyłączania antybiotyku – od 3. do 51. miesięcy
-
istotny statystycznie spadek oporności drobnoustrojów
istotny statystycznie spadek oporności drobnoustrojów
na
na
aminoglikozyd wyłączony w danym okresie ze stosowania
aminoglikozyd wyłączony w danym okresie ze stosowania
-
dla zmniejszenia oporności konieczny dłuższy okres
dla zmniejszenia oporności konieczny dłuższy okres
wyłączenia ze stosowania
wyłączenia ze stosowania

ROTACJA ANTYBIOTYKÓW
ROTACJA ANTYBIOTYKÓW
Raymond DP, Pelletier SJ, Crabtree TD et al: Impact of a rotating empiric
Raymond DP, Pelletier SJ, Crabtree TD et al: Impact of a rotating empiric
antibiotic schedule on infectious mortality in an intensive care unit. Crit Care
antibiotic schedule on infectious mortality in an intensive care unit. Crit Care
M
M
ed,
ed,
2001; 29: 1101-1108
2001; 29: 1101-1108
-
kwartalna, jednoczesna rotacja antybiotyków z różnych
kwartalna, jednoczesna rotacja antybiotyków z różnych
grup
grup
-
2 lata obserwacji
2 lata obserwacji
-
w grupie badanej istotne statystycznie zmniejszenie
w grupie badanej istotne statystycznie zmniejszenie
śmiertelności z powodu zakażeń szpitalnych
śmiertelności z powodu zakażeń szpitalnych
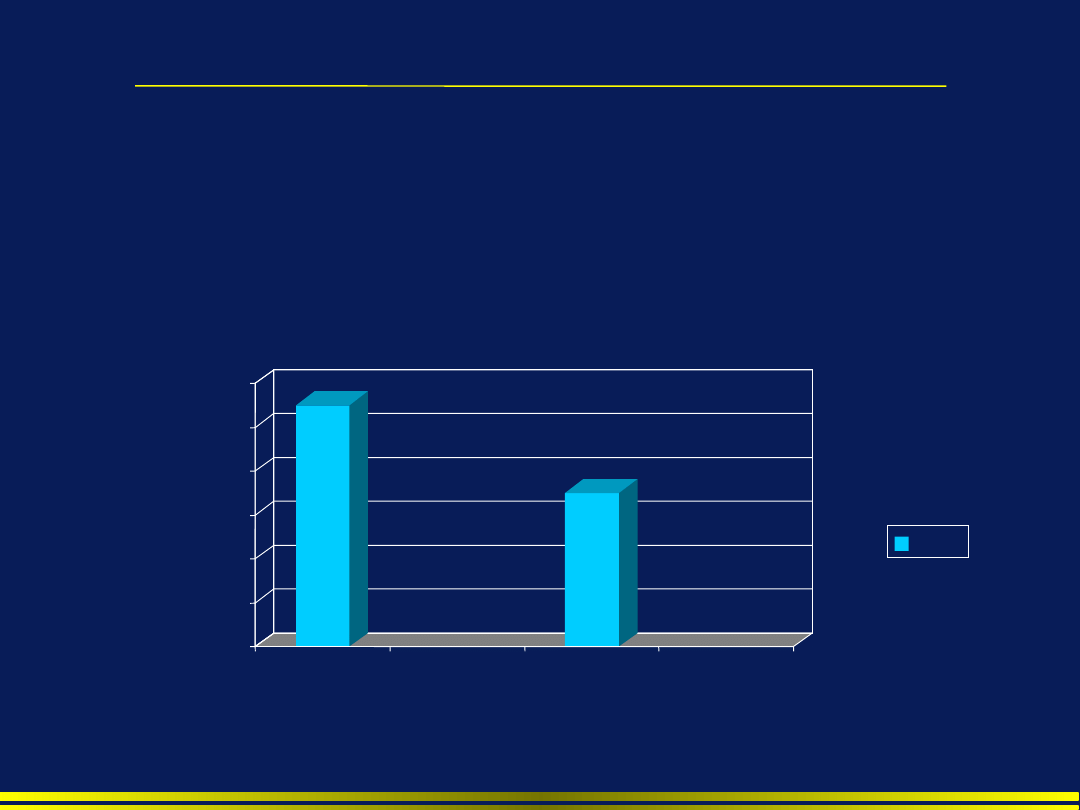
Oporność a czas pobytu w szpitalu
0
2
4
6
8
10
12
grupa badana
grupa
kontrolna
Dni
•
33 przypadki zakażenia
szczepami opornymi
porównano z 66 kontrolnymi
przypadkami zakażenia szczepami wrażliwymi (porównywalne szczepy,
lokalizacja zakażenia, czas rozwoju zakażenia).
•
Chorzy w grupie badanej byli dłużej hospitalizowani po wystąpieniu
zakażenia niż chorzy grupy kontrolnej
(odpowiednio 11 i 7 dni, p=0,01)
Lautenbach E i wsp. Clin Infect Dis 2001;32:1162-1171.
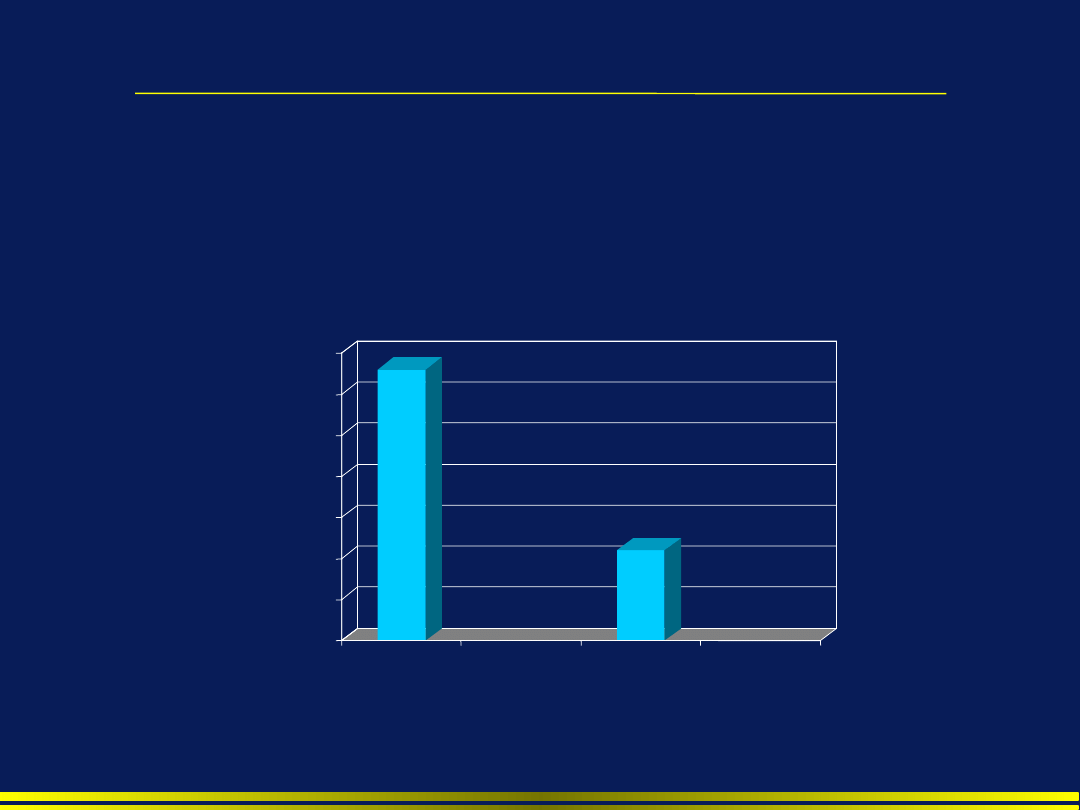
0
10 000 $
20 000 $
30 000 $
40 000 $
50 000 $
60 000 $
70 000 $
Grupa badana
Grupa kontrolna
Średni koszt leczenia chorych z zakażeniem z grupy
badanej był 2,9 razy większy niż w grupie kontrolnej.
*(p<0,001)
Lautenbach E i wsp. Clin Infect Dis 2001; 32: 1162-1171
.
*
Oporność a koszty hospitalizacji

Monitorowanie zakażeń w OIT
Monitorowanie zakażeń w OIT

Monitorowanie zakażeń w OIT
1.
Ciągła kontrola kolonizacji i zakażeń u chorych
leczonych w OIT
2.
Okresowa analiza zbiorcza rodzajów
izolowanych szczepów drobnoustrojów oraz ich
wrażliwości na antybiotyki
3.
Kontrola stanu klinicznego chorych
4.
Kontrola badań laboratoryjnych (leukocytoza,
rozmaz, CRP, prokalcytonina, RTG klp., USG j.
brzusznej itp.)

Monitorowanie zakażeń w OIT
Ad 1.
Ciągła kontrola kolonizacji i zakażeń u
chorych
leczonych w OIT
W dobie przyjęcia:
-
wymaz z gardła i odbytu
-
wydzielina z drzewa oskrzelowego w
przypadku intubacji
-
mocz (przez świeżo założony cewnik) –
najpierw bad. ogólne moczu na obecnośc
zmian zapalnych
-
krew (u chorych gorączkujących lub z
podejrzeniem zapalenia płuc, sepsy)
-
inne (materiał z potencjalnego źródła infekcji-
płyn mózgowo-rdzeniowy, ropa z rany, płyn
opłucnowy itp.)

Monitorowanie zakażeń w OIT
Ad 1.
Ciągła kontrola kolonizacji i zakażeń u
chorych
leczonych w OIT
W trakcie leczenia:
-
1x w tygodniu (z wyjątkiem gardła i
odbytu) materiały z potencjalnych
źródeł zakażenia (oskrzela, mocz,
odleżyny, itp.)
-
w dowolnym momencie, w przypadku
poszukiwania źródła zakażenia (krew,
oskrzela, cewniki naczyniowe, itp.)
Warunek: odpowiednie pobieranie,
przechowywanie i transport próbek do
laboratorium mikrobiologicznego !!!

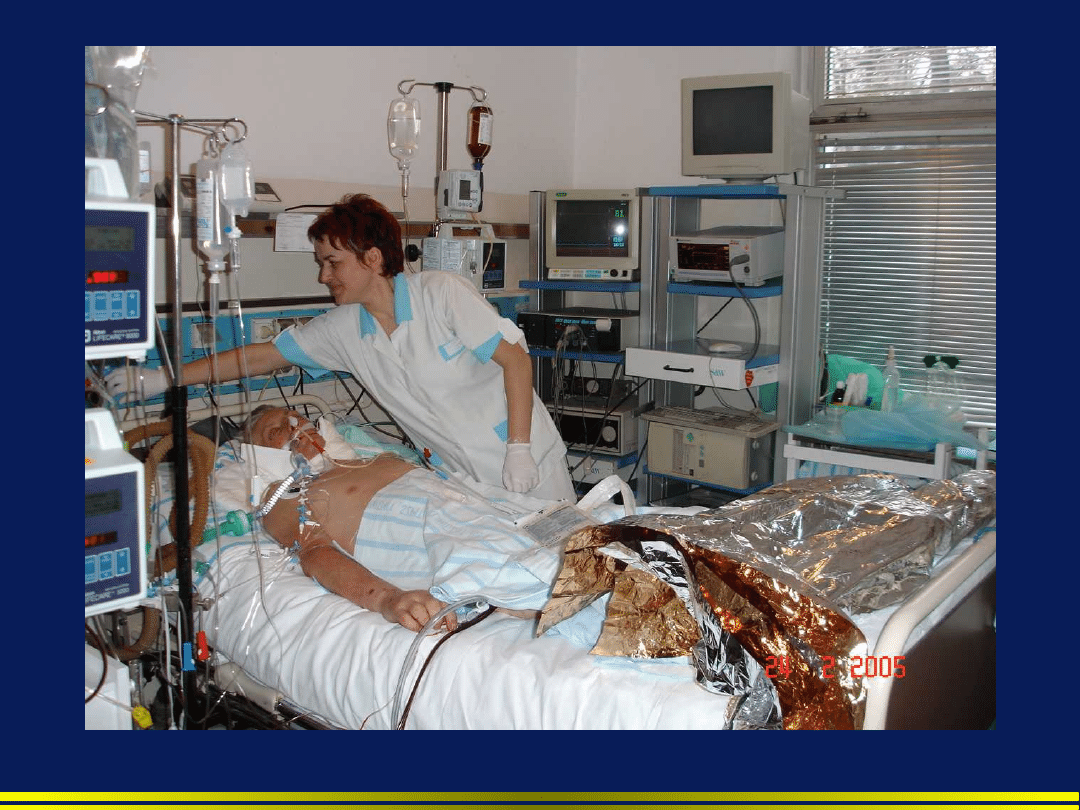
Mini-BAL
Mini-BAL

Korzyści monitorowania zakażeń w OIT
1.
Poprawa jakości empirycznego stosowania
antybiotyków (
antybiotykoterapia de-
eskalacyjna
)
2.
Wczesne wdrażanie antybiotykoterapii
celowanej
3.
Wychwytywanie „alert patogenów”, tzn.
szczepów wieloopornych z ewent.
wprowadzeniem wzmożonego reżimu
sanitarnego np. z izolacją chorych
4.
Restrykcje, rotacje w stosowaniu antybiotyków
5.
Możliwość rejestracji zakażeń szpitalnych
6.
Analiza dróg szerzenia się zakażeń, szczególnie
wieloopornymi szczepami pałeczek Gram-
ujemnych, MRSA, MRSE, VRE, ESBL
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
Wyszukiwarka
Podobne podstrony:
Przestrzenie międzypowięziowe głowy i szyi jako drogi szerzenia się stanów zapalnych
Metody zapobiegania szerzeniu sie zakazen w gabinecie kosmetycznym(1), COSINUS, PRACOWNIA KOSMETYCZN
10 Zakażenia szpitalne Rodzaje, drogi i zapobieganie zakażeniom szpitalnym
Podaj źródła i drogi przenoszenia zakażeń szpitalnych, Mikrobiologia
Monitorowanie zakażeń szpitalnych na oddziale OIT
Definicja zakażenia szpitalnego
Zakażenia szpitalne, Mikrobiologia
WYKŁAD 8- c.d.7 i Zakażenia szpitalne, GUMed, Medycyna, Mikrobiologia, Mikrobiologia, III KOLOKWIUM
zapobieganie zakażeniom szpitalnym, opieka nad os starsza
10 Zakażenia szpitalne. Rodzaje, opiekun medyczny
8 Zakażenia szpitalne TSM
10 Zakażenia szpitalne. Rodzaje, Opiekun Medyczny(1)
Zakażenia szpitalne, dokumenty, szkoła ola
CP5 Zakażenia szpitalne, Medycyna Ratunkowa - Ratownictwo Medyczne
Kontrola zakażeń szpitalnych w oddziałach pediatrycznych, pielęgniarstwo
wzw c - 2, mikrobiologia+ zakażenia szpitalne
Mikrobiologia sciaga pomniejszona, mikrobiologia+ zakażenia szpitalne
więcej podobnych podstron