Reguła Hunda
Stan o najniższej energii to stan o maksymalnej liczbie niesmarowanych elektronów na danej podpowłoce.

dobrze żle
Dopiero po obsadzeniu wszystkich orbitali danej podpowłoki pojedynczo przez elektrony, tworzą się pary elektronów o przeciwnych spinach
![]()
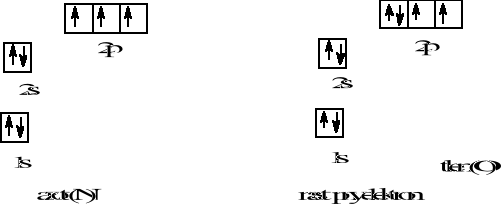
Elektrony niesparowane w orbitalach określonej podpowłoki maja jednakową orientacje spinu
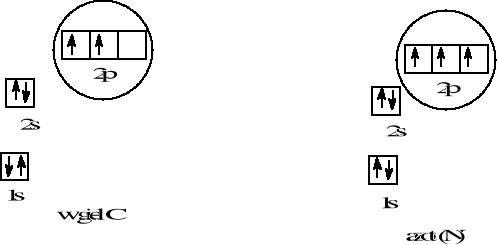
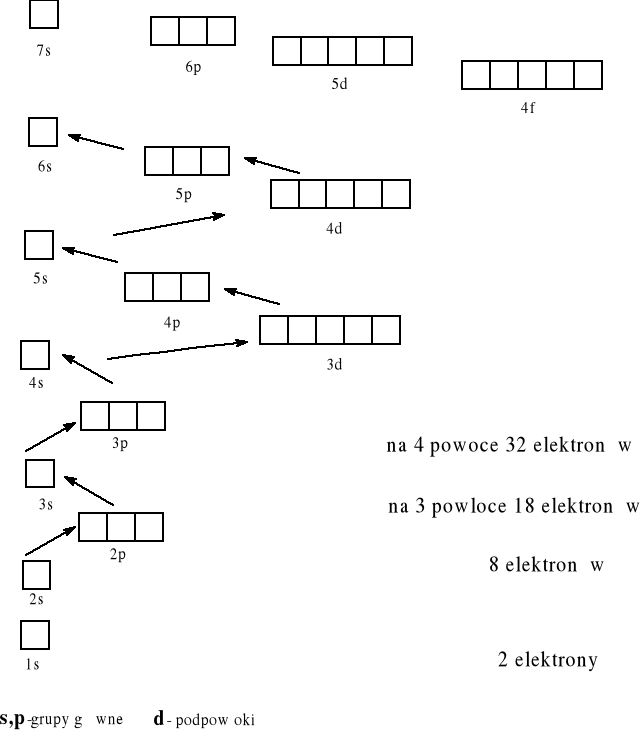
He 1s2, 1 2 3 -okres x5 elektrony na podpowłoce
Be 1s22s2
P 1s2 2s2 2p63s23p3 15 elektronów
V 1s2 2s2 2p6 3s2 3p6 4s2 3d3 23 elektrony
Ga 1s2 2s2 2p6 3s2 3p6 3d10 4s24p1 31 elektronów
Zr 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 5s2 4d2 40 elektrony
Ce 1s2 2s2 2p6 3s2 3d6 3p10 4s24p6 5s2 4d105d6 6s2 4f2 - 58 elektronów
Są niestety wyjątki w kolejności zapełniania powłok np. Cr (24) 3d5 4s1,
Cu (29) 3s2 3d63p104s1
Jaka jest struktura elektronowa kationów metali metali?
Sód atom Sód kation Na+
1s2 2s2 2p6 3s1 1s2 2s2 2p6
Rubid atom
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s1
Rubid kation Rb+
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6
Wapń atom Wapń kation Ca2+
1s2 2s2 2p6 3s2 3p6 4s2 1s2 2s2 2p6 3s2 3p6
Glin atom glin kation Al3+
1s2 2s2 2p6 3s2 3p1 1s2 2s2 2p6
Gal atom gal kation Ga3+
1s2 2s2 2p6 3s2 3p6 4s2 3d10 5p1 1s2 2s2 2p6 3s2 3p6 3d10
Analogicznie struktura anionów
Chlor Chlor anion Cl-
1s2 2s2 2p6 3s2 3p5 1s2 2s2 2p6 3s2 3p6
Selen atom Selen anion Se2-
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p4 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6
Chlor atom
1s2 2s2 2p6 3s2 3p5
Chlor + (NaClO)
1s2 2s2 2p6 3s23p4
Chlor Cl3+ (KClO2)
1s2 2s2 2p6 3s2 3p2
Chlor Cl5+ (KClO3)
1s2 2s2 2p6 3s2
Chlor 7+ (KClO4)
1s2 2s2 2p6
Wyszukiwarka
Podobne podstrony:
heisenberg, Studja, Chemia Nieorganiczna, Wykłady, Wykłady pozostałe
Redox, Studja, Chemia Nieorganiczna, Wykłady, Wykłady pozostałe
skala Paulinga, Studja, Chemia Nieorganiczna, Wykłady, Wykłady pozostałe
OSMOZA, Studja, Chemia Nieorganiczna, Wykłady, Wykłady pozostałe
wiązania, Studja, Chemia Nieorganiczna, Wykłady, Wykłady pozostałe
Równanie Schroedingera, Studja, Chemia Nieorganiczna, Wykłady, Wykłady pozostałe
teoriac, Studja, Chemia Nieorganiczna, Wykłady, Wykłady pozostałe
ZWIĄZKI KOMPLEKSOWE, Studja, Chemia Nieorganiczna, Wykłady, Wykłady pozostałe
terzykZestaw B, I semestr, Chemia, nieorganiczna, wyklad
chemia nieorganiczna wykłady cz II
chemia nieorganiczna wykłady cz 1
Pierwiastki o liczbach atomowych 104-111, WAT chemia zaocznie, chemia nieorganiczna wyklady
Chemia- pytania na egzamin, ROK 1 Technologia żywności Kraków UR, CHEMIA NIEORGANICZNA, Wyklady, Che
chemia nieorganiczna wykład, Górnictwo i Geologia AGH, chemia
Wodor, WAT chemia zaocznie, chemia nieorganiczna wyklady
terzykZestaw A, I semestr, Chemia, nieorganiczna, wyklad
9. Przegląd podstawowych klas związków pierwiastków bloków d i f, pwr biotechnologia(I stopień), II
4. Budowa ciala stałego, pwr biotechnologia(I stopień), II semestr, Chemia nieorganiczna, Wykłady Ap
więcej podobnych podstron