
1
P
otencjał
S
poczynkowy
Po obu stronach błony komórkowej istnieje różnica potencjałów (napię-
cie) tzw.
potencjał błonowy.
Jego wartość odgrywa ważną rolę w pro-
cesach transportu błonowego (np. w kanałach nerkowych), przy
prze-
twarzaniu informacji w neuronach, komórkach receptorowych oraz w
procesach skurczu komórek mięśniowych.
Poniżej pokazano schemat układu do rejestracji potencjałów błonowych.
Budowa elektrody pomiarowej oraz schemat układu do pomiaru poten-
cjałów błonowych ΔV = V
wew
− V
zew
, czyli różnicy potencjałów pomię-
dzy wnętrzem V
wew
i zewnętrzem V
zew
komórki.
szklana elektroda
kapilarna
roztwór KCl
drut srebrny pokryty
chlorkiem srebra
średnica
około 1 µm
ΔV
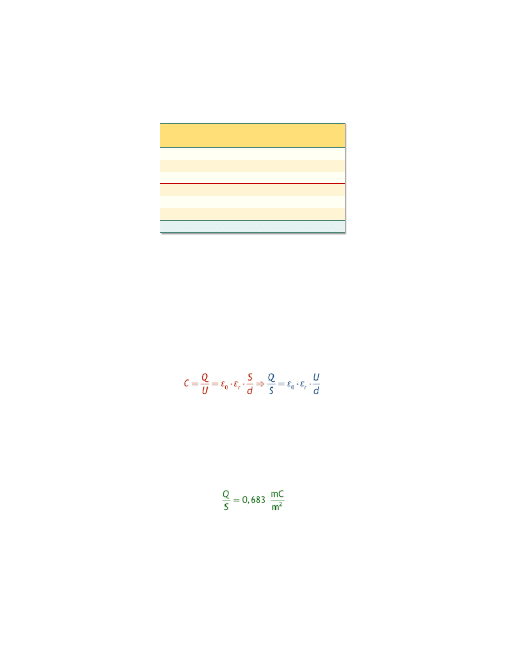
2
W tabeli zebrano wartości stężeń wybranych jonów
c
W
wewnątrz
i c
Z
na
zewnątrz komórek mięśniowych zwierząt stałocieplnych.
Wnętrze komórki i środowisko zewnętrzne są
elektrycznie skompenso-
wane (obojętne elektrycznie).
Lokalny brak kompensacji występuje
jedynie na powierzchni błony komórkowej.
Rodzaj
jonów
c
W
[mmol/l]
c
Z
[mmol/l]
c
Z
/c
W
Na
+
12
145
12:1
K
+
155
4
1:39
Inne kationy
0
5
Cl
−
4
120
32:1
B
−
155
−
Inne aniony
8
34
1:4
Zmierzony potencjał spoczynkowy: −90 mV
Z definicji pojemności elektrycznej C:
(
Q – ładunek, U – napięcie, S – powierzchnia, d – grubość, ε
r
iε
0
oznaczają odpo-
wiednio względną przenikalność elektryczną i przenikalność elektryczną próżni
)
można wyznaczyć powierzchniową gęstość ładunku.
Do obliczeń przyjmujemy następujące wartości:
potencjał spoczynkowy U = −90 mV,
grubość błony d = 7 nm
względna przenikalność elektryczna błony
ε
r
=
6.
W wyniku obliczeń otrzymujemy:
Zatem na powierzchni 1 μm
2
błony komórkowej występuje nadmiar około
4269
jonów jednowartościowych jednego znaku, odpowiednio ujemnych
po wewnętrznej stronie błony i dodatnich po zewnętrznej.
A ile i jakich jonów jest w
1 μm
3
cytoplazmy i płynu śródkomórko-
wego?

3
Rodzaj jonów
c
W
[mmol/l]
c
Z
[mmol/l]
c
Z
/c
W
N
W
[10
6
/μm
3
]
N
Z
[10
6
/μm
3
]
Na
+
12
145
12:1
7,2
87,3
K
+
155
4
1:39
93,3
2,4
Inne kationy
0
5
0,0
3,0
Cl
−
4
120
32:1
2,4
72,2
B
−
155
−
93,3
0,0
Inne aniony
8
34
1:4
4,8
20,5
Zmierzony potencjał spoczynkowy: −90 mV
Z definicji stężenia molowego c
m
:
gdzie n – liczba moli ładunek, V – objętość, N
A
– liczba Avogadro, N – liczba cząste-
czek.
Korzystając z przedstawionych wyżej danych wartości stężeń poszczegól-
nych jonów, można obliczyć przeciętną liczbę jonów odpowiednio
wew-
nątrz komórki N
W
i na zewnątrz N
Z
. Wyniki obliczeń zestawiono w tabeli.
R
ozkład jonów
K
+
a potencjał spoczynkowy
Jony
K
+
mogą dosyć swobodnie przechodzić przez błonę:
P
K+
:
P
Cl−
:
P
Na+
=
1 :
0,4 :
0,04
gdzie P − przepuszczalność błony dla odpowiednich jonów w stanie spoczynku.
Ponadto ich stężenie wewnątrz
[K
+
]
W
komórki jest większe niż na ze-
wnątrz
[K
+
]
Z
:
Pod wpływem różnicy stężeń (potencjałów chemicznych) jonów
K
+
na-
stępuje
ich wypływ
z komórki. Konsekwencją wypływu jest ładowanie
środowiska zewnętrznego ładunkiem dodatnim, co jest
przyczyną ko-
lejnego bodźca
− różnicy potencjałów elektrycznych − wywołującej
wsteczny przepływ K
+
.
Wypływający z komórki strumień K
+
stopniowo maleje (maleje różnica
stężeń) z kolei strumień K
+
wpływający
do komórki stopniowo
narasta
(rośnie różnica potencjałów). Po pewnym czasie strumienie K
+
wypły-
wający z komórki i wpływający do niej stają się równe.
4
Od tego momentu wartość różnicy potencjałów nie ulega już dalszej
zmianie. Tę różnicę potencjałów nazywamy
potencjałem równo-
wagi
dla jonów potasowych.
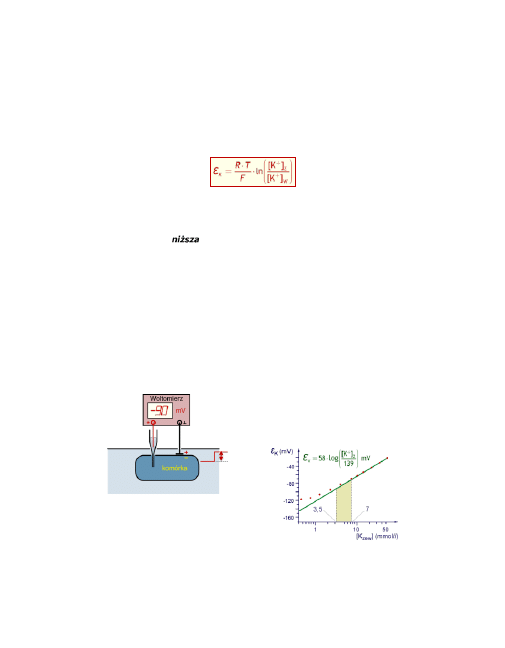
Wyraża się on wzorem Nernsta:
Dla koncentracji jonów takiej jak w komórce mięśniowej ssaków
1:39
potasowy potencjał równowagowy wynosi:
ε
K
= –
96 mV
Jest to wartość
niższa
od tej rejestrowanej jako bonowy potencjał spo-
czynkowy w tych komórkach.
Eksperymentalnie wykazano, że stężenie jonów K
+
na zewnątrz komór-
ki wpływa na wartość potencjału spoczynkowego (błonowego).
Doświadczenie Adriana:
Zależność potencjału błonowego od zewnątrz-
komórkowej koncentracji potasu.
Linia ciągła pokazuje zależność potencjału ró-
wnowagowego wyliczoną z wzoru Nernsta.
Mięsień krawiecki żaby [Adrian R.H., 1956].
Małe zmiany koncentracji potasu w płynie
międzykomórkowym zmieniają w istotny
sposób błonowy potencjał spoczynkowy, a
zatem i funkcjonowanie komórek.
Dla dużych stężeń [K
+
]
zew,
potasowy potencjał równowagowy dobrze opisuje war-
tość potencjału spoczynkowego.
Dla stężeń fizjologicznych K
+
(3,5
7 mmol/l) rejestrowany potencjał błonowy
jest mniej ujemny
niż to wynika z wzoru Nernsta.
ΔV
płyn fizjologiczny, w którym zmieniano
stężenie jonów potasowych
5
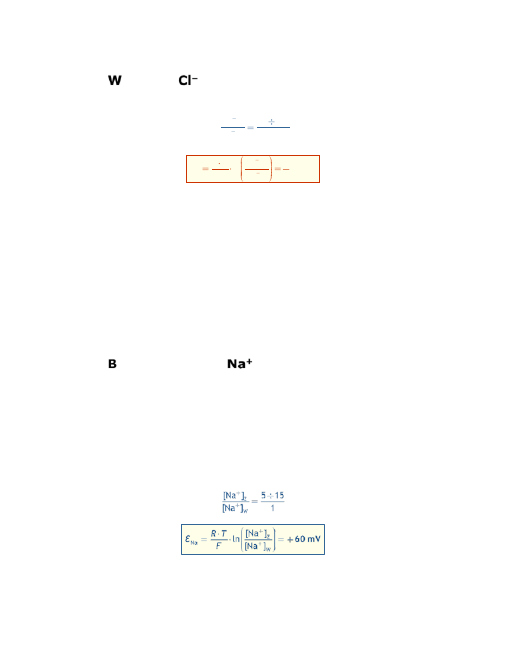
Z
W
[Cl ]
20 100
[Cl ]
1
W
Cl
Z
[Cl ]
ln
[Cl ]
R T
F
ε
90 mV
W
kład jonów
Cl
−
do potencjału spoczynkowego
Jony Cl
−
mogą dosyć swobodnie przechodzić przez błonę w stanie spo-
czynku. Ponadto stężenie jonów Cl
−
wewnątrz komórki jest mniejsze
niż na zewnątrz:
Potencjał równowagowy dla jonów chloru przyjmuje wartość:
Jest to wartość równa tej rejestrowanej, jako potencjał spoczynkowy
w tych komórkach.
Rozkład
Cl
−
ustala się w zależności od stężenia
K
+
(równowaga Donnana). Kon-
centracja
K
+
w komórce nie może zmieniać się w szerokich granicach − gdyż
jony te kompensują ujemny ładunek anionów białkowych. Stężenie
K
+
wew-
nątrz komórki nie może być regulowane przez potencjał spoczynkowy. Ale
koncentracja
Cl
−
tak. Można więc powiedzieć, że podstawową przyczyną uje-
mnego potencjału wnętrza komórki jest zawartość anionów białkowych. W ko-
mórkach, których błony mają zbliżoną przepuszczalność dla
K
+
i
Cl
−
właśnie te
jony w podobnym stopniu biorą udział w utworzeniu potencjału spoczynkowe-
go.
B
ierny transport jonów
Na
+
Potasowy potencjał równowagowy jest bardziej ujemny niż obserwowa-
ny potencjał spoczynkowy. Różnica ta wywołana jest biernym napływem
Na
+
do wnętrza komórki. Jony sodu napływają do wnętrza komórki mi-
mo małej dla nich przepuszczalności błony w stanie spoczynku.
Napływowi
Na
+
do wnętrza komórki sprzyja zarówno gradient ich stę-
żenia, jak i różnica potencjałów elektrycznych w błonie.
Jeśli w doświadczeniu Adriana w płynie fizjologicznym zastąpić jony Na
+
inny-
mi
większymi jonami dodatnimi (cholina), to potencjał błonowy przyjmie war-
tość równowagowego potencjału potasowego, nawet przy niskich stężeniach
potasu na zewnątrz komórki.
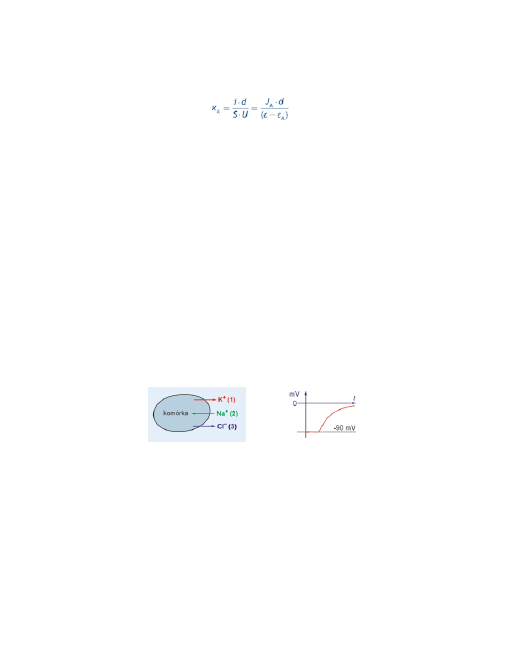
Stężenie jonów
Na
+
wewnątrz komórki jest mniejsze niż na zewnątrz:
Potencjał równowagowy dla jonów sodu przyjmuje wartość:
Jest to wartość przeciwna do tej rejestrowanej jako potencjał spo−
czynkowy w tych komórkach.
6
Przewodność elektryczną
κ
A
błony dla jonów A można obliczyć z wzoru:
gdzie: J
A
= i/S całkowita gęstość prądu jonów A,
d − grubość błony,
U = ε − ε
A
napięcie powodujące przepływ jonów = różnicy potencjału
spoczynkowego i potencjału równowagowego dla tych jonów.
Stąd:
J
Na
=
κ
Na
∙(−90 − 60)/d = −150∙κ
Na
/d
jeśli założyć, że
κ
K
:κ
Na
=
25:1,
jak to wynika z przepuszczalności błony
dla jonów sodowych i potasowych, to w stanie stacjonarnym, gdy:
J
Na
= −J
K
(wtedy potencjał spoczynkowy będzie stały) znajdziemy:
−150∙ κ
Na
= −(ε − ε
K
)∙ κ
K
(ε − ε
K
) = 150/25 = 6 mV
Przyczyną większej wartości potencjału błonowego w porównaniu z warto-
ścią równowagowego potencjału potasowego, jest
niewielka
przepuszczal-
ność błony dla jonów sodowych, jest niewielki ich prąd dokomórkowy.
Istnienie ciągłego napływu sodu do wnętrza komórki oraz wypływu
potasu prowadzi jednak do niestabilności takiego układu.
Rośnie ciśnienie osmotyczne
wewnątrz komórki. Wywołuje to
napływ
wody do wnętrza
, co powoduje kolejny spadek stężenia jonów potaso-
wych. W końcu prowadzi to do
pękania
(lizy) komórki.
Procesy takie nie zachodzą w normalnych (fizjologicznych)
warunkach. Jednak w skrajnej
anoksii
i/lub przy
skrajnych niedostat-
kach energetycznych
taki scenariusz będzie miał miejsce.
Wskazuje to, że komórka nie znajduje się w stanie równowagi, a stę-
żenie jonów sodowych dalekie jest od stanu równowagi. Istniejący w
komórce i otoczeniu rozkład stężeń jonów sodowych i potasowych jest
wynikiem transportu: biernego, biernego ułatwionego oraz aktywne-
go.

7
T
ransport aktywny
Transportem aktywnym danej substancji nazywamy transport zachodzą-
cy w kierunku przeciwnym niż ich bierny, samoistny przepływ,
wyma-
ga zatem nakładu energii.
Zachodzi on z udziałem wyspecjalizowanych
struktur błonowych (białek integralnych) sprzęgających transport z pro-
cesem uwalniania energii.
Źródłem energii często jest hydroliza ATP i dlatego białka biorące u-
dział w tym procesie traktowane są jako enzymy posiadające własno-
ści ATPazy.
Transport aktywny odbywa się wbrew różnicy stężeń danej substancji
(w stronę większego stężenia) stąd białka biorące udział w tym tran-
sporcie często nazywane są
„pompami”.
Dobrze poznanym przykładem jest pompa sodowo−potasowa (Na
+
/K
+
ATPaza).
Transportuje ona Na
+
z wnętrza komórki na zewnątrz, jednocześnie przeno-
sząc K
+
w kierunku przeciwnym (antyport). Hydroliza jednej cząsteczki ATP
dostarcza energii koniecznej do transportu trzech Na
+
i dwóch K
+
. Działanie
pompy sodowo−potasowej ma olbrzymie znaczenie dla utrzymania stałości
stężeń tych jonów, zwłaszcza w komórkach pobudliwych. Bierny transport jo-
nów zachodzący zarówno podczas spoczynku komórki, jak i w czasie trwania
potencjału czynnościowego po pewnym czasie prowadziłby do wyrównania
stężeń jonów sodu i potasu wewnątrz i na zewnątrz komórki.
Na
+
/K
+
ATPaza ma podstawowe znaczenie dla funkcjonowania wszys-
tkich żywych komórek, utrzymując stałą wartość potencjału błono-
wego i objętość komórki. Za badania nad tą cząsteczką Jens C. Skou
otrzymał nagrodę Nobla z 1997 r.
Pompa sodowo−potasowa składa się z dwóch podjednostek:
α
(112 kDa)
i
β
(35 kDa).
Miejsce wiązania ATP znajduje się na podjednostce α.
Na
tej podjednostce, na powierzchni skierowanej do płynu śródkomórkowego, z-
najdują się również miejsca wiązania steroidów kardiotonicznych (np.: digit-
oksygenina), które hamują aktywność pompy przez blokowanie defosforylacji.
Hydroliza ATP jest źródłem energii dla tego enzymu, koniecznej do
pompowania jonów sodu i potasu.
ATPaza jest
fosforylowana
przez ATP w obecności jonów
Na
+
i
Mg
+
2
.
Do podje-
dnostki
α
, która jest związana z ATP wiązane są trzy jony sodu. Następnie ATP
ulega
hydrolizie,
a uwolniona energia prowadzi do zmiany konformacji białka,
co pozwala na przetransportowanie jonów sodu na zewnątrz komórki, gdzie
jony
Na
+
zostają uwolnione z kompleksu. Następuje teraz związanie dwóch jo-
nów potasu
K
+
,
a następnie
defosforylacja
− wywołująca ponowną zmianę
konformacji, pozwalającą na przeniesienie jonów potasu do wnętrza komórki.
Tu uwolnienie jonów następuje po przyłączeniu cząsteczki ATP.

8
Jens Christian
Skou
(ur. 8. X. 1918 r. w Lemvig) − duński chemik. Laureat na-
grody Nobla w dziedzinie chemii w 1997 roku za odkrycie enzymu, pompy sodo-
wo-potasowej (Na
+
/K
+
ATP-azy).
W 1944 roku ukończył studia medyczne na Uniwersytecie Kopenhaskim, w 1947 r.
rozpoczął pracę na Uniwersytecie w Aarhus, a w 1954 r. obronił doktorat.
Obecnie jest tam profesorem emerytowanym.
Nagrodę Nobla razem z nim otrzymali Paul D. Boyer i John E. Walker (za ATP).
Schemat działania pompy jonowej
. Gęstość rozmieszczenia pomp w błonie
neuronu: 100÷200 pomp na 1 μm
2
. Neuron posiada ich około 1 miliona.
Stan zdefosforylowany pompy. Centra wiążące Na
+
eksponowane są do
wnętrza komórki. Następuje przyłączenie 3 kationów Na
+
.
Duże stężenie
Na
+
Duże stężenie
K
+

9
Przyłączenie jonów Na
+
zmienia konformację enzymu umożliwiając
przyłączenie ATP.
Schemat działania pompy jonowej
. Gęstość rozmieszczenia pomp w błonie
neuronu: 100÷200 pomp na 1 μm
2
. Neuron posiada ich około 1 miliona.
Duże stężenie
Na
+
Duże stężenie
K
+
Przyłączenie ATP.
Schemat działania pompy jonowej
. Gęstość rozmieszczenia pomp w błonie
neuronu: 100÷200 pomp na 1 μm
2
. Neuron posiada ich około 1 miliona.
Duże stężenie
Na
+
Duże stężenie
K
+

10
Fosforylacja wywołuje przemieszczenie centrów wiążących Na
+
na zew-
nętrzną stronę błony.
Schemat działania pompy jonowej
. Gęstość rozmieszczenia pomp w błonie
neuronu: 100÷200 pomp na 1 μm
2
. Neuron posiada ich około 1 miliona.
Duże stężenie
Na
+
Duże stężenie
K
+
Odłączenie 3 jonów Na
+
po zewnętrznej stronie błony zwiększa podat-
ność centrów wiążących K
+
.
Schemat działania pompy jonowej
. Gęstość rozmieszczenia pomp w błonie
neuronu: 100÷200 pomp na 1 μm
2
. Neuron posiada ich około 1 miliona.
Duże stężenie
Na
+
Duże stężenie
K
+

11
Przyłączenie K
+
wywołuje defosforylację enzymu i powrót do wyjścio-
wej konformacji.
Schemat działania pompy jonowej
. Gęstość rozmieszczenia pomp w błonie
neuronu: 100÷200 pomp na 1 μm
2
. Neuron posiada ich około 1 miliona.
Duże stężenie
Na
+
Duże stężenie
K
+
Towarzyszy temu przeniesienie 2 jonów K
+
do wnętrza komórki oraz
zmiana powinowactwa centrów wiążących K
+
i Na
+
.
Schemat działania pompy jonowej
. Gęstość rozmieszczenia pomp w błonie
neuronu: 100÷200 pomp na 1 μm
2
. Neuron posiada ich około 1 miliona.
Duże stężenie
Na
+
Duże stężenie
K
+

12
Następuje uwolnienie K
+
i możliwym staje się ponowne związanie Na
+
.
W ten sposób pompa, kosztem energii uwolnionej w wyniku rozpadu ATP,
przeniosła trzy jony sody z wnętrza komórki do płynu śródkomórkowe-
go i dwa jony potasu w kierunku przeciwnym. W obu wypadkach trans-
port odbywał się w kierunku większych stężeń odpowiednich jonów.
Schemat działania pompy jonowej
. Gęstość rozmieszczenia pomp w błonie
neuronu: 100÷200 pomp na 1 μm
2
. Neuron posiada ich około 1 miliona.
Duże stężenie
Na
+
Duże stężenie
K
+
Fosforylacja zależna od Na
+
i defosforylacja zależna od K
+
są krytyczny-
mi reakcjami enzymu.
Cykl enzymatyczny trwa
ok.
10 ms. Pojedyncza ATPaza kosztem hydro-
lizy jednej cząsteczki ATP transportuje, przy maksymalnej prędkości
100 obrotów na s, w ciągu sekundy 300 Na
+
i 200 K
+
.
Gradient sodowo−potasowy utrzymywany dzięki enzymatycznej a-
ktywności Na
+
/K
+
−ATPazy:
kontroluje objętość komórki,
jest niezbędny dla pobudzenia nerwów i mięśni,
jest siłą napędową transportu aktywnego cukrów oraz
aminokwasów.
Działanie pompy wymaga:
stałego dopływu glukozy i tlenu,
stałej resyntezy ATP,
zachowania temperatura ok. 37ºC,
odprowadzania CO
2
,
odpowiedniego stężenia jonów Mg²
+
,
odpowiedniego stężenia jonów Na
+
i K
+
.
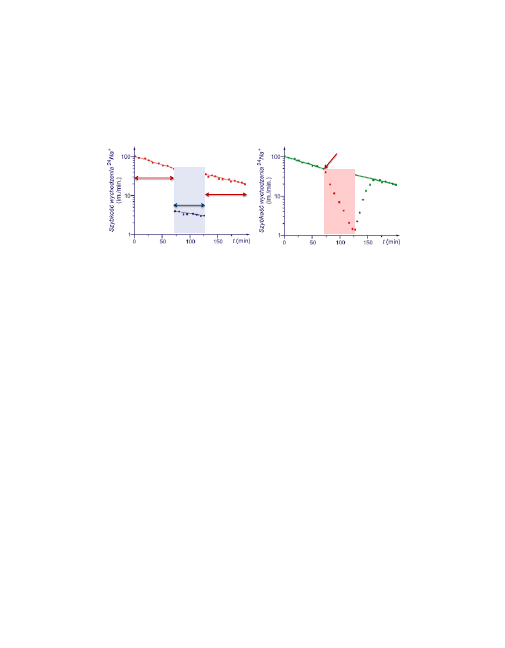
13
Aktywny transport znakowanego sodu z wnętrza komórki.
Doświadczenie A.L. Hodgkina dowodzi, że obniżenie szybkości resyn-
tezy
ATP hamuje transportu Na
+
(można podejrzewać, że i K
+
).
W doświadczeniu tym do wnętrza komórki (neuronu) wprowadzono radio-
aktywny izotop
24
Na
+
. Następnie badano aktywność płynu fizjologiczne-
go, w którym umieszczono badany neuron. Wyniki ilustrują rysunki.
Obniżenie szybkości transportu ak-
tywnego w wyniku szybkiego obni-
żenia temperatury.
Obniżenie szybkości transportu ak-
tywnego w wyniku zatrucia chemi-
cznego, blokującego przemiany e-
nergetyczne w komórce.
18,3ºC
18,3ºC
0,5ºC
Zatrucie 0,2 mmol/l
dinitrofenolem
Zatrzymanie pompy prowadzi do:
zmian w składzie płynu wewnątrzkomórkowego,
zmian w składzie płynu zewnątrzkomórkowego, w którym
stężenie Na
+
zmniejsza się i zwiększa stężenie K
+
,
utraty przez komórki pewnych właściwych,
braku reakcji komórek pobudliwych na bodźce, prowadzi do ich
niepobudliwości.
W przypadku pompy Na−K występuje bezpośrednie sprzężenie trans-
portu z procesem uwalniania energii − hydrolizą ATP − i dlatego trans-
port ten nazywamy
„aktywnym pierwotnym”.
Jeśli pomiędzy procesem uwalniania energii a transportem
istnieją mechanizmy pośredniczące, to taki transport nazywamy
akty-
wnym wtórnym.
Przykładem transportu wtórnego jest proces resorpcji
glukozy w jelitach − gdzie aktywnie transportowana pierwsza substan-
cja np. Na
+
tworzy gradient potencjału elektrochemicznego, który wa-
runkuje transport innej substancji, np. cukru, aminokwasu, zgodny z
jej gradientem stężenia.
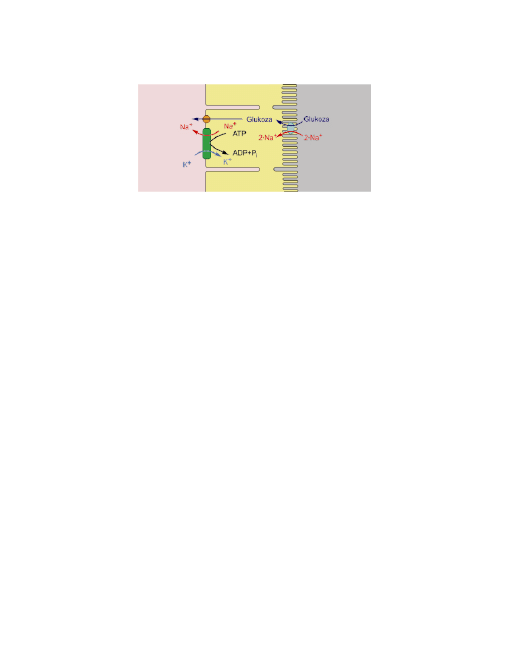
14
Proces resorpcji glukozy w jelitach.
Aktywny transport Na
+
(z komórek nabłonka do osocza) obniża jego stę-
żenie w komórkach nabłonka jelit; zwiększa się gradient stężenia sodu
pomiędzy światłem jelita a komórkami nabłonka. Wspomniany gradient
stężenia Na
+
warunkuje transport glukozy z jelit do komórek nabłonka
zgodnie z gradientem stężenia glukozy. Odbywa się on na drodze sym-
portu jednoczesnego transportu sodu i glukozy. Następnie, znów zgod-
nie z gradientem stężenia, glukoza przenoszona jest z komórek nabłon-
ka do osocza za pomocą przenośnika
Glut 2
(akronim
glu
cose
t
ranspor-
ters).
Krew:
Dużo Na
+
Mało K
+
Światło jelita:
Pożywienie
Dużo glukozy
Dużo Na
+
Komórki nabłonka:
Mało Na
+
Dużo K
+
Na
+
/K
+
ATPaza
Na
+
/Glukoza
symport
Glut 2
Przykłady transportu aktywnego:
Transport jonów H
+
do soków żołądkowych ([H
+
]=1 mol/l) z komó-
rek nabłonkowych ściany żołądka ([H
+
] = 10
−7
mol/l),
Transport jonów sodowych i potasowych w komórkach nerwowych
i mięśniowych dla potrzymania potencjału spoczynkowego (pompa
jonowa),
Transport jonów wapniowych w komórkach mięśniowych,
Aktywny transport sodu w kanalikach nerkowych.
Praca transportu aktywnego jest duża, np. w stanie spoczynku komórka mięśniowa
zużywa około 20% energii metabolizmu na podtrzymanie transportu aktywnego.
Pompy mogą być
nieelektrogenne
(przenoszą tyle samo jonów sodu i potasu w je-
dnym cyklu). Istnieją też pompy elektrogenne (na przykład w komórkach nerwo-
wych, mięśniowych, komórkach mięśnia sercowego) przenoszące 3 jony sodu oraz
dwa jony potasu kosztem hydrolizy jednej cząstki ATP.
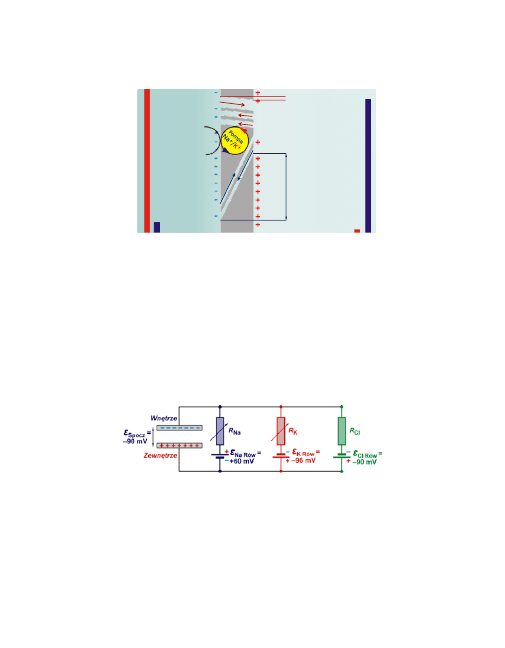
15
Przepływy jonów K
+
i Na
+
w błonie w stanie spoczynku.
A jak wyglądają przepływ Cl
−
?
K
+
Na
+
K
+
Cytoplazma
Środowisko
zewnętrzne
Błona
K
+
(stężenie)
Hydroliza
ATP
Na
+
(aktywnie)
K
+
6 mV
K
+
(potencjał elektryczny)
Na
+
(stężenie i potencjał
elektryczny)
K
+
(aktywnie)
Na
+
Na
+
150
mV
A.L. Hodgkin i A.F. Huxley
zaproponowali następujący elektrycz-
ny model dla opisu transportu jonów przez błonę komórkową.
Błona (kondensator) jest ładowana przez trzy baterie „sodową”, „po-
tasową” i „chlorkową”.
Każda z nich ładuje błonę poprzez opór o odpowiednio dobranej war-
tości, zależnej od przepuszczalności błony dla odpowiednich jonów.
W warunkach spoczynku:
R
K+
:
R
Cl−
:
R
Na+
=
1 :
2,5 :
25
Wyszukiwarka
Podobne podstrony:
potencjal spoczynkowy i jego pochodzenie
Potencjał spoczynkowy i czynności w tkankach, Biologia, Fizjologia zwierząt
Potencjal spoczynkowy
4 Potencjał spoczynkowy
Potencjał spoczynkowy i czynnościowy nerwu, rejestracja skurczów mięśni szkieletowych po pobudzeniu
Prezentacja SGH 16122010 OPT [ www potrzebujegotowki pl ]
Potencjał spoczynkowy, Biologiczne podstawy zachowania
potencjal spoczynkowy i jego pochodzenie
Potencjał spoczynkowy
Potencjał spoczynkowy 4
Potencjal Czynnosciowy WWW
potencjał spoczynkowy
73 Polaryzacja blony komorkowej potencjal spoczynkowy
potencjal spoczynkowy i jego pochodzenie
Potencjał spoczynkowy i czynności w tkankach, Biologia, Fizjologia zwierząt
więcej podobnych podstron