
SPOIWA POWIETRZNE
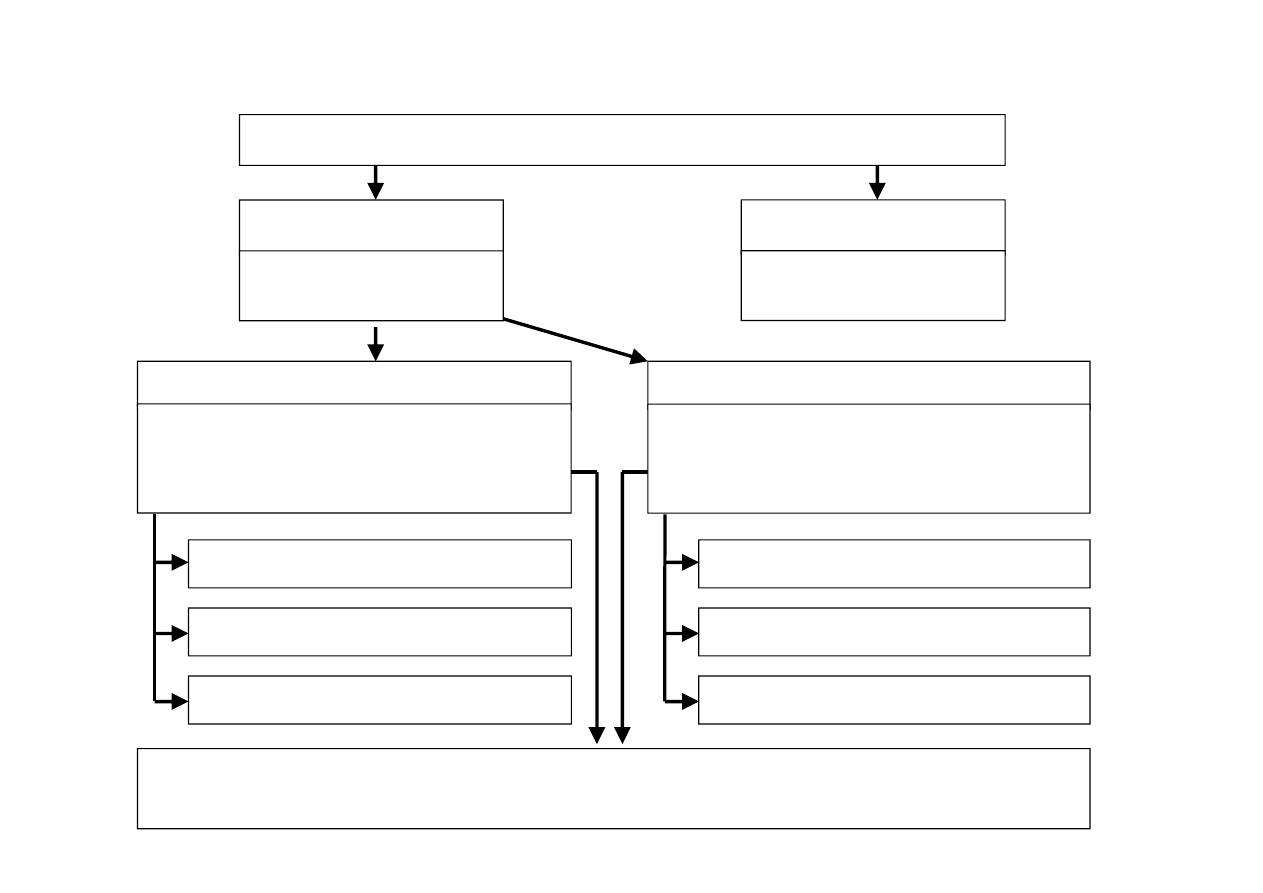
PODZIAŁ MATERIAŁÓW WIĄŻĄCYCH
MATERIAŁY WIĄŻĄCE
SPOIWA
LEPISZCZA
wiązanie przez
reakcję chemiczną
wiązanie przez
proces fizyczny
SPOIWA POWIETRZNE
wiążą tylko przy dostępie
powietrza, po związaniu nie są
odporne na wodę
SPOIWA HYDRAULICZNE
wiążą przy dostępie powietrza lub
pod wodą, po związaniu są
odporne na wodę
WAPNO
GIPS I ANHYDRYT
SPOIWA KRZEMIANOWE
CEMENT PORTLANDZKI
WAPNO HYDRAULICZNE
INNE CEMENTY
SPOIWA ŻYWICZNE:
zwykle nie wiążą pod wodą, ale po związaniu są odporne na wodę
P.Łukowski, 2

SPOIWA POWIETRZNE
Wapno
Wapno budowlane - jedno z najstarszych znanych ludzkości
spoiw budowlanych. Pierwsze piece do wypalania wapna, w
postaci ziemnych komór, powstały w 7 tysiącleciu p.n.e.
Spoiwa wapienne stosowano w
starożytnych Chinach i Indiach,
na Bliskim Wschodzie, w
antycznej Grecji i Rzymie. Przy
użyciu zaprawy wapiennej
wzniesiono jedną z najbardziej
imponujących budowli w historii
– Wielki Mur Chiński.
P.Łukowski, 3

Wapno
Najstarsze zachowane polskie budowle wzniesione przy
użyciu spoiwa wapiennego: Opactwo Benedyktynów w Tyńcu
i kościół św. Andrzeja w Krakowie (XI wiek).
P.Łukowski, 4

Otrzymywanie wapna
Wapno powietrzne:
- tlenek wapnia CaO – wapno palone, lub
- wodorotlenek wapnia Ca(OH)
2
– wapno gaszone.
Surowiec do produkcji wszystkich rodzajów spoiw wapiennych:
skała wapienna (wapień), zawierająca głównie węglan wapnia
CaCO
3
.
P.Łukowski, 5
Wapień poddaje się wypalaniu
w temperaturze 1100-1200
°C,
zachodzi reakcja:
CaCO
3
→ CaO + CO
2
↑
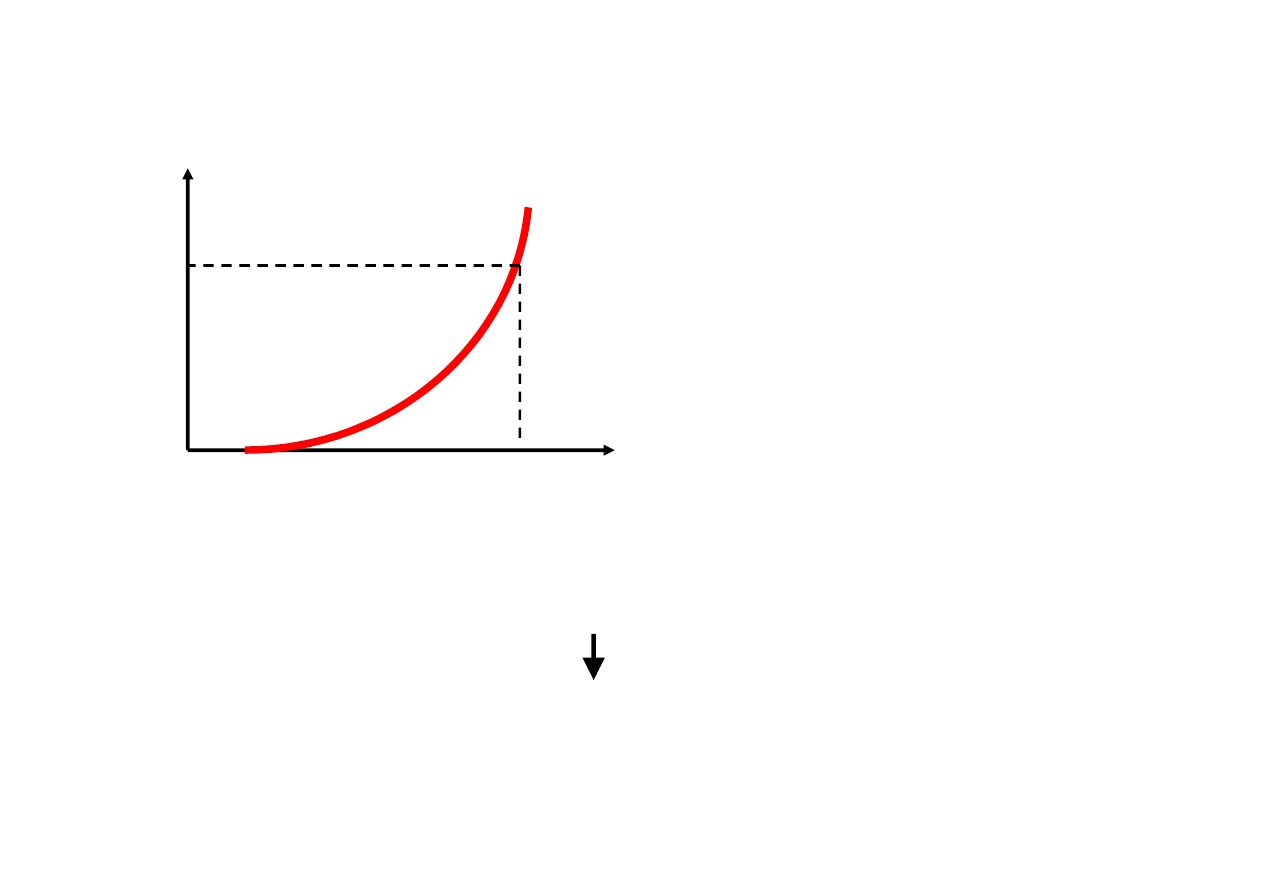
Otrzymywanie wapna
W temperaturze 898
°C
dwutlenek węgla uzyskuje
ciśnienie 1 atm, czyli równe
atmosferycznemu,
i swobodnie opuszcza
środowisko reakcji.
CaCO
3
→
→
→
→
CaO + CO
2
↑
CaCO
3
⇔
⇔
⇔
⇔
CaO + CO
2
t,
°C
898
p, MPa
0,1
Reakcja staje się nieodwracalna.
P.Łukowski, 6
Za wysoka temperatura wypalania (> 1300ºC)
Otrzymywanie wapna
Za niska temperatura wypalania (< 1000
°C)
Duża zawartość nierozłożonego CaCO
3
(wapno niedopalone).
Wapno spieczone, co utrudnia jego późniejsze gaszenie
(wapno przepalone lub martwo palone).
P.Łukowski, 7

tradycyjny piec
komorowy
prymitywny
piec szybowy
nowoczesny piec
opalany gazem
Wypalanie skały wapiennej
Wypalanie wapna prowadzi się w piecach wapienniczych.
Produktem wypału jest wapno palone (CaO)
w bryłach, które jest poddawane dalszej przeróbce.
P.Łukowski, 8

Gaszenie wapna
Wapno palone poddawane jest procesowi gaszenia, czyli
hydratacji:
CaO + H
2
O
→ Ca(OH)
2
Jest to reakcja silnie egzotermiczna (wydziela się duża ilość
ciepła – temperatura może osiągnąć nawet 100
°C).
P.Łukowski, 9
Produktem reakcji jest wapno hydratyzowane (gaszone), które
występuje w trzech postaciach, zależnie od ilości użytej wody:
- wapno suchogaszone – proszek uzyskany przy użyciu
minimalnej (stechiometrycznej) ilości wody,
- ciasto wapienne – plastyczna mieszanina wodorotlenku
wapnia i jego nasyconego roztworu,
- mleko wapienne – zawiesina wodorotlenku wapnia w wodzie.

Po zarobieniu wodą wapno powoli twardnieje w powietrzu
przez odparowanie wody i krystalizację wodorotlenku
wapnia, a następnie reakcję z atmosferycznym dwutlenkiem
węgla (karbonatyzacja):
Ca(OH)
2
+ CO
2
→ CaCO
3
+ H
2
O.
Wiązanie wapna
P.Łukowski, 10
Spoiwo wapienne jest najczęściej stosowane do wytwarzania
zapraw (spoiwo wapienne + piasek + woda).
Rola piasku:
- wypełniacz,
- dzięki porowatej strukturze ułatwia wnikanie dwutlenku
węgla i przyspiesza karbonatyzację spoiwa wapiennego.

Wiązanie zaprawy wapiennej
(powiększenie 5000x)
Kryształy Ca(OH)
2
Ziarno piasku
P.Łukowski, 11
Wiązanie wapna

Klasyfikacja wapna wg PN-EN 459 „Wapno budowlane”
Rodzaje wapna ze względu na rodzaj surowca:
- wapno wapniowe (CL) – wytwarzane z wapieni czystych,
- wapno dolomitowe (DL) – wytwarzane z wapieni
zawierających dolomit CaMg(CO
3
)
2
P.Łukowski, 12
Odmiany wapna ze względu na zawartość sumy
tlenków wapnia i magnezu:
- wapno wapniowe: CL 90, CL 80, CL 70
- wapno dolomitowe: DL 85, DL 80.
CL 90
⇒ CaO + MgO ≥ 90 % masy

WAPNO HYDRAULICZNE
Obecność w skale wapiennej minerałów ilastych (czyli gliny)
powoduje, że produkt wypalania zawiera, oprócz tlenku wapnia
CaO, również:
- krzemian dwuwapnia 2CaO·SiO
2
- glinian trójwapnia 3CaO·Al
2
O
3
- żelazian dwuwapnia 2CaO·Fe
2
O
3
i inne podobne związki.
Otrzymywanie
P.Łukowski, 13
Jeśli zawartość gliny w surowcu przekracza 6 % (wapienie
margliste)
⇒ wymienione wyżej krzemiany, gliniany i żelaziany
powstają w ilościach wystarczających, aby wytwarzane spoiwo
uzyskało właściwości hydrauliczne, to znaczy zdolność
twardnienia pod wodą –
wapno hydrauliczne
.

Wapno hydrauliczne gasi się niewielką ilością wody,
tak aby tlenek wapnia przeszedł w wodorotlenek wapnia,
a krzemiany, gliniany i żelaziany nie uległy uwodnieniu.
wapno powietrzne
wapno hydrauliczne
P.Łukowski, 14
Gaszenie i wiązanie wapna hydraulicznego
Proces wiązania i twardnienia wapna hydraulicznego:
krystalizacja i karbonatyzacja wodorotlenku wapnia (jak w
wapnie powietrznym) + uwodnienie glinianów, krzemianów i
żelazianów wapnia.

Kanał Augustowski (1824–1844)
„Wodotrwałe wapno augustowskie” uzyskiwano przez:
- zanurzenie świeżo wypalonego wapna w wodzie,
w naczyniach z otworami, przez które woda mogła wyciekać,
- dogaszanie w stosach,
- mieszanie z gliną i formowanie cegiełek,
- suszenie, wypalanie i mielenie.
P.Łukowski, 15
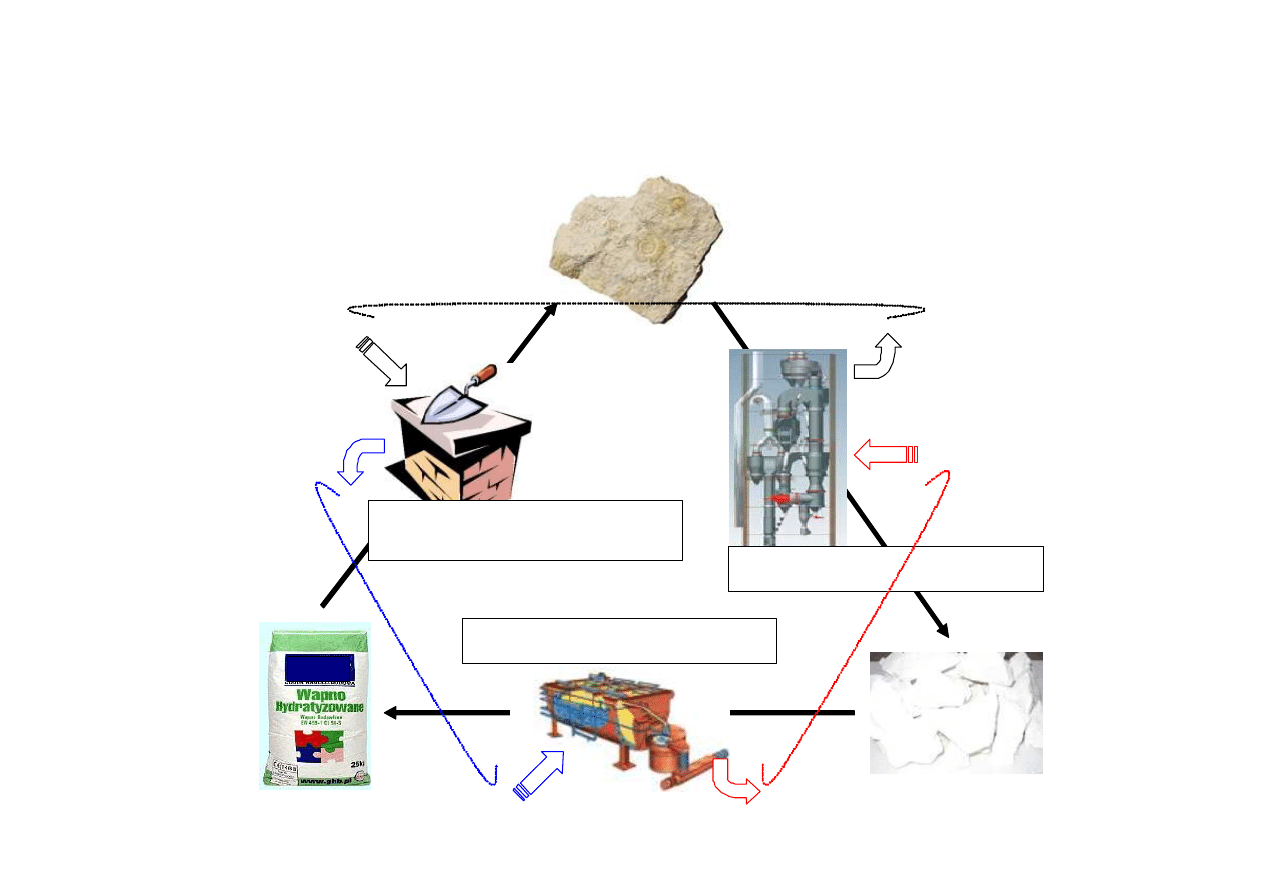
„Cykl życia” wapna
H
2
O
wapno palone
wapno gaszone
kamień wapienny
wypalanie CaCO
3
→ CaO + CO
2
gaszenie CaO + H
2
O → Ca(OH)
2
karbonatyzacja
Ca(OH)
2
+ CO
2
→ CaCO
3
+ H
2
O
CO
2
Q
CO
2
H
2
O
Q
P.Łukowski, 16

SPOIWA GIPSOWE I ANHYDRYTOWE
Otrzymywanie
Surowiec do produkcji spoiw
gipsowych: skała gipsowa
(gips surowy), zawierająca
dwuwodny siarczan wapnia
CaSO
4
⋅⋅⋅⋅2H
2
O (gips dwuwodny).
Gips surowy poddaje się
wypałowi.
Surowiec do produkcji spoiw
anhydrytowych: skała
anhydrytowa, zawierająca
bezwodny siarczan wapnia
CaSO
4
. Skałę anhydrytową
miele się z dodatkiem
odpowiednich aktywatorów.
P.Łukowski, 17

Przebieg wypalania gipsu surowego
CaSO
4
⋅ 2H
2
O
gips surowy
↓ 150-180
°
C
CaSO
4
⋅ ½H
2
O
spoiwo gipsowe (gips półwodny)
↓ 180-250
°
C
CaSO4 III
anhydryt III
↓ 350-600
°
C
CaSO4 II
spoiwo anhydrytowe, anhydryt II
↓ 800-1000
°
C
CaSO4 II + ~5 % CaO
estrichgips (gips jastrychowy)
↓ 1200
°
C
CaSO4 I
anhydryt I, trwały tylko w t > 1200
°C
↓ 1350
°
C
stopienie
P.Łukowski, 18

Spoiwo gipsowe – gips półwodny
Odmiana
α
α
α
α
:
- powstaje podczas prażenia w atmosferze nasyconej parą
wodną
- kryształy w kształcie wydłużonych słupków
⇒ mniejsza
powierzchnia właściwa
⇒ trudniej rozpuszcza się w wodzie
⇒ wolniejsze wiązanie, ale większa wytrzymałość
uzyskanych tworzyw
P.Łukowski, 19
Odmiana
β
ββ
β:
- prażenie w atmosferze suchej
- nie tworzy kryształów o wyraźnym pokroju, a jedynie
płatkowe agregaty o budowie włóknistej lub łuseczkowatej
⇒
większa powierzchnia właściwa
⇒ łatwiej rozpuszcza się w
wodzie
⇒ szybsze wiązanie, ale mniejsza wytrzymałość
uzyskanych tworzyw.

β
α
Gips budowlany i gips modelarski
≡
≡≡
≡ mieszanina odmian
α
i
β.
Gips wysokowytrzymałościowy
≡ głównie odmiana
α
.
Spoiwo gipsowe – gips półwodny
P.Łukowski, 20

Wiązanie gipsu półwodnego
Mechanizm wiązania spoiw gipsowych i anhydrytowych
wynika z różnic w rozpuszczalności siarczanów wapnia
o różnym uwodnieniu. Etapy wiązania gipsu półwodnego:
1. Rozpuszczenie półwodnego siarczanu wapnia w wodzie.
2. Uwodnienie półwodnego siarczanu wapnia do trudniej
rozpuszczalnego, dwuwodnego siarczanu wapnia
CaSO
4
⋅½H
2
O + 1½ H
2
O
→ CaSO
4
⋅2H
2
O
i powstanie roztworu przesyconego w stosunku do
dwuwodnego siarczanu wapnia.
3. Krystalizacja dwuwodnego siarczanu wapnia.
P.Łukowski, 21
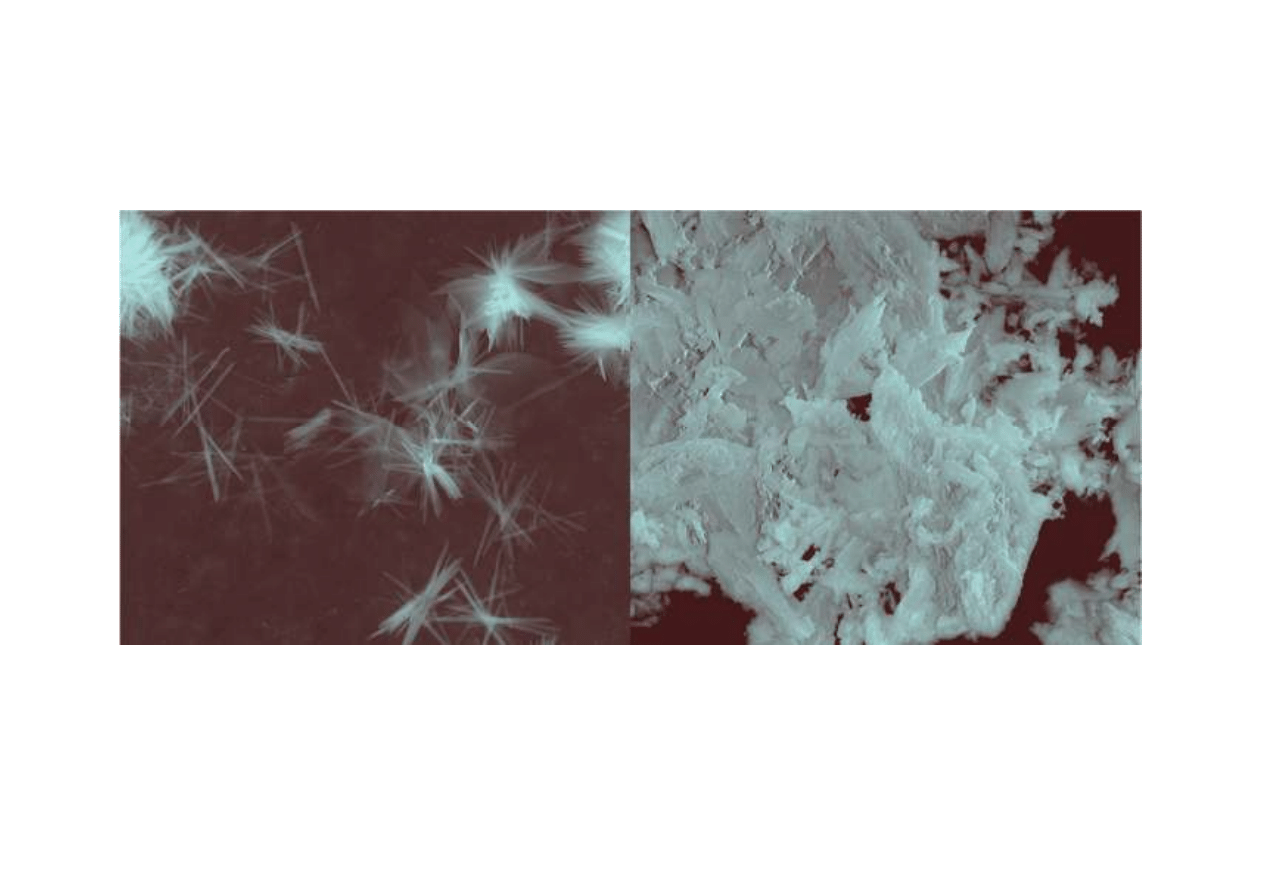
Wiązanie gipsu półwodnego
P.Łukowski, 22

Anhydryt II
Anhydryt II jest identyczny z występującym w przyrodzie
anhydrytem naturalnym. Jony SO
4
2–
są rozmieszczone
równomiernie z jonami Ca
2+
we wszystkich kierunkach,
dlatego anhydryt II jest trwały i bardzo trudno rozpuszczalny.
Kryształy mają kształt prostopadłościenny.
P.Łukowski, 23

Wiązanie spoiwa anhydrytowego, podobnie jak gipsowego,
polega na uwodnieniu do gipsu dwuwodnego i jego
krystalizacji:
CaSO
4
+ 2 H
2
O
→ CaSO
4
⋅2H
2
O
Spoiwo anhydrytowe jest znacznie wytrzymalsze od
gipsowego. Jest jednak praktycznie nierozpuszczalne w
wodzie, dlatego do wiązania wymaga obecności aktywatorów
(wapno palone i gaszone, siarczany, ałuny i inne).
Wiązanie anhydrytu
P.Łukowski, 24

Estrichgips
W temperaturze 800-1000
°C następuje częściowy rozkład
anhydrytu II:
CaSO
4
II → CaO + SO
2
↑ + ½O
2
↑
Powstały CaO spełnia rolę aktywatora wiązania anhydrytu.
Estrichgips charakteryzuje się korzystnymi właściwościami
użytkowymi: twardością i odpornością na ścieranie, a także
odpornością na wilgoć i mróz.
P.Łukowski, 25

„Cykl życia” gipsu i anhydrytu
Skała gipsowa
CaSO
4
⋅2H
2
O
wypalanie
dehydratacja
wiązanie
hydratacja
Spoiwo gipsowe
CaSO
4
⋅½H
2
O
P.Łukowski, 26

Spoiwa krzemianowe
Otrzymywanie szkła wodnego
Surowce: krzemionka (piasek) + soda lub potaż; t > 800
°C
SiO
2
+ Na
2
CO
3
→ Na
2
SiO
3
+ CO
2
SiO
2
+ K
2
CO
3
→ K
2
SiO
3
+ CO
2
Powstaje mieszanina krzemianów sodu (szkło wodne sodowe)
lub potasu (szkło wodne potasowe).
P.Łukowski, 27

Wiązanie szkła wodnego
1 etap: hydroliza krzemianów w roztworze wodnym:
Na
2
SiO
3
+ 2H
2
O
→ H
2
SiO
3
+ 2NaOH
2 etap
:
zobojętnienie i koagulacja
:
- kwas krzemowy jest utrzymywany w postaci zolu przez
NaOH, dlatego najpierw NaOH musi być
zobojętniony
dwutlenkiem węgla z powietrza:
2NaOH + CO
2
→ Na
2
CO
3
+ H
2
O
potem następuje
koagulacja
z utworzeniem żelu krzemowego
3 etap
:
polikondensacja
:
żel kwasu krzemowego ulega stopniowemu odwodnieniu z
utworzeniem łańcuchów krzemowo-tlenowych
P.Łukowski, 28

H
H
Szkło wodne jest:
- odporne na kwasy (z wyjątkiem fluorowodorowego),
- słabo odporne na wilgoć.
Właściwości szkła wodnego
|
|
|
— Si — O — Si — O — Si — O —
|
|
|
O
O
|
|
|
HO
OH
O
OH
— Si —
H
O
O
|
|
|
P.Łukowski, 29
Odwadnianie i polikondensacja szkła wodnego:
Wyszukiwarka
Podobne podstrony:
spoiwa powietrzne W R
Spoiwa powietrzne (wapno i gips)
BUDOWLANE SPOIWA POWIETRZNE(1), Budownictwo Politechnika Rzeszowska, Rok II, Technologia Betonu, śc
13-spoiwa wapienne
Spoiwa powietrzne i hydrauliczne
II 2 spoiwa powietrzne
spoiwa powietrzne W R
13 Ochrona powietrza przed zanieczyszczeniami
Duże odstępy powietrzne 13 14 1, Prywatne, EN-DI semestr 4, Elektroenergetyka, wykład + ćwiczenia
C5 (X7) B1HB01HEP0 13 02 12 2014 Momenty dokręcania Układ zasilania powietrzem
D19220761 Ustawa z dnia 23 września 1922 r o ratyfikacji konwencji, urządzającej żeglugę powietrzną
13 ZMIANY WSTECZNE (2)id 14517 ppt
13 zakrzepowo zatorowa
Zatrucia 13
pz wyklad 13
więcej podobnych podstron